A microbiota vulvovaginal da mulher: como pode ser útil na prática clínica?
Dr. Pedro Vieira Baptista
Hospital Lusíadas Porto, Porto, Portugal; Departamento de Ginecologia-Obstetrícia e Pediatria, Faculdade de Medicina da Universidade do Porto; Faculdade de Medicina e Ciências da Saúde, Universidade de Gante, Gante, Bélgica
Área para o público geral
Encontre aqui o seu espaço dedicado
en_sources_title
en_sources_text_start en_sources_text_end
Capítulos
Sobre este artigo
O mundo do microbioma vaginal humano é fascinante, apesar da existência do conhecimento limitado sobre o mesmo. A evolução levou a um cenário único, em que a predominância de espécies específicas de lactobacilos constitui o estado ideal durante os anos reprodutivos, apesar das enormes variações entre indivíduos — e mesmo a variação que se verifica na mesma mulher ao longo do tempo. Compreender o microbioma vaginal e o seu potencial é a chave para melhorar a saúde das mulheres em áreas como as infeções sexualmente transmissíveis e as vaginites recorrentes. Além disso, e este ponto é de suma importância, pode ser a resposta a um problema para o qual até ao momento não existem respostas satisfatórias: o parto pré-termo. Neste artigo, abordamos o microbioma vaginal através de uma perspetiva evolutiva, destacando a aparente ausência de um continuum entre espécies. Discutimos o conhecimento atual, mas também nos focamos nas possibilidades futuras.
Perspetiva histórica
O início do longo percurso rumo à compreensão do microbioma vaginal pode ser atribuído a Albert Döderlein, no final do século XIX. No seu livro Das Scheidensekret und seine Bedeutung für das Puerperalfieber salientou que as mulheres “normais” e saudáveis têm predominância de bacilos Gram-positivos na vagina, a que chamou Lactobacillus acidophilus.
- O estudo do microbioma vaginal ainda está em evolução, apesar dos enormes progressos das últimas décadas.
- O microbioma vaginal humano ideal em mulheres em idade reprodutiva é predominado por lactobacilos.
- A não predominância de lactobacilos no microbioma vaginal humano está associada a um risco acrescido de infeções sexualmente transmissíveis, cancro do colo do útero e desfechos obstétricos negativos.
- Exames futuros poderão permitir um diagnóstico mais preciso de vaginites e a avaliação do risco associado a perfis disbióticos específicos.
- Embora a investigação sobre o microbioma esteja a avançar rapidamente, é fundamental distinguir entre exames experimentais e as suas aplicações clinicamente relevantes.
Este conceito ainda molda as interpretações contemporâneas do microbioma vaginal, mas a realidade é provavelmente muito mais complexa.
A compreensão das vaginites ainda é incompleta e o seu tratamento é na grande maioria dos casos empírico, apesar de ser uma das causas mais comuns para as mulheres procurarem atendimento médico1.
Em 2011, Ravel et al. publicaram um dos artigos mais importantes e que mudou o paradigma em termos de compreensão do microbioma vaginal humano. Nesse artigo, demonstraram que assintomático não é sinónimo de "normal" (o que leva também à questão do que seria um microbioma vaginal "normal" ou, mais precisamente, "ideal") e que existem diferenças significativas entre etnias2.
A diversidade é a regra na natureza, mas a vagina humana parece ser uma exceção: o microbioma vaginal “ideal” aceite consiste na prevalência de uma ou duas espécies de lactobacilos (baixa diversidade alfa). Se pensarmos noutros órgãos ou regiões anatómicas, a predominância de uma espécie é geralmente sinónimo de doença (infeção). Se realizarmos o mesmo exercício considerando qualquer sistema ecológico, tal representa o último passo antes do colapso (ex.: nunca ocorrem monoculturas de plantas na natureza e, quando realizadas artificialmente, devem ser limitadas no tempo). Podemos procurar outras explicações para esta aparente "anormalidade" (ou "exceção") na natureza, mas tal parece levar a um beco sem saída.
Deveríamos, em vez disso, passar a investigar os conjuntos de genes em vez das espécies ou géneros para ultrapassar esta aparente anormalidade biológica?
O objetivo final dos seres vivos parece ser a transmissão dos genes para as gerações seguintes e a evolução parece ser muito impulsionada por este “instinto” primordial. Como tal, podemos facilmente supor que o microbioma vaginal humano deve ser uma parte fulcral do produto final da evolução para otimizar o processo reprodutivo. Se esta premissa estiver correta, podemos esperar:
- congruência evolutiva (como foi demonstrado, por exemplo, no caso do intestino);
- quaisquer diferenças devem ser relativamente fáceis de explicar (processo de acasalamento, alimentação, localização geográfica, etc.) e; naturalmente
- maior semelhança em espécies estreitamente relacionadas.
Surpreendentemente, nenhuma das três premissas é satisfeita. Na natureza, a filogenia não pode ser relacionada com o pH vaginal (um marcador muito indireto da composição do microbioma vaginal), e a predominância dos lactobacilos é exclusiva da espécie humana. Mesmo quando se comparam os seres humanos com outros primatas, as diferenças são enormes e, atualmente, não são facilmente explicáveis3,4. O que é que tornou a vagina humana tão única? Terá sido fruto do acaso ou o corolário evolutivo do ciclo ovárico contínuo, do elevado risco de lacerações e infeções à nascença, ou da agricultura e consequente elevado consumo de amido3?
O microbioma e a gravidez
Uma questão parece não suscitar dúvidas: os lactobacilos são fundamentais para o sucesso da gravidez, mas não é assim tão claro se o mesmo se aplica a conseguir engravidar5.
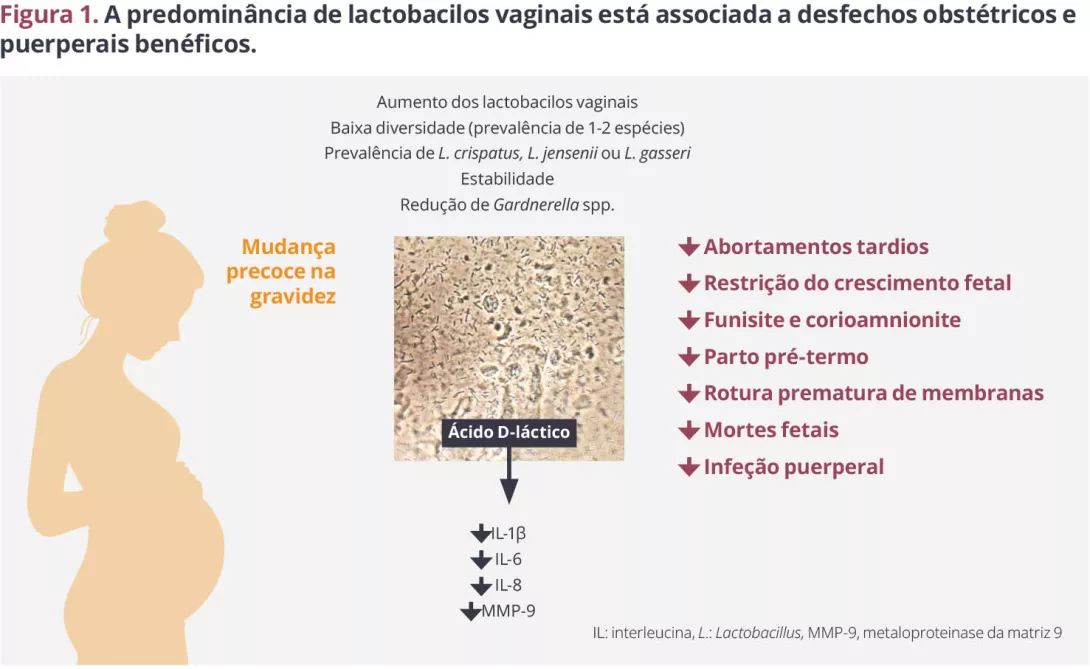
Os dados disponíveis mostram claramente que uma vagina sem predominância de lactobacilos durante a gravidez está associada a desfechos obstétricos e puerperais negativos, incluindo parto pré-termo, rotura prematura de membranas e infeções puerperais (Figura 1). É de salientar que um milhão de bebés morrem todos os anos devido a complicações relacionadas com a prematuridade6.
Temos o hábito de repetir que os lactobacilos têm um papel protetor e que a sua presença é desejável, porém, supor isso significa que temos de ignorar alguns factos óbvios, como o facto de esta predominância não ocorrer em crianças, durante a amamentação, nem em mulheres pós-menopáusicas. Assim, podemos teorizar que a nossa relação simbiótica com os lactobacilos tem um propósito durante a idade reprodutiva. Podemos considerar que este propósito inclui uma redução do risco de infeções sexualmente transmissíveis (IST) (que constituem um risco para o sucesso reprodutivo e para a prole), de infeções genitais ascendentes (e consequentes abortamentos, mortes fetais e partos pré-termo), bem como de complicações puerperais. O papel do microbioma na concretização de uma gravidez parece ser mais limitado. Por exemplo, as populações com elevadas taxas de disbiose vaginal não parecem ser menos férteis7.
Figura 1. A predominância de lactobacilos vaginais está associada a desfechos obstétricos e puerperais benéficos
Da mesma forma, o impacto do microbioma cervicovaginal no desfecho dos tratamentos de fertilidade também não é claro5.
Uma das maiores diferenças evolutivas entre os seres humanos e os outros mamíferos tem a ver com o parto: o difícil equilíbrio entre nascer com um grande perímetro cefálico e compatibilizar esse perímetro com uma pélvis que teve de se adaptar ao bipedismo. Os humanos têm os partos mais difíceis — talvez só ultrapassados pelos das hienas. Poderá residir aqui a chave para compreender a singularidade do microbioma vaginal humano? Qualquer que tenha sido o propósito evolutivo, para a maioria das mulheres em idade reprodutiva, mesmo não estando grávidas, a predominância de lactobacilos na vagina é desejável. No entanto, a falta de lactobacilos, apesar de representar um estado disbiótico, não é sinónimo de doença.
A nossa compreensão do papel da microbiota vaginal é ainda muito limitada. Mesmo questões aparentemente simples, como a forma como os lactobacilos colonizam a vagina, ainda carecem de uma resposta clara.
O microbioma vulvovaginal na saúde e na doença
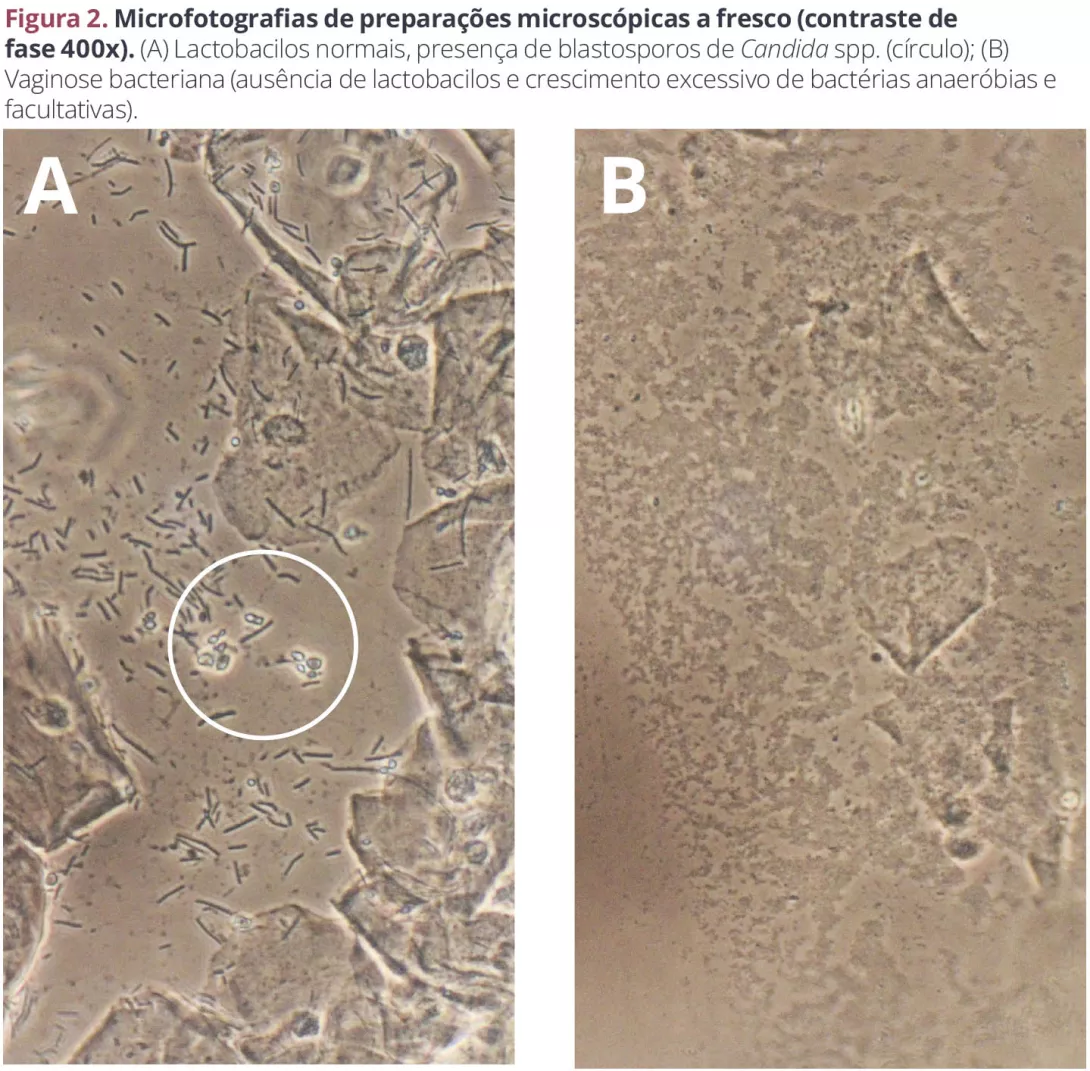
O efeito mais visível de um microbioma alterado é a vaginite. A maioria das mulheres sofrerá pelo menos um episódio de candidíase e, em algumas populações, mais de metade das mulheres em idade reprodutiva têm vaginose bacteriana (VB), assintomática na maioria das vezes (figura 2A e 2B). Temos uma compreensão limitada do que está na origem destas alterações (“normal” — colonização/ estado assintomático — sintomático)8.
Figura 2. Microfotografias de preparações microscópicas a fresco (contraste de fase 400x)
((A) Lactobacilos normais, presença de blastosporos de Candida spp. (círculo); (B) Vaginose bacteriana (ausência de lactobacilos e crescimento excessivo de bactérias anaeróbias e facultativas).
O microbioma vaginal pode proporcionar diferentes perfis de risco ou de proteção.
O perfil bacteriano da vagina, independentemente dos sintomas, pode proporcionar diferentes perfis de risco ou de proteção. Em geral, considera-se que os Lactobacillus spp. tendem a proporcionar benefícios para a saúde. No entanto, nem todas as espécies são iguais e apenas um número limitado das espécies existentes é normalmente encontrado em estados de predominância na vagina. O L. iners, com um genoma significativamente menor e um perfil metabólico diferente, está geralmente associado a estados disbióticos ou de transição9.
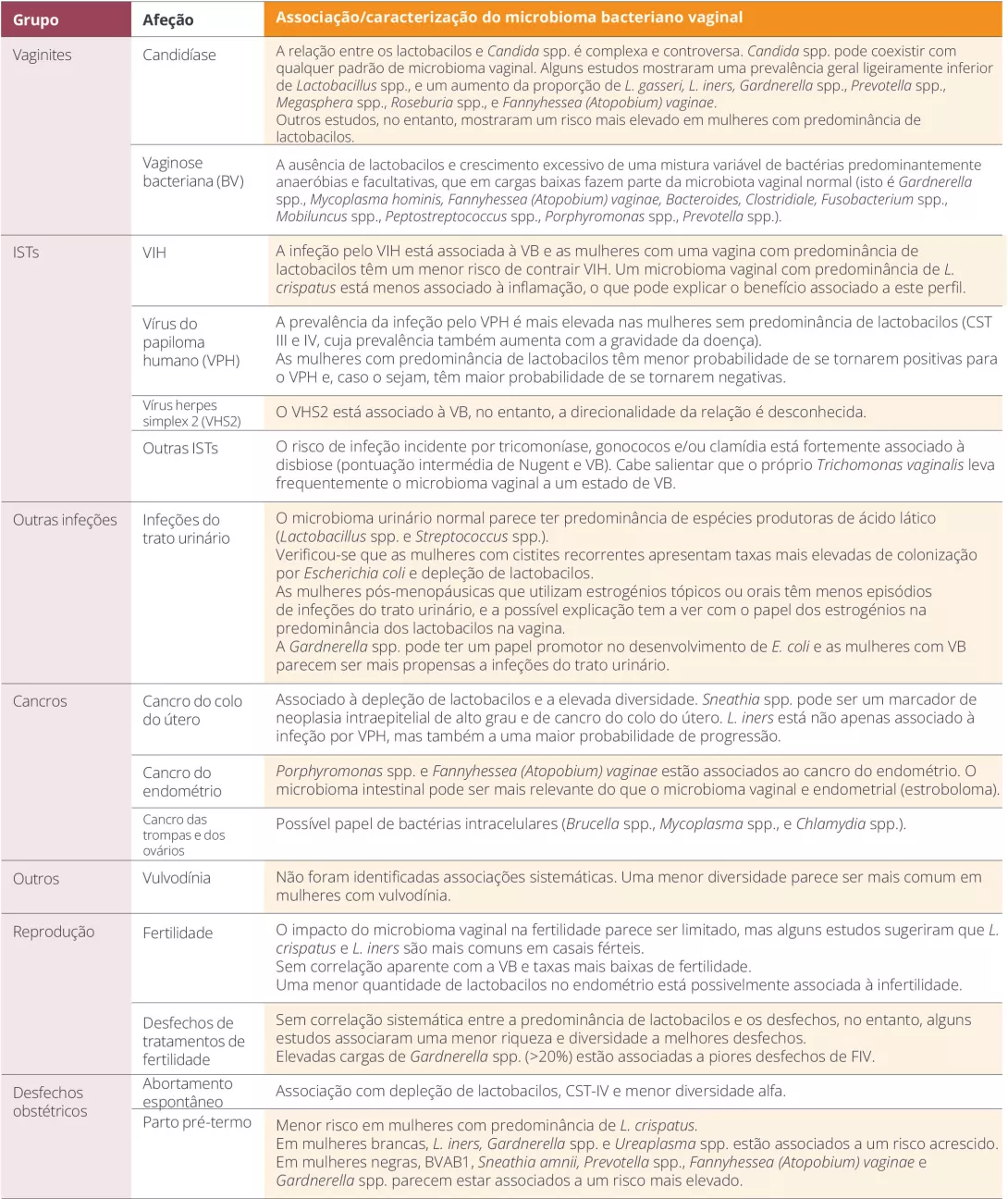
Tabela 1. Afeções ginecológicas e obstétricas e as suas associações com o microbioma vulvovaginal.
Pouco se conhece sobre a relação entre Candida spp. e o microbioma vaginal
Embora não existam atualmente recomendações para tratar a disbiose assintomática (por exemplo, VB), esta tem sido associada a complicações obstétricas e não obstétricas (incluindo o risco de contrair ISTs [VPH, VIH])8 (Tabela 1).
Quando estiverem disponíveis estratégias eficazes (de preferência sem recurso a antibióticos), poderá ser aconselhável rastrear e tratar a disbiose em mulheres com risco acrescido de ISTs ou mesmo em mulheres infetadas pelo VPH. No entanto, isto pode revelar-se mais complexo do que aparenta. O comportamento semelhante a uma IST que a VB apresenta é reconhecido há já bastante tempo, no entanto, dados recentes confirmamno e sugerem que a redução das recorrências pode necessitar do tratamento dos parceiros, o que poderá constituir um grande obstáculo às estratégias de prevenção10.
BA VB é uma síndrome comum, na qual existe uma depleção de lactobacilos e um crescimento excessivo de várias bactérias anaeróbias estritas e facultativas, associada à formação de um biofilme que parece contribuir para as frequentes recorrências após o tratamento. A composição da VB varia de mulher para mulher, e provavelmente varia até na mesma mulher ao longo do tempo11. Atualmente, é possível diagnosticar a VB através de exames moleculares, mas espera-se que, com o aumento do conhecimento do microbioma vaginal, estes exames permitam traçar o “perfil” da VB, avaliar o resistoma e escolher tratamentos mais adequados8.
A relação entre Candida spp. e o microbioma vaginal é muito complexa e está longe de ser totalmente compreendida. Embora a candidíase possa existir em qualquer microbioma vaginal, tende a ser mais comum com a predominância de lactobacilos (e o consequente pH reduzido)12.
Várias patologias ginecológicas foram associadas a caraterísticas específicas do microbioma e, quase sistematicamente, uma redução dos lactobacilos constitui um risco acrescido de ISTs e cancros ginecológicos (mesmo do trato genital superior). No entanto, nem sempre é fácil estabelecer uma relação causal entre os desvios do microbioma e patologias específicas. Podemos, no entanto, esperar um dia conseguir avaliar ou modular o risco de cancro através da avaliação do microbioma vaginal, especialmente no caso do cancro do colo do útero13.
TO interesse e o conhecimento relativo ao microbioma vulvar são mais recentes e a quantidade de dados é escassa, no entanto, o seu papel em afeções como a vulvodínia, as dermatoses vulvares, a neoplasia intraepitelial vulvar e o cancro está a ser estudado14-16.
O que se segue?
Estão a ser dados grandes passos para a compreensão do microbioma vulvovaginal. Até compreendermos totalmente o microbioma, podemos começar por respeitá-lo e ao seu papel funcional, reconhecendo que cada mulher é única (e que esta singularidade é mutável), evitando o uso desnecessário de antibióticos e antissépticos e diagnosticando corretamente as ISTs e as vaginites, em vez de confiarmos no empirismo. Um diagnóstico preciso minimizará tratamentos incorretos, com um potencial impacto a longo prazo.
Nesta fase, é essencial distinguir o que é experimental e o que é clinicamente relevante. Estamos num processo de aprendizagem e de tentativa de utilização de técnicas e conceitos experimentais na prática clínica que, muitas vezes, levam a exames, despesas e tratamentos desnecessários. Por exemplo, a metagenómica é uma ferramenta de investigação muito útil, mas atualmente não tem lugar na avaliação clínica das vaginites.
Nas últimas duas décadas, acumulámos uma enorme quantidade de informação, que em breve se traduzirá em melhores cuidados de saúde para as mulheres, incluindo recomendações dietéticas específicas, bem como em prebióticos e probióticos. É expectável que este conhecimento reduza substancialmente os partos pré-termo e cancros ginecológicos, bem como a recorrência das vaginites e cistites.
Os próximos capítulos serão, sem dúvida, os mais entusiasmantes!
CONCLUSÃO
O microbioma vaginal humano ainda não é totalmente compreendido e alguns dos nossos pressupostos atuais poderão ter de ser atualizados ou adaptados à medida surgem novos dados. A sua plena compreensão e o potencial para o manipular poderão ser desvendados quando a aparente ausência de lógica evolutiva for totalmente compreendida.
No entanto, podemos estar certos que os lactobacilos são benéficos para a maioria das mulheres em idade reprodutiva e que são fundamentais para o sucesso da gravidez, independentemente da localização geográfica ou etnia.
O conhecimento crescente nesta área está a levar a progressos no diagnóstico e tratamento das vaginites e, num futuro próximo, permitirá reduzir o risco de problemas graves como ISTs e partos pré-termo.