Reconstitution du microbiote intestinal par transplantation de microbiote fécal autologue chez des patients traités par antibiotiques
Article commenté - Rubrique adulte
Par le Pr. Harry Sokol
Gastro-entérologie et nutrition, Hôpital Saint-Antoine, Paris, France
Section grand public
Retrouvez ici votre espace dédié
en_sources_title
en_sources_text_start en_sources_text_end
Chapitres

Faecal transplant preparation. A technician storing a prepared sample of human faecal matter in cold storage.
A propos de cet article
Auteur
Commentaire de l’article original de Taur et al. (Science Translational Medicine 2018 [1])
Un traitement antibiotique peut appauvrir en bactéries commensales le microbiote intestinal (MI) du patient et, paradoxalement, augmenter le risque d’infections ultérieures. Dans l’allogreffe de cellules souches hématopoïétiques (allo-CSH), l’administration d’antibiotiques est essentielle pour des résultats cliniques optimaux mais perturbe considérablement la diversité du MI, entraînant la perte de nombreux micro-organismes bénéfiques. Bien que la perte de diversité du microbiote au cours de l’allo-CSH soit associée à une mortalité accrue, les approches visant à rétablir les bactéries commensales décimées n’ont pas encore été développées. Un essai clinique contrôlé et randomisé a été initié, pour comparer la transplantation de microbiote fécal autologue (auto-TMF) à l’absence d’intervention ; les profils de microbiote de 25 patients ayant été traités par allo-CSH (14 qui ont reçu une auto-TMF et 11 patients contrôles qui n’ont pas reçu ce traitement) ont été analysés. Les changements dans la diversité et la composition du MI ont révélé que l’auto- TMF avait stimulé la diversité microbienne et rétabli la composition de microbiote que le patient avait avant le traitement antibiotique et l’allo-CSH. Dans le contexte d’une allo-CSH, ces résultats montrent l’utilité potentielle du stockage d’échantillons de selles en vue d’une auto-TMF visant à rétablir le MI chez des patients ayant subi un traitement antibiotique lourd.
Que sait-on déjà à ce sujet ?
Les traitements antibiotiques endommagent le microbiote intestinal et augmentent le risque d’infections gastro-intestinales. Bien que cet effet soit reconnu depuis plus de 60 ans, la correction des altérations du microbiote intestinal induites par les antibiotiques n’est toujours pas une pratique clinique standard. Chez les patients subissant une greffe allogénique de cellules souches hématopoïétiques (allo- CSH), des antibiotiques sont systématiquement administrés pour traiter ou réduire le risque d’infection grave. Des études prospectives sur des patients recevant une allo-CSH ont démontré que le microbiote intestinal est nettement altéré pendant le traitement, avec de profondes pertes de bactéries anaérobies obligatoires, y compris des espèces immunomodulatrices telles que celles appartenant à la classe des Clostridia et au phylum des Bacteroidetes [2]. Les conséquences cliniques de ces altérations sont également apparentes dans une allo-CSH : les perturbations des anaérobies obligatoires bénéfiques sont corrélées aux complications incluant les infections systémiques à Entérocoque Résistant à la Vancomycine (ERV), les infections à Clostridium difficile, et la maladie du greffon contre l’hôte (GVHD) [2, 3]. Dans l’ensemble, les patients qui perdent la diversité de leur microbiote intestinal au moment de la prise de greffe des cellules souches hématopoïétiques ont des taux plus élevés de décès liés à la greffe [4].
Quels sont les principaux résultats apportés par cette étude?
Les patients recevant une allo-CSH restent immunodéprimés pendant de nombreux mois après la greffe, et bien que des patients immunodéprimés, y compris ceux traités par allo-CSH, aient été traités sans effets secondaires par TMF hétérologue [5], les auteurs ont considéré qu’une TMF autologue serait plus sûre, car de nature à minimiser, notamment, le risque d’exposition du patient à des micro-organismes potentiellement pathogènes non encore détectés. Les auteurs ont initié un essai clinique contrôlé randomisé pour déterminer la faisabilité de l’auto-TMF pour restaurer le microbiote intestinal et pour diminuer les complications liées à l’allo-CSH. Ici, ils présentent une analyse des modifications de la composition du microbiote intestinal chez 25 patients randomisés dans cette étude et pour lesquels des échantillons de selles ont été collectés longitudinalement.
Les auteurs ont tout d’abord confirmé sur leur cohorte de 753 patients (3 237 échantillons fécaux collectés longitudinalement) que l’allo-CSH et les différents traitements antibiotiques associés induisaient une diminution nette de la diversité du microbiote intestinal avec un nadir 5 jours après l’allo- CSH, une persistance des altérations pendant au moins 6 semaines et une absence de récupération pour la plupart des patients à 100 jours post-allo-CSH.
POINTS CLÉS
-
Le microbiote intestinal est fortement perturbé au cours du traitement par allo-CSH et ces perturbations pourraient jouer un rôle dans les complications associées
-
L’auto-TMF est une stratégie faisable et efficace sur la reconstitution du microbiote après les perturbations induites par l’allo-CSH
-
Les conséquences de la reconstitution du microbiote en termes de pronostic hématologique restent à évaluer
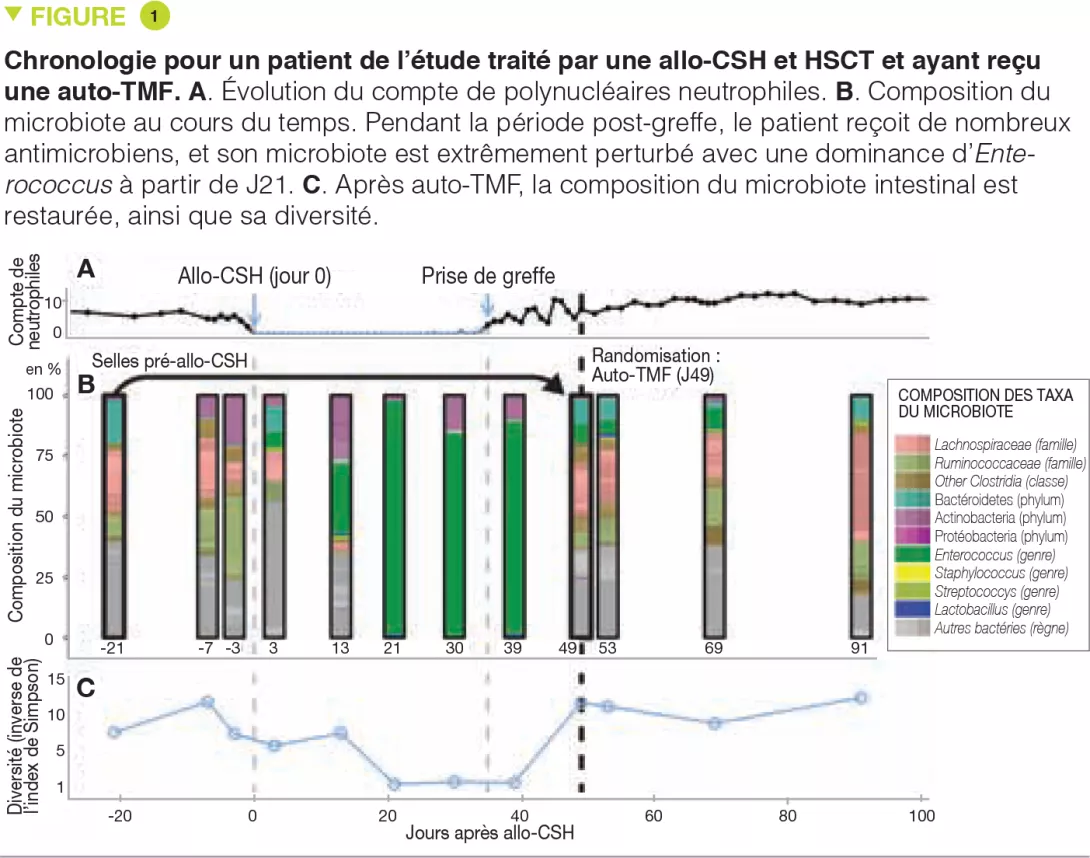
Dans le cadre de l’étude randomisée, les selles des patients, prélevées avant l’allo- CSH étaient congelées à -80°C et conservées. Une à cinq semaines (13 jours en moyenne) après l’allo-CSH, au moment de la prise de greffe (définie par la remontée des polynucléaires neutrophiles au-delà de 500/mm3), les patients étaient réévalués, et un autre échantillon de selles était prélevé. Si une diminution des bactéries appartenant au phylum des Bacteroidetes était mise en évidence, les patients étaient randomisés. Le résultat des analyses de microbiote des 25 premiers patients évaluables (14 du groupe auto-TMF et 11 du groupe contrôle) est présenté. L’auto-TMF était réalisée par un lavement unique, après une préparation colique par polyéthylène glycol, similaire à la préparation réalisée avant une coloscopie. Les auteurs montrent que l’auto-TMF permet de restaurer non seulement la diversité du microbiote intestinal mais aussi sa composition pré-allo-CSH.
Quelles sont les conséquences en pratique ?
Plusieurs études montrent que le microbiote intestinal et ses perturbations pourraient jouer un rôle dans la survenue des complications infectieuses et non infectieuses habituelles au cours de l’allo-CSH. Cette première étude montre que la collection de selles du patient avant une allo-CSH et leur conservation afin de les réadministrer une fois la prise de greffe effectuée est une stratégie faisable et efficace sur la reconstitution du microbiote. Il reste maintenant à savoir si les patients ayant bénéficié d’une telle auto-TMF ont un meilleur pronostic vis-à-vis de ces complications et une meilleure survie globale. Si l’efficacité de cette stratégie se confirme, elle pourrait être également envisagée dans d’autres situations où des perturbations importantes du microbiote sont attendues, comme un traitement antibiotique large et prolongé ou d’autres chimiothérapies anticancéreuses
Conclusion
Bien qu’il faille encore en estimer les bénéfices en termes de pronostic hématologique et de survie globale, l’auto-TMF est une option stratégique prometteuse pour reconstituer le microbiote intestinal après les perturbations induites par le traitement antibiotique associé à l’allo-CSH.