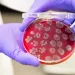
Polyarthrite : le microbiote intestinal altéré dès les stades précoces
Le microbiote intestinal connaît une dysbiose dès les stades précoces de la polyarthrite rhumatoïde, caractérisée à la fois par une diversité microbienne réduite, des taxons sur ou sous représentés et des fonctions génétiques modifiées.
en_sources_title
en_sources_text_start en_sources_text_end
A propos de cet article
Parmi les maladies auto-immunes, la polyarthrite rhumatoïde (PR) est une maladie chronique des articulations caractérisée par une inflammation de la membrane synoviale qui s’étend aux cartilages et os alentours. Le microbiote intestinal reçoit depuis quelques années une attention toute particulière de la part de la communauté scientifique, qui suspecte son implication dans la PR.
La dysbiose présente dès les stades précoces
Alors que des travaux ont déjà rapporté des états de dysbiose chez des patients présentant un stade avancé de la maladie, une équipe coréenne s’est intéressée aux stades précoces, et ce exclusivement chez des femmes, qui sont davantage touchées par la PR. Les 29 patientes incluses se trouvaient ainsi soit à un stade préclinique (SP, n=17), soit un stade clinique précoce (SCP, début de manifestations cliniques apparentes, n=12), et étaient naïves de médicaments antirhumatismaux modificateurs de la maladie (ARMM). L’ADN bactérien fécal prélevé chez les patientes a été comparé à celui de 25 femmes témoins en bonne santé. Premier constat : le microbiote des patientes PR était caractérisé par une moindre diversité bactérienne (sans différence entre les patientes SP et SCP). En outre, des différences étaient observées au niveau des espèces bactériennes présentes : notamment, des bactéries appartenant au phylum des Bacteroidetes étaient sur-représentées chez les patientes PR, tandis que celles appartenant aux Actinobacteria étaient sous représentées, en particulier celles du genre Collinsella.
Des fonctions génétiques altérées
Ces différences de composition se traduisaient par des différences génétiques : les gènes intervenant dans la synthèse d’ubiquinone (coenzyme Q10) et de ménaquinone (Vitamine K2) étaient davantage présents chez les témoins, tandis que les gènes intervenant dans le transport et l’absorption du fer étaient plus abondants chez les patientes PR. Cette particularité, qui facilite l’absorption du fer par les bactéries du microbiote, pourrait expliquer l’anémie souvent observée chez les personnes souffrant de PR. Enfin, les gènes codant pour la synthèse de lipopolysaccharides – molécules exprimées à la surface des bactéries Gram négatif qui traversent la barrière intestinale et créent une inflammation systémique – étaient particulièrement représentés chez les patientes PR présentant des manifestations cliniques. Un résultat interpellant au regard du caractère inflammatoire de la PR. Des études plus larges et fondées sur des technologies complémentaires de séquençage pourraient préciser le rôle du microbiote intestinal dans la PR et déterminer si la dysbiose observée est une cause ou une conséquence de la maladie.