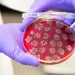
Вакцинация после приема антибиотиков: влияние на иммунитет и роль микробиоты
У людей с низким иммунитетом к гриппу до вакцинации* прием антибиотиков приводит к дисбиозу кишечника, что нарушает иммунный ответ на вакцину от гриппа. Группа ученых попыталась выяснить причину.
Раздел для широкой публики
Найдите здесь свое выделенное место
en_sources_title
en_sources_text_start en_sources_text_end
Делиться - значит заботиться
Возможно, эта тема заинтересует ваших коллег. Почему бы не поделиться ею?
Об этой статье
Несколько исследований подтвердили ведущую роль микробиоты кишечника в иммунитете, хотя клинические данные по-прежнему ограниченны. Более тщательное изучение лежащих в основе механизмов имеет решающее значение для здравоохранения, в частности, для разработки методов лечения, ориентированных на микробиоту, в случаях с нарушениями иммунитета. В этом контексте и основываясь на наблюдении, что эффективность вакцины варьируется в той же степени, что и микробиота кишечника у людей в разных частях света, исследователи сосредоточились на влиянии антибиотиков в отношении иммунного ответа на вакцинацию.
Влияние антибиотиков на вакцинацию
С этой целью ученые изучили две группы людей с различным уровнем антител против гриппа перед началом исследования. В первой группе 22 здоровых взрослых испытуемых были вакцинированы против сезонного гриппа (вакцина, содержащая 3 штамма ослабленных вирусов); за 3 дня до вакцинации половина из них начала лечение антибиотиками продолжительностью 5 дней. Как и ожидалось, антибиотики оказали глубокое и длительное влияние на состав микробиоты кишечника. Но вопреки гипотезе исследователей, применение антибиотиков не влияло на выработку антител при ответе на вакцинацию. Эффект наблюдался только во второй когорте, состоящей из 11 испытуемых, не имевших ранее существовавшего иммунитета против гриппа (без недавно перенесенного гриппа или вакцинации*): антибиотики вызывали снижение выработки антител IgG1 и IgA против штамма вируса H1N1. Таким образом, антибиотики широкого спектра действия могут в некоторых случаях нарушать иммунный ответ на вакцинацию.
Желчные кислоты: вестники воспаления
Исследователи также отметили, что изменения на уровне метаболитов крови, вызванные вакцинацией, были различными в группе, получавшей антибиотики, и в контрольной группе, особенно в отношении веществ, полученных в результате метаболизма желчных кислот. Следует напомнить, что микробиота трансформирует первичные желчные кислоты, выделяемые желчным пузырем и поступающие в кишечник, во вторичные желчные кислоты. Затем происходит их частичное обратное всасывание. Но у испытуемых, получавших антибактериальную терапию, наблюдалось повышение уровня первичных желчных кислот в крови и значительное снижение уровня вторичных желчных кислот. Антибиотикотерапия может даже сократить в 1000 раз концентрацию наиболее важной из них - литохолевой кислоты. Данное сокращение вторичных желчных кислот было тесно связано с увеличением уровня провоспалительных веществ. Это говорит о том, что изменение соотношения желчных кислот, вызванное антибиотикотерапией, может быть одним из механизмов, регулирующих воспалительную реакцию.
Два разных вида реакции
Существует ли связь между реакцией с модулированием выработки антител, и реакцией, влияющей на желчные кислоты и воспаление? По словам исследователей, такой связи нет: они сопоставили разнообразные сигнальные пути, от нарушения микробиоты после введения антибиотиков, до изменений метаболитов крови; и пришли к выводу, что эти два пути независимы. В заключение следует отметить, что глубокое повреждение микробиоты, вызванное применением антибиотиков, может модулировать иммунную функцию с помощью двух различающихся механизмов: путем прямого взаимодействия с иммунными клетками или системным путем, за счет модулирования выработки некоторых ключевых метаболитов.
* Без недавней вакцинации или перенесенного гриппа, что подтверждается низким уровнем антител (1 когорта: уровни в сыворотке < 320 в отношении по меньшей мере 2 из 3 штаммов, включенных в вакцину; 2 когорта: уровни в сыворотке ≤ 320 в отношении 3 штаммов, содержащихся в вакцине).