Поможет ли трансплантация фекальной микробиоты предотвратить антибиотикорезистентность у пациентов с ослабленным иммунитетом?
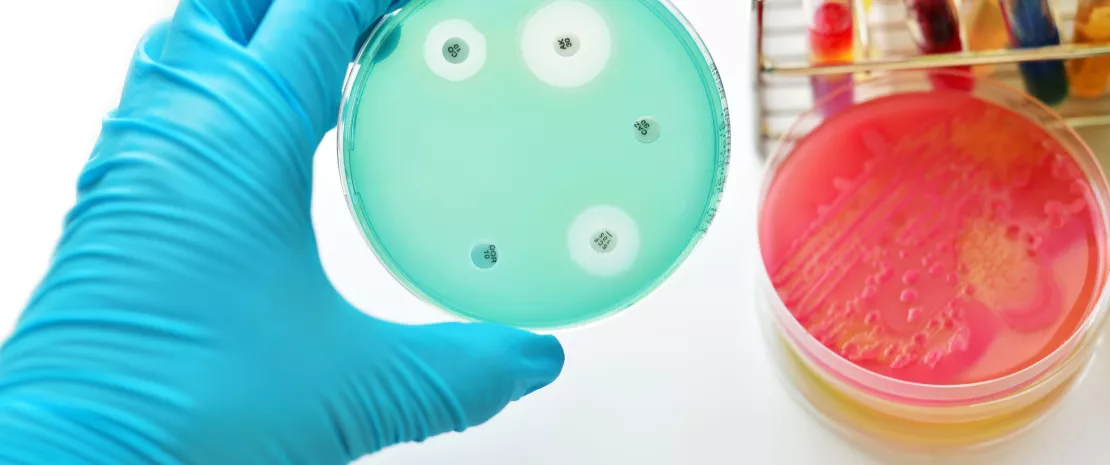
Согласно исследованию, проведенному учеными из Франции и Италии, эффективность и безопасность трансплантации фекальной микробиоты подтверждена при лечении инфекций, вызванных бактериями с множественной лекарственной устойчивостью, даже в отношении пациентов с ослабленным иммунитетом.
Раздел для широкой публики
Найдите здесь свое выделенное место
en_sources_title
en_sources_text_start en_sources_text_end
Делиться - значит заботиться
Возможно, эта тема заинтересует ваших коллег. Почему бы не поделиться ею?
Об этой статье
«Одна из самых серьезных угроз для глобального здравоохранения, безопасности продуктов питания и развития». Так ВОЗ охарактеризовала антибиотикорезистентность, которая приводит к более длительным срокам госпитализации, увеличению расходов на медицинское обслуживание и повышению уровня смертности. В качестве одного из потенциальных решений в исследовании предлагается трансплантация фекальной микробиоты (ТФМ), что позволяет надеяться на возможность борьбы с мультирезистентными бактериями, но оставляет открытым вопрос об их безопасности, особенно в отношении пациентов с ослабленным иммунитетом.
Проведено испытание на 10 пациентах с ослабленным иммунитетом
Одноцентровое исследование было основано на ретроспективном анализе историй болезни 10 пациентов с заболеваниями крови, которым проводилась трансплантация костного мозга и трансплантация (в данный период или ранее) энтеробактерий, продуцирующих карбапенемазу, или ванкомицин-резистентных бактерий. Последняя процедура была классифицирована как процедура с повышенным риском (риск появления бактерий с ШЛУ – широкой лекарственной устойчивостью). Пациенты готовились к аллогенной (когда донор и реципиент – разные люди) трансплантации гемопоэтических стволовых клеток (ТГСК). ТФМ проводилась с помощью клизмы или назогастрального зонда; для четырех пациентов она была проведена до ТГСК, для остальных шести пациентов (тех, кто во время процедуры получал иммунодепрессанты) – после нее.
Подтверждение эффективности
В 7 случаях из 10 исследователи наблюдали значительную деколонизацию бактерий с множественной лекарственной устойчивостью. У трех других бактериальных культур рост отсутствовал. У 6 из 10 пациентов деколонизация продолжалась в течение всего последующего периода (4–40 месяцев). Три случая отсутствия роста бактериальных культур можно объяснить методологическими затруднениями (прием антибиотиков нельзя было прекратить в течение 72 часов после ТФМ, период лечения был слишком коротким или объем образца кала был недостаточным для исследования и т. д.). В конце концов, после того как первая ТФМ не привела к эрадикации бактерий с множественной лекарственной устойчивостью, в двух случаях из трех удалось произвести вторую трансплантацию фекальной микробиоты, и она оказалась эффективной.
Подтверждение безопасности
У всех 10 пациентов ТФМ не была связана с каким-либо серьезным риском: у одного пациента в первые дни после трансплантации наблюдался запор; у двух других – незначительная, слабо выраженная диарея. Было зарегистрировано три смертельных случая, но, по утверждению исследователей, ни один из них не был связан с ТФМ. В двух случаях болезнь еще до трансплантации была прогрессирующей; в третьем случае пациент подвергся двум фекальным трансплантациям в связи с острой (sidenote: РТПХ РТПХ – реакция «трансплантат против хозяина» ) , вызванной трансплантацией гемопоэтических стволовых клеток, и лечение иммунодепрессантами привело к возникновению вирусной и грибковой инфекций в течение шести месяцев после ТФМ. Таким образом, для пациентов, инфицированных бактериями с множественной лекарственной устойчивостью, ТФМ, видимо, является эффективным и безопасным решением даже в случаях тяжелой иммуносупрессии.
Объясните пациентам, что такое трансплантация фекалий, с помощью этого специального материала: