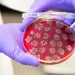
Что, если манипуляции с микробиотой смогут улучшить ответ на иммунотерапию?
Возможно, кишечная микробиота способна модулировать ответ на иммунотерапию. Хотя еще слишком рано предлагать разработанный на научной основе коктейль из пробиотиков, применение антибиотиков во время лечения должно быть более обоснованным.
Раздел для широкой публики
Найдите здесь свое выделенное место
en_sources_title
en_sources_text_start en_sources_text_end
Делиться - значит заботиться
Возможно, эта тема заинтересует ваших коллег. Почему бы не поделиться ею?
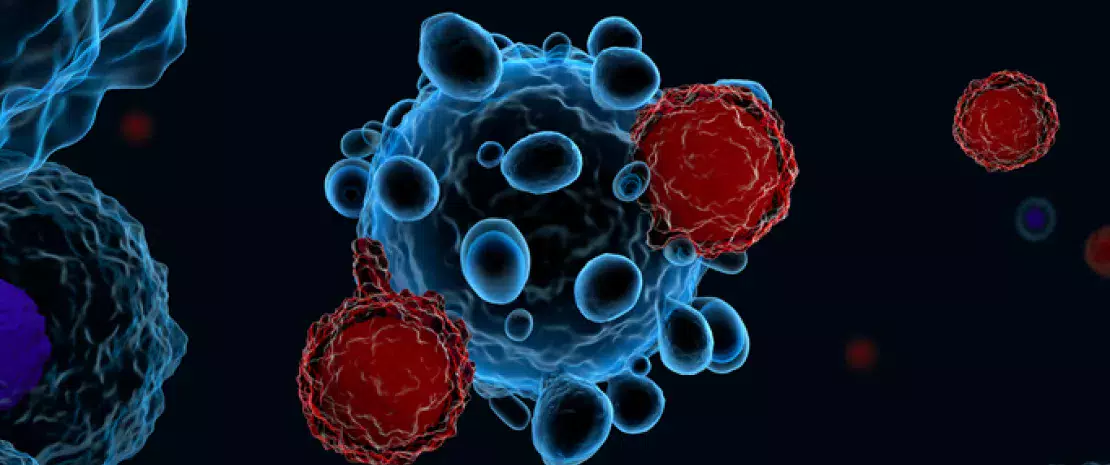
Об этой статье
Иммунотерапия CAR T-клетками, которая является более эффективной и менее токсичной, чем химиотерапия, становится предметом все большего числа клинических исследований. В рамках этого вида лечения Т-клетки подвергаются генетической модификации, при которой они получают химерный антигенный рецептор (Chimeric Antigen Receptor, CAR), позволяющий им распознавать и уничтожать исключительно опухолевые клетки. Несмотря на впечатляющие результаты у некоторых пациентов, клинический ответ на терапию CAR Т-клетками остается достаточно вариабельным.
Гипотеза авторов
В данном обзоре авторы предположили, что манипуляции с кишечной микробиотой могут улучшить ответ на терапию CAR Т-клетками, однако опубликованные результаты, подтверждающие эту гипотезу, в настоящее время отсутствуют. В единственном доступном одноцентровом обсервационном исследовании с участием 25 пациентов, получавших терапию CAR Т-клетками, было показано, что у пациентов, ответивших на лечение, состав микробиоты отличался от такового у не ответивших на лечение, что позволяет предположить возможную связь между кишечной микробиотой и ответом на терапию CAR Т-клетками. Тем не менее, в основу своей гипотезы авторы закладывают ряд аспектов: нарастающий объем данных доклинических и клинических исследований, проясняющих механизмы ускользания опухоли от иммунного ответа у пациентов, не отвечающих на терапию CAR Т-клетками, клинические данные об улучшении ответа на терапию ингибиторами контрольных точек иммунного ответа (ИКТ*) при манипуляциях с кишечной микробиотой (ее разнообразием и составом), а также общие иммунологические характеристики CAR Т-клеток и ИКТ.
Каковы практические рекомендации?
В случае, если ответ на терапию CAR Т-клетками связан с микробиотой, применение антибиотиков широкого спектра во время иммунотерапии может привести к дисбактериозу, ухудшению ответа на лечение и снижению выживаемости. Что касается пробиотиков, несмотря на то, что определенные группы бактерий могут улучшать ответ на иммунотерапию, результаты клинических исследований не всегда в достаточной степени согласуются, чтобы четко разделить таксоны на «благоприятные» и «неблагоприятные». Таким образом, «коктейль» из живых бактерий, приготовленный на основе научных данных, все еще не доступен. На данном этапе исследовательская группа рекомендует отказаться от применения доступных на рынке пробиотиков во время лечения злокачественных новообразований, поскольку они могут ослабить естественную кишечную микрофлору и теоретически сделать ее менее разнообразной. Аналогичным образом, группа рекомендует отказаться от необоснованного применения антибиотиков широкого спектра во время иммунотерапии и терапии CAR Т-клетками.
* для восстановления функционирования иммунной системы контрольные точки иммунного ответа, которые опухолевые клетки используют для защиты от воздействия иммунной системы, можно заблокировать с помощью терапии ИКТ.