Vías interconectadas relacionan los lípidos plasmáticos, la microbiota fecal y la actividad cerebral con la cognición asociada a la desnutrición infantil
ARTÍCULO COMENTADO - Niño
Por el Prof. Emmanuel Mas
Gastroenterología y nutrición, Hospital de Niños, Toulouse, Francia
Comentario del artículo de Portlock et al., Nat Commun 1
Espacio para el público general
Encuentra aquí tu espacio dedicado
en_sources_title
en_sources_text_start en_sources_text_end
Capítulos

Acerca de este artículo
La desnutrición afecta a más de 30 millones de niños cada año, con profundas repercusiones inmediatas y duraderas. Los niños que sobreviven suelen presentar secuelas neurocognitivas duraderas, que afectan al rendimiento escolar y su situación socioeconómica. Aún no se conocen bien los mecanismos que provocan estos efectos. Mediante modelos SHAP interpretados por análisis multisistémicos de bosques aleatorios y redes, los autores muestran que la desnutrición aguda moderada (DAM) se asocia a un aumento de la presencia de Rothia mucilaginosa y Streptococcus salivarius en las heces y a una disminución de Bacteroides fragilis en un grupo de niños de un año de Dacca, (Bangladés). Estas modificaciones del microbioma forman vías interconectadas que implican una reducción de los niveles plasmáticos de ácidos grasos de cadena impar, una reducción de la potencia de las onda gamma y beta del encefalograma en las regiones temporales y frontales del cerebro, y una reducción de la vocalización. Estos resultados confirman la hipótesis según la cual una colonización prolongada por especies comensales orales retrasa el desarrollo del microbioma intestinal y del cerebro. Aunque hay que confirmar los vínculos causales con datos empíricos, este estudio aporta información útil para mejorar las intervenciones dirigidas a los déficits del neurodesarrollo asociados a la DAM.
¿Qué se sabe ya sobre este tema?
La desnutrición infantil es un grave problema de salud pública y una de las principales causas de mortalidad antes de los cinco años de edad. La desnutrición aguda moderada (DAM) se asocia a un retraso del desarrollo neurocognitivo, pero aún se desconoce la relación. Se asocia también a una disbiosis de la microbiota intestinal (MI), cuyo desarrollo se ralentiza y está marcado por un enriquecimiento en especies de Bifidobacterium y Escherichia. Es posible que estas alteraciones de la MI repercutan en el desarrollo cerebral a través del eje intestino-cerebro, debido a una absorción defectuosa de nutrientes o a la acumulación de metabolitos tóxicos. En esta comunicación entre órganos podrían intervenir indirectamente los lípidos plasmáticos, ya que los lípidos son el constituyente esencial del cerebro y están modulados por metabolitos de la MI, como los ácidos biliares.
¿Cuáles son los principales resultados aportados por este estudio?
Este estudio se realizó en la región de Mirpur (Bangladés) y comparó a 159 niños con DAM con 75 testigos bien nutridos a la edad de 12 meses. La DAM se definió por una relación peso/altura entre - 2 y – 3 puntuaciones Z. El grupo DAM se asoció significativamente con factores sociodemográficos (tipo de parto, inodoros y agua tratada–hervidor).
La DAM se asoció con una disminución de la diversidad alfa bacteriana (Shannon), un aumento de la prevalencia y abundancia de Rothia mucilaginosa y Streptococcus salivarius (figura 1), y con un aumento de la relación Bacteroidetes/ Firmicutes. No se observaron diferencias en los análisis funcionales de la MI.
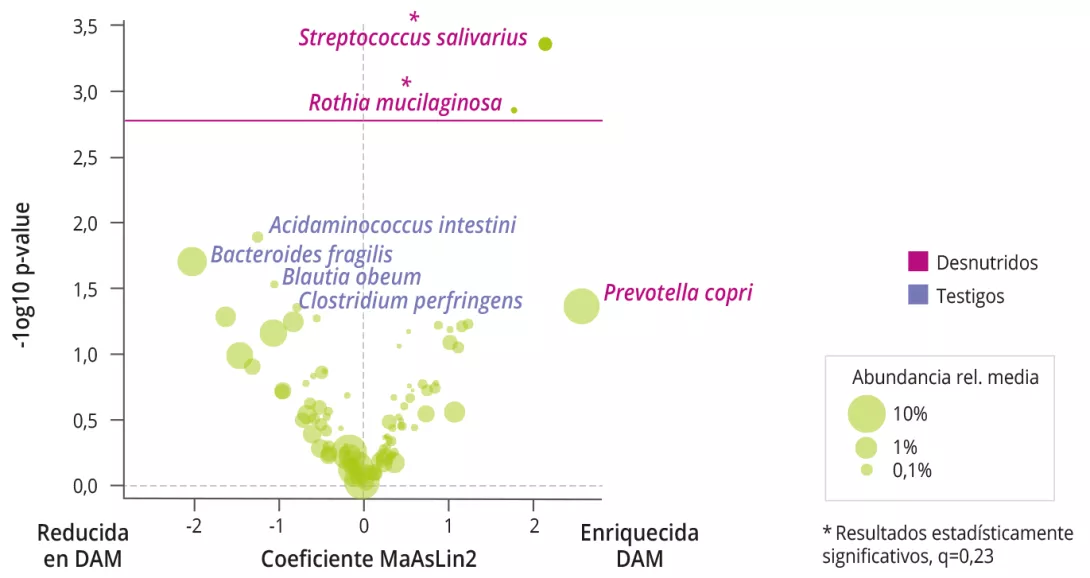
En el electroencefalograma (EEG) se observó una disminución significativa de las frecuencias beta (12-30 Hz) y gamma (30-45 Hz) en la región temporal y frontal en los niños con DAM. Además, se detectó una reducción significativa de las puntuaciones de comunicación expresiva, motricidad fina y gruesa y vocalización.
Después de ajustar por tipo de parto, sexo y duración de la lactancia materna exclusiva, la DAM se asoció con cambios en el lipidoma plasmático, con un aumento de la abundancia relativa de 128 (16 %) compuestos y una disminución de 189 (24 %) (figura 2).
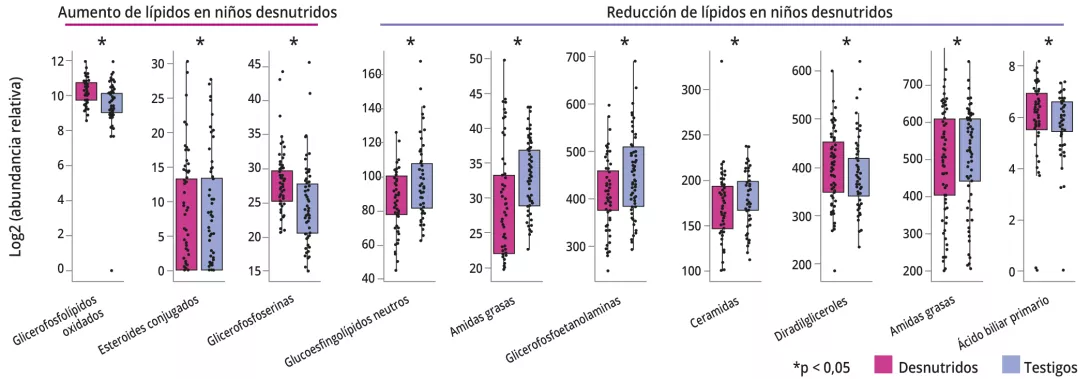
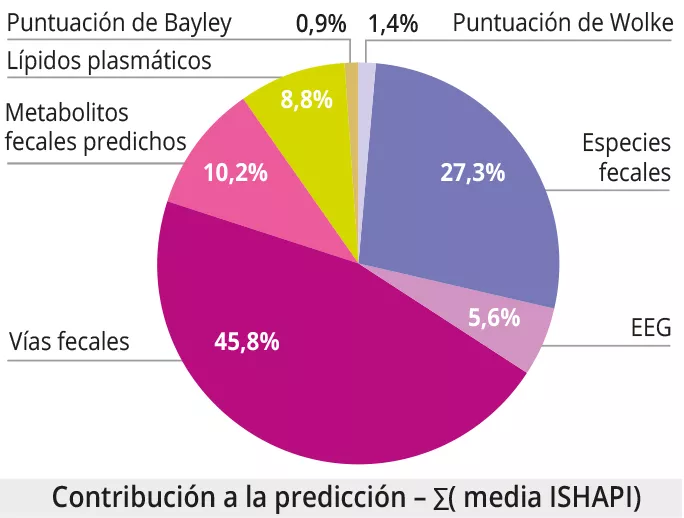
La integración de datos multimodales demostró que los mejores predictores de DAM a los 12 meses eran: 1) los lípidos plasmáticos (AUROC = 0,95 0,05); 2) las mediciones cerebrales y conductuales (puntuación de Wolke, EEG, puntuación de Bayley) (AUROC = 0,73 0,05, 0,71 0,10, 0,68 0,07 respectivamente); 3) el perfil taxonómico, funcional y de metabolitos predichos del microbioma fecal (AUROC = 0,56 0,07, 0,53 0,07, 0,52 0,06). Hay que señalar que el microbioma fecal desempeña una función importante en la predicción de la DAM en el análisis multimodal, a pesar de los malos resultados del microbioma fecal (figura 3).
El análisis de redes multimodales permitió predecir que una agrupación de B. fragilis, de vías de fermentación del piruvato, de ceramidas plasmáticas, de EEG y de comunicación expresiva estaba estrechamente correlacionada con un buen estado nutricional a los 12 meses. Por último, el efecto más fuerte como interacción entre especies se observó entre R. mucilaginosa y S. salivarius, cuya presencia combinada amplificó la predicción de DAM a los 12 meses.
¿Cuáles son las consecuencias en la práctica?
Este estudio demuestra la importancia de la MI en el estado nutricional del lactante. La presencia de bacterias orales grampositivas comensales y anaerobias facultativas como R. mucilaginosa y S. salivarius podría ser la causa de la desregulación de los ácidos biliares. Esto a su vez podría provocar modificaciones lipídicas, importantes para el desarrollo cerebral.
Además, es importante destacar el beneficio de B. fragilis en relación con las vías de fermentación sobre el estado nutricional a los 12 meses.
- La persistencia de las bacterias comensales Rothia mucilaginosa y Streptococcus salivarius en el intestino de los niños del grupo DAM reemplaza la colonización por Bacteroides fragilis. Esto interfiere en la síntesis de ácidos grasos, fundamentales para el desarrollo del cerebro
CONCLUSIÓN
Este estudio demuestra que la disbiosis de la microbiota intestinal se asocia con anomalías en el desarrollo cerebral de niños
con DAM, mediante modificaciones de los lípidos plasmáticos.

