Quand une dysbiose bactérienne signe les MICI
Les maladies inflammatoires chroniques intestinales (MICI) se caractérisent par une inflammation de la paroi du tube digestif, tout au long du tractus intestinal (maladie de Crohn, ou MC) ou localisée au niveau du rectum et du côlon (rectocolite hémorragique, ou RCH). Elles sont associées à des altérations de la biodiversité et de la composition des microbiotes bactériens, fongiques et viraux, suspectés de contribuer à leur pathogénèse et/ou à la progression de la maladie.
en_sources_title
en_sources_text_start en_sources_text_end
Chapitres
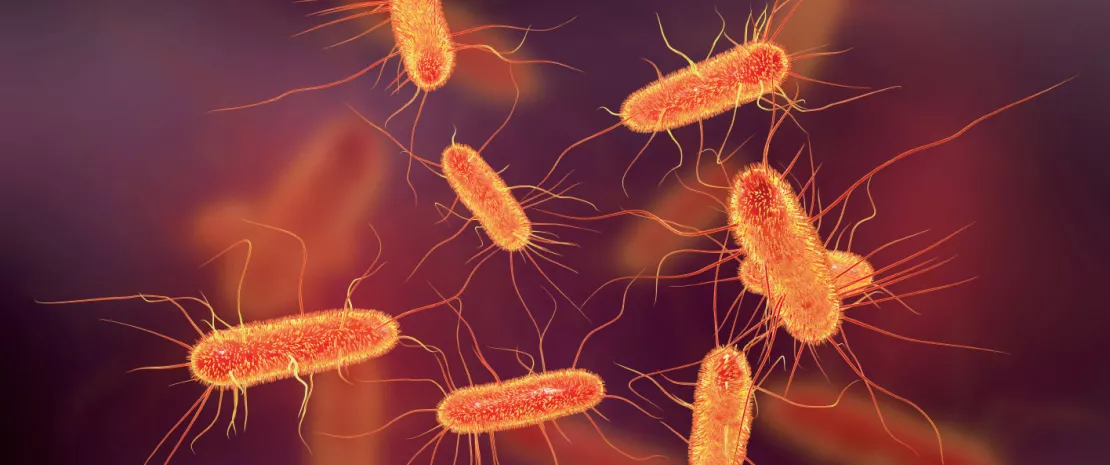
Escherichia coli
A propos de cet article
Une double dysbiose bactérienne intestinale, caractérisée par une réduction de certaines souches bénéfiques et une augmentation de souches pathogènes, est associée aux MICI. Ces anomalies de composition pourraient être à la fois la cause et la conséquence de ces pathologies, induisant un cercle vicieux
Chez les patients atteints de MICI, on observe des altérations structurelles et fonctionnelles du microbiote intestinal ; ces perturbations sont également complétées par une différence de composition chez les patients en phase aiguë, comparativement à ceux en rémission2.
Moins de bactéries bénéfiques, plus de pathogènes
Première caractéristique : une diminution du ratio Firmicutes/Bacteroidetes. Certaines bactéries bénéfiques appartenant au phylum des Firmicutes sont diminuées. Par exemple, on observe une moindre présence de Faecalibacterium prausnitzii, une bactérie commensale aux propriétés anti-inflammatoires et dont la réduction semble signer la MC3 ; par ailleurs, des proportions réduites de Firmicutes, communément observées chez les patients souffrant de MICI , ou encore une abondance nettement réduite de Bacteroides fragilis (Bacteroidetes), une bactérie ayant montré ses effets protecteurs dans des modèles murins de colite induite5. Chez les patients MICI en phase aiguë, on observe également une moindre abondance de Clostridium coccoides, Clostridium leptum, Faecalibacterium prausnitzii et Bifidobacterium2. Seconde caractéristique : un excès de micro-organismes potentiellement délétères, notamment des espèces appartenant aux gammaprotéobactéries et aux actinobactéries. Chez un patient sur trois souffrant de MC, la muqueuse est ainsi envahie par une souche d’Escherichia coli nommée AIEC (pour Adherent-invasive Escherichia coli)3. Or, à la différence d’autres agents infectieux, ces souches parviennent à traverser la barrière formée par le mucus intestinal, y adhèrent, envahissent les cellules épithéliales intestinales, survivent et se répliquent parmi les macrophages, provoquant la sécrétion de grandes quantités de TNFα, ce qui déclenche l’inflammation.
La dysbiose, cause et conséquence des MICI ?
Cette dysbiose intestinale bactérienne, qui semble signer les MICI, est suspectée de participer à leur pathogenèse. Une étude menée chez des souris prédisposées génétiquement à la RCH a mis en évidence une relation bidirectionnelle entre cette maladie et la dysbiose intestinale6. La dysbiose bactérienne pourrait donc, non seulement contribuer à l’apparition de la MICI, mais aussi constituer une conséquence secondaire de l’inflammation de l’intestin. Différentes pistes sont évoquées pour expliquer ce double phénomène : certaines espèces appartenant au phylum des Firmicutes possèdent des propriétés anti-inflammatoires, et sont également d’importantes productrices d’acides gras à chaîne courte (AGCC) (butyrate notamment), qui représentent le principal substrat énergétique des colonocytes. Aussi, une réduction du nombre de Firmicutes pourrait provoquer ou intensifier une inflammation locale en diminuant les taux de cytokines anti-inflammatoires (important régulateur de l’immunité des muqueuses) et/ ou en altérant la fonction barrière du côlon induite par un déficit en AGCC4.