Дитячі кольки
"Плач моєї новонародженої дитини - самий несамовитий звук, який я коли-небудь чула".1 Отже, багато батьків, які виявляються безпорадними в кабінеті свого педіатра, не в силі заспокоїти незрозумілі крики своєї дитини. Симптоми часто важко виявити, і вони можуть стати важким випробуванням для батьків, тому важливо знати, як їх розпізнати і зрозуміти. Чи прихована відповідь на це питання у складі мікробіоти кишківника новонародженого?
Мікробіота кишківника
Що таке дитячі кольки?
Дитяча колька характеризується надмірним плачем з невідомих причин у здорових немовлят. Причиною таких розладів є незрілість шлунково-кишкового тракту, алергія або непереносимість коров'ячого молока, шлунковий рефлюкс,2,3 але також вивчалися й інші причини, не пов'язані з шлунково-кишковою системою,2,3 такі як батьківський стрес,4 або куріння матері.2.
Кольки часто зустрічаються у немовлят, але їх симптоми, такі як постійний плач, можуть викликати занепокоєння у батьків.
Чи ви знали?
Слово "колька" походить з грецької - "κoλικóς" (колікос), що відноситься до товстої кишки. Однак, незважаючи на роки досліджень, причина дитячих кольок залишається невідомою, тому немає достовірної інформації щодо участі в цьому кишківника (товстого кишківника)5.
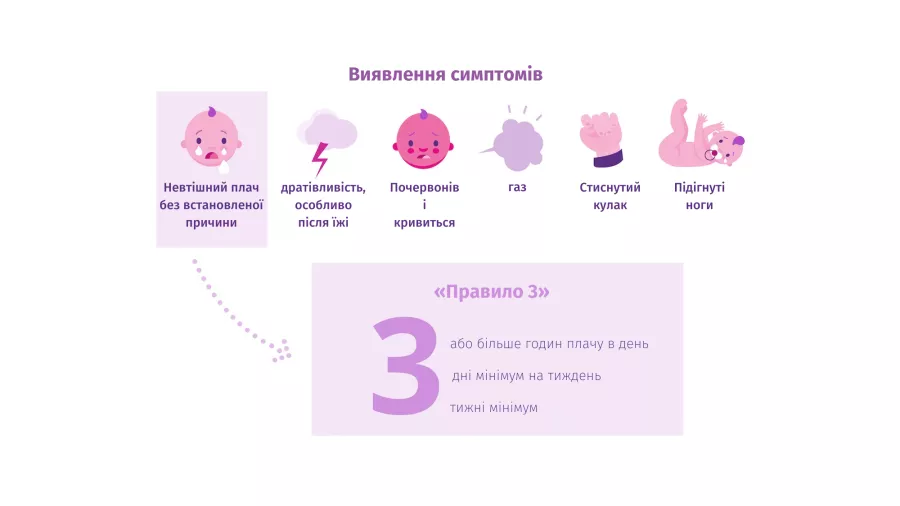
Які симптоми дитячих кольок?
Дитина багато плаче, капризує, лаштує гримаси, стискає кулаки - ймовірно, це кишкові гази.5 Педіатри вже давно використовують "правило трьох" для діагностики дитячих кольок.6 Саме ці критерії були введені у 1954 році та були адаптовані міжнародною організацією як: повторювані і тривалі періоди занепокоєння; плач або дратівливість без очевидної причини, такої як затримка росту, лихоманка або погане самопочуття, яка не може бути усунуте особами, які здійснюють догляд за малюком.7
Яка роль кишкової мікробіоти?
Нещодавно було встановлено зв'язок між дитячими кольками і кишковою мікробіотою, також відомої як кишкова флора.8 Декілька досліджень показали, що мікробіота кишківника немовлят, які страждають на кольки, відрізняється від мікробіоти інших дітей:9
- їх мікробіота менш багата корисними бактеріями, особливо
(sidenote:
біфідобактеріями
Рід Y-подібних бактерій, більшість видів яких корисні для людини. Вони містяться в кишечнику людини, а також у деяких йогуртах.
Вони:
- Захищають кишковий бар'єр
- Беруть участь у розвитку імунної системи та допомагають боротися із запаленням
- Сприяють травленню та покращують симптоми шлунково-кишкових розладів Sung V, D'Amico F, Cabana MD, et al. Lactobacillus reuteri to Treat Infant Colic: A Meta-analysis. Pediatrics. 2018 Jan;141(1):e20171811. O'Callaghan A, van Sinderen D. Bifidobacteria and Their Role as Members of the Human Gut Microbiota. Front Microbiol. 2016 Jun 15;7:925. Ruiz L, Delgado S, Ruas-Madiedo P, et al. Bifidobacteria and Their Molecular Communication with the Immune System. Front Microbiol. 2017 Dec 4;8:2345. ) та (sidenote: лактобактерій Паличкоподібні бактерії, основною характеристикою яких є вироблення молочної кислоти, звідки вони і отримали назву "молочнокислі бактерії". Лактобактерії присутні в мікробіоті ротової порожнини, піхви та кишечника людини, а також у рослин і тварин. Вони містяться у ферментованих продуктах, таких як молочні продукти (наприклад, деякі сири та йогурти), соління, квашена капуста тощо. Лактобактерії також містяться у пробіотиках, деякі види яких відомі своїми корисними властивостями. W. H. Holzapfel et B. J. Wood, The Genera of Lactic Acid Bacteria, 2, Springer-Verlag, 1st ed. 1995 (2012), 411 p. « The genus Lactobacillus par W. P. Hammes, R. F. Vogel Tannock GW. A special fondness for lactobacilli. Appl Environ Microbiol. 2004 Jun;70(6):3189-94. Smith TJ, Rigassio-Radler D, Denmark R, et al. Effect of Lactobacillus rhamnosus LGG® and Bifidobacterium animalis ssp. lactis BB-12® on health-related quality of life in college students affected by upper respiratory infections. Br J Nutr. 2013 Jun;109(11):1999-2007. ) ,8 які, насправді, формують імунні реакції захисту від кольок.5 - натомість їхня мікробіота, колонізована кишковою паличкою,5 клебсіеллою або іншими потенційно патогенними видами.5
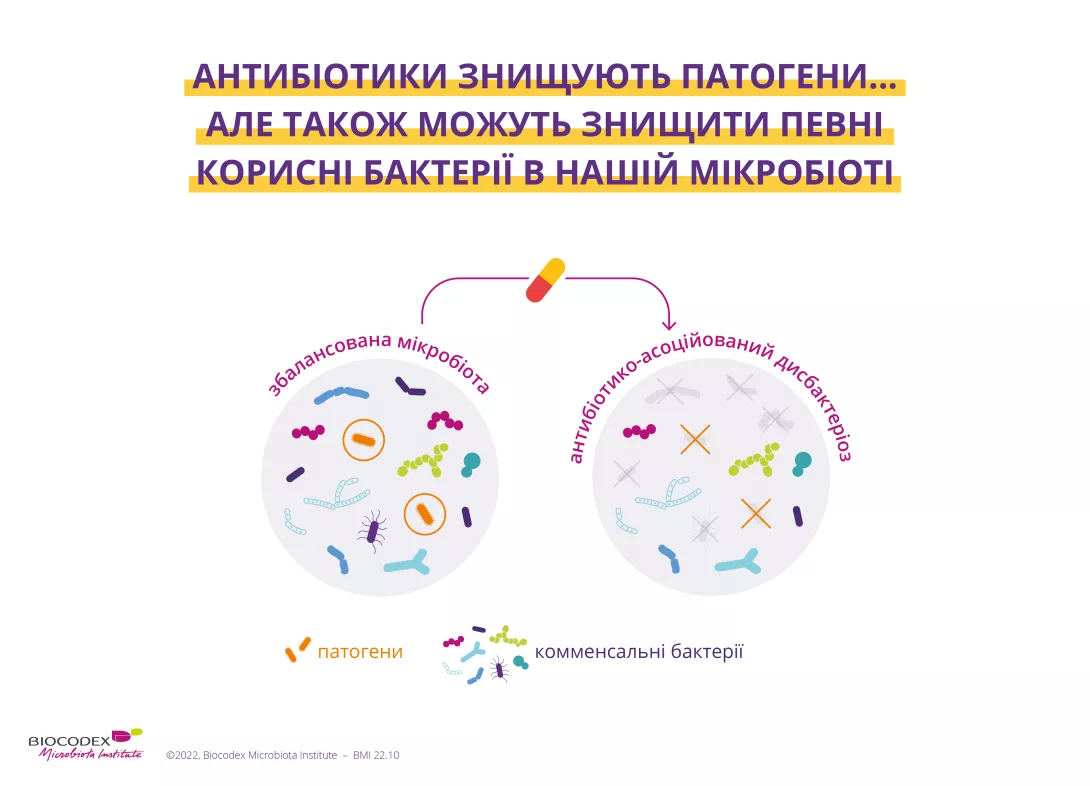
Цей дисбаланс кишкової мікробіоти, відомий як “
(sidenote:
Дисбіоз
Зазвичай визначається як зміна складу та функції мікробіоти, спричинена поєднанням факторів навколишнього середовища та індивідуальних особливостей людини.
Levy M, Kolodziejczyk AA, Thaiss CA, et al. Dysbiosis and the immune system. Nat Rev Immunol. 2017;17(4):219-232.
)
”, тісно пов'язаний з кольками. Згідно з однією з гіпотез - змінений склад кишкової мікробіоти змінює перистальтику кишківника (спосіб, яким їжа проходить через травну систему), що призводить до надмірного виділення газів.5
Запалення кишківника: слідкуйте за рівнем кальпротектина
Визначення рівня білку - кальпротектину може бути використане для виявлення запалення кишківника. Він міститься у великих кількостях у немовлят, які страждають коліками, і пов'язаний зі зниженням різноманітності кишкової мікробіоти.9
Як батьки можуть допомогти немовляті?
Сімейний лікар залишається першим пунктом призначення, який діагностує коліки у немовляти та може заспокоїти батьків.10 Ліків від кольок не існує, але кілька простих щоденних практик можуть допомогти полегшити симптоми. До них відносяться грудне вигодовування, виношування дитини і збалансування кишкової мікробіоти вашої дитини, особливо за допомогою пробіотиків.5 Пробіотики, мабуть, є перспективним напрямком, оскільки споживання "хороших" бактерій протягом декількох місяців може зменшити запалення кишківника,6 допомогти скоротити щоденну тривалість плачу.11 Оскільки вони допомагають підтримувати хороший кишковий баланс то пробіотики також можна використовувати в якості профілактичних засобів.5
Ця стаття заснована на науково підтверджених джерелах, але не є заміною медичної консультації. Якщо у вашої дитини проявляються симптоми, будь ласка, проконсультуйтеся з вашим сімейним лікарем чи педіатром.
1 Groopman J. The Colic Conundrum. The crying that doctors can’t stop. Annals of Medicine, Sept 17, 2007 Issue. https://www.newyorker.com/magazine/2007/09/17/the-colic-conundrum
3 Gupta SK. Is colic a gastrointestinal disorder? Curr Opin Pediatr. 2002 Oct;14(5):588-92.
8 Verduci E, Arrizza C, Riva E, et al. Microbiota and infantile colic: what’s new? Int J Probiotics Prebiotics. 2013; 8(1):25–28
15 Tannock GW. A special fondness for lactobacilli. Appl Environ Microbiol. 2004 Jun;70(6):3189-94.
BMI-21.18