Międzynarodowe Obserwatorium Mikrobioty: druga edycja
Rośnie poziom świadomości znaczenia mikrobioty dla zdrowia, ale przed nami jeszcze długa droga: główną rolę do odegrania w edukacji i informowaniu mają pracownicy opieki zdrowotnej!



Rośnie poziom świadomości znaczenia mikrobioty dla zdrowia, ale przed nami jeszcze długa droga: główną rolę do odegrania w edukacji i informowaniu mają pracownicy opieki zdrowotnej!

Mikrobiota składająca się z bilionów mikroorganizmów (bakterii, wirusów, grzybów itp.) występuje w naszych jelitach, na skórze, w jamie ustnej, nosie i płucach. Organizmy te odgrywają kluczową rolę w utrzymaniu dobrego samopoczucia, ułatwiając trawienie, stymulując nasz układ odpornościowy i chroniąc nas przed chorobami zakaźnymi. Jednak niezależnie od tych funkcji mikrobiota wpływa również na nasz nastrój, metabolizm, a nawet długowieczność. Zaburzenia tej delikatnej równowagi, często spowodowane czynnikami takimi jak dieta, styl życia czy przyjmowane leki, mogą prowadzić do poważnych chorób, począwszy od chorób układu pokarmowego, a skończywszy na zaburzeniach sercowo-naczyniowych i depresji. Z tego względu dbałość o prawidłową mikroflorę bakteryjną we wszystkich tych obszarach naszego ciała ma zasadnicze znaczenie dla ogólnego zdrowia i dobrego samopoczucia.
Drugi rok z rzędu instytut Biocodex Microbiota Institute zlecił firmie Ipsos przeprowadzenie dużego międzynarodowego badania dotyczącego mikrobioty: International Microbiota Observatory. Czy w tym roku wiedza społeczeństwa na temat mikrobioty jest większa? Czy poszerzyła się ich wiedza na temat jej roli i funkcji? Jaką rolę odgrywają obecnie pracownicy opieki zdrowotnej w przekazywaniu pacjentom informacji na temat mikrobioty?
Badanie zostało przeprowadzone przez Ipsos wśród 7500 osób w 11 krajach (Francja, Hiszpania, Portugalia, Polska, Finlandia, Maroko, Stany Zjednoczone, Brazylia, Meksyk, Chiny i Wietnam). W każdym kraju badana próba stanowiła reprezentatywną część populacji kraju w wieku 18 lat i wyższym pod względem płci, wieku, zawodu i regionu. Badanie zostało przeprowadzone przez Internet w okresie od 26 stycznia do 26 lutego 2024 r.
Biocodex Microbiota Institute to międzynarodowy ośrodek wiedzy zajmujący się ludzką mikrobiotą. Funkcjonujący w 7 językach instytut ma na celu zwiększenie świadomości zarówno pracowników opieki zdrowotnej, jak i ogółu społeczeństwa dotyczącej istotnej roli, jaką ten organ odgrywa w przypadku naszego zdrowia. Główną misją Biocodex Microbiota Institute jest edukacja: propagowanie znaczenia mikrobioty dla zdrowia każdego człowieka.
Olivier Valcke
kierownik ds. public relations i redakcji
+33 6 43 61 32 58
o.valcke@biocodex.com
Etienne Mercier
dyrektor działu opinii i zdrowia – Ipsos
+33 6 23 05 05 17
etienne.mercier@ipsos.com
Badanie wykazało, w jaki sposób niektóre bakterie pochwowe mogą wpływać na środowisko w obrębie szyjki macicy i pochwy oraz wywierać negatywny wpływ na rozrodczość. Ich narzędzie: pęcherzyki przenoszące białka.
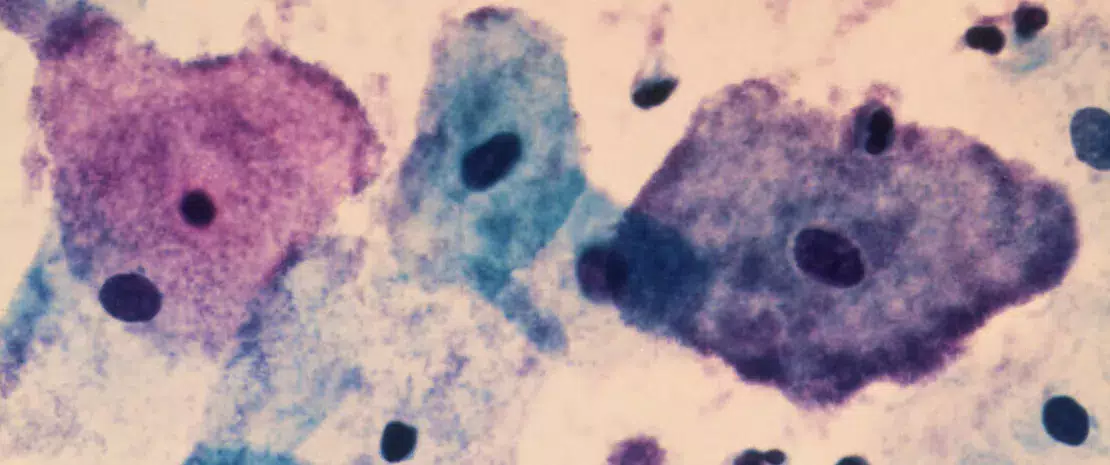
Cechą charakterystyczną mikrobioty pochwy jest fakt, że zachowuje ona równowagę, jeśli jest w dużej mierze zdominowana przez bakterie Lactobacillus crispatus. Z drugiej strony obecność bakterii beztlenowych, takich jak Gardnerella vaginalis i Mobiluncus mulieris, wiąże się ze zwiększonym ryzykiem infekcji przenoszonych drogą płciową, bakteryjnego zapalenia pochwy i przedwczesnego porodu. Mechanizmy te wciąż pozostają nie do końca wyjaśnione, choć w literaturze wspomina się o możliwej produkcji pęcherzyków zewnątrzkomórkowych przez niektóre bakterie. Czy ten mechanizm może występować w układzie rozrodczym? Tę hipotezę 1 wysunął i potwierdził zespół kierowany przez profesora Michala A. Elovitza z nowojorskiej uczelni Icahn School of Medicine at Mount Sinai 2 , który badał in vitro pęcherzyki zewnątrzkomórkowe wytwarzane przez dobroczynne bakterie L. crispatus oraz szkodliwe bakterie G. vaginalis i M. mulieris.
Wykorzystując mikroskopię elektronową do zaobserwowania rzeczywistej obecności pęcherzyków o średnicy od 90 do 420 nm w podłożu hodowlanym, zespół przeanalizował ich zawartość. Pęcherzyki wytwarzane przez bakterie G. vaginalis, M. mulieris i L. crispatus zawierały odpowiednio 491, 336 i 247 białek bakteryjnych. Niektóre z nich miały znaczenie funkcjonalne: ładunek G. vaginalis okazał się bogaty w waginolizynę, toksynę zdolną do wywoływania lizy komórek nabłonka szyjki macicy i pochwy, bardzo obecną w przypadkach bakteryjnego zapalenia pochwy; ładunek M. mulieris zawierał białka zdolne do stymulowania odpowiedzi immunologicznej, podczas gdy kilka białek w pęcherzykach L. crispatus chroni barierę nabłonkową.
Co więcej, te bakteryjne pęcherzyki ulegały szybkiej internalizacji (od 1 do 4 godzin) w komórkach nabłonka szyjki macicy i pochwy. Pozostało tylko określić zakres ich wpływu.
Wystawienie komórek nabłonka szyjki macicy i pochwy na działanie zawartości pęcherzyków bakteryjnych G. vaginalis i M. mulieris wywołało zależną od dawki odpowiedź immunologiczną. Reakcja komórek szyjki macicy okazała się silniejsza niż komórek pochwy. Z kolei bakterie L. crispatus nie wywoływały znaczącej nadekspresji cytokin.
Tak więc komórki nabłonka szyjki macicy i pochwy wykazują reakcję multicytokinową po wystawieniu na działanie pęcherzyków bakterii G. vaginalis i M. mulieris, ale nie L. crispatus. W procesie odpowiedzi immunologicznej pośredniczą szlaki sygnałowe aktywowane przez (sidenote: Receptor TLR2 Receptor błony komórkowej toll-podobny (rozpoznawanie wzorców molekularnych), kodowany przez gen TLR2 i uczestniczący w rozpoznawaniu różnych patogenów, w tym bakterii, wirusów, grzybów i pasożytów. Źródło: Oliveira-Nascimento L, Massari P, Wetzler LM. The Role of TLR2 in Infection and Immunity. Front Immunol. 2012 Apr 18;3:79. ) .
Bakterie oddziałują zatem, zarówno w sposób szkodliwy, jak i korzystny, na zdrowie reprodukcyjne za pośrednictwem bakteryjnych pęcherzyków zewnątrzkomórkowych, które działają niczym kurierzy, zapewniając ochronę białek bakteryjnych podczas ich transportu, a następnie dostarczając je do komórek nabłonka i in fine, wywołując odpowiedź immunologiczną u gospodarza.
 Bakteryjne zapalenie pochwy: przenoszenie drogą płciową i spostrzeżenia dotyczące genomu
Bakteryjne zapalenie pochwy: przenoszenie drogą płciową i spostrzeżenia dotyczące genomu
 Zespół wstrząsu toksycznego: zrównoważona flora stanowi bufor przed atakami S. aureus
Zespół wstrząsu toksycznego: zrównoważona flora stanowi bufor przed atakami S. aureus
Przeprowadzone właśnie badanie wykazało, że skrobia oporna wywołuje zmiany w strukturze mikrobioty jelitowej, które sprzyjają utracie wagi i mają korzystny wpływ na zdrowie. Suplementacja dawką 40 g dziennie umożliwiła ochotnikom utratę prawie 3 kilogramów w ciągu 2 miesięcy – bez stosowania diety!
Mikrobiota jelit
To mogłoby być kolejne „wiosenne wydanie specjalne” magazynu dla kobiet wychwalające zalety najnowszej modnej diety… Jednak w tym przypadku chodzi o wyniki szczególnie wnikliwego badania opublikowanego w czasopiśmie Nature Metabolism 1 , które wzbudziło ogromne zainteresowanie i ukazało potencjalne korzyści płynące ze stosowania skrobi opornej w procesie odchudzania. Ze względu na modulowanie struktury naszej mikrobioty jelitowej błonnik ten – występujący w roślinach strączkowych, zbożach i zielonych bananach – może pomóc nam w zrzuceniu zbędnych kilogramów i poprawie naszego zdrowia. Przyjrzyjmy się bliżej wynikom badań…
Naukowcy przeprowadzili rekrutację 22 mężczyzn z nadwagą i 15 kobiet z nadwagą ( (sidenote: BMI Wskaźnik masy ciała ocenia tuszę jednostki na podstawie oceny masy tłuszczowej ciała obliczanej jako stosunek między wagą (kg) a kwadratem wzrostu (m2). https://www.nhlbi.nih.gov/health/educational/lose_wt/BMI/bmicalc.htm https://www.euro.who.int/en/health-topics/disease-prevention/nutrition/a-healthy-lifestyle/body-mass-index-bmi ) > 24) stosujących normalną zbilansowaną dietę (nie niskokaloryczną), a następnie podawali im skrobię oporną lub „normalną” skrobię placebo (patrz ramka). Dokonano pomiaru zmian w ich BMI, mikrobiocie jelitowej i różnych parametrach metabolicznych.
Uzyskane wyniki wykazały, że spożywanie 40 g skrobi dziennie przez 2 miesiące wiąże się ze średnim spadkiem masy ciała o 2,8 kg, a w szczególności z:
Żadnego z tych efektów nie stwierdzono w przypadku skrobi placebo.
Badanie to ma charakter „randomizowanej, podwójnie ślepej, kontrolowanej placebo próby krzyżowej” – jednej z najbardziej rygorystycznych metod naukowych stosowanych w badaniach medycznych. Uczestnicy zostali losowo podzieleni na dwie grupy:
Aby wykluczyć jakikolwiek czynnik ludzki, który mógłby wpłynąć na wyniki, ani badacze, ani uczestnicy nie znali rodzaju skrobi.
Analizy wskazują, że skrobia oporna doprowadziła do rzeczywistej przebudowy struktury mikrobioty jelitowej ochotników, ze wzrostem kilku szczepów bakterii, w szczególności Bifidobacterium adolescentis. Obliczenia naukowców pokazują, że obfitość Bifidobacterium adolescentis wykazuje silną korelację z redukcją BMI i trzewnej tkanki tłuszczowej.
Przenosząc mikrobiotę kałową ochotników, którzy spożywali oporną skrobię, do myszy (sidenote: Przeszczep mikrobioty jelitowej (FMT) Procedura terapeutyczna mająca na celu przywrócenie mikrobioty jelitowej poprzez przeniesienie bakterii kałowych od zdrowego dawcy do biorcy. Więcej informacji https://www.science.org/doi/10.1126/scitranslmed.abo2750 ) , naukowcy odkryli ten sam rodzaj wpływu na wagę i wrażliwość na insulinę. Te same efekty uzyskano poprzez suplementację myszy korzystnymi bakteriami zidentyfikowanymi jako B. adolescentis.
Wzmacnia to hipotezę, że zmiany wywołane przez skrobię oporną w mikrobiocie jelitowej odpowiadają za jej korzystne działanie.
Skrobia to forma, w jakiej rośliny (ryż, ziemniaki, pszenica, kukurydza itp.) przechowują węglowodany. Skrobia oporna to rodzaj skrobi, który nie ulega rozkładowi przez nasze enzymy trawienne i dlatego dociera do jelita grubego w stanie nienaruszonym. Jest ona fermentowana przez bakterie mikrobioty, które z kolei uwalniają różne korzystne substancje, w szczególności krótkołańcuchowe kwasy tłuszczowe
(sidenote:
Krótkołańcuchowe kwasy tłuszczowe
Krótkołańcuchowe kwasy tłuszczowe są źródłem energii (paliwa) dla komórek organizmu, współdziałają z układem odpornościowym i biorą udział w komunikacji między jelitami a mózgiem.
Silva YP, Bernardi A, Frozza RL. The Role of Short-Chain Fatty Acids From Gut Microbiota in Gut-Brain Communication. Front Endocrinol (Lausanne). 2020;11:25.
)
. 2 Owies, ryż, sorgo, jęczmień, fasola i rośliny strączkowe, a także zielone banany dostarczają dużych ilości błonnika i skrobi opornej. 3
Gotowanie zmniejsza zawartość skrobi opornej w żywności, ale chłodzenie (na przykład ryżu lub sałatki ziemniaczanej) pomaga ją przywrócić. 2
Zmiany w mikrobiocie jelitowej umożliwiły:
Powyższe wyniki wymagają potwierdzenia w większym badaniu. Sugerują one jednak, że zwiększenie zawartości skrobi opornej w diecie jest prostą, ale skuteczną strategią odchudzania… lub unikania przybierania na wadze po zakończeniu diety!
 Analiza trendów dotyczących zdrowia jelit w mediach społecznościowych
Analiza trendów dotyczących zdrowia jelit w mediach społecznościowych
Nazwa brzmi barbarzyńsko, ale to zaburzenie trawienne objawiające się bólem i/lub dyskomfortem skoncentrowanym w żołądku jest powszechne. Jak się go pozbyć? Modulacja mikrobioty jelitowej probiotykami wydaje się rozwiązaniem zarówno skutecznym, jak i interesującym.
Mikrobiota jelit
Dyspepsja (niestrawność) czynnościowa: barbarzyńska nazwa choroby, którą z pewnością znasz, bo dotyka praktycznie jedną osobę na dziesięć, zwłaszcza kobiety, palaczy i osoby przyjmujące niesterydowe leki przeciwzapalne (ibuprofen, ketoprofen). Niestrawność czynnościowa to częsty problem trawienny charakteryzujący się bólem lub przewlekłym dyskomfortem w okolicy żołądka.
Jej objawy są opisywane zazwyczaj jako nieprzyjemne uczucie pełności w żołądku po posiłku (który wcale nie był tak ogromny jak dla pułku wojska!), wrażenie sytości w chwilę po rozpoczęciu jedzenia lub bóle i/lub pieczenie w dołku. I tak od tygodni.
250-400 m2 ludzki układ pokarmowy jest ma największą w całym organizmie powierzchnię wymiany.
98% Proteobakterie, Firmicutes, Actinobacterie i Bacteroidetes stanowią u zdrowych osób ponad 98% mikrobioty jelitowej.
Wprawdzie przyczyny – liczne – i mechanizmy niestrawności czynnościowej są jeszcze słabo znane, ale na cenzurowanym znalazła się mikrobiota jelitowa Przede wszystkim zaś bakteria Helicobacter pylori, która czasem rozgaszcza się w żołądku. Wydaje się, że w dużym stopniu przyczynia się do rozwoju niestrawności czynnościowej, niewątpliwie poprzez zapalenie błony śluzowej układu pokarmowego oraz zaburzenia ruchu jelit.
40% Ponad 40% chorych na świecie cierpi z powodu czynnościowych zaburzeń układu pokarmowego. Niestrawność czynnościowa jest jednym z najczęstszych.
3–5% Niestrawność czynnościowa jest powodem od 3 à 5% wizyt u lekarzy podstawowej opieki zdrowotnej.
Mówiąc bardziej ogólnie, udział w tym zaburzeniu ma cała mikrobiota jelitowa. Jest to udział bezpośredni (zaburzenie równowagi składu i obfitości może pociągać za sobą nieprawidłowe funkcjonowanie jelit) i za pośrednictwem wytwarzanych przez bakterie metabolitów działających ochronnie (na przykład (sidenote: Krótkołańcuchowe kwasy tłuszczowe Krótkołańcuchowe kwasy tłuszczowe są źródłem energii (paliwa) dla komórek organizmu, współdziałają z układem odpornościowym i biorą udział w komunikacji między jelitami a mózgiem. Silva YP, Bernardi A, Frozza RL. The Role of Short-Chain Fatty Acids From Gut Microbiota in Gut-Brain Communication. Front Endocrinol (Lausanne). 2020;11:25. ) przez Firmicutes) lub szkodliwie (prozapalne sfingolipidy wytwarzane przez Bacteroidetes i Prevotellaceae) dla gospodarza.
2/3 osób dotkniętych niestrawnością czynnościową dotykają trwałe i nieregularnie występujące objawy, które mogą wpłynąć na jakość ich życia, a nawet na dobrostan psychiczny.
8 razy Osoby dotknięte niestrawnością czynnościową są około 8 razy bardziej narażone na zespół jelita drażliwego niż ogół populacji.
Bezpośrednia konsekwencja udziału mikrobioty żołądkowo-jelitowej w niestrawności czynnościowej: poszukiwanie rozwiązań, które uzdrowią tę mikrobiotę, a tym samym jej gospodarza (czyli pacjenta). Badacze przeprowadzili 1 na pacjentach kilka badań, z których wynikałoby, że probiotyki mogą w dużym stopniu złagodzić objawy, poprzez przywrócenie równowagi mikrobioty jelitowej.
Jest też inne, nieco bardziej agresywne podejście: antybiotyki o szerokim spektrum działania, eliminujące niepożądane bakterie. Takie odkurzanie jest bardzo skuteczne, zwłaszcza w przypadku kobiet, ale powoduje dużo szkód ubocznych wśród pożytecznych bakterii. Dlatego potrzebne są kolejne badania, których celem będzie lepsze poznanie mechanizmów tego zaburzenia, aby zaproponować precyzyjne, skuteczne metody diagnostyki i leczenia.
Niestrawność czynnościowa – bardzo częsty powód wizyt u lekarza – często jest leczona antybiotykami. Niedawny artykuł wskazuje na możliwość stosowania mniej agresywnego rozwiązania: modulacji mikrobioty.
Uczucie ciężkości w żołądku po posiłku, zbyt szybkie uczucie sytości podczas jedzenia i pieczenie w nadbrzuszu to tylko niektóre utrudniające życie objawy dyspepsji czynnościowej – częstego zaburzenia trawiennego, które jest powodem wielu wizyt u lekarza. Należy stwierdzić, że jest to częsty problem. Szacuje się, że dotyka 7,2% ludności świata. Kobiety, palacze i chorzy przyjmujący niesterydowe leki przeciwzapalne są szczególnie narażeni. A mikrobiota jelitowa może mieć na ten problem wpływ.
250-400 m2 ludzki układ pokarmowy jest ma największą w całym organizmie powierzchnię wymiany.
98% Proteobakterie, Firmicutes, Actinobacterie i Bacteroidetes stanowią u zdrowych osób ponad 98% mikrobioty jelitowej.
Przewód pokarmowy jest siedliskiem mikrobioty, której obfitość rośnie w miarę przechodzenia od żołądka (który nie jest sterylny) do jelita grubego. Proteobacterie, Firmicutes, Promieniowce i Bacteroidetes stanowią u zdrowych osób ponad 98% mikrobioty jelitowej. Mikroorganizmy te mają wielkie znaczenie dla zdrowia układu pokarmowego: chronią integralność bariery jelitowej, regulują układ odpornościowy błony śluzowej itp.
Zdarza się, że równowaga tej społeczności zostaje zaburzona, co powoduje dysbiozę: obecność Helicobacter pylori w żołądku prawdopodobnie ma związek z rozwojem niestrawności czynnościowej. Wygląda też na to, że dysbioza dwunastnicy (wzrost liczby Steptococcus, Firmicutes, Bacteroides, Proteobacterii i spadek rodzajów Prevotella, Veillonella, Leptotrichia, Actinomyces, Neisseria, Porphyromonas) jest skorelowana z niestrawnością czynnościową.
40% Ponad 40% chorych na świecie cierpi z powodu czynnościowych zaburzeń układu pokarmowego. Niestrawność czynnościowa jest jednym z najczęstszych.
3-5% Niestrawność czynnościowa jest powodem od 3 à 5% wizyt u lekarzy podstawowej opieki zdrowotnej.
Mikrobiota jelitowa prawdopodobnie ma w niej udział na dwa sposoby: bezpośrednio (zaburzenie równowagi składu i obfitości może pociągać za sobą nieprawidłowe funkcjonowanie jelit) i za pośrednictwem wytwarzanych przez bakterie metabolitów działających korzystnie (jak na przykład krótkołańcuchowe kwasy tłuszczowe wytwarzane przez Firmicutes) lub szkodliwie (prozapalne sfingolipidy wytwarzane przez Bacteroidetes i Prevotellaceae) dla gospodarza.
2/3 2/3 osób dotkniętych niestrawnością czynnościową dotykają trwałe i nieregularnie występujące objawy, które mogą wpłynąć na jakość ich życia, a nawet na dobrostan psychiczny.
8 razy Osoby dotknięte niestrawnością czynnościową są około 8 razy bardziej narażone na zespół jelita drażliwego niż ogół populacji.
Modulacja mikrobioty jelitowej jest więc szeroko rozważanym podejściem terapeutycznym. Kilka badań klinicznych wykazuje jej potencjał: zestaw probiotycznych szczepów należących do niektórych gatunków rodzaju Bacillus (Bacillus coagulans, Bacillus clausii i Bacillus subtilis) łagodzi niektóre objawy (odbijanie, refluks, wzdęcia). To samo dotyczy probiotyku łączącego Bacillus coagulans MY01 i Bacillus subtilis. Jogurt wzbogacony probiotykiem (Lactobacillus gasseri) nie zmienia objawów zgłaszanych przez pacjentów, ale zmniejsza ich częstotliwość (17,3% w porównaniu do 35,2% w grupie, której podawano placebo).
Lepsze poznanie mechanizmów tego zjawiska pozwoliłoby zaproponować precyzyjniejsze metody diagnostyki i leczenia oparte przede wszystkim na mikrobiocie jelitowej, a przy tym równie skuteczne.
Biegunka infekcyjna jest powszechnym i często niepokojącym stanem, który może zakłócać życie. Klucz do zrozumienia i przezwyciężenia tego problemu może leżeć w twoim własnym ciele. Zagłęb się w naukę stojącą za biegunką wirusową, pasożytniczą, bakteryjną lub podróżną, badając, w jaki sposób inwazje patogenów mogą zakłócać delikatną równowagę mikroflory jelitowej, prowadząc do zaburzeń trawienia.
Mikrobiota jelit
Co najmniej trzy luźne lub płynne stolce dziennie – taka jest według WHO powszechnie przyjęta definicja biegunki. Należy pamiętać, że konieczne jest spełnienie obu kryteriów (częstotliwość + konsystencja): częste oddawanie uformowanych stolców (a zatem o normalnej konsystencji) nie jest biegunką, podobnie jak oddawanie miękkich stolców z normalną częstotliwością, jak to ma miejsce w przypadku dzieci karmionych piersią.
Chociaż „powszechna” w łagodnych postaciach, biegunka nie jest niczym błahym: w 2016 r.była odpowiedzialna za 1,6 miliona zgonów, głównie wśród dzieci niedożywionych lub z obniżoną odpornością lub osób zakażonych HIV.1 Główną przyczyną tych zgonów było poważne odwodnienie związane z utratą płynów podczas powtarzających się wypróżnień.
Większość przypadków ostrej biegunki jest spowodowana zakażeniem drobnoustrojami chorobotwórczymi, które mogą być wirusami, bakteriami lub pasożytami. 1-3
„Choroby biegunkowe pozostają trzecią główną przyczyną zgonów dzieci w wieku poniżej pięciu lat” 1
Biegunka zakaźna może być wywoływana przez bakterie (biegunka bakteryjna), pasożyty (biegunka pasożytnicza) lub wirusy (biegunka wirusowa). Istnieje pięć głównych wirusów odpowiedzialnych za biegunkę wirusową, z których najczęstszy jest rotawirus będący główną przyczyną zgonów związanych z biegunką u dzieci w wieku poniżej pięciu lat. Dzieje się tak, chociaż niemowlęta są szczepione przeciwko temu podstępnemu wirusowi od 2006 roku. W rzeczywistości szczepienia są mniej skuteczne w krajach o niskich dochodach, prawdopodobnie ze względu na skład mikrobioty jelitowej.
Mikrobiota jelit Biegunka podróżnych Biegunka poantybiotykowa
Biegunka występuje, gdy w ciągu dnia oddawane są co najmniej trzy luźne lub płynne stolce. Biegunka zakaźna występuje, gdy jest wywołana zakażeniem czynnikiem chorobotwórczym (wirusem, bakterią lub pasożytem). 1-3 Jeśli patogenem jest wirus, biegunkę określa się jako „wirusową”.
Chociaż istnieje kilka niezakaźnych przypadków biegunki (np. w przypadku chorób układu trawiennego, takich jak choroba Leśniowskiego-Crohna), zdecydowaną większość wywołują patogeny. W zależności od danego patogenu wyróżniamy następujące rodzaje biegunek:
Co więcej biegunka może być również częstym skutkiem ubocznym (do 35% pacjentów) 4,5 leczenia antybiotykami. Takie zaburzenie jest określane jako biegunka związana z antybiotykami
Podczas gdy rotawirus jest najbardziej śmiercionośny (szacuje się, że w 2016 r. odnotowano 210 000 zgonów wśród dzieci w wieku poniżej pięciu lat), nie jest on jedynym wirusem odpowiedzialnym za ostrą biegunkę, a nawet śmierć: adenowirusy, norowirusy, sapowirusy i astrowirusy zabijają od 17 000 do 37 000 małych dzieci rocznie. 6
Uwaga: uważa się, że SARS-Cov-2, nazwa kodowa wirusa odpowiedzialnego za pandemię COVID-19, również powoduje biegunkę, której częstotliwość jest trudna do określenia ilościowego, a liczby różnią się znacznie w zależności od badania – niektórzy badacze zgłaszają takie epizody w 2% przypadków, inni w 50%! 7
W przypadku biegunki wirusowej, podobnie jak biegunki zakaźnej, wszystko zaczyna się od konfrontacji między patogenem (w tym przypadku wirusem) a żywicielem. Wynik tego spotkania zależy od złożonej równowagi, która w dużej mierze obejmuje mikrobiotę jelitową: na przykład wydaje się, że niektóre bakterie występujące u myszy mogą być zdolne do zapobiegania infekcji rotawirusowej, a nawet jej leczenia. 8 Tak więc ten sam wirus będzie miał różny wpływ w zależności od stanu mikrobioty jelitowej osoby, którą zainfekował. Mniej zróżnicowana mikrobiota jest bardziej wrażliwa. 12
Kiedy wirus wygrywa bitwę, proces jest zawsze taki sam: infekuje komórki wyściełające jelito cienkie i powoduje zmiany, które zakłócają wchłanianie płynów. 9 Rezultatem jest bardzo wodnista biegunka (bez krwi), której mogą towarzyszyć inne objawy (wymioty, nudności, skurcze brzucha i gorączka). 10 To słynne wirusowe zapalenie żołądka i jelit, które powraca każdej zimy. Jest to szczególnie poważne w przypadku zakażenia rotawirusem, które powoduje bardziej wyraźne objawy i któremu na ogół towarzyszy dysbioza mikrobioty jelitowej, wywróconej do góry nogami przez inwazję wirusów. 11,12
Biorąc pod uwagę, jak niebezpieczny jest rotawirus dla wrażliwych osób, opracowano szczepionki zapobiegawcze w celu zmniejszenia śmiertelności wśród małych dzieci – szacuje się, że szczepienie niemowląt przeciwko rotawirusowi zapobiegnie 139 000 zgonów wśród dzieci w wieku poniżej pięciu lat w latach 2006–2019. Jest to zarówno dużo, jak i mało w porównaniu z nadziejami, jakie pokłada się w szczepieniach – skuteczność szczepionki wydaje się być niższa w krajach o niskich i średnich dochodach (które paradoksalnie są najbardziej dotknięte).
Jednym z czynników mogących tłumaczyć tę niższą skuteczność jest skład mikrobioty, który wpływa na odpowiedź immunologiczną na szczepienie jelitowe. 13-16 Oprócz tego środka zapobiegawczego istnieją oczywiście te same porady dotyczące higieny i zachowywania odpowiedniej odległości od innych, które mają zastosowanie do wszystkich biegunek zakaźnych.
Zapobieganie biegunce zakaźnej, spowodowanej przez bakterie, wirusy lub pasożyty, jest przede wszystkim kwestią higieny:
Ponieważ za dużą część tych infekcji odpowiada zanieczyszczenie wody fekaliami, biegunka zakaźna występuje częściej tam, gdzie brakuje czystej wody (kraje o niskich dochodach, prowizoryczne obozowiska, tymczasowe obozy po trzęsieniach ziemi itp.).
Bardzo powszechna i na ogół niegroźna biegunka wirusowa może jednak prowadzić do poważnego odwodnienia u najbardziej narażonych osób (niemowląt, niedożywionych dzieci, dorosłych z obniżoną odpornością, osób starszych). Leczenie opiera się na nawadnianiu i uzupełnianiu elektrolitów (w celu zastąpienia utraconych jonów sodu, potasu i chlorku), na przykład:
Pracownicy służby zdrowia mogą zalecać określone szczepy probiotyczne w leczeniu ostrego zapalenia żołądka i jelit u dzieci: te dobroczynne bakterie skracają czas trwania biegunki lub długość hospitalizacji, lub zmniejszają objętość stolca (ESPGHAN 2023).
Tak jak nie użylibyśmy łapki na muchy, by pozbyć się myszy, ani łapki na myszy, by złapać muchę, tak antybiotyki w walce z wirusami są bezużyteczne. Wynika to z tego, że antybiotyki zabijają bakterie, a nie… wirusy. Co gorsza, w niektórych przypadkach efektem ubocznym antybiotyków jest biegunka – co, szczerze mówiąc, nie byłoby pożądane u pacjenta już cierpiącego na biegunkę wirusową!
 Biegunka pasożytnicza: czy mikrobiota jest kluczowym czynnikiem wpływającym na rokowanie?
Biegunka pasożytnicza: czy mikrobiota jest kluczowym czynnikiem wpływającym na rokowanie?
 Biegunka bakteryjna: jedyny przypadek, w którym antybiotyki mogą być konieczne
Biegunka bakteryjna: jedyny przypadek, w którym antybiotyki mogą być konieczne
Biegunka zakaźna może być wywoływana przez bakterie (biegunka bakteryjna), pasożyty (biegunka pasożytnicza) lub wirusy (biegunka wirusowa). Biegunka pasożytnicza może być spowodowana przez małe mikroorganizmy, takie jak Giardia intestinalis (odpowiedzialna za giardiozę) lub Entamoeba histolytica (wywołująca przerażającą amebozę), lub robaki, z których najbardziej znany jest niewątpliwie Ascaris lumbricoides. Nie wszyscy reagują w ten sam sposób na infekcję pasożytniczą: podczas gdy u większości z nas nie występują najmniejsze objawy, inni cierpią na biegunkę, która może być ciężka, a nawet śmiertelna. Mikrobiota jelitowa jest coraz częściej wymieniana jako kluczowy czynnik wyjaśniający tę zmienność.
Mikrobiota jelit Biegunka podróżnych Biegunka poantybiotykowa
Biegunka występuje, gdy w ciągu dnia oddawane są co najmniej trzy luźne lub płynne stolce. Biegunka zakaźna występuje, gdy jest wywołana zakażeniem czynnikiem chorobotwórczym (wirusem, bakterią lub pasożytem). 1-3 Jeśli patogenem jest pasożyt, biegunkę określa się jako „pasożytniczą”.
Chociaż istnieje kilka niezakaźnych przypadków biegunki (np. w przypadku chorób układu trawiennego, takich jak choroba Leśniowskiego-Crohna), zdecydowaną większość wywołują patogeny. W zależności od danego patogenu wyróżniamy następujące rodzaje biegunek:
Co więcej biegunka może być również częstym skutkiem ubocznym (do 35% pacjentów4,5) leczenia antybiotykami. Takie zaburzenie jest określane jako biegunka związana z antybiotykami.
Pasożyty jelitowe można podzielić na dwie szerokie kategorie : 6-8
Zakażenia tymi dwoma rodzajami pasożytów są powszechne: uważa się, że 350 milionów ludzi jest zarażonych trzema najpowszechniej występującymi pierwotniakami, a 895 milionów helmintami przenoszonymi przez glebę. Globalizacja żywności, podróże międzynarodowe i fale migracji sprawiły, że na Zachodzie częstsze są infekcje wywołane przez pierwotniaki niż przez robaki. 6
W przypadku biegunki pasożytniczej, podobnie jak biegunki zakaźnej, wszystko zaczyna się od konfrontacji między patogenem (w tym przypadku pasożytem), zwykle przenoszonym przez skażoną żywność lub zanieczyszczoną wodę, a żywicielem (naszym ciałem). Jednak infekcja pasożytnicza niekoniecznie musi się wiązać z objawami takimi jak biegunka – infekcje wywołane pierwotniakiem Entamoeba histolytica są na ogół bezobjawowe, ale mogą powodować inwazyjną chorobę jelita grubego u pacjentów z obniżoną odpornością.7 To samo dotyczy robaków: niski poziom inwazji często pozostaje niezauważony, podczas gdy bardzo wysoka obecność robaków może powodować cały szereg objawów, aż do upośledzenia wzrostu i rozwoju fizycznego włącznie, ponieważ robaki żywią się tkankami żywiciela, powodując utratę krwi w jelitach i utrudniając wchłanianie składników odżywczych. 8,9
Każdy pasożyt ma swoje własne nawyki : 7
jeśli chodzi o pierwotniaki, Giardia intestinalis infekuje górną część jelita cienkiego i może powodować ostrą, bardzo wodnistą biegunkę od 6 do 15 dni po zakażeniu, podczas gdy Entamoeba histolytica atakuje jelito grube i może powodować krwawą biegunkę ze śluzem;
robakiem Ascaris lumbricoides można się zarazić poprzez spożycie jaj znajdujących się na niedokładnie umytej żywności (owocach i warzywach) lub w zanieczyszczonej wodzie. Jaja te uwalniają do przewodu pokarmowego larwy, które przechodzą przez ścianę przewodu pokarmowego i krwioobiegiem docierają do płuc, gdzie mogą powodować pierwsze objawy (wczesna faza płucna). Ale na tym historia się nie kończy: larwy wspinają się po tchawicy do przełyku i wślizgują się do niego, a następnie do przewodu pokarmowego, gdzie przekształcają się w dorosłe robaki (późna faza jelitowa, z biegunką, lekkim bólem brzucha, anoreksją, nudnościami i wymiotami), które składają jaja usuwane z organizmu z kałem.
Zapobieganie bazuje przede wszystkim na stosowaniu zaleceń dotyczących higieny, które mają zastosowanie do wszystkich biegunek zakaźnych (patrz ramka).
Inne podejście opiera się na obserwacji: nie wszyscy jesteśmy równi, jeśli chodzi o pasożyty, niektórzy ludzie nie wykazują żadnych objawów, a inni cierpią na ostrą biegunkę. Mikrobiota jelitowa może wyjaśniać tę zmienność kliniczną – na przykład w Bangladeszu niska liczebność bakterii Megasphaera przed wykryciem i w momencie wykrycia pasożyta Cryptosporidium była związana z pasożytniczą biegunką u niemowląt, co sugeruje, że mikrobiota jelitowa może odgrywać rolę w nasileniu kryptosporydiozy. 10
Jeśli chodzi o helminty, powiązania między tymi robakami a mikrobiotą jelitową są również przedmiotem licznych badań, ponieważ istnieją złożone zależności nie tylko między tymi dwoma czynnikami, ale również w odniesieniu do odporności żywiciela. Co więcej robaków jelitowych niekoniecznie należy unikać – w małych ilościach mogą mieć korzystny wpływ na zdrowie, taki jak zapewnienie odporności na inne patogeny w układzie pokarmowym, a nawet zapobieganie chorobom alergicznym. 11
Zapobieganie biegunce zakaźnej, spowodowanej przez bakterie, wirusy lub pasożyty, jest przede wszystkim kwestią higieny:
Ponieważ za dużą część tych infekcji odpowiada zanieczyszczenie wody fekaliami, biegunka zakaźna występuje częściej tam, gdzie brakuje czystej wody (kraje o niskich dochodach, prowizoryczne obozowiska, tymczasowe obozy po trzęsieniach ziemi itp).
Biegunka pasożytnicza, jak każda biegunka, wiąże się przede wszystkim z ryzykiem odwodnienia u osób młodych, starszych i pacjentów z osłabionym układem odpornościowym. Leczenie bazuje zatem przede wszystkim na leczeniu objawów, tj. nawadnianiu i uzupełnianiu elektrolitów (jonów sodu, potasu i chlorków):
Jeśli pracownik służby zdrowia podejrzewa, że przyczyną biegunki może być infekcja pasożytnicza (na przykład gdy pacjent dopiero co wrócił z podróży do tropików), zazwyczaj zleca badanie kału w celu zidentyfikowania pasożytów. Nie jest to jednak takie proste: pasożyt niekoniecznie jest obecny we wszystkich odchodach (co może wymagać pobrania kilku próbek), a obecność niewielkiej ilości pasożyta nie musi oznaczać, że znaleziono właściwą przyczynę. Ostatecznie infekcje pasożytnicze, takie jak lamblioza, mogą być trudne do zdiagnozowania, a decyzja o leczeniu zależy również od historii i objawów pacjenta. 12
Jeśli zakażenie robakami nie budzi wątpliwości, pracownicy służby zdrowia mogą przepisać bezpieczne i skuteczne leki, takie jak albendazol lub mebendazol 9. Leki te są często dystrybuowane w ramach kampanii odrobaczania, szczególnie wśród dzieci i kobiet w wieku rozrodczym (15–49 lat) na obszarach endemicznych. 8
 Biegunka wirusowa: gdy podstępny wirus atakuje jelita
Biegunka wirusowa: gdy podstępny wirus atakuje jelita
 Biegunka bakteryjna: jedyny przypadek, w którym antybiotyki mogą być konieczne
Biegunka bakteryjna: jedyny przypadek, w którym antybiotyki mogą być konieczne
Wydaje się, że potencjał medyczny mikrobioty otwiera furtkę dla dochodowego rynku samodzielnie wykonywanych badań diagnostycznych. Ze względu na brak regulacji pojawiają się mylące stwierdzenia oraz ryzyko dla pacjentów gotowych zrobić wszystko, by złagodzić dolegliwości związane z chorobami przewlekłymi.

Skutkiem potencjału zdrowotnego mikrobioty, na który w ostatnich latach rzuciła światło nauka jest rozkwit rynku domowych testów diagnostycznych, obiecujący konsumentom złote góry. Przeciwko tym stwierdzeniom stanęli w apelu opublikowanym w czasopiśmie Science amerykańscy naukowcy i badacze kliniczni. Wzięli oni pod lupę dostępne w sieci usługi i obietnice 31 firm, z czego 17 znajdujących się w Stanach Zjednoczonych. Ich oferta dotyczy głównie mikrobioty jelit, w mniejszym stopniu mikrobioty pochwy czy skóry.
W praktyce testy te przypominają testy genetyczne: klient zamawia zestaw do badania, a pobrana próbka wysyłana jest do laboratorium, w którym wykonuje się sekwencjonowanie w celu określenia składu taksonomicznego mikrobioty. Klient otrzymuje raport, często w formie graficznej, oraz wynik (zdrowa mikrobiota bądź dysbioza), otrzymany w wyniku porównania z bazami danych, których reprezentatywność jest wątpliwa. W przypadku dysbiozy podawane są zalecenia i polecane są suplementy diety, sprzedawane przez 45% firm oferujących tego rodzaju testy. Rzecz jasna firmy te zalecają regularne wykonywanie testów w celu monitorowania poprawy.
63% ludzi na świecie uważa, że warto jest przebadać swoją mikrobiotę jelit.
Według autorów apelu trzy wymogi zapewniające precyzyjność oraz przydatność testu nie są spełnione, gdy:
Trzeba jednak przyznać, że wiele firm zadbało o to, by doprecyzować, że oferowane przez nie testy nie mają wartości „diagnostycznej”. Tymczasem ich twierdzenia marketingowe sugerują co innego, tym bardziej, że wyniki wydają się mieć wartość naukową.
Konsekwencje tych testów mogą być jednak katastrofalne dla pacjentów cierpiących na poważne choroby przewlekłe: błędna diagnoza w warunkach domowych, opóźnione podjęcie leczenia, a nawet zaprzestanie leczenia na rzecz alternatywnych metod o nieudowodnionych efektach. Jeden z pacjentów planował na przykład przeprowadzić domową transplantację kału. Stąd potrzeba, zdaniem sygnatariuszy apelu, wprowadzenia przepisów prawnych zobowiązujących firmy wprowadzające takie testy do obrotu do określenia ich metodologii, przyjęcia standardów (które należy określić) i publikacji wyników... a także zakazujących stosowania wprowadzających w błąd twierdzeń i fałszywych obietnic. Faktem jest, że – ogólnie rzecz biorąc – nauka musi jeszcze pójść do przodu, by stworzyć definicję zdrowej mikrobioty oraz potwierdzić (lub obalić) ewentualną skuteczność zmian w żywieniu i/lub suplementów diety.
 Transplantacja mikrobioty fekalnej a IBS: gdzie, kiedy, ile, żeby efekty były jak najlepsze?
Transplantacja mikrobioty fekalnej a IBS: gdzie, kiedy, ile, żeby efekty były jak najlepsze?
 Publikacje naukowe: dr nauka i pan przekręt
Publikacje naukowe: dr nauka i pan przekręt
Biegunka zakaźna może być wywoływana przez bakterie (biegunka bakteryjna), pasożyty (biegunka pasożytnicza) lub wirusy (biegunka wirusowa). W przypadku biegunki bakteryjnej bakterie te to Shigella, które odpowiadają za chorobę znaną jako szigeloza, Vibrio cholerae, odpowiedzialne za przerażające epidemie cholery, a także Salmonella lub Escherichia coli, które czasami trafiają na pierwsze strony gazet w krajach zachodnich. Biegunka zazwyczaj leczy się samoistnie: wystarczy unikać odwodnienia i dać mikrobiocie jelitowej kilka tygodni na odzyskanie równowagi. Jednak w niektórych populacjach ryzyka lub w przypadku rozprzestrzeniania się infekcji konieczne może być stosowanie antybiotyków, a czasem nawet probiotyków w celu przywrócenia mikrobioty jelitowej.
Mikrobiota jelit Biegunka podróżnych Biegunka poantybiotykowa
Biegunka występuje, gdy w ciągu dnia oddawane są co najmniej trzy luźne lub płynne stolce. Biegunka zakaźna występuje, gdy jest wywołana zakażeniem czynnikiem chorobotwórczym (wirusem, bakterią lub pasożytem)[1-3]. Jeśli patogenem są bakterie, biegunkę określa się jako „bakteryjną”.
Chociaż istnieje kilka niezakaźnych przypadków biegunki (np. w przypadku chorób układu trawiennego, takich jak choroba Leśniowskiego-Crohna), zdecydowaną większość wywołują patogeny. W zależności od danego patogenu wyróżniamy następujące rodzaje biegunek:
Co więcej biegunka może być również częstym skutkiem ubocznym (do 35% pacjentów[4;5]) leczenia antybiotykami. Takie zaburzenie jest określane jako biegunka związana z antybiotykami.
Bakterie wywołujące biegunkę to [6]:
Nie są one jednak jedyne: bakterie takie jak Salmonella czy Escherichia coli czasami trafiają na pierwsze strony gazet w krajach zachodnich, gdy zanieczyszczają produkty spożywcze (surowe mięso mielone, sery itp.), prowadząc do głośnych przypadków wycofywania produktów z supermarketów.
W przypadku biegunki pasożytniczej, podobnie jak biegunki zakaźnej, wszystko zaczyna się od konfrontacji między patogenem (w tym przypadku bakterią), przenoszonym przez skażoną żywność, zanieczyszczoną wodę lub kontakt z chorą osobą, a gospodarzem (naszym ciałem). Ale uwaga: zagrożenie stwarzane przez bakterie różni się, a za tą samą nazwą bakterii kryje się w rzeczywistości wiele różnych rodzajów bakterii – na przykład istnieje nie jedna, ale ponad 2500 różnych salmonelli, które są mniej lub bardziej agresywne [7]. To samo dotyczy Escherichia coli: nie wszystkie E. coli są patogenne, a wśród tych patogennych istnieje wiele różnych typów [2;8].
Wynik konfrontacji między bakteriami a organizmem zależy od złożonej równowagi, która w dużej mierze obejmuje mikrobiotę jelitową. Zwierzęta pozbawione flory jelitowej są bardzo wrażliwe na bakterie wywołujące biegunkę – wystarczy mikrodawka niektórych salmonelli, aby wywołać śmiertelną infekcję, podczas gdy do zabicia myszy z nienaruszoną mikrobiotą jelitową potrzebna jest dawka od 100 do 100 000 000 razy większa [9]. Jak można wyjaśnić taką różnicę? W przypadku braku mikrobioty układ odpornościowy pozostaje niedojrzały, a zatem nieuzbrojony w obliczu inwazji patogenów, które mogą się swobodnie osiedlać, ponieważ żadne inne bakterie nie zajmują tego terenu [9].
Kiedy bakterie przejmują kontrolę, wydzielają specyficzne toksyny, co wyjaśnia, dlaczego każdy przypadek biegunki bakteryjnej jest specyficzny [2;10]:
Ostra biegunka bakteryjna wywołana przez czynnik zakaźny generuje poważną dysbiozę jelitową [2]. Odzyskanie pewnej równowagi przez mikrobiotę zajmie kilka tygodni, czasami bez możliwości powrotu do stanu początkowego [2;11].
Niebezpieczna natura Shigelli podsyca nadzieje na opracowanie szczepionki, która mogłaby ostatecznie zapobiec około 200 000 zgonów spowodowanych przez tę bakterię każdego roku, a także zmniejszyć zapotrzebowanie na antybiotyki i przeciwdziałać pojawieniu się oporności, która sprawiłaby, że leczenie byłoby nieskuteczne. Obecnie opracowywanych jest kilka szczepionek przeciwko bakterii Shigella, ale żadna z nich nie została jeszcze zatwierdzona[12].
Inną drogą jest mikrobiota jelitowa. U ludzi „zdrowa” mikrobiota jelitowa jest uważana za środek zapobiegający cholerze [13]. Probiotyki są również uważane za środek ograniczający nasilenie niektórych infekcji bakteryjnych [2]: probiotyczne drożdże Saccharomyces boulardii mogą ułatwiać odbudowę mikrobioty jelitowej u dzieci cierpiących na ostrą biegunkę [14]; probiotyczne bakterie E. coli (niepatogenne) hamują tworzenie biofilmów przez bakterie patogenne, w tym patogenne bakterie E. Coli[2]; trio określonych szczepów Lactobacillus, Bifidobacterium i Streptococcus skraca czas trwania krwawej biegunki (czerwonki) i hospitalizacji[2].
Oprócz tych środków zapobiegawczych istnieją oczywiście zalecenia dotyczące higieny i zachowania odpowiedniej odległości, które mają zastosowanie do wszystkich biegunek zakaźnych (patrz ramka). W szczególnym przypadku infekcji przenoszonych przez żywność (salmonella, E. coli), żywność powinna być dokładnie ugotowana (E. coli jest zabijana przez ciepło, co wyjaśnia, dlaczego często dochodzi do zanieczyszczenia żywności przez surowe lub niedogotowane mięso).
Zapobieganie biegunce zakaźnej, spowodowanej przez bakterie, wirusy lub pasożyty, jest przede wszystkim kwestią higieny:
Ponieważ za dużą część tych infekcji odpowiada zanieczyszczenie wody fekaliami, biegunka zakaźna występuje częściej tam, gdzie brakuje czystej wody (kraje o niskich dochodach, prowizoryczne obozowiska, tymczasowe obozy po trzęsieniach ziemi itp.).
Biegunka bakteryjna jest bardzo powszechna i ogólnie nieszkodliwa, często ustępuje samoistnie. Należy jednak uważać na ryzyko odwodnienia u osób bardzo młodych, starszych i pacjentów z osłabionym układem odpornościowym: utrata wody i elektrolitów (jonów sodu, potasu i chlorku) musi zostać zrekompensowana:
Nie zaleca się stosowania antybiotyków u zdrowych osób cierpiących na łagodne lub umiarkowane postacie choroby, aby uniknąć selekcji szczepów opornych [7]. Antybiotyki mogą być natomiast przepisywane osobom z grup ryzyka (niemowlęta, osoby starsze, pacjenci z obniżoną odpornością) lub gdy infekcja rozprzestrzenia się z jelit na inne części ciała[7].
Pracownicy służby zdrowia mogą również zalecać niektóre szczepy probiotyczne w leczeniu ostrej biegunki zakaźnej u dzieci: te dobre bakterie skracają czas trwania biegunki, długość hospitalizacji lub zmniejszają objętość stolca (ESPGHAN 2023).
Te liczby mrożą krew w żyłach: na każdych 100 pacjentów przyjętych do szpitala 7 w krajach o wysokim dochodzie i 15 w krajach o niskim i średnim dochodzie zachoruje podczas pobytu na co najmniej jedną infekcję. Średnio 1 na 10 pacjentów dotkniętych tą chorobą ulega tzw. zakażeniu szpitalnemu [15].
Patogeny, o których mowa, obejmują bakterię Clostridioides difficile (wcześniej znaną jako Clostridium difficile), która jest główną przyczyną szpitalnej biegunki zakaźnej u dorosłych. Szacuje się, że w Europie występuje około 120 000 przypadków rocznie, a w Stanach Zjednoczonych 450 000 [16].
Problem polega na tym, że z czasem pojawiły się bardziej zjadliwe szczepy C.difficile, które słabiej reagowały na antybiotyki, a wskaźnik wyleczeń gwałtownie spadł. Stąd poszukiwanie alternatywnych metod leczenia. Zgodnie z zaleceniami Światowej Organizacji Gastroenterologii z 2023 r. „Probiotyki są skuteczne w zapobieganiu biegunce związanej z C. difficile u pacjentów otrzymujących antybiotyki”. W przypadku nawracających przypadków występowania C. difficile u dorosłych i dzieci skuteczny okazał się przeszczep mikrobioty kałowej (FMT)[17], zapobiegając nawrotom w 90% przypadków.
 Biegunka wirusowa: gdy podstępny wirus atakuje jelita
Biegunka wirusowa: gdy podstępny wirus atakuje jelita
 Biegunka pasożytnicza: czy mikrobiota jest kluczowym czynnikiem wpływającym na rokowanie?
Biegunka pasożytnicza: czy mikrobiota jest kluczowym czynnikiem wpływającym na rokowanie?