Każdego roku wczesne dojrzewanie płciowe dotyka 20 na 10 000 dziewcząt na całym świecie, a otyłość dziecięca zwiększa ryzyko jego wystąpienia. Od 2010 roku większą uwagę zwraca się na wpływ mikrobioty jelitowej na homeostazę energetyczną i otyłość. Chociaż wiele czynników może wpływać na mikrobiotę jelitową (stosowanie antybiotyków itp.), karmienie piersią wydaje się odgrywać kluczową rolę w jej rozwoju. Naukowcy zmodyfikowali więc dietę karmiących samic myszy, aby ocenić wpływ diety na ryzyko otyłości i wczesnego dojrzewania płciowego u ich potomstwa. Przez trzy tygodnie od narodzin młodych samice myszy były karmione albo dietą o normalnej kaloryczności (NCD) zawierającą 12% tłuszczu, albo dietą wysokotłuszczową (HFD) zawierającą 60% tłuszczu. 21 dni po urodzeniu wszystkie młode myszy zostały odstawione od mleka, karmione dietą o normalnej kaloryczności i losowo umieszczone w klatkach wraz z czterema młodymi od matek NCD, czterema młodymi od matek HFD lub dwoma młodymi od matek NCD i dwoma od matek HFD. Celem było zmierzenie wpływu wspólnego przebywania oraz ocena, czy odwraca ono skutki wysokotłuszczowej diety matek u potomstwa.
Wpływ diety matki podczas karmienia piersią
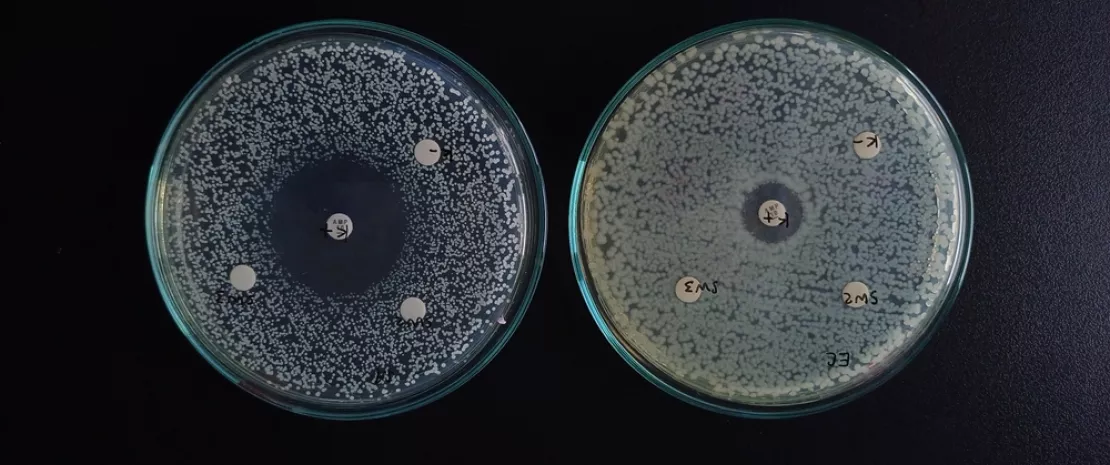
Dieta wysokotłuszczowa u matek w okresie laktacji wpływała na rozwój mikrobioty potomstwa. Na przykład zaobserwowano wzrost udziału Streptococcaceae i Peptostreptococcaceae w mikrobiocie jelitowej młodych myszy. Ponadto potomstwo matek HFD miało mikrobiotę o istotnie mniejszej różnorodności. Dieta wysokotłuszczowa matek prowadziła również do otyłości dziecięcej, wczesnego dojrzewania płciowego, nieregularnych cykli menstruacyjnych oraz oznak zaburzeń metabolizmu glukozy u potomstwa płci żeńskiej. Jednak wczesnego dojrzewania nie zaobserwowano u młodych samców.
Efekty współdzielenia mikrobioty
Ponieważ myszy są zwierzętami koprofagicznymi, dzielą swoją mikrobiotę drogą fekalno-oralną. Po wspólnym przebywaniu z potomstwem matek NCD, u potomstwa matek HFD zwiększyła się obfitość mikrobioty, co odwróciło skutki diety wysokotłuszczowej matek. Chroniło to również samice przed wczesnym dojrzewaniem płciowym oraz niewrażliwością na insulinę. Nie zaobserwowano jednak efektu ochronnego w odniesieniu do masy ciała ani ilości tkanki tłuszczowej u potomstwa HFD.
Nowe podejście terapeutyczne w zaburzeniach metabolicznych?
Zdaniem autorów karmienie piersią odgrywa kluczową rolę w rozwoju prawidłowych funkcji metabolicznych i rozrodczych potomstwa. Insulinooporność związana z dysbiozą mikrobioty zwiększa prawdopodobieństwo wczesnego dojrzewania płciowego, gdy wynika ono z diety wysokotłuszczowej matki w okresie karmienia piersią. W związku z tym mikrobiota może stanowić nowy cel terapeutyczny w leczeniu zaburzeń metabolicznych i rozrodczych.

 Czynniki wpływające na rozwój mikrobioty i dojrzewanie układu odpornosciowego na wczesnym etapie życia
Czynniki wpływające na rozwój mikrobioty i dojrzewanie układu odpornosciowego na wczesnym etapie życia
 Mikrobiota niemowlęcia: dziedziczy się ją także od ojca
Mikrobiota niemowlęcia: dziedziczy się ją także od ojca