Od urodzenia do śmierci stykamy się z ekspozomem, który na różne sposoby wpływa na nasze zdrowie
Nasza wrażliwość na środowisko zmienia się na przestrzeni całego życia. Już od ciąży eksposom kształtuje odporność, wpływa na mikrobiotę niemowlęcia i decyduje o przyszłym ryzyku astmy lub alergii. W okresie dojrzewania oddziałuje na zdrowie psychiczne i kondycję skóry. W dorosłości wpływa na poziom stanu zapalnego i ogólne samopoczucie. U osób starszych może wspierać lub zaburzać długowieczność – co potwierdzają badania nad mikrobiotą stulatków.
Odkryj, jak każdy etap życia wchodzi w interakcję z eksposomem.

1000 pierwszych dni
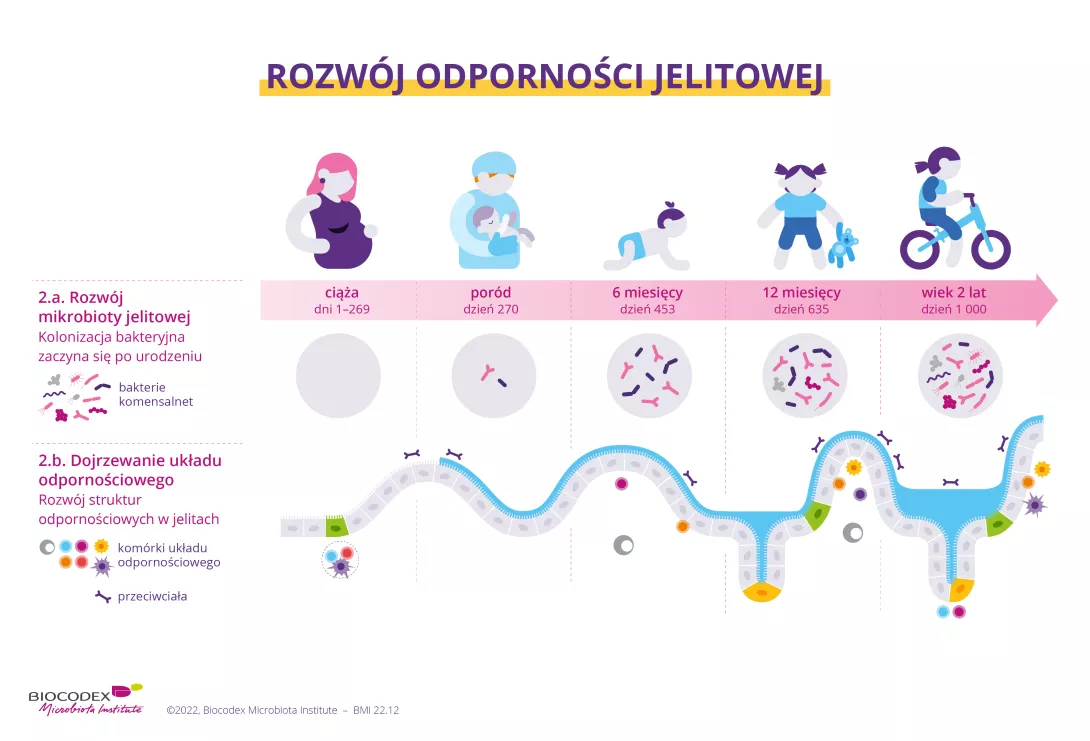
Od kilku lat wiadomo, że mikroorganizmy zawarte w mikrobiocie jelitowej są niezbędne do rozwoju układu odpornościowego. Udział w tym procesie mogą mieć również jednak inne mechanizmy związane z przedwczesną ekspozycją płodu na czynniki środowiskowe.
Okres okołoporodowy
- Ciąża: mikrobiota matki (jelitowa, skórna, płucna i – potencjalnie – łożyskowa) prawdopodobnie ma duży wpływ na dojrzewanie układu odpornościowego potomstwa. Jedno z badań wykazało na przykład, że ekspozycja kobiet ciężarnych na bakterie pochodzące z obory zmniejsza ryzyko zachorowania ich dzieci w przyszłości na astmę. Istnieje też mikrobiota łożyskowa – bardziej podobna do mikrobioty jamy ustnej matki niż do mikrobioty pochwy lub jelit – która może grać rolę w tym dojrzewaniu.
- Poród: niemowlęta urodzone siłami natury są kolonizowane przez mikroorganizmy podobne do tych, które są obecne w pochwie matki. Mają one również bogatszą i bardziej zróżnicowaną mikrobiotę niż dzieci urodzone przez cesarskie cięcie, co wiąże się z mniejszym ryzykiem astmy.
- Karmienie piersią
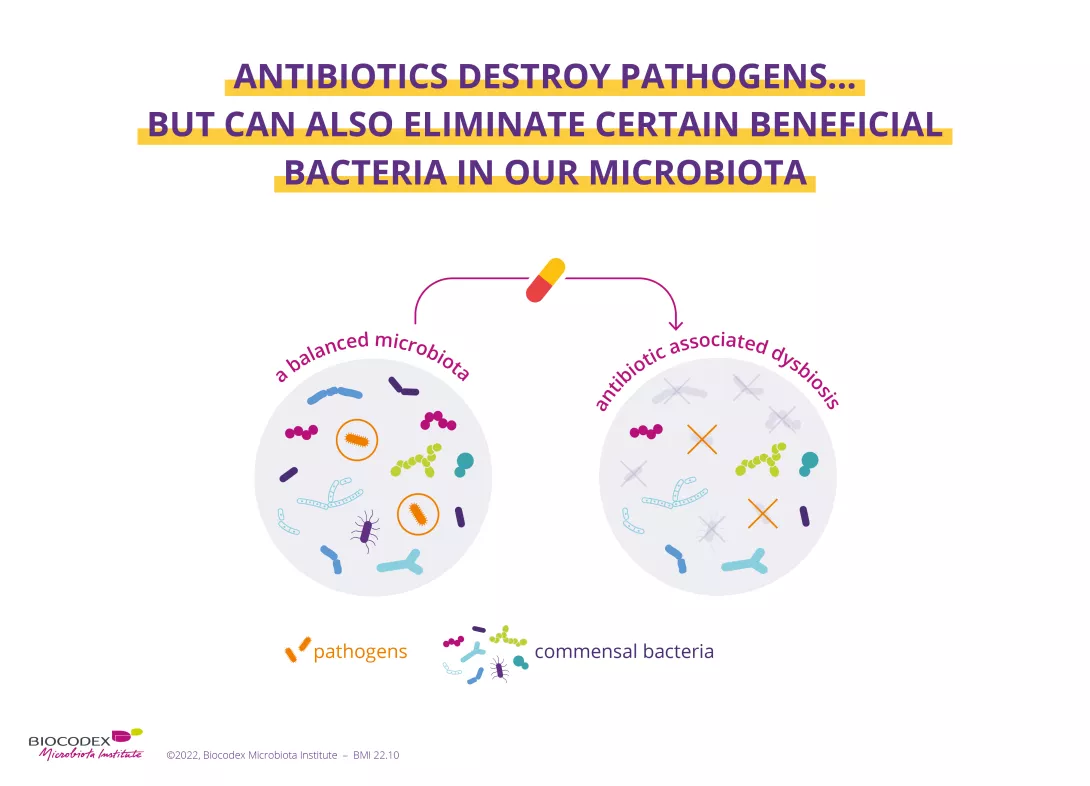
Znaczenie mają również inne czynniki ekspozomu okołoporodowego (leczenie antybiotykami, karmienie piersią, nawyki związane z żywieniem itp.).
Małe bakterie, duże zagrożenia: jak drobnoustroje pochwy kształtują zdrowie w ciąży
Wczesne dzieciństwo
Od połowy ubiegłego stulecia zmiana stylu życia na wygodniejszy, a mieszkań na nowocześniejsze i bardziej „higieniczne” zaburzyła ekspozycję ludzi na mikroorganizmy. Zmiany te mogą zwiększać podatność dzieci na przewlekłe choroby zapalne.
Są mocne dowody na to, że wczesna ekspozycja na bogate, zróżnicowane populacje mikroorganizmów działa ochronnie pod warunkiem, że ma miejsce na początku życia. Nazywa się to „okienkiem okazji”.
Wbrew temu, co mówi intuicja, różne badania wykazały, że obecność zwierząt towarzyszących, gryzoni, grzybów lub bakterii w środowisku, w którym żyje niemowlę lub małe dziecko, poprawia różnorodność bakterii jego mikrobioty i może chronić je przed astmą.
Pies a mikrobiota kurzu w zapobieganiu astmie, czyżby strzał w dziesiątkę?
Dzieciństwo i okres dojrzewania
To, że ekspozom może mieć znaczenie, zostało wykazane przez badanie prowadzone przez 8 lat na 504 dzieciach w wieku od 6 do 9 lat. Badacze zmierzyli wpływ różnych ekspozycji (na żywność, aktywność fizyczną, sen, zanieczyszczenie powietrza, status społeczno-gospodarczy) na markery krwi (metabolity).
Wskaźnik eksposomu
Dla każdego dziecka badacze obliczyli „scoring ekspozomu” mierzący globalny wpływ różnych ekspozycji na zdrowie.
Wyniki pokazują, że scoring ten ma związek z 31 metabolitami, z czego 12 nie miało związku z żadną ekspozycją rozpatrywaną indywidualnie. Wskazuje to, że ekspozycje środowiskowe i związane z trybem życia nie wywierają swojego fizjologicznego wpływu samodzielnie.
Miejsce ma raczej złożona interakcja między ekspozycjami zewnętrznymi a powiązanymi z nimi wewnętrznymi odpowiedziami fizjologicznymi.
Co więcej, wysoki scoring ekspozomu ma związek z obniżonym poziomem octanu, (sidenote: Krótkołańcuchowe kwasy tłuszczowe Krótkołańcuchowe kwasy tłuszczowe są źródłem energii (paliwa) dla komórek organizmu, współdziałają z układem odpornościowym i biorą udział w komunikacji między jelitami a mózgiem. Silva YP, Bernardi A, Frozza RL. The Role of Short-Chain Fatty Acids From Gut Microbiota in Gut-Brain Communication. Front Endocrinol (Lausanne). 2020;11:25. ) wytwarzanego przez mikrobiotę jelitową. Badania sugerują, że octan może mieć korzystny wpływ na zdrowie metaboliczne oraz zdrowie układu sercowo-naczyniowego i układu nerwowego.
Nasz starszy brat (albo starsza siostra) pomagają dorosnąć naszej malutkiej mikrobiocie!
Trądzik
Inne badanie, przeprowadzone wśród dorastającej młodzieży, wykazało, że wiele czynników związanych z trybem życia (spożywanie odtłuszczonego mleka i suplementów zawierających białka z serwatki – takich jak „whey”, stres, zanieczyszczenia, leki, czynniki klimatyczne itp.) wyraźnie wpływają na rozwój i nasilenie trądziku oraz skuteczność leczenia.
Produkty do pielęgnacji i kosmetyki należące do ekspozomu zewnętrznego mogą pobudzać stan zapalny i zaostrzyć trądzik, modyfikując barierę skórną i równowagę mikrobioty skórnej, co sprzyja wydzielaniu sebum, modyfikacji mikroorganizmów i pobudzeniu wrodzonej odporności.
Zdrowie psychiczne
Wiadomo również, że w okresie dojrzewania stres, często silniejszy niż w innych okresach życia, a także wzrost ilości wytwarzanych przez organizm androgenów (na przykład testosteronu) mogą modyfikować mikrobiotę, a tym samym oś jelita-mózg.
Badania sugerują, że te zmiany ekspozomu wewnętrznego mogą grać rolę w występowaniu chorób psychicznych, z których wiele objawia się po raz pierwszy w okresie dojrzewania.
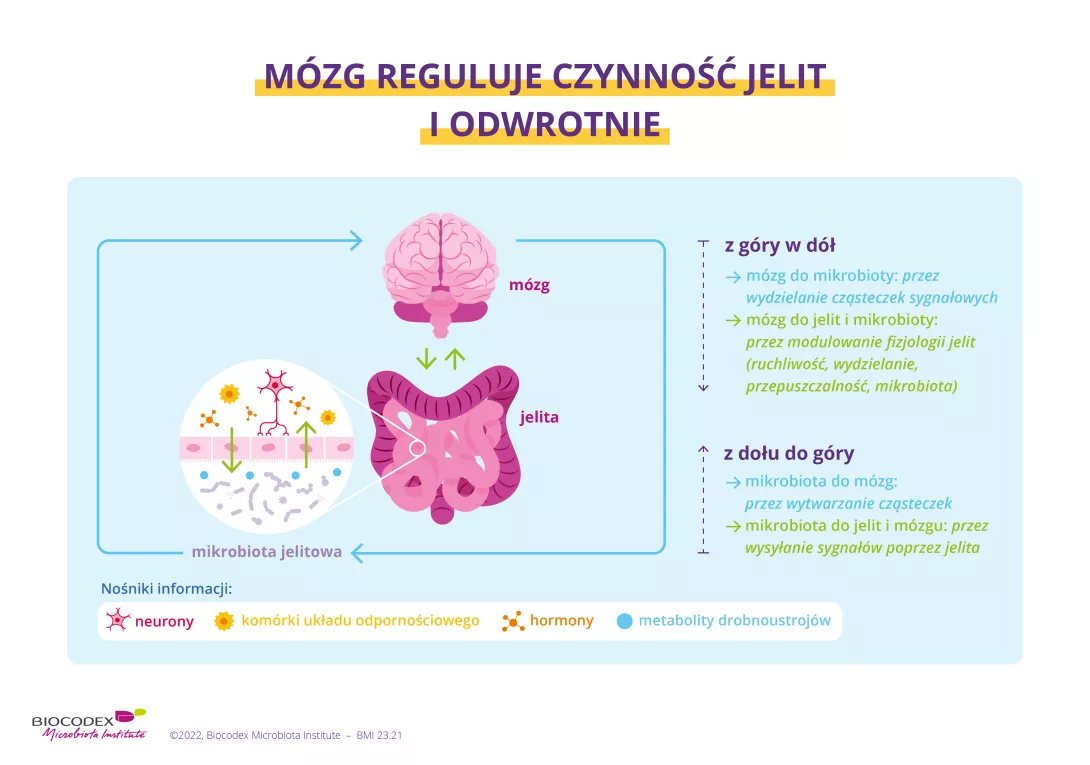
Oś jelita-mózg: Jaką rolę odgrywa mikrobiota?
Dorosłość
Jest coraz bardziej oczywiste, że mikrobiota jelitowa uczestniczy w różnych aspektach samopoczucia fizycznego i psychicznego. A także, że jej struktura i funkcjonowanie w dużym stopniu zależą od trybu życia.
O ile wpływ ekspozomu na początku życia ma fundamentalne znaczenie, to wiadomo, że jego szkodliwe działanie może się ujawnić w wieku dorosłym. Zachodnie nawyki dietetyczne (dieta uboga w zboża, owoce, warzywa i zboża pełnoziarniste, a bogata w produkty pochodzenia zwierzęcego i żywność wysoko przetworzoną) mogą na przykład powodować zaburzenia biofilmu i bariery jelitowej, które mogą skutkować większą przepuszczalnością jelit.
Fragmenty bakterii przenikają wtedy do krwi (endotoksyny albo lipopolisacharydy), powodując przewlekły stan zapalny niskiego stopnia, który może mieć szkodliwe konsekwencje metaboliczne i behawioralne. I odwrotnie – dieta bogata w błonnik i substancje fitochemiczne pochodzenia roślinnego może sprzyjać różnorodności mikroorganizmów i zmniejszać stres oksydacyjny oraz ilość czynników zapalnych.
Niezrównoważona dieta w połączeniu ze stresem, brakiem kontaktu z przyrodą, środowiskiem ubogim w mikroorganizmy i brakiem aktywności fizycznej na wolnym powietrzu mogą też prowadzić do zaburzenia różnorodności mikroorganizmów zawartych w mikrobiocie jelitowej i skórnej. A mniejsze zróżnicowanie mikrobioty oznacza zaburzenia funkcjonowania układu odpornościowego i przewlekły stan zapalny, który może uderzyć we wszystkie narządy i utorować drogę przewlekłym chorobom.
Jak zachować zdrową mikrobiotę?
Seniorzy
Zaawansowany wiek ma zazwyczaj związek ze zmianami mikrobioty jelitowej. Z biegiem czasu ma ona tendencję do utraty różnorodności i równowagi (dysbioza), co przyczynia się do nasilenia procesów zapalnych i większej podatności na choroby atakujące osoby starsze.
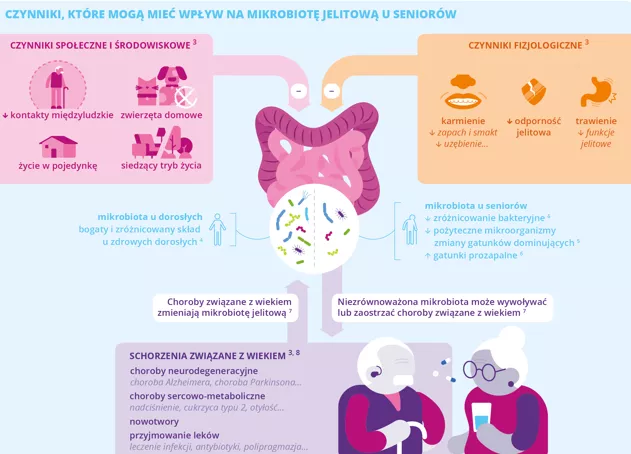
Natomiast utrzymywanie z biegiem czasu zrównoważonej mikrobioty sprzyja prawidłowemu funkcjonowaniu metabolizmu i układu odpornościowego oraz utrzymaniu dobrego stanu serca, kości i funkcji poznawczych.
O ile wciąż trwają badania zaburzeń mikrobioty pojawiających się z upływem czasu, to z badań nad mikrobiotą stulatków wynika, że istotne mogą być niektóre czynniki ekspozomu.
Na przykład nawyki dietetyczne, a zwłaszcza praktykowanie diety śródziemnomorskiej (bogatej w błonnik i antyoksydanty), są skorelowane z gatunkami mikroorganizmów jelitowych związanymi z długowiecznością. Uprawianie aktywności fizycznej, brak palenia tytoniu i zadowalające warunki pracy również mogą mieć znaczenie.
Przeczytaj resztę artykułu
Kierunek: bardziej przyjazny ekspozom
Wróć do poprzedniej strony
Ekspozycja wyjaśniona przez naszego eksperta
 Ekspozom, ekspozycja mikrobioty to zagrożenie dla zdrowia!
Ekspozom, ekspozycja mikrobioty to zagrożenie dla zdrowia!
 Mikrobiota i ekspozom : dialog u podstaw naszego zdrowia
Mikrobiota i ekspozom : dialog u podstaw naszego zdrowia