Wszystko, co musisz wiedzieć o antybiotykach i oporności na środki przeciwdrobnoustrojowe
Oporność na środki przeciwdrobnoustrojowe (AMR) zagraża skuteczności opieki zdrowotnej. Nadszedł czas, aby podjąć działania: na tej stronie znajdziesz praktyczne narzędzia, które pomogą Ci przygotować się i zwiększyć świadomość pacjentów na temat tego globalnego problemu.

Antybiotyki: zrozumienie zagrożeń dla mikroflory człowieka
Antybiotyki zrewolucjonizowały współczesną medycynę, ratując życie niezliczonej liczbie osób. Jednak ich powtarzające się lub niewłaściwe stosowanie powoduje głębokie zaburzenia mikroflory jelitowej, zmniejszając jej różnorodność i zdolności ochronne. Ten dwojaki aspekt postępu terapeutycznego i zaburzeń równowagi mikrobiologicznej podkreśla potrzebę rozważnego stosowania antybiotyków.
70 % osób twierdzi, że wie, iż antybiotyki mają wpływ na mikrobiom
35 % Tylko 1 na 3 osoby zostało poinformowanych przez pracownika służby zdrowia, że przyjmowanie antybiotyków może mieć negatywny wpływ na równowagę mikroflory jelitowej.
Z okazji corocznego Światowego Tygodnia Świadomości AMR organizowanego przez WHO, Instytut Biocodex Microbiota podsumowuje dotychczasowe działania.
Czym jest Światowy Tydzień Świadomości AMR?
Od 2015 roku WHO organizuje co roku Światowy Tydzień Świadomości AMR (WAAW), którego celem jest zwiększenie świadomości na temat globalnej oporności na środki przeciwdrobnoustrojowe.
Kampania, która odbędzie się w dniach 18–24 listopada, ma na celu zachęcenie ogółu społeczeństwa, pracowników służby zdrowia i decydentów do ostrożnego stosowania antybiotyków, leków przeciwwirusowych, przeciwgrzybiczych i przeciwpasożytniczych, aby zapobiec dalszemu rozprzestrzenianiu się oporności na środki przeciwdrobnoustrojowe.
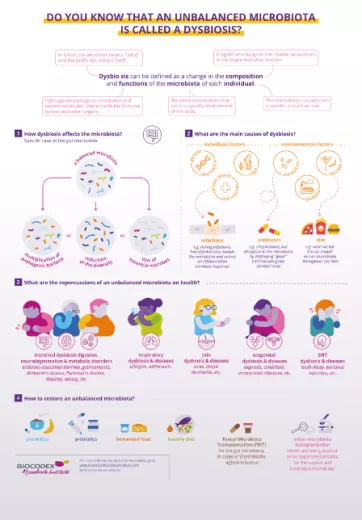
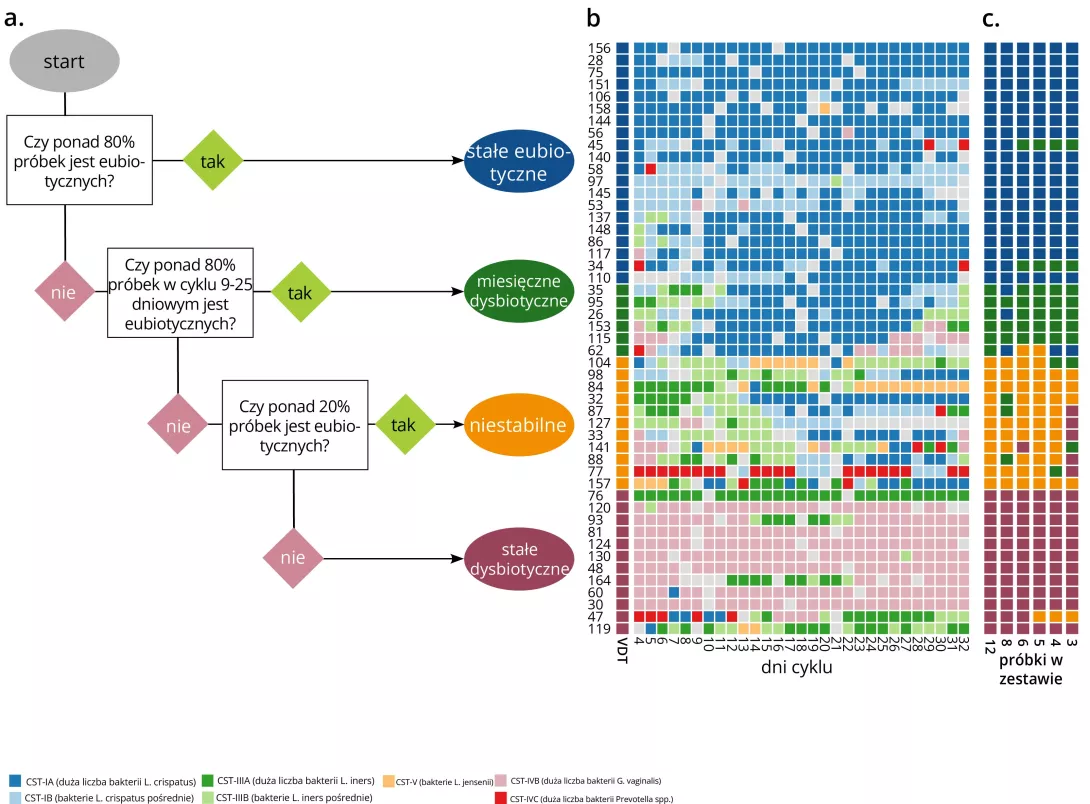
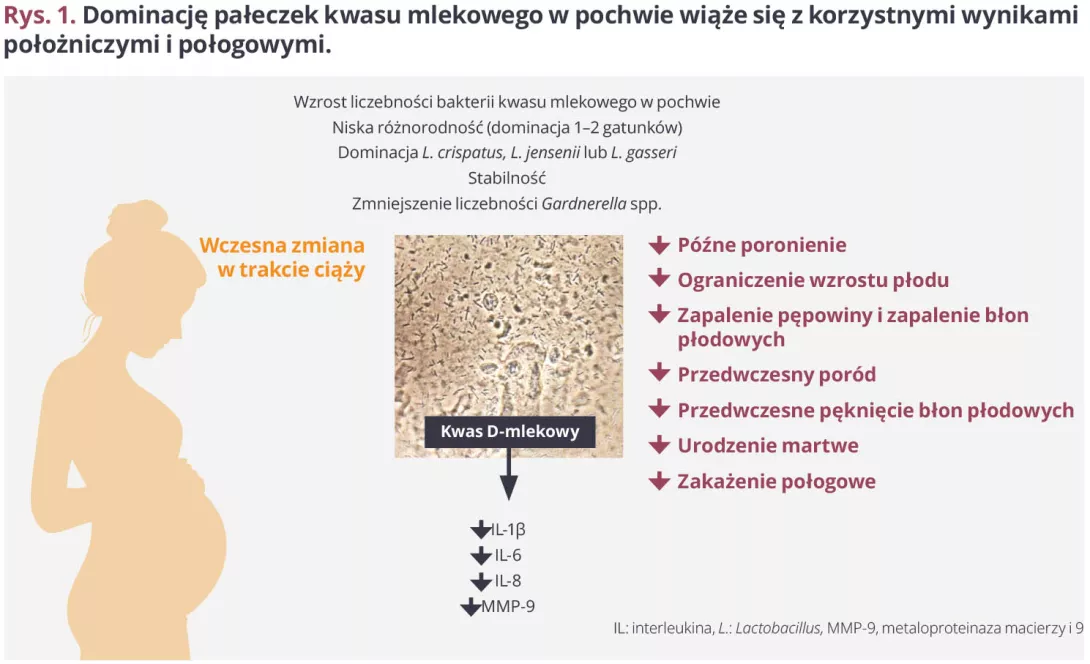
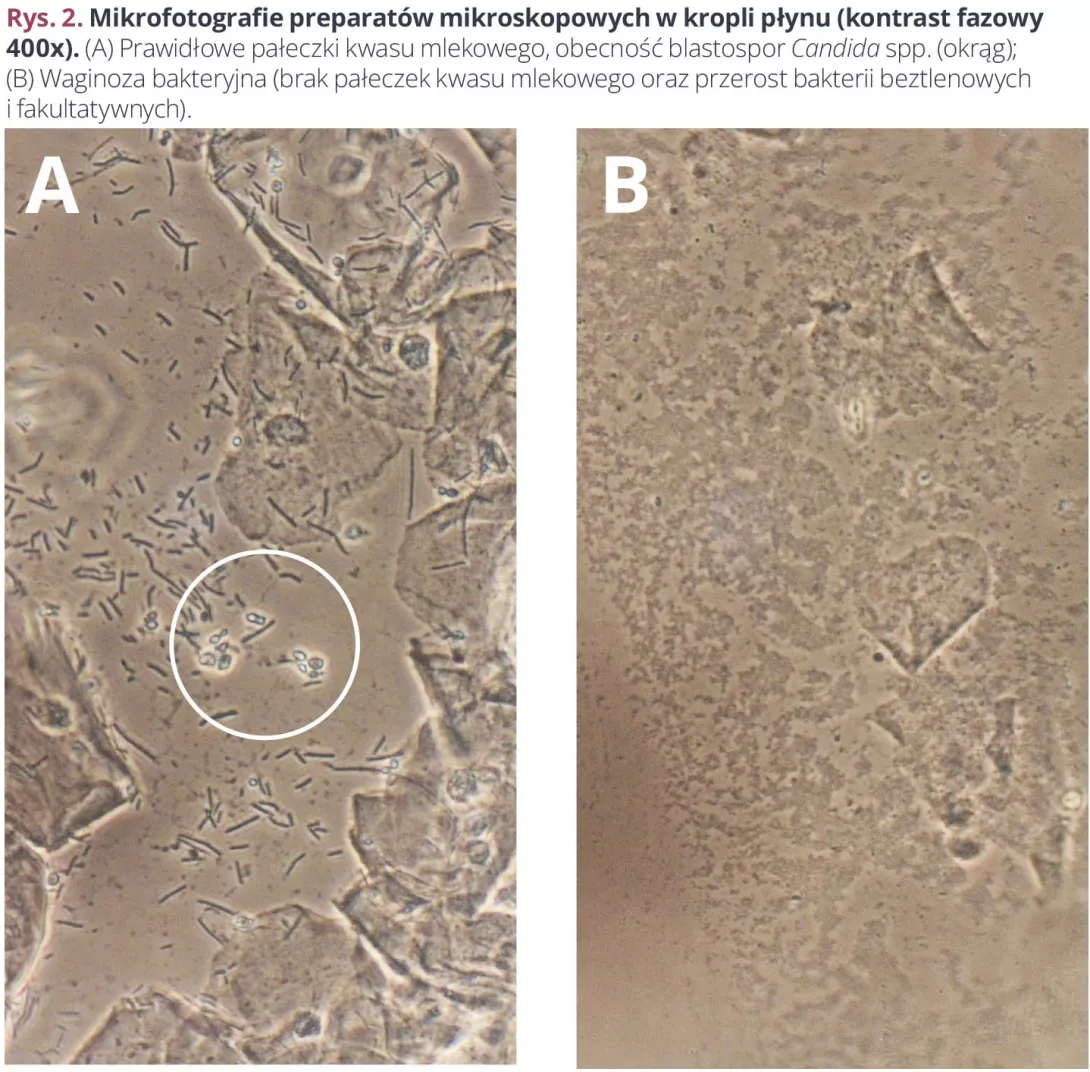
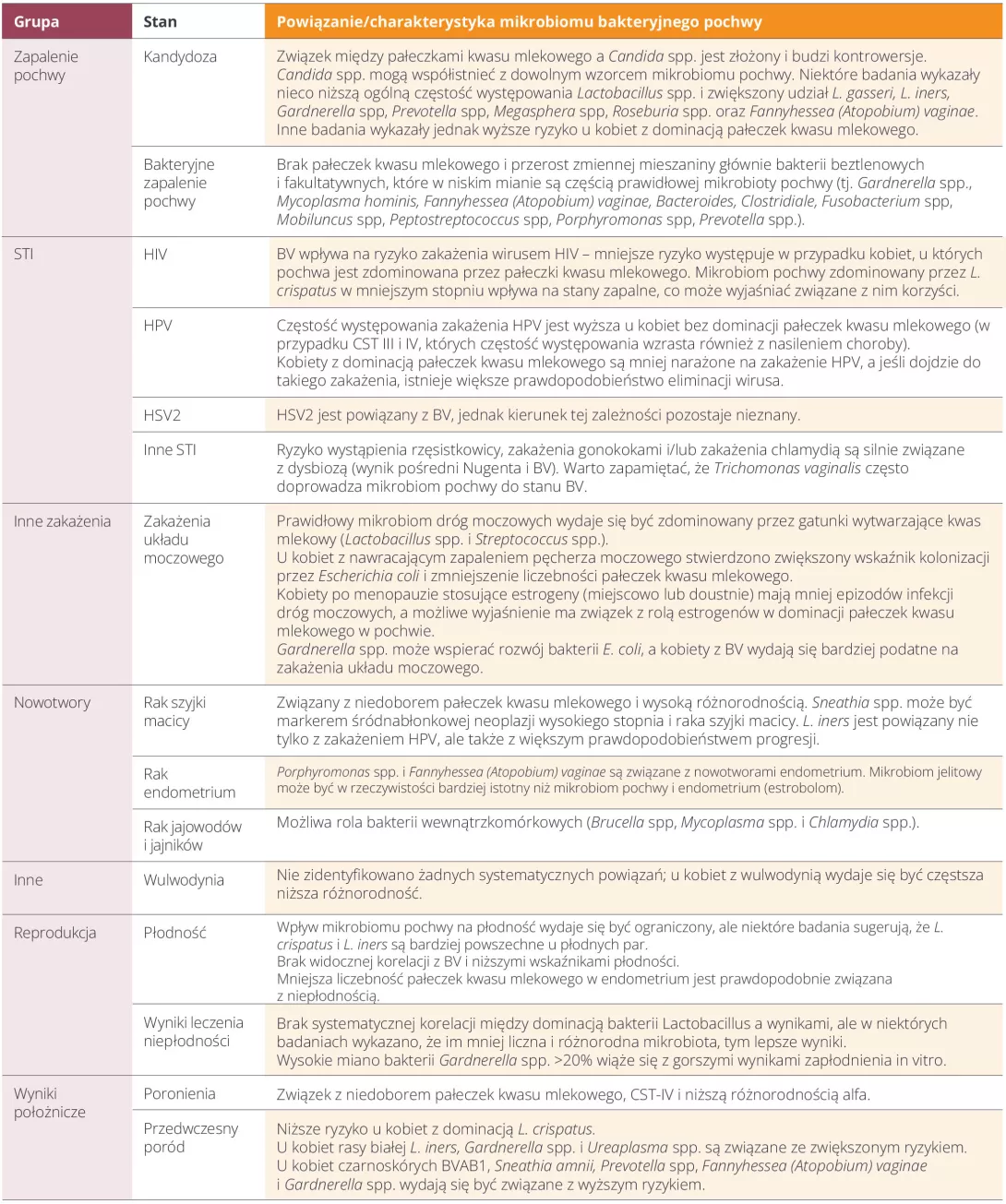
Dysbioza: wpływ antybiotyków na zdrowie i mikroflorę jelitową
Powtarzające się narażenie na antybiotyki może poważnie zaburzyć równowagę mikroflory jelitowej, prowadząc do dysbiozy, która ma różne konsekwencje kliniczne. Te zmiany w mikroflorze jelitowej są obecnie uznawane za czynnik ryzyka wielu chorób. Lepsze ich zrozumienie oznacza wzmocnienie profilaktyki i spersonalizowaną opiekę.
Oporność na środki przeciwdrobnoustrojowe: poważne zagrożenie dla zdrowia ludzkiego
Powszechne i czasami niewłaściwe stosowanie antybiotyków sprawia, że stają się one coraz mniej skuteczne w leczeniu infekcji, a wiele bakterii jest obecnie opornych na antybiotyki. Nadzór, badania i świadomość pozostają niezbędne do kontrolowania tego poważnego problemu zdrowotnego.
Microbiotalk: krótkie konferencje na temat oporności na środki przeciwdrobnoustrojowe
Konferencja Microbiotalk ma na celu rzucenie światła na wielowymiarowe wyzwania związane z opornością na środki przeciwdrobnoustrojowe (AMR), badając złożone powiązania między mikroflorą jelitową, czynnikami środowiskowymi i zdrowiem publicznym. W wydarzeniu wezmą udział międzynarodowi eksperci i rzecznicy pacjentów, którzy omówią takie tematy, jak wpływ antybiotyków na mikroflorę jelitową, pojawianie się oporności we wczesnym dzieciństwie, środowiskowe rezerwuary opornych bakterii oraz kluczowa rola zaangażowania pacjentów i społeczeństwa.
Konferencje Microbiotalk: globalna dyskusja na temat oporności na środki przeciwdrobnoustrojowe

Fresk poświęcony oporności na środki przeciwdrobnoustrojowe: ucz się, baw się i działaj już teraz
W walce z opornością na środki przeciwdrobnoustrojowe liczy się każda inicjatywa. Wizualizacja danych, dzielenie się wiedzą i wzmacnianie współpracy między pracownikami służby zdrowia to kluczowe czynniki. Świadomość zbiorowa stanowi sedno globalnej strategii zapobiegania.
Odkryj pierwszy kolaż ilustrujący wyzwania związane z opornością na środki przeciwdrobnoustrojowe.
Pierwszy fresk poświęcony oporności na środki przeciwdrobnoustrojowe
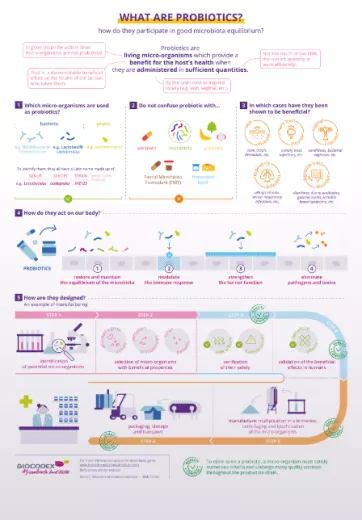
Probiotyki: przywracają równowagę mikroflory po kuracji antybiotykowej
Po kuracji antybiotykowej przywrócenie równowagi mikroflory zajmuje trochę czasu. Podejścia oparte na zrozumieniu interakcji między antybiotykami a florą jelitową torują drogę dla nowych strategii wsparcia. Wiedza ta otwiera obiecujące perspektywy dla utrzymania zdrowej mikroflory i zapobiegania dysbiozie po leczeniu.
Jak odbudować mikroflorę jelitową po kuracji antybiotykowej?
Jak rozmawiać o zdrowiu jelit: porady prof. Sokola. Ta seria filmów edukacyjnych ma na celu pomóc pracownikom służby zdrowia w lepszej komunikacji z pacjentami na temat mikroflory jelitowej.
Jak odbudować mikroflorę jelitową po kuracji antybiotykowej?

Oporność na antybiotyki: poznaj wszystkie skutki
Skutki oporności na antybiotyki wykraczają poza sferę kliniczną: wpływają również na środowisko, mikroflorę i zdrowie na całym świecie. To globalne zjawisko wymaga zintegrowanego podejścia „jedno zdrowie”, aby było skuteczne. Nadszedł czas na zrozumienie, zapobieganie i współpracę.
Zapoznaj się z naszymi artykułami, aby poznać pełen zakres skutków oporności i rozwiązania rozważane w skali globalnej:
 11.01.2024
Gdy podróże prowadzą do oporności na antybiotyki
Czytaj więcej
11.01.2024
Gdy podróże prowadzą do oporności na antybiotyki
Czytaj więcej
 07.09.2023
W chmurach wykryto mnóstwo genów oporności na antybiotyki
Czytaj więcej
07.09.2023
W chmurach wykryto mnóstwo genów oporności na antybiotyki
Czytaj więcej
 22.02.2022
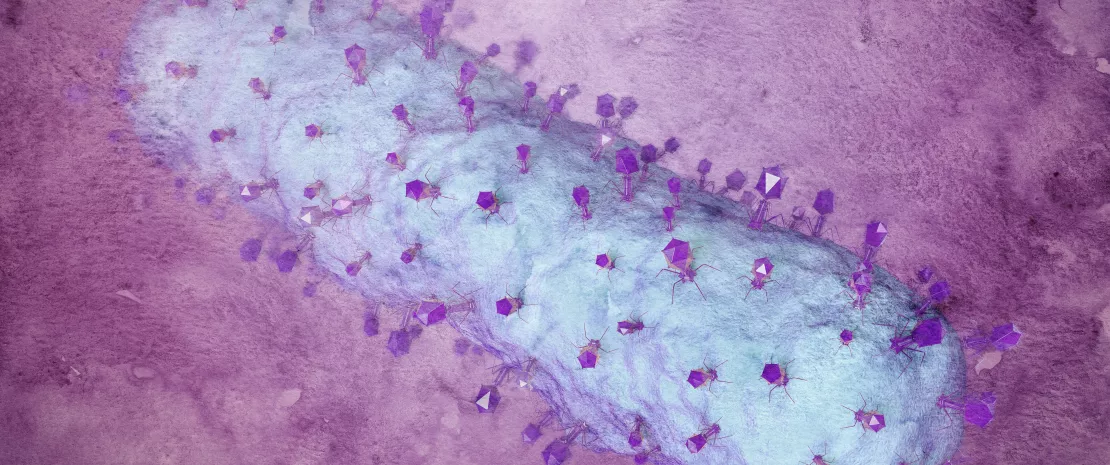
Fagi jako ratunek przy wieloopornych infekcjach?
Czytaj więcej
22.02.2022
Fagi jako ratunek przy wieloopornych infekcjach?
Czytaj więcej
 10.04.2024
Jelito w podróży: W jaki sposób podróże kształtują nasz wewnętrzny krajobraz
Czytaj więcej
10.04.2024
Jelito w podróży: W jaki sposób podróże kształtują nasz wewnętrzny krajobraz
Czytaj więcej