Mikrobiota skóry, przez długi czas uznawana głównie za źródło infekcji, jest obecnie powszechnie akceptowana jako ważny czynnik wspierający zdrowie i dobre samopoczucie1. Poprzez promowanie reakcji immunologicznych i obrony, ma ona kluczowe znaczenie dla procesu naprawy tkanek oraz dla funkcji bariery poprzez hamowanie kolonizacji lub infekcji patogenami oportunistycznymi2.
KAŻDY ZAKĄTEK SKÓRY MA WŁASNĄ MIKROBIOTĘ
Mikrobiota skóry zawiera miliony bakterii oraz, w mniejszej względnej obfitości, grzyby i wirusy. Corynebacterium, Cutibacterium (dawniej znany jako Propionibacterium), Staphylococcus, Micrococcus, Actinomyces, Streptococcusi Prevotella są najczęściej spotykanymi rodzajami bakterii żyjącymi na ludzkiej skórze3. Jednak względna obfitość bakteryjnych grup taksonomicznych w dużej mierze zależy od lokalnego mikrośrodowiska danego kawałka skóry, a zwłaszcza od jego cech fi zjologicznych, tj. od tego, czy jest on łojowy, wilgotny czy suchy. Stąd też gatunki lipofi lowe Cutibacterium dominują w miejscach łojowych, podczas gdy gatunki Staphylococcus i Corynebacterium występują szczególnie obfi cie na obszarach wilgotnych4.
OD FIZJOLOGII DO PATOLOGII, NIEJEDNOZNACZNA ROLA C. ACNES
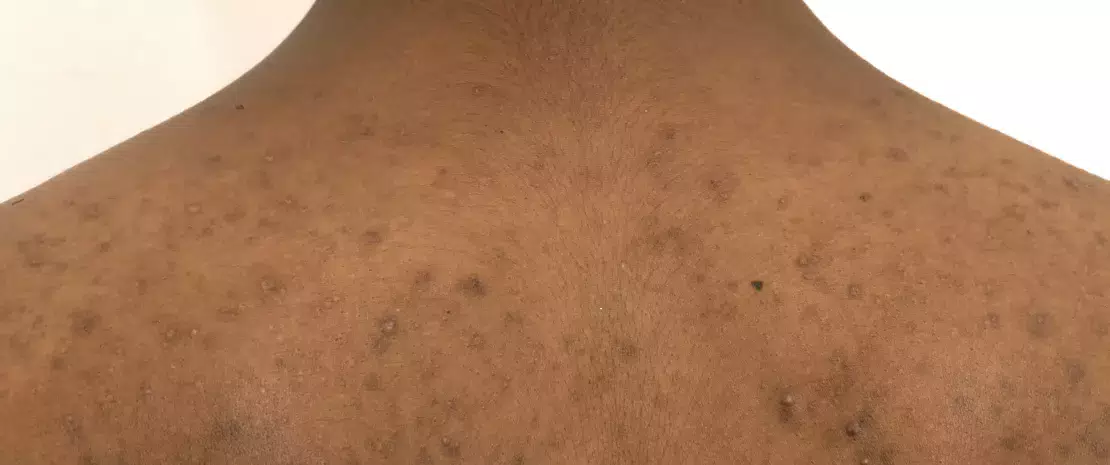
Aerotolerancyjny anaerob C. acnes jest jednym z najczęściej występujących gatunków bakterii w mikrobiomie skóry. Przyczynia się on do powstawania trądziku, przewlekłego zaburzenia zapalnego skóry o złożonej patogenezie5. W przeciwieństwie do tego, co sądzono dotychczas, ostatnie badania wykazują, że hiperproliferacja C. acnes nie jest jedynym czynnikiem zaangażowanym w rozwój trądziku6. W istocie to zaburzenie równowagi między różnymi szczepami C. acne swraz z dysbiozą mikrobioty skóry powoduje trądzik6. Ponadto interakcje między S. epidermidis a C. acnes mają kluczowe znaczenie w regulacji homeostazy skóry: S. epidermidis hamuje wzrost C. acnes i zapalenie skóry. Z kolei C. acnes, poprzez wydzielanie kwasu propionowego, który uczestniczy między innymi w utrzymaniu kwaśnego odczynu pH mieszka łojowo-włosowego, hamuje rozwój S. epidermidis. Malassezia, najczęściej występujący na skórze grzyb uważa się również za istotny czynnik występowania trądziku opornego na leczenie, ponieważ angażuje on komórki odpornościowe. Jego rola w tym procesie powinna jednak zostać lepiej zbadana6.
LECZENIE TRĄDZIKU: WAŻNA PRZYCZYNA ROZWIJANIA OPORNOŚCI NA ANTYBIOTYKI
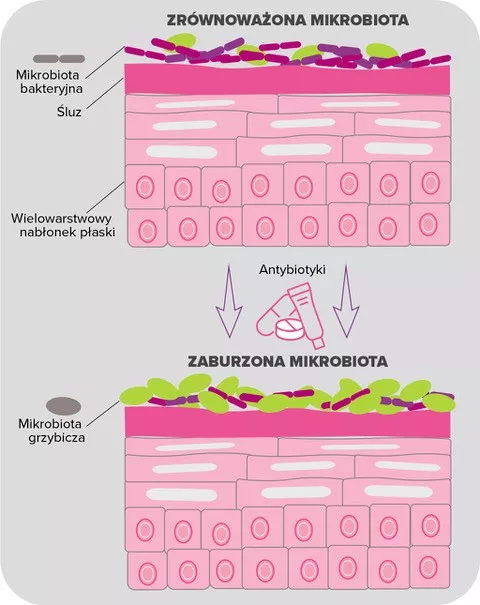
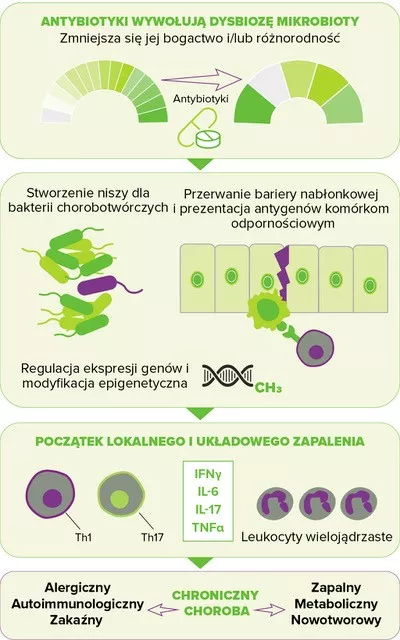
Pomimo rutynowego stosowania w leczeniu trądziku, miejscowe i doustne antybiotyki okazały się problematyczne pod wieloma względami. Największą obawą, którą wyrażają eksperci jest zakłócenie mikrobioty skóry, chociaż dokładne dane na ten temat pozostają ograniczone. W tym kontekście przeprowadzono w niedawnym czasie badania długoterminowe, w których porównano mikrobiotę policzkową 20 pacjentów z trądzikiem przed i po sześciu tygodniach doustnego leczenia doksycykliną. Co ciekawe, ekspozycja na antybiotyki wiązała się ze wzrostem różnorodności bakteryjnej; według autorów może to być spowodowane zmniejszoną kolonizacją przez C. acnes, co stworzyło przestrzeń umożliwiającą wzrost populacji innych bakterii7.
Jednak najpoważniejsze zastrzeżenie związane ze stosowaniem antybiotyków w leczeniu trądziku dotyczy oporności bakterii. Cechę tę zaobserwowano po raz pierwszy w latach 70. XX wieku, natomiast od lat 80. stanowi ona główny przedmiot niepokoju wśród dermatologów8. Oporność C. acnes jest zdecydowanie najlepiej udokumentowana: najnowsze dane potwierdzają, iż wskaźnik oporności na erytromycynę w niektórych krajach wynosi ponad 50%, a wskaźnik oporności na azytromycynę i klindamycynę odpowiednio 82 -100% i 90%. Jeśli chodzi o tetracykliny, choć nadal w dużej mierze skuteczne wobec większości szczepów C. acnes, ich wskaźniki oporu rosną, wahają się od 2% do 30% w różnych regionach geografi cznych9.Oporność na antybiotyki nie ogranicza się do C. acnes: jak wykazano, antybiotyki stosowane miejscowo u pacjentów z trądzikiem (zwłaszcza w monoterapii) zwiększają występowanie opornych bakterii skóry, takich jak S. epidermidis, natomiast antybiotyki stosowane doustnie przyczyniają się do częstszego pojawienia się opornych na antybiotyki bakterii ustno-gardłowych S. pyogenes10,8. Ponadto zaobserwowano, iż zwiększenie częstości występowania infekcji górnych dróg oddechowych i zapalenia gardła wiąże się ze stosowaną wobec trądziku antybiotykoterapią11,12.
APEL O OGRANICZENIE STOSOWANIA ANTYBIOTYKÓW W LECZENIU TRĄDZIKU
Potencjalne konsekwencje oporności na antybiotyki wywołane leczeniem trądziku są rozliczne: niepowodzenie samego leczenia trądziku (patrz Przypadek kliniczny), zakażenie patogenami oportunistycznymi (miejscowo lub ogólnoustrojowo) czy też rozprzestrzenianie się oporności wśród populacji8.Mimo to ilość antybiotyków przepisywanych na trądzik wciąż pozostaje na wysokim poziomie, a długość ich stosowanie znacznie przekracza czas zalecany w wytycznych13. W obliczu rosnącej listy obaw, eksperci wzywają do ograniczenia stosowania antybiotyków w leczeniu trądziku13. Szczególna strategia w tym zakresie została zaproponowana przez Globalny Sojusz na rzecz Poprawy Efektów Leczenia Trądziku (patrz ramka poniżej).