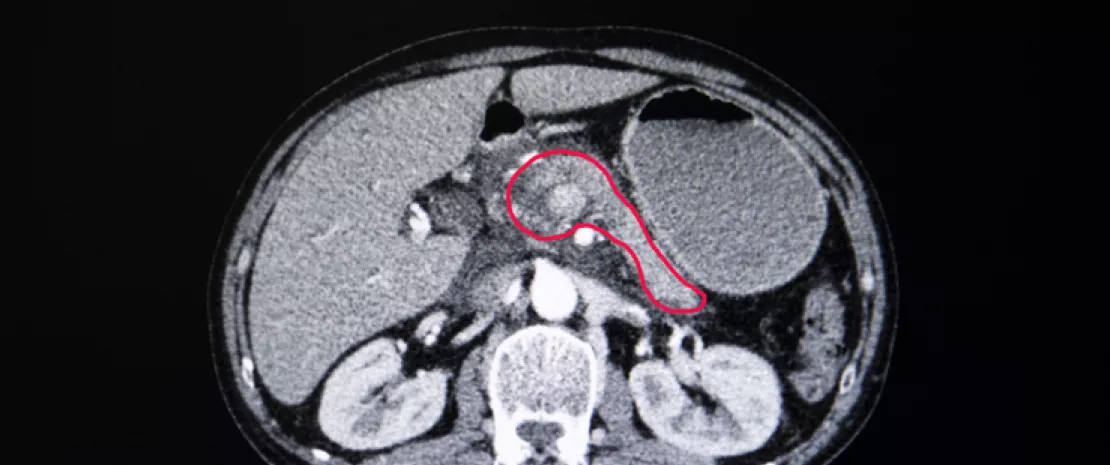
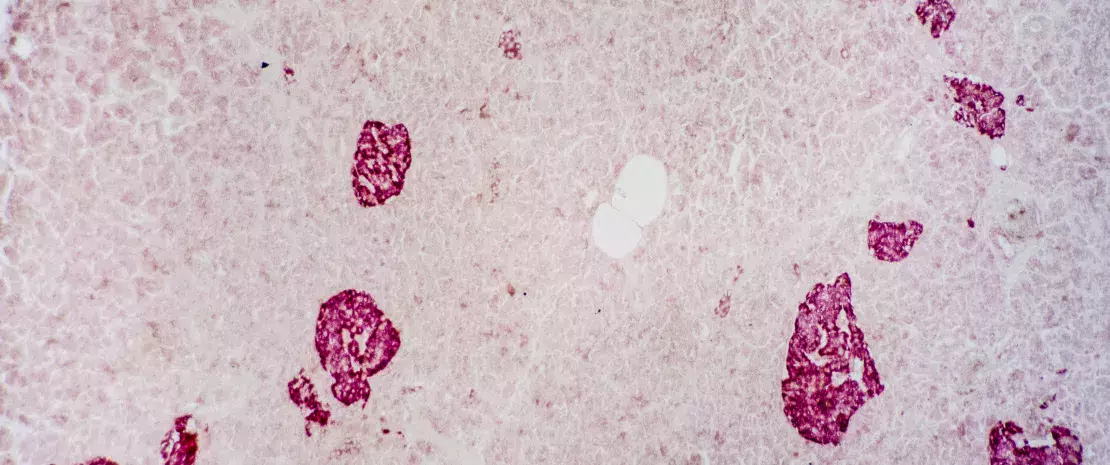
Cukrzyca typu 1 (DT1) to choroba autoimmunologiczna prowadząca do zniszczenia komórek β trzustki. Dane z badań na myszach wskazują, że interakcje między mikrobiotą jelit a systemem wrodzonej odporności mają udział w rozwoju tej choroby, a jej postępy można spowolnić przeszczepem mikrobioty kałowej (FMT).
Transplantacja autologiczna a allogeniczna
W randmizowanym badaniu kontrolowanym pacjenci, u których niedawno zdiagnozowano DT1 otrzymali 3 FMT przez sondę nosowo-dwunastnicową w czasie t = 0, 2 lub 4 miesiące. Przeszczep pochodził z ich własnego stolca (FMT autologiczny, n = 10) lub od zdrowych dawców (FMT allogeniczny, n = 10). W ciągu roku po pierwszym FMT naukowcy oceniali resztkowe działanie komórek β (poprzez wydzielanie peptydu C w reakcji na posiłek testowy), a także zmiany metabolizmu, odporności i mikrobioty wynikające z obu FMT.
Zachowane działanie trzustki
Przeciwnie niż oczekiwali badacze, w rok po pierwszym FMT funkcjonowanie komórek β w grupie autologicznej zostało utrzymane. Pogorszyło się natomiast w grupie allogenicznej, ale w mniejszym stopniu niż u chorych na DT1 pacjentów, którzy nie otrzymali leczenia w ciągu roku po diagnozie1. Zdaniem naukowców korzystne działanie FMT jest wyraźniejsze i trwalsze w przypadku wysokiej zgodności immunologicznej dawcy i biorcy.
Czy Desulfovibrio piger ma z tym coś wspólnego?
Okazało się, że zmiany składu mikrobioty mają związek z pewnymi zmianami metabolizmu i odporności. W dwunastnicy Prevotella spp. była odwrotnie skorelowana z resztkowym działaniem komórek β. W okrężnicy ilość Desulfovibrio piger znaczne rosła tylko w wyniku autologicznego FMT. Znaczna liczebność tej bakterii wiąże się z lepszym resztkowym działaniem komórek β, a także z poziomem 1-arachidonoilu-GPC (A-GPC) – metabolitu bakteryjnego związanego ze zwiększonym wytwarzaniem peptydu C. Co więcej, duża liczebność D. piger była ujemnie skorelowana z poziomem niektórych limfocytów T związanych z odpornością. Jak to tłumaczą autorzy? D. piger może hamująco wpływać na odporność poprzez niszczenie limfocytów w drodze produkcji A-GPC. Biorąc pod uwagę znaczną liczbę stwierdzonych korelacji, badacze wybrali mechanizmy oddziaływania, które będą badać bardziej szczegółowo w celu ustalenia wpływu FMT na DT1, a także nowo zidentyfikowanego potencjału terapeutycznego niektórych gatunków.
1. Overgaard AJ, Weir JM, Jayawardana K, et al. Plasma lipid species at type 1 diabetes onset predict residual beta-cell function after 6 months. Metabolomics 2018;14:158; Lachin JM, McGee PL, Greenbaum CJ, et al. Sample size requirements for studies of treatment effects on beta-cell function in newly diagnosed type 1 diabetes. PLoS One 2011;6:e26471.