Długo uznawane za źródło infekcji mikroorganizmy są dziś często dzielone na „dobre” i „złe”. Czy tego manichejskiego punktu widzenia nie należałoby zniuansować?
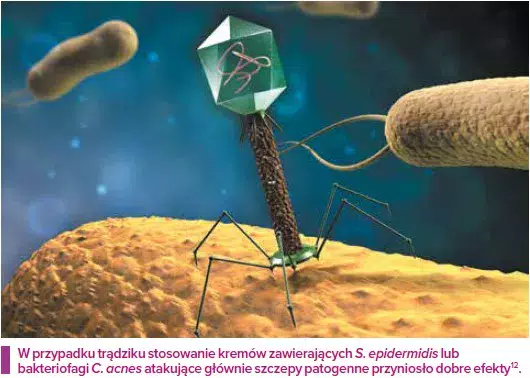
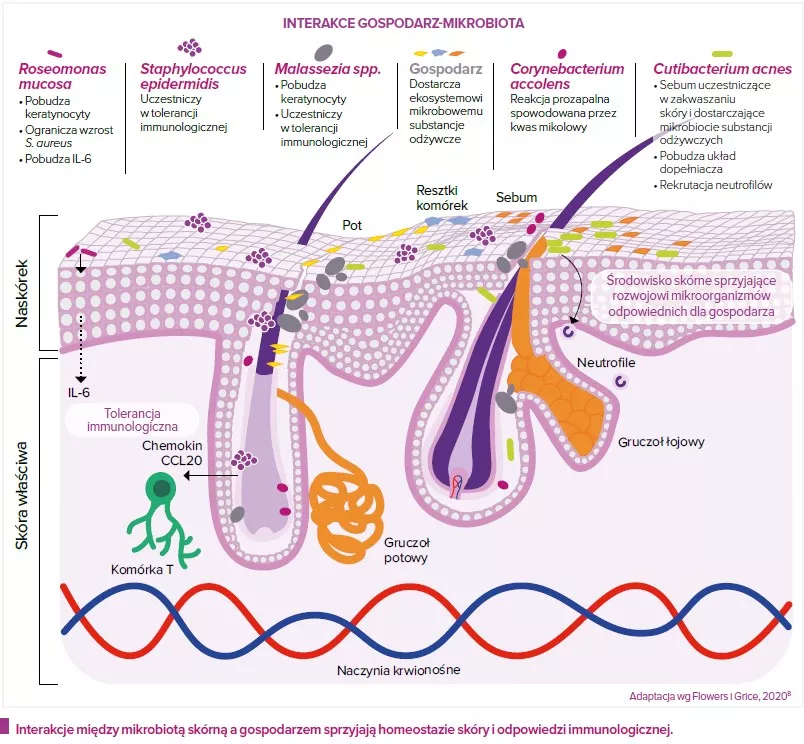
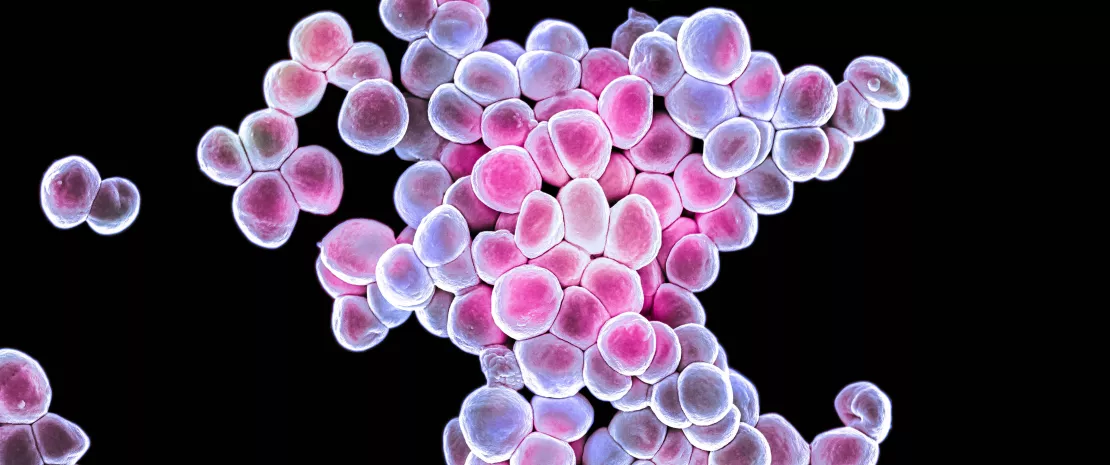
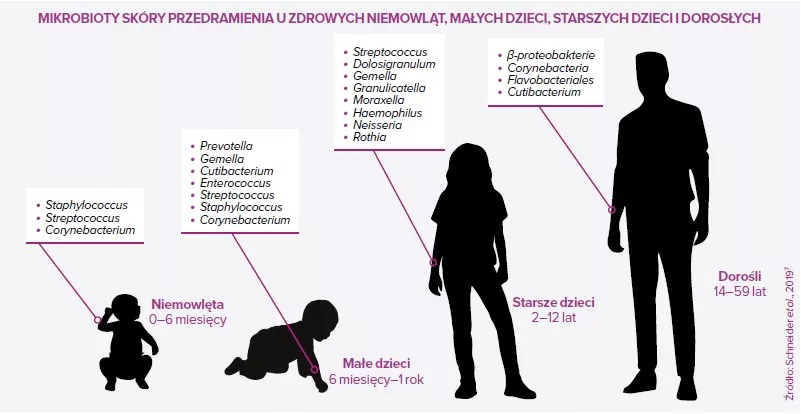
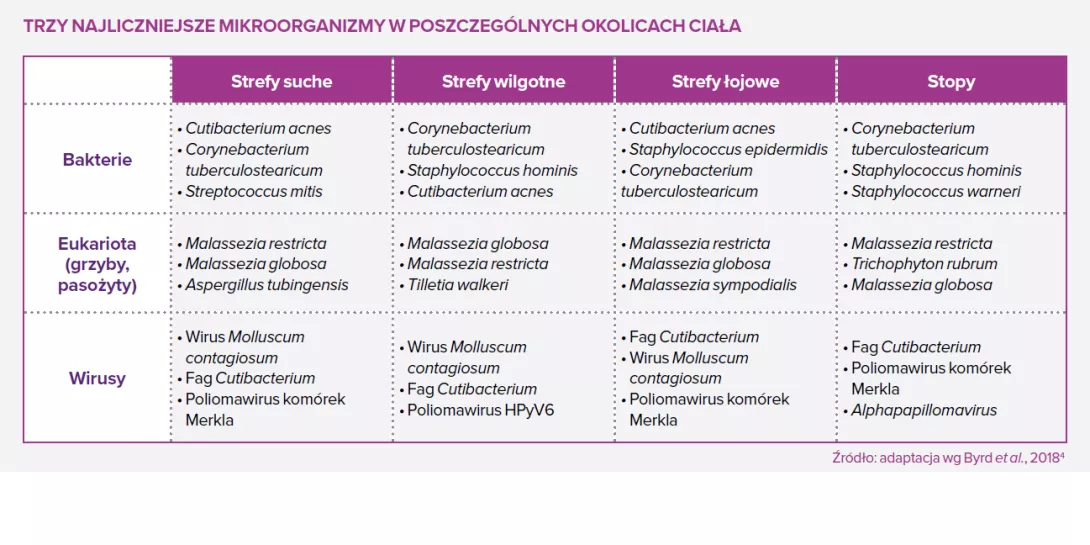
Mikroby nie są ani „dobre”, ani „złe”. Nie są naszymi „przyjaciółmi” ani „wrogami”. Ta ludzka klasyfikacja nie ma do nich zastosowania. Nawet najłagodniejszy mikroorganizm może zabić, jeżeli układ odpornościowy jest osłabiony. Jednak dobrze wiadomo, że istnieje wiele mikroorganizmów, które w pewnych okolicznościach mogą być korzystne dla gospodarza, natomiast inne są na ogół chorobotwórcze. Na przykład bakterii staphylococci na skórze człowieka żyje bardzo wiele. S. aureus ma raczej złą opinię: kojarzy się go z infekcjami ran i z licznymi patologiami skóry. Zawiera wiele genów wirulencji, a jego postać wieloodporna (MRSA) jest postrachem szpitali. Natomiast wiele badań wykazało ostatnio, że S. epidermidis może pobudzać układ odpornościowy i mechanizmy obronne skóry, a nawet niszczyć biofilmy S. aureus. S. epidermidis jest jednak częstą przyczyną infekcji związanych z implantami i również może stać się wieloodporny na antybiotyki (MRSE), a wielu osób, których organizmy są skolonizowane przez S. aureus, nie odczuwa z tego powodu żadnych problemów. W związku z tym samo obniżenie proporcji S. aureus w porównaniu z S. epidermidis na skórze czasem może nie być dobrą metodą poprawy jej stanu. Należy dążyć do właściwej równowagi między tymi dwoma gatunkami.
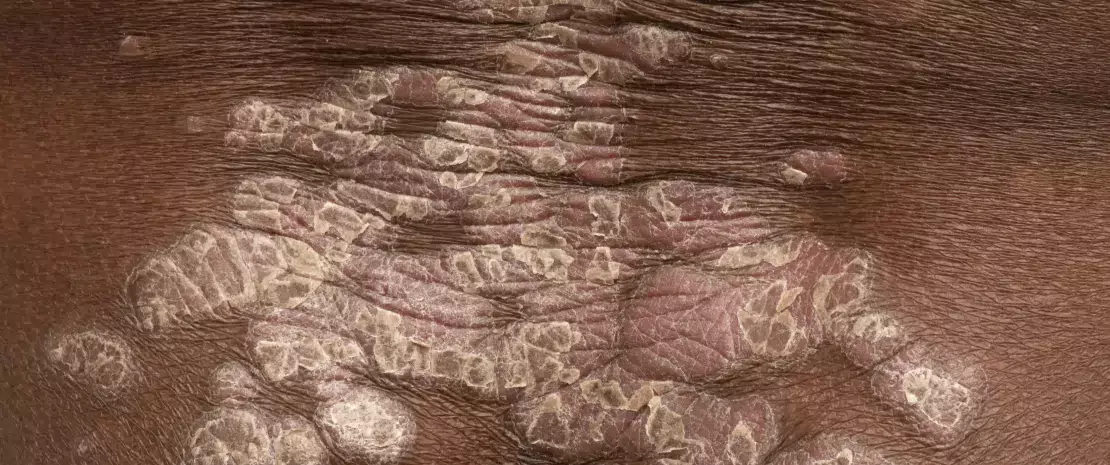
Jakie mikroorganizmy wchodzą w grę w przypadku atopowego zapalenia skóry?
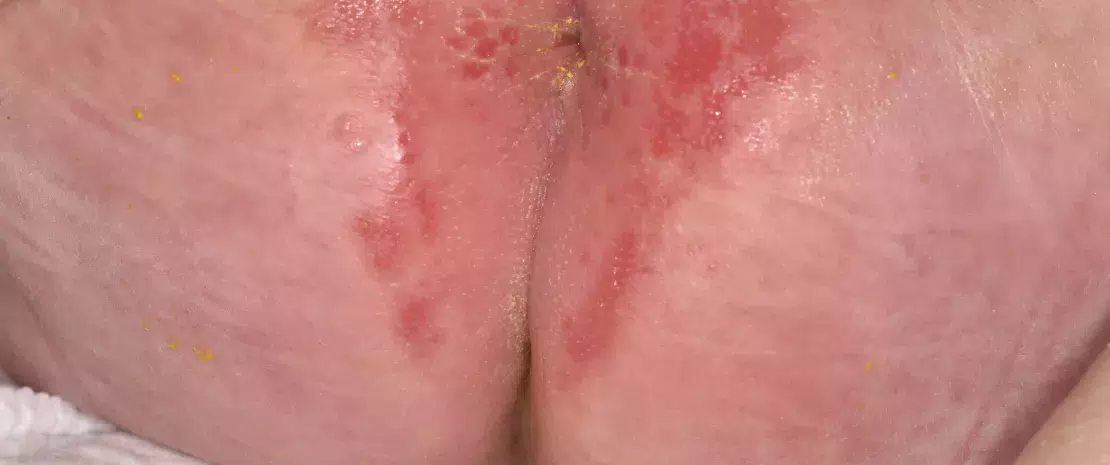
Mikroorganizmy prawdopodobnie nie są pierwotną przyczyną tej choroby, ale bardzo się przyczyniają do jej intensywności. Dotknięte nią obszary skóry może charakteryzować dysbioza mikrobowa: większa liczebność S. aureus, a mniej typowych bakterii skórnych, takich jak Cutibacterium i Corynebacterium. Możliwe, że S. aureus korzysta z osłabienia bariery skóry spowodowanego na przykład przez zaburzenie wytwarzania antymikrobowych peptydów skórnych i/lub mutacjami genów filagryny1 powodującymi suchość i pękanie skóry. Stany zapalne skóry leczy się zazwyczaj antybiotykami, ryzykując wielkie szkody w pożytecznej części mikrobioty skórnej i powstanie odporności na antybiotyki. Strategie probiotyczne zmierzające do zwiększenia/odtworzenia liczebności gronkowców koagulazoujemnych (SCN) są rozpatrywane jako metoda opcjonalna i/lub uzupełniająca.
Czy probiotyki stosowane miejscowo i/lub doustnie mogą zapobiegać chorobom skóry albo je leczyć? Jakie jest, a jakie będzie ich miejsce w strategiach terapeutycznych?
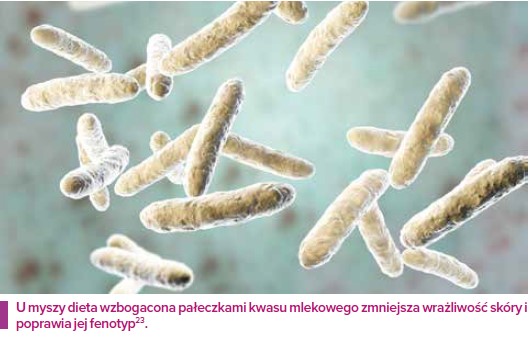
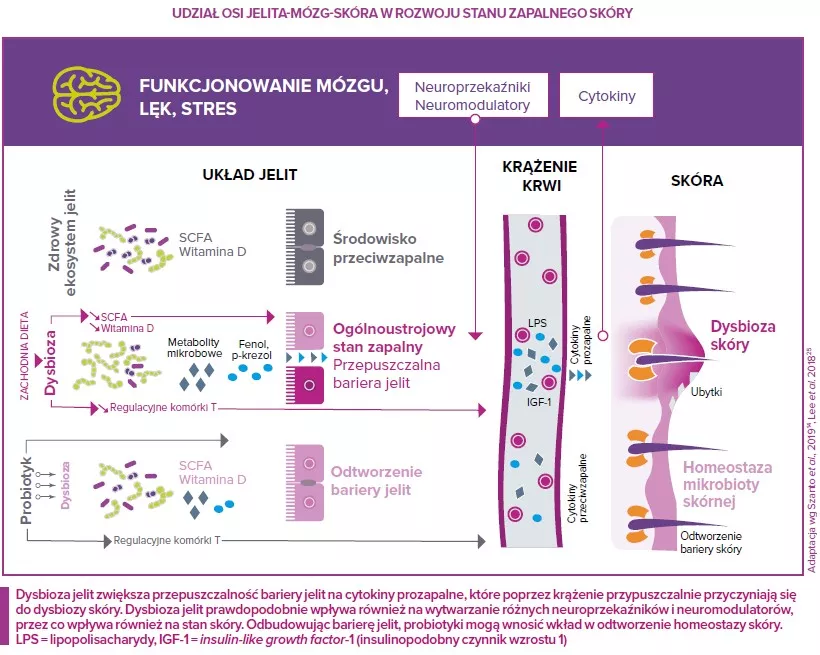
Dodatek żywych mikroorganizmów (probiotyków) z pewnością może korzystnie wpływać na zdrowie gospodarza, na przykład poprzez zmniejszenie liczebności patogenów lub pobudzenie mechanizmów obronnych i układu odpornościowego gospodarza. Istnienie osi jelita-skóra sugeruje możliwość, że doustne przyjmowanie probiotyków również może mieć korzystny wpływ na skórę. Jednak w przypadku większości (o ile nie wszystkich) poważnych chorób skóry rola mikrobioty skórnej nie jest jeszcze jasna. Towarzyszą im wyraźne zmiany struktury (składu kolonii) i funkcjonowania (właściwości fizjologicznych) mikrobioty skórnej, ale nie jest jasne, czy zmiany te są przyczyną, czy skutkiem choroby. Klasyczny problem: „jajko czy kura”. Moim zdaniem jest zatem zbyt wcześnie na nadzieję, że zwykły krem lub kapsułka z probiotykiem może wnieść istotny wkład w zapobieganie, a nawet leczenie poważnych chorób skóry. Poza tym badania przewodu pokarmowego wykazały, że w porównaniu z klasyczną terapią chemiczną działanie probiotyków jest raczej łagodne i zależy od tylu czynników, że trudno przejść od wysoko wystandaryzowanych modeli zwierzęcych do człowieka. Tylko solidne badania kliniczne pozwolą wykazać skuteczność probiotyków. O ile jednak jest zbyt wcześnie, aby wypowiadać się na temat najcięższych chorób, stosowanie probiotyków wydaje mi się uzupełniająca opcją terapeutyczną w przypadku niezbyt poważnych chorób skóry oraz cenną metodą doskonalenia produktów do pielęgnacji skóry. Wiadomo już bowiem, że zrównoważona, różnorodna mikrobiota charakteryzuje skórę zdrową, zatem logiczna wydaje się ochrona i utrzymanie tego stanu, również przy użyciu probiotyków, na przykład w przypadku skóry zanieczyszczonej, wrażliwej, swędzącej itp.
Polecane przez naszą społeczność