Zakaźny nieżyt żołądka i jelit
Dzieci, młodzież, dorośli... Trudno przeżyć życie bez zetknięcia się chociaż raz z nieżytem żołądka i jelit. Jest on drugą najczęstszą przyczyną śmierci na świecie.1 Spokojnie – nieżytu tego można uniknąć, zachowując higienę. Jest jednak coraz lepiej leczony.2 Ponadto działania zmierzające do odtworzenia mikrobioty jelit mogą złagodzić objawy i skrócić czas ich występowania.3
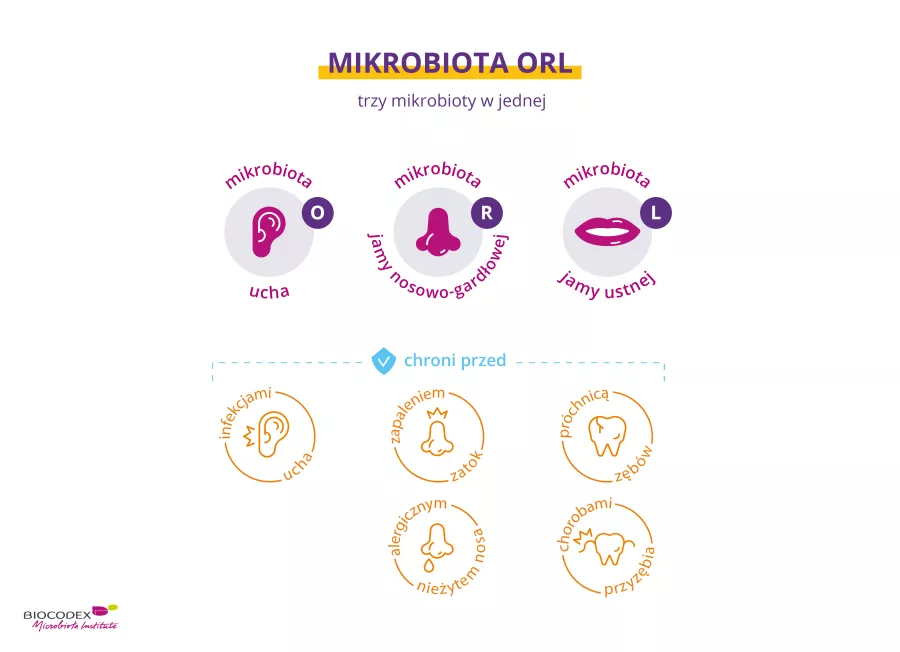
Mikrobiota jelit Biegunka podróżnych
Co to jest zakaźny nieżyt żołądka i jelit? Jaki ma związek z mikrobiotą jelit?
Nieżyt żołądka i jelit to choroba biegunkowa, często o bardzo silnych objawach, które w większości przypadków szybko ustępują.4 U dotkniętych nią pacjentów obserwuje się zaburzenie równowagi mikrobioty jelit.5 Może ona trwać po wyleczeniu infekcji. Wiąże się z podwyższonym ryzykiem wystąpienia chorób przewlekłych.6
Czy wiesz, że...?
Czy wiesz, że...? Angielska nazwa tej choroby, gastroenteritis, pochodzi od greckich słów gastron (żołądek) i enteron (jelito cienkie). Nazwa ta oznacza zapalenie żołądka i jelita cienkiego.7
Stosunkowo łagodny w krajach Zachodu nieżyt żołądka i jelit jest jedną z głównych przyczyn zgonów w krajach rozwijających się, zwłaszcza u dzieci w wieku poniżej 5 lat.4 Jest on w tych krajach wielkim problemem z dziedziny zdrowia publicznego, ponieważ odpowiada za 10% zgonów dzieci.1 Największą śmiertelnością charakteryzują się kraje rozwijające się,8 gdzie hospitalizacja często9 jest związana z ciężkim odwodnieniem powodowanym przez tę chorobę. Skąd to się bierze? Przyczyną jest połknięcie (sidenote: Patogen To mikroorganizm, który powoduje lub może spowodować chorobę Pirofski LA, Casadevall A. Q and A: What is a pathogen? A question that begs the point. BMC Biol. 2012 Jan 31;10:6. ) mikroorganizmu. Najczęściej jest to wirus. Mamy wtedy do czynienia z wirusowym nieżytem żołądka i jelit.
Rotawirus jest jedną z głównych przyczyn wirusowego nieżytu żołądka i jelit na świecie oraz śmiertelnych biegunek u dzieci w krajach rozwijających się, mimo że istnieje szczepionka.10 Oczywiście, chorobę mogą powodować również inne wirusy (norowirus, adenowirus itp)4. Nieżyt żołądka i jelit może jednak być spowodowany również przez bakterię (bakteryjny nieżyt żołądka i jelit) lub przez pasożyta, zwłaszcza podczas podróży.7 Rzadko jednak udaje się ustalić, z jakim patogenem mamy do czynienia.11
Źródłem zakażenia jest skażone pożywienie lub woda, a także bezpośrednie kontakty międzyludzkie połączone z zaniedbaniem higieny.6 Dane wykazujące związek między mikrobiotą jelit a nieżytem żołądka i jelit są na razie bardzo ograniczone. Niemniej jednak podczas infekcji – niezależnie od jej przyczyny – u pacjentów obserwuje się zaburzenie równowagi jelit ( (sidenote: Dysbioza Dysbioza nie jest zjawiskiem jednorodnym; przybiera różne formy zależne od stanu zdrowia danej osoby. Zazwyczaj definiuje się ją jako zaburzenie składu i funkcjonowania mikrobioty spowodowane przez zestaw czynników środowiskowych i osobniczych zakłócających ekosystem mikroorganizmów. Levy M, Kolodziejczyk AA, Thaiss CA, et al. Dysbiosis and the immune system. Nat Rev Immunol. 2017;17(4):219-232. ) ).5,12,13 Z badań wynika, że dzieci cierpiące na ciężki nieżyt żołądka i jelit z powikłaniami– zwłaszcza dzieci zakażone rotawirusem – wykazują zmniejszone zróżnicowanie mikrobioty jelit w porównaniu z dziećmi zdrowymi.14 Inne badania sugerują, że zmiany mikrobioty jelit mogą trwać długo i niekorzystnie wpływać na zdrowie. Sprzyjają przede wszystkim występowaniu zespołu jelita drażliwego.15 Aktualne dane dotyczące roli mikrobioty jelit w powstawaniu, rozwoju, powikłaniach i ewolucji choroby wymagają szerzej zakrojonych badań.
Objawy bywają bardzo silne, ale nie trwają długo
Oprócz biegunki (czyli co najmniej trzech miękkich lub płynnych wypróżnień w ciągu dnia)6 mogą wystąpić inne objawy, takie jak mdłości, wymioty, bóle brzucha, gorączka lub jadłowstręt.16 Objawy wirusowego nieżytu żołądka i jelit zazwyczaj trwają krócej niż tydzień. Najczęściej ustępują po 1–3 dniach.4 Największej uwagi wymagają dzieci, osoby starsze i o osłabionej odporności, które są najbardziej narażone na odwodnienie.4 W niektórych przypadkach lekarz może zlecić dodatkowe badania (analizę stolca, morfologię krwi itp.), żeby wykluczyć inne choroby.4
Antybiotyki często są bezużyteczne, a nawet przeciwskuteczne
Niezależnie od przyczyny nieżytu żołądka i jelit leczy się go objawowo.4 W przypadku biegunki podstawowym leczeniem jest nawadnianie.6 Leczenie antybiotykami ma uzasadnienie tylko w przypadku ustalenia, że biegunka ma charakter bakteryjny.11 W przypadku zakażenia wirusowego antybiotyki mogą się okazać wręcz przeciwskuteczne!11 Natomiast przyjmowanie probiotyków, których celem jest odtworzenie mikrobioty jelit, może ograniczyć nasilenie i czas trwania objawów.7,17
Niniejszy artykuł jest oparty na potwierdzonych źródłach naukowych, ale nie zastępuje porady lekarza. W przypadku wystąpienia objawów należy zasięgnąć porady lekarza rodzinnego lub pediatry.