КИШЕЧНАЯ МИКРОБИОТА #21
Проф. Сату Пеккала (Satu Pekkala)
Научный сотрудник Академии Финляндии, Факультет спорта и здравоохранения, Университет Ювяскюля, Финляндия

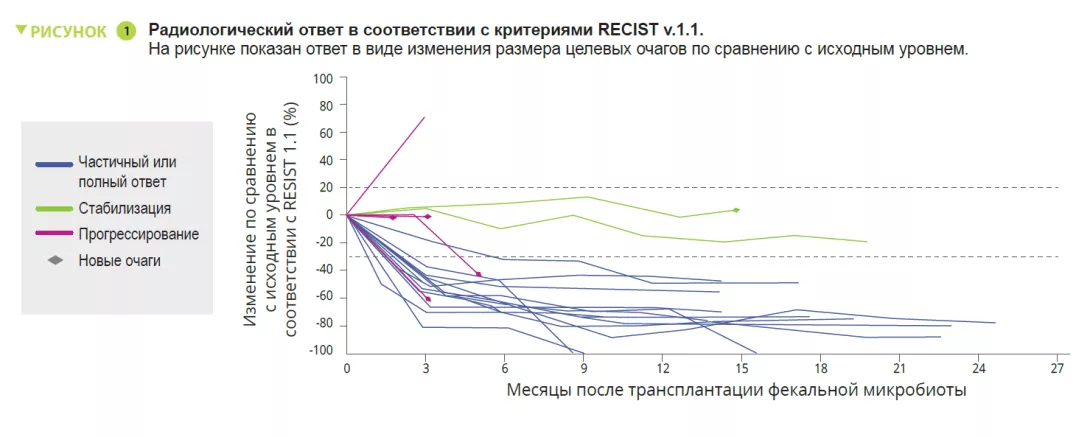
Кишечная микробиота как предиктор тяжести острого панкреатита
У пациентов с тяжелым острым панкреатитом (ОП) высок риск смерти, поэтому важно определить характер течения заболевания в первые несколько часов. Существующие сложные системы подсчета баллов не могут предсказать тяжесть ОП достаточно рано, поэтому необходимы новые маркеры.
Хотя, по-видимому, существует двусторонняя связь между ОП и кишечным микробиомом, крупные проспективные клинические исследования, доказывающие это, отсутствуют. В данной работе представлены результаты исследования микробиома полости рта и кишечника 450 пациентов с ОП из 15 европейских центров. Состав микробиоты определяли методом полноразмерного секвенирования 16S рРНК и метагеномного секвенирования с использованием Oxford Nanopore. Согласно пересмотренной Атлантской классификации (RAC) выделяют следующие категории тяжести ОП: легкий, умеренный и тяжелый (RAC I-III, соответственно). Результаты исследования показали, что расстояние Брея-Кертиса для ректальных микробиомов отличалось при RAC III по сравнению с RAC I и RAC II. Кроме того, отмечалось дифференциальное преобладание нескольких видов бактерий в зависимости от категории RAC. Расстояния Брей-Кертиса также различались между живыми и умершими пациентами в ректальных, но не буккальных микробиомах. Помимо смертности, продолжительность пребывания в стационаре также была связана с ранними изменениями ректального микробиома.
Авторы обнаружили различия между 16 видами бактерий при тяжелой форме ОП по сравнению с нетяжелыми формами. При использовании регрессии Риджа эти виды вместе с наличием синдрома системного воспалительного ответа могли точно прогнозировать тяжесть заболевания. Интересно, что все эти виды производят короткоцепочечные жирные кислоты (КЦЖК). Соответственно, функциональные пути продукции КЦЖК были более активными при тяжелом ОП. Несмотря на интригующие результаты, до сих пор неизвестно, являются ли бактерии, продуцирующие КЦЖК, причиной или следствием тяжелого ОП.

Связь кишечного микробиома и сахарного диабета 2 типа в Объединенных Арабских Эмиратах
Заболеваемость сахарным диабетом 2 типа (СД2) в странах Ближнего Востока быстро растет. Несколько западных исследований показали влияние кишечного микробиома на возникновение резистентности к инсулину, связанной с СД2, и слабого воспаления, однако подобных исследований в популяциях Ближнего Востока мало. Кроме того, в имеющихся исследованиях получены непоследовательные данные о том, как состав и функции микробного сообщества влияют на патогенез СД2.
Чтобы получить больше информации, авторы проанализировали образцы кала 84 человек из Объединенных Арабских Эмиратов с СД2 или без него, используя метод нанопорового секвенирования метагенома. В отличие от многих более ранних западных исследований, в этом исследовании не удалось найти различий в альфа-разнообразии кишечной микробиоты между здоровыми людьми и пациентами с СД2. Кроме того, после поправки на множественные сравнения авторы не обнаружили специфических изменений преобладания каких-либо микробных видов или признаков из биологической базы данных KEGG orthology (KO) между группами. Однако, по результатам анализа представленности групп генов удалось выявить 8 функций с более высокой распространенностью в контрольной группе и 5 — в группе СД2. Эти различно представленные функции были связаны с катаболизмом мочевины, аминокислот, таких как аргинин, и гомоацетогенезом. Эти функции, по-видимому, оказывают провоспалительное действие и, таким образом, могут способствовать развитию слабого воспаления, что является отличительной чертой СД2. Наконец, авторы использовали прогностический анализ, по результатам которого были выявлены 3 потенциальных биомаркера СД2: уменьшение популяции Enterococcus faecium и Blautia, а также увеличение популяций Absiella spp или Eubacterium limosum. Интересно, что E. faecium ассоциировалась со снижением уровней липидов и уменьшением выраженности ожирения, из чего можно сделать вывод, что она может в той или иной мере участвовать в развитии СД2.
В заключение можно сказать, это в этом исследовании были выявлены специфические микробные биомаркеры, включая функции и таксоны, которые могут помочь в прогнозировании риска возникновения специфических заболеваний, связанных с СД2.

Микробный бутират ингибирует иммуносупрессивные факторы при раке желудка
Рак желудка (РЖ) является одной из ведущих причин смерти от онкологических заболеваний в мире. Раннее выявление очень важно для успешного лечения РЖ. Лиганд белка программируемой гибели-1 (PD-L1), мишень иммунотерапии рака, в больших количествах экспрессируется в опухоль-ассоциированных макрофагах, и эта экспрессия может регулироваться кишечным микробиомом. Одним из возможных способов, посредством которого микробиом может оказывать противоопухолевое действие, является производство короткоцепочечных жирных кислот, включая бутират.
В этом исследовании у пациентов с распространенным РЖ отмечалась более выраженная экспрессия иммуносупрессивных маркеров, а именно PD-L1 и интерлейкина (IL)- 10, в макрофагах, дендритных клетках и слизистой оболочке желудка, чем у здоровых добровольцев из контрольной группы. Кишечная микробиота пациентов с РЖ характеризовалась меньшим разнообразием и дисбиозом. На уровне рода у пациентов с РЖ содержалось меньше бактерий, продуцирующих бутират, таких как Faecalibacterium и Bifidobacterium. Интересно, что введение бутирата и Faecalibacterium в мононуклеарные клетки периферической крови пациентов с РЖ снижало количество макрофагов, экспрессирующих PD-L1 и IL-10. Кроме того, бутират подавлял рост культивируемых клеток РЖ. Однако оставалось неясным, какой штамм
Faecalibacterium «работал» в эксперименте in vitro. Наконец, мышам вводили клетки РЖ, а затем мононуклеарные клетки периферической крови от здоровых добровольцев или онкологических пациентов с бутиратом или без него. Эксперимент показал, что бутират значимо уменьшал размеры опухолей и уровни иммуносупрессивных маркеров PD-L1 и IL- 10. Таким образом, бутират может обладать терапевтическим потенциалом за счет подавления роста раковых клеток при РЖ.