Интимная гигиена и женская микробиота: вульва, влагалище, мочевой пузырь и перианальная область
В чем разница между вульвой и влагалищем? (смущенный смайлик) Интимная гигиена? (Второй смущенный смайлик)... Женщины часто стараются избегать подобных вопросов. Практический урок анатомии и разбор полезных привычек.
Несмотря на успехи феминисток 2000-х, молодых людей и девушек намного больше смущают вопросы о женских гениталиях, чем представителей старших поколений. Женщины за сорок чаще покупают «освежающие» интимные дезодоранты, в то время как молодежь предпочитает (sidenote: Вульвопластика пластическая операция на вульве, направленная на увеличение или уменьшение размера или объема больших половых губ. ) 1, заботясь больше о внешнем виде. Кажется, у каждого поколения - свое представление об интимности. Тем не менее, гигиена и здоровье интимной зоны важны в любом возрасте; эти советы помогут развеять связанные с ними стереотипы.

Немного анатомии
Женские гениталии — анатомически малоизученная и табуированная тема, даже среди самих женщин. Медицинским работникам часто трудно понять жалобы пациенток из-за нечетких объяснений или путаницы между вульвой (наружная часть) и влагалищем (внутренняя часть) 1.
Объясняем разницу простыми словами:
вульва снаружи, а влагалище внутри!
Вульва
— это совокупность наружных половых органов женщины, видимых при осмотре 1:
- часть лобкового бугорка (лобкового возвышения или Венериного бугорка) — мясистой волосистой области над лобковой костью
- клитор — орган, отвечающий за сексуальное удовольствие, женский аналог головки полового члена
- большие половые губы — крупные внешние защитные складки кожи
- малые половые губы — расположены внутри от больших половых губ и содержат многочисленные сальные железы
- преддверие влагалища — область между малыми половыми губами, где находится вход во влагалище и, чуть выше него, наружное отверстие уретры (отверстие мочевыделительной системы).
Кожа лобкового бугорка и больших половых губ содержит сальные железы 1, выделяющие защитную гидролипидную пленку 1,2.
Вульва содержит бартолиновы железы и железы Скина, которые выделяют смазку для малых половых губ и преддверия влагалища во время полового акта 1.
Влагалище
— это внутренняя полость длиной около десяти сантиметров.
Влагалище соединяет вульву (точнее, преддверие влагалища) с шейкой матки 1.
Во влагалище можно вводить тампоны/менструальные чаши (во время менструации), пенис (во время секса), секс-игрушки и гинекологическое зеркало (во время осмотра гинекологом).
Раз мы уже здесь, давайте рассмотрим остальные отверстия. Женская промежность содержит три отверстия в следующем порядке с передней стороны:
- наружное отверстие уретры, соединенное через уретру с мочевым пузырем, который накапливает мочу и обеспечивает ее выведение наружу при мочеиспускании 2
- вход во влагалище (половая система)
- анальное отверстие (анус) (пищеварительная система)
Также выделяют:
область вокруг ануса
включает вульву и перианальную область 1.
Женская интимная микробиота
Наша интимная зона не является исключением; как и другие органы, она — дом для нескольких микробиот, а именно:
Начнем с микробиоты вульвы. Кажется, мы должны хорошо ее знать, ведь она снаружи. Тем не менее, это не так 1,3. Некоторые исследования указывают на возможное присутствие различных бактерий (Lactobacillus, Corynebacterium, Staphylococcus и Prevotella) и дрожжеподобных грибков 1,3.
Микробиота вульвы неоднородна и варьируется в зависимости от области вульвы: лобкового бугорка, больших и малых половых губ и т. д. 3.
Однако, разнообразие — ключевое слово:
- для микробиоты вульвы каждой женщины, в которой сосуществуют разнообразные (sidenote: Микроорганизмы очень мелкие живые организмы, неразличимые невооруженным глазом. К ним относятся бактерии, вирусы, грибы, археи и простейшие, обычно называемые «микробами». What is microbiology? Microbiology Society. )
- для различных женщин (ни один из перечисленных видов не встречается у всех женщин) 1.
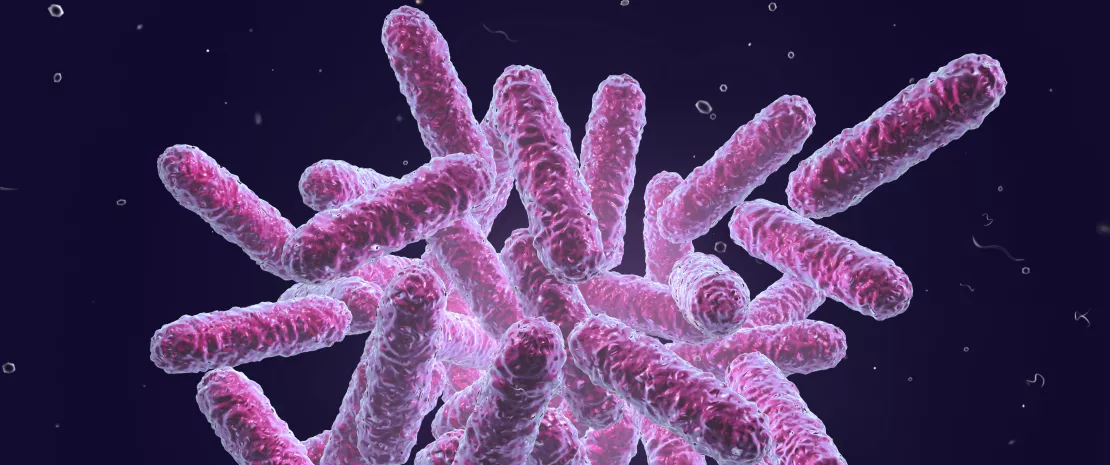
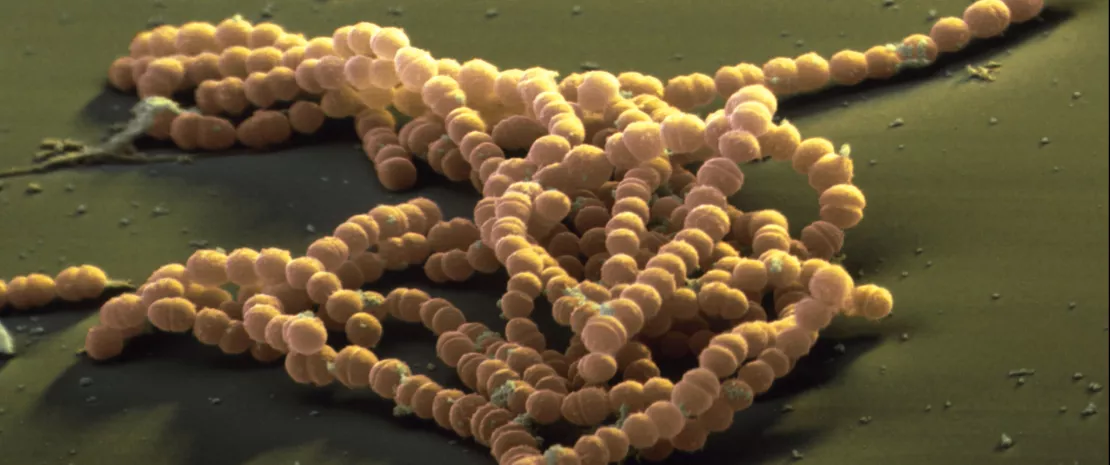
С вагинальной микробиотой (или вагинальной флорой) все обстоит иначе. Во влагалище лактобациллы (особенно Lactobacillus crispatus, Lactobacillus iners, Lactobacillus gasseri и Lactobacillus jensenii) доминируют, поддерживая кислотность за счет выработки молочной кислоты 1,4.
Кислый pH (4,0-4,5), а также перекись водорода и бактериоцины, производимые лактобациллами, подавляют (sidenote: Патоген микроорганизм, который вызывает или может вызвать заболевание Pirofski LA, Casadevall A. Q and A: What is a pathogen? A question that begs the point. BMC Biol. 2012 Jan 31;10:6. ) , включая наиболее устойчивые.
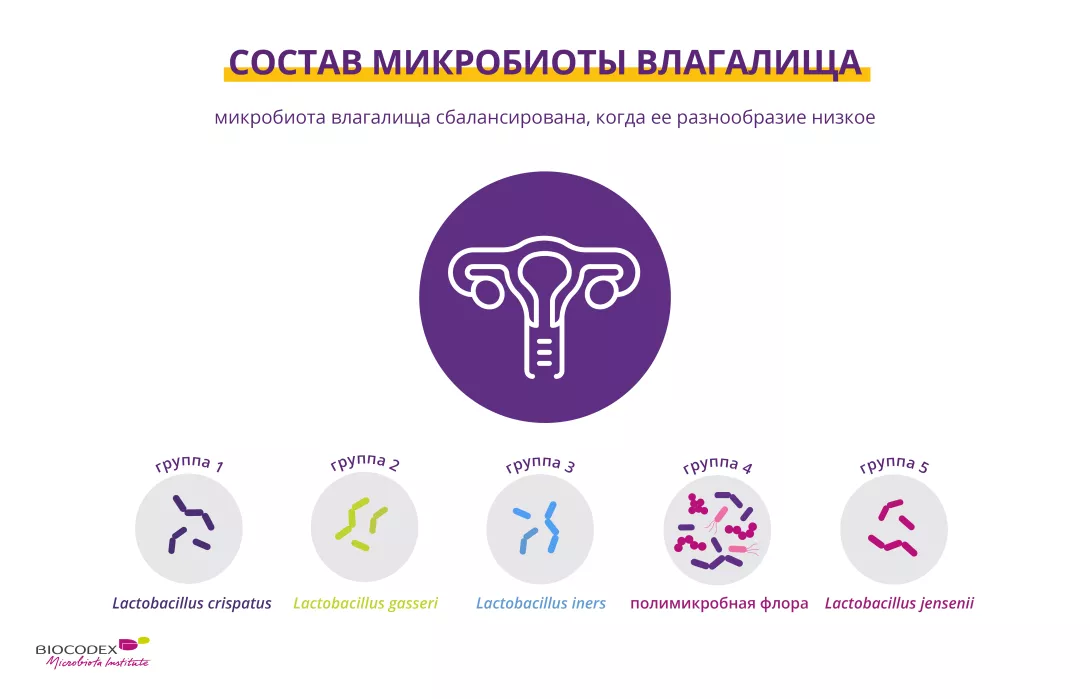
Изображение основных групп бактерий вагинального микробиота, включая лактобактерии, которые являются ключевыми для интимного баланса и профилактики инфекций.
Долгое время считалось, что микробиота мочевыводящих путей стерильна. Это ошибка, поскольку моча, содержащаяся в мочевом пузыре, также имеет микробную экосистему. Несмотря на существенные различия между микробиотой мочевыводящих путей и соседними микробиотами (анальной, вагинальной и вульварной), они имеют общие микроорганизмы 5. Она гораздо менее населена и часто характеризуется преобладанием одного типа бактерий. К ним относятся в основном лактобациллы, а также Gardnerella, Streptococcus и Corynebacterium 6.
Перианальная микробиота отражает богатое разнообразие кишечной микробиоты, особенно толстой кишки, поскольку бактерии попадают в эту область при дефекации и могут там поселиться 1.
1 из 5 Только 22% опрошенных женщин точно знали, что такое «вагинальная микробиота» (+2 балла по сравнению с 2023 годом).
Микробиоты находятся в тесном взаимодействии и обмениваются представителями
Микробиота вульвы, влагалища и перианальной области меняется со временем. Возраст, половые гормоны и внешние факторы (загрязнение, стресс, антибиотики и др.) влияют на вагинальную микробиоту 4. Дисбаланс, например, при снижении уровня эстрогена в менопаузе, приводит к потере лактобацилл, повышению pH и, как следствие, дисбиозу влагалища 7. Анальная микробиота зависит от питания и стресса: последний вкупе с тревогой вызывает воспаление, способствующее развитию патогенных бактерий в желудочно-кишечном тракте, которые затем попадают в перианальную область 1.
Близость мочеиспускательного, вагинального и анального отверстий способствует обмену микрофлорой между этими тремя областями, включая потенциальное инфицирование влагалища кишечной палочкой Escherichia coli из перианальной области 1.
Бактериальный вагиноз
Антибиотики

Чрезмерная гигиена, эпиляция и тесная одежда — неудачное сочетание
Парадоксально, но неправильная интимная гигиена может нарушить микрофлору. Чрезмерно агрессивное (особенно неподходящими средствами) или частое (более одного раза в день) мытье вульвы может повредить ее естественный защитный барьер. Вода сама по себе может вызывать сухость, зуд и жжение 8. Ароматизированное мыло, интимные спреи, лубриканты и дезодоранты, используемые женщинами для устранения запаха, зуда, боли и сухости, часто дают обратный эффект 4.
Избегайте средств:
Избегайте средств не предназначенных для интимной гигиены дезинфицирующих средств для рук, детских салфеток, масел, кремов для бритья и лосьонов для тела. Исследование показало, что 41,6% женщин используют детские салфетки для очищения вульвы, а 2,1% — для очищения влагалища 4!
Помните:
влагалище очищается самостоятельно.
Распространенная ошибка — эпиляция воском или бритье всей вульвы 1,9. Это модное явление затрагивает 84% американских женщин в пременопаузе, причем для двух третей из них это ежедневная или еженедельная практика. Хотя это часто оправдывают гигиеной, на самом деле это вредит, облегчая проникновение бактерий и вирусов. У женщин, полностью удаляющих волосы с вульвы, выявлены изменения в вагинальной микробиоте 9.
Тесная синтетическая одежда, создавая теплую и влажную среду, способствует размножению патогенов, что может вызывать зуд и урогенитальные проблемы 1.
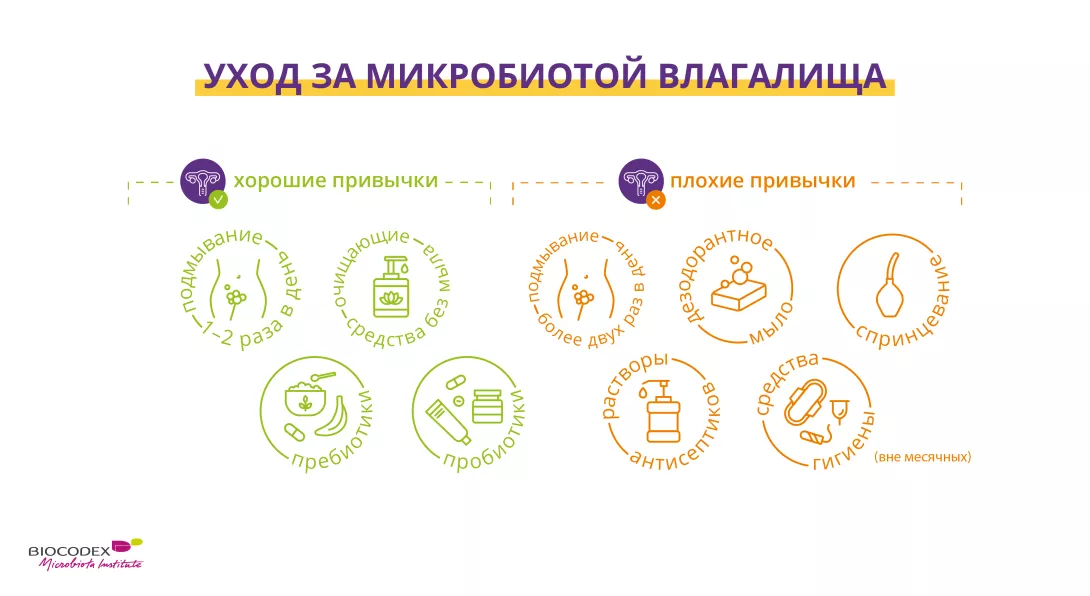
Правильный уход для сохранения вагинального микробиота: мягкая интимная гигиена, пребиотики и пробиотики — в отличие от вагинальных душей, агрессивных мыл и антисептических растворов.

Больше информации для женщин
1 из 2 52% опрошенных женщин никогда не получали информации об интимной гигиене, а 25% были проинформированы об этом лишь однажды врачом.
Почему существует такой разрыв между теорией и практикой? Есть много причин:
- слишком мало женщин получают информацию о правилах гигиены от врачей: 52% опрошенных никогда не получали такой информации, а 25% — только один раз
- частая путаница между вульвой и влагалищем искажает понимание информации
- самые глупые мифы часто оказываются наиболее живучими 1.
Важность этой проблемы обусловлена тем, что вульва — первая линия защиты женской половой системы 10.

(Правильные!) гигиенические привычки
Как сохранить микробиоту и защитную гидролипидную пленку женских половых органов? С помощью процедур ухода за вульвой, учитывающих возрастные и индивидуальные потребности.
Необходимо соблюдать 3 основных принципа 10:
- мыть только снаружи (= вульву, без подмывания влагалища), спереди назад (сначала вульва, затем анус)
- чистыми руками, без мочалки (которая может содержать бактерии)
- один раз в день. Частое наружное мытье оправдано только для женщин с частой диареей, из-за более частого опорожнения кишечника. Или во время менструации, когда может потребоваться повторное подмывание в течение дня.
Мытье только водой может высушить кожу и усилить зуд 10. Лучше всего использовать мягкое очищающее средство без мыла, которое не нарушает микросреду вульвы и поддерживает баланс ее микробиоты 1. И это все. В этой деликатной области лучше меньше, да лучше.
В заключение, вот несколько советов для формирования правильных привычек в течение дня 10:
- ночью лучше спать без нижнего белья
- после душа (предпочтительнее ванны) тщательно высушите промежность личным полотенцем, аккуратно промокая, а не растирая
- носите хлопковое белье вместо синтетики, избегайте ежедневных прокладок, выбирайте свободную одежду и чулки вместо колготок
- вытирайтесь неароматизированной и неокрашенной бумагой спереди назад, чтобы избежать попадания анальных бактерий на вульву
- Здесь также важно соблюдать основные принципы интимной гигиены (только наружное мытье; руками; один раз в день и т. д.) 10
- после полового акта (защищенного!, ведь ваш партнер может быть носителем ИППП) найдите возможность сходить в туалет, особенно если вы склонны к циститу
- во время менструации используйте неароматизированные прокладки или тампоны и регулярно меняйте их 10.

Пробиотики и пребиотики
Здоровая вагинальная микробиота зависит от хорошей интимной гигиены. Но иногда требуется дополнительная помощь для увеличения количества полезных бактерий в микробиоте:
пробиотики
пробиотики, живые микроорганизмы, оказывающие благоприятное воздействие на здоровье хозяина при употреблении в адекватных количествах 11, 12. При пероральном или вагинальном применении они способствуют восстановлению вагинальной флоры, облегчают симптомы и снижают риск рецидивов вагинальных инфекций в разные периоды жизни 13.
пребиотики
пребиотики, неперевариваемые волокна, избирательно стимулирующие рост полезной микрофлоры кишечника и улучшающие здоровье 12, 14. Другими словами, пробиотикам нужны благоприятные для их роста продукты. Например, пребиотики для женщин стимулируют рост вагинальных лактобацилл и нормализуют кислотность влагалища 15,16.
В чем разница между пребиотиками, пробиотиками и постбиотиками?
Подведем итоги...
Женские половые органы включают вульву (наружные органы) и влагалище — полость, соединяющую вульву с маткой, куда, например, вводится тампон во время менструации.
Половые органы содержат несколько микробиот: разнообразную микробиоту вульвы, вагинальную микробиоту с преобладанием лактобацилл, малочисленную микробиоту мочевыводящих путей (которые ранее ошибочно считали стерильными) и богатую перианальную микробиоту (из-за контакта с фекалиями).
Близость уретры, влагалища и ануса способствует обмену микрофлорой между их микробиотами, особенно при ненадлежащей интимной гигиене: агрессивном мытье, эпиляции/бритье всей области, ношении тесной одежды и т. п.
Недостаток информации мешает многим женщинам соблюдать правила гигиены для поддержания здоровой микробиоты. Еще не поздно поговорить с врачом — не теряйте времени!
При ослабленной вагинальной микробиоте пребиотики и пробиотики способствуют восстановлению сбалансированной вагинальной флоры.
2. Biology of the Kidneys and Urinary Tract. MSD Manuel. https://www.msdmanuals.com/home/kidney-and-urinary-tract-disorders/biology-of-the-kidneys-and-urinary-tract
6. Mueller ER, Wolfe AJ, Brubaker L. Female urinary microbiota. Curr Opin Urol. 2017 May;27(3):282-286.
7. Auriemma RS, Scairati R, Del Vecchio G et al. The Vaginal Microbiome: A Long Urogenital Colonization Throughout Woman Life. Front Cell Infect Microbiol. 2021 Jul 6;11:686167.