бактериальная диарея: кишечная микробиота — потенциальная жертва или защитник?
Патогенные бактерии, такие как Shigella, Vibrio cholerae, Salmonella, E. coli… вызывают бактериальную диарею посредством механизмов, зависящих от конкретного возбудителя. Бактериальная диарея сопровождается дисбиозом кишечника. И наоборот, кишечная микробиота влияет на течение бактериальной инфекции. Поскольку «здоровая» кишечная микробиота более устойчива к инфекциям, пробиотики могут снижать тяжесть многих бактериальных инфекций.
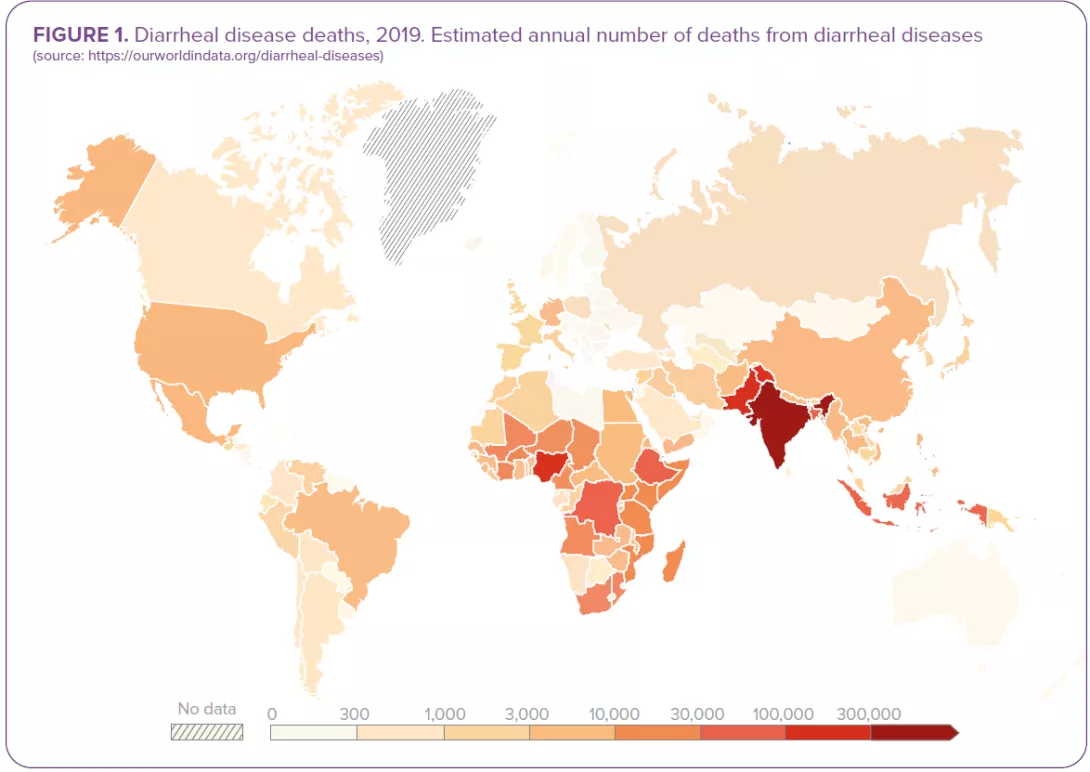
Бактериальная диарея может быть летальной: эти 8 бактерий ответственны более чем за треть из 1,65 миллиона смертей от инфекционной диареи в мире в 2016 году. 2
Эти 8 бактерий
- Shigella: 212 438 смертей.
- Vibrio cholerae: 107 290 смертей.
- Salmonella spp (не вызывающие тиф): 84 799 смертей.
- Campylobacter spp: 75 135 смертей.
- Энтеротоксигенные E. coli: 51 186 смертей.
- Clostridioides difficile: 22 417 смертей.
- Aeromonas: 16 881 смерть.
- Энтеропатогенные Escherichia coli: 12 337 смертей.
ОТ ИНФЕКЦИИ К ДИАРЕЕ
Механизмы, приводящие к бактериальной диарее, зависят от конкретных бактерий. Shigella передается через зараженную пищу, воду или при контакте с человеком, поражает желудочно-кишечный тракт, вырабатывает энтеротоксин и токсин серотипа 1, разрушающие эпителий кишечника и вызывающие тяжелую диарею с кровью и слизью.3,5
Патогенные варианты Vibrio cholerae продуцируют холерный токсин, который активирует секрецию анионов, ингибирует абсорбцию электронейтрального NaCl и нарушает барьерную функцию кишечника, что вызывает массивную секрецию жидкости в просвет тонкой кишки и потерю большого количества воды, натрия, хлоридов, бикарбонатов и калия.3,5,13
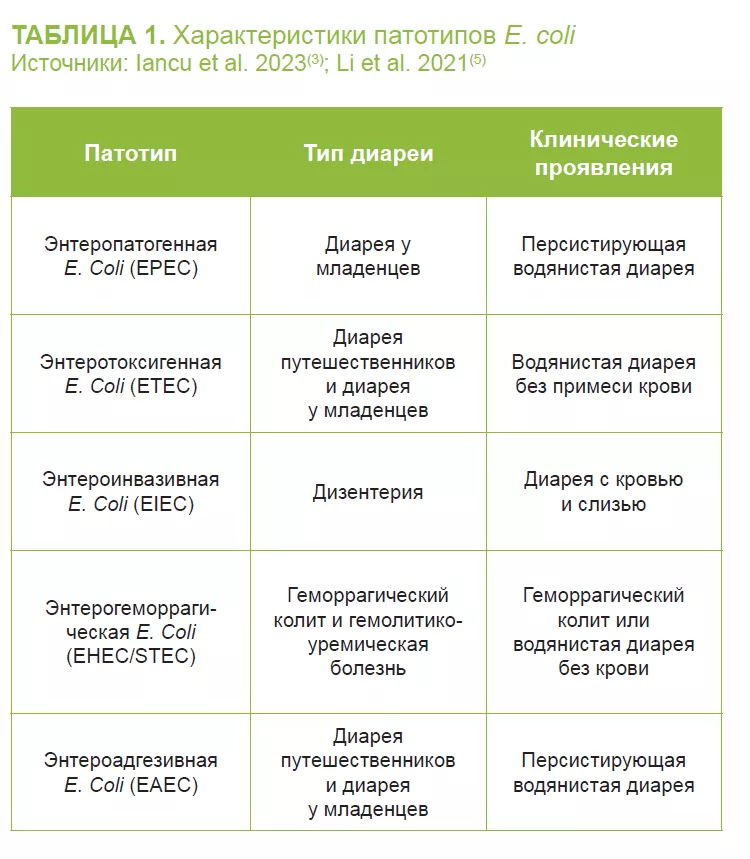
Патогенные штаммы E. coli, подразделяемые на различные патотипы (таблица 1), вызывают диарею от легкой до тяжелой степени, обычно сопровождающуюся лихорадкой. E. coli прикрепляется к эпителиальным клеткам кишечника с помощью адгезивных фимбрий, продуцирует токсины и оказывает свое патогенное действие.3,5
ВЛИЯНИЕ ПАТОГЕНОВ И ДИАРЕИ НА МИКРОБИОТУ
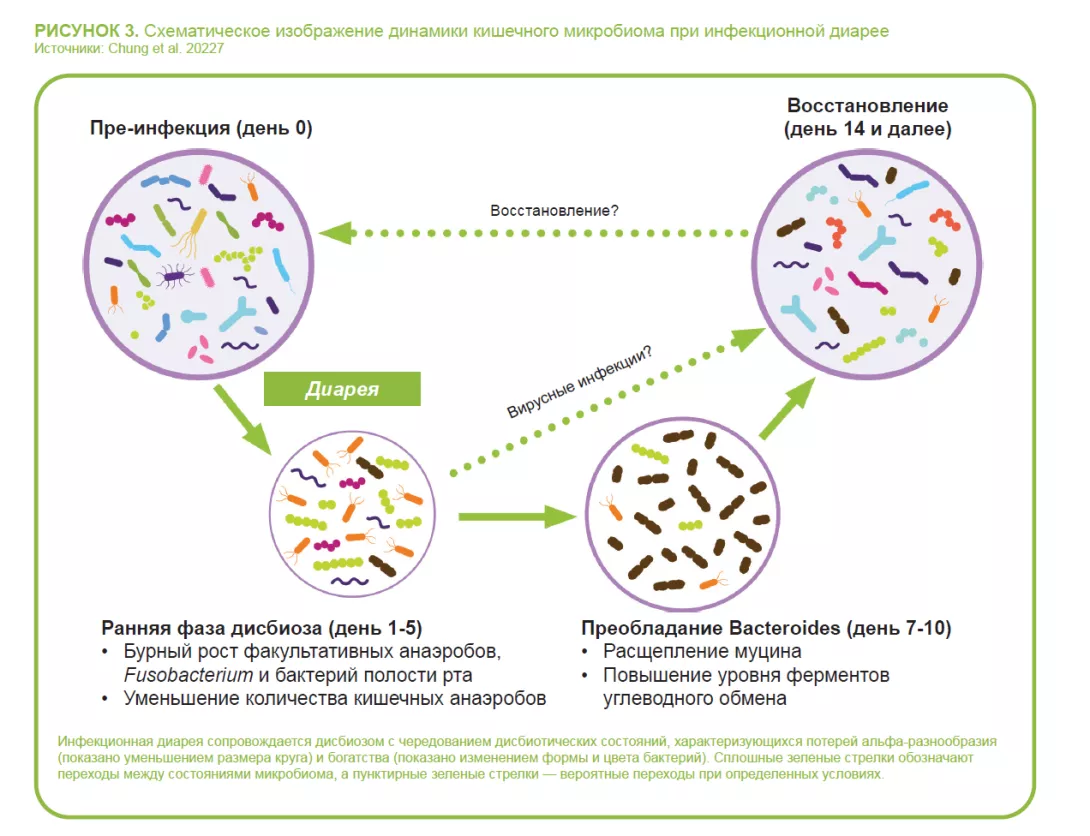
Бактериальная диарея сопровождается дисбиозом, обычно с преобладанием факультативных анаэробов (Escherichia, Streptococcus, Enterococcus и др.) при дизентерийной диарее, и истощением популяций бактерий с иммуномодулирующим действием (Lactobacillus ruminis, Bifidobacterium pseudocatenulatum)7 (рисунок 3).
При холере кишечная микробиота претерпевает существенные изменения как во время, так и после инфекции. Это происходит из-за удаления слизистого слоя вместе с обитающим в нем микробным сообществом, а также из-за воздействия токсина V. cholerae.13 Во время выздоровления кишечная микробиота пациентов с холерой медленно восстанавливается по модели, аналогичной наблюдаемой при созревании кишечной микробиоты у детей.3
Аналогичным образом, у детей, инфицированных диареегенной E. coli (DEC) , наблюдается особый состав кишечной микробиоты с высокой долей Bacteroidetes и Proteobacteria и снижением численности Firmicutes.13 Увеличение количества Proteobacteria может быть частично объяснено увеличением количества видов Escherichia/Shigella (как причины диареи), а также других представителей Enterobacteriaceae, таких как Citrobacter и Enterobacter (связанных с продукцией гистамина, индуцированной провоспалительным окружением, и ассоциированных с адгезией E. coli).14
Частое использование противомикробных препаратов также может частично объяснять наблюдаемый дисбиоз.7
ЗАЩИТНОЕ ДЕЙСТВИЕ КИШЕЧНОЙ МИКРОБИОТЫ ПРОТИВ ИНФЕКЦИЙ
В свою очередь, кишечная микробиота влияет на течение бактериальной инфекции. У безмикробных животных отсутствие кишечной микробиоты и экологической конкуренции приводит к незрелости иммунной системы, что делает их очень восприимчивыми к диарейным патогенам: 10 колониеобразующих единиц (КОЕ) Salmonella становится достаточно, 16чтобы вызвать летальную инфекцию, в то время как для гибели 50% мышей с интактной кишечной микробиотой требуется 103-109 КОЕ. 8
“В желудочно-кишечном тракте содержится примерно в 1‑10 раз больше бактериальных клеток, чем клеток в организме человека.” 16
ПРОБИОТИКИ НА ОСНОВЕ БАКТЕРИЙ И ДРОЖЖЕЙ, ПРЕБИОТИКИ И ТФМ
Тяжесть течения ряда бактериальных инфекций может быть снижена с помощью пробиотиков: например, пробиотическая E. coli ингибирует образование биопленок другими штаммами E. coli, а также патогенными Staphylococcus aureus и S. epidermidis.3 При дизентерии комбинация штаммов Lactobacillus, Bifidobacterium и Streptococcus сокращает продолжительность диареи с примесью крови и время пребывания в стационареl.3
Существует множество механизмов, объясняющих, почему пробиотики облегчают диарею:3 продукция антимикробных веществ, конкурентное исключение, конкуренция за места связывания с клетками, продукция кислот и метаболитов, снижающих pH окружающей среды, укрепление слизистого барьера кишечника, модуляция иммунитета слизистой оболочки кишечника и разнообразия кишечной микробиоты..15
Например, пробиотические дрожжи Saccharomyces boulardii способствуют восстановлению кишечной микробиоты у детей с острой диареей.15
Пребиотики также могут оказывать положительное влияние на диарею: увеличивая продукцию бактериями короткоцепочечных жирных кислот (КЦЖК), таких как бутират, которые способствуют поддержанию целостности кишечного барьера; противодействуя адгезии патогенов к эпителиальным клеткам, тем самым подавляя колонизацию и способствуя элиминации патогенов из кишечника.3
Трансплантация фекальной микробиоты (ТФМ), целью которой является восстановление здоровой микробиоты, доказала свою эффективность и показана только при лечении рецидивирующей инфекции, вызванной C. difficile, у взрослых и детей.14
ОПИСАНИЕ СЛУЧАЯ проф. Альдо Мори (Aldo Maruy)
- У двухлетнего мальчика наблюдались лихорадка, боль в животе и диарея со слизью и кровью. Ребенок дважды за последние полгода испытывал похожие симптомы, которые лечились только антибиотиками.
- Во избежание рецидива было решено назначить ему антибиотики и пробиотики. Диарея прекратилась в течение 48 часов, прием антибиотика был прекращен на 5-й день, в то время как прием пробиотика был продолжен в течение двух недель; ребенок получал диету, богатую пребиотиками.
- Помимо лечения инфекции антибиотиками, для профилактики новых эпизодов диареи было рекомендовано восстанавливать состав кишечной микробиоты с помощью диеты в сочетании с приемом пребиотиков и пробиотиков.

МНЕНИЕ ЭКСПЕРТА
На протяжении всей жизни человека здоровая микробиота играет важную роль в профилактике и лечении бактериальной диареи. Доказано, что определенные виды бактерий обладают защитным действием: так, Lactobacillus защищает от диареи, вызванной Shigella spp., а наличие Sutterella sp., Prevotella copri и Bacteroides vulgatus ассоциируется с резистентностью к энтеротоксигенной E. coli (ETEC).
С другой стороны, воздействие на микробиоту путем изменения рациона и использования пребиотиков, пробиотиков и ТФМ может регулировать состав кишечной микробиоты в контексте профилактики и лечения диареи. Дальнейшие исследования помогут расширить наши знания о микробиоме в контексте инфекционной диареи, а также разработать более эффективные подходы к профилактике и лечению.
ПОСЛЕДСТВИЯ ДИАРЕИ ПУТЕШЕСТВЕННИКОВ
От 10% до 70% путешественников из стран с низким уровнем инфекционных болезней страдают от диареи при посещении регионов со средним и высоким уровнем риска. Диарея путешественников в основном вызывается бактериями (≥80-90% случаев), при этом на кишечные вирусы приходится не менее 5-15% случаев.52 Инфекции, вызванные простейшими, могут составлять около 10% случаев, в основном у тех, кто путешествует длительное время. Микробиота путешественников с диареей более изменчива во время поездок по сравнению с микробиотой здоровых путешественников. Это обусловлено меньшим исходным разнообразием микробиоты и связано с повышенным риском инфекций.51
Более того, диарея снижает способность микробиоты к восстановлению (вследствие значительного отклонения от исходного состояния) и способствует приобретению микроорганизмов с множественной лекарственной устойчивостью.51 Согласно исследованию, в котором приняли участие 267 американцев, путешествовавших за пределы Соединенных Штатов, треть из них вернулась с диареей, 61% — с кишечным дисбиозом и 38% — с устойчивыми к антибиотикам бактериями (большинство из них — E. coli), что способствует глобальному распространению устойчивости к противомикробным препаратам.58
E. coli, Dorea fomigenerans, Bacteroïdes vulgarus, B. caocae, Odoribacter splanchnicus…,
Ruminococcus bromii, coprococcus, Clostridioides bartlett