Obesidad, diabetes tipo 2, enfermedades cardiovasculares, cáncer: el consumo de refrescos está relacionado con numerosos problemas de salud, cuyos efectos a veces se subestiman. Esta lista podría alargarse e incluir ahora la depresión, según los intrigantes resultados de un nuevo estudio alemán 1.
Cuando la ciencia se interesa por tu lata de refresco
Para llegar al fondo de esta cuestión, un equipo de investigadores analizó los datos de más de 900 alemanes de entre 18 y 65 años, reclutados en dos grandes ciudades (Marburgo y Münster).
Entre ellos había 405 personas (dos tercios de las cuales eran mujeres) que padecían un trastorno depresivo mayor y 527 controles sanos de edad y sexo comparables.
Su objetivo era comprender si la cantidad de refresco consumida podía predecir un diagnóstico de depresión o la gravedad de los síntomas.
El papel inesperado de la microbiota intestinal
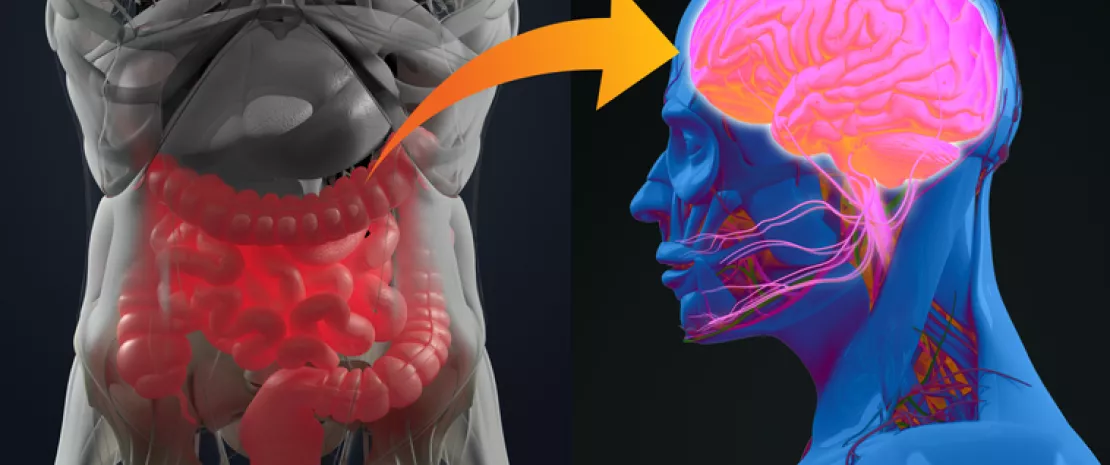
Los investigadores continuaron profundizando, yendo más allá de la simple relación entre los refrescos y la depresión. Analizaron lo que ocurría en la microbiota intestinal, el vasto ecosistema microbiano que influye en la digestión, la inmunidad e incluso el estado de ánimo... y cuya composición y equilibrio varían con nuestra dieta, incluidos los refrescos.
En concreto, se centraron en dos bacterias intestinales que, según estudios anteriores, podrían estar relacionadas con los trastornos depresivos mayores:
- Eggerthella
- y Hungatella.
El resultado: en las mujeres de este estudio, el consumo de refrescos se asoció efectivamente con un aumento de Eggerthella en la microbiota; Hungatella, por su parte, no parecía estar relacionada.
Eggerthella por sí sola podría explicar el 3,8 % de la relación entre los refrescos y la depresión y el 5 % de la relación entre los refrescos y la gravedad de los síntomas. .
Por lo tanto, el consumo de refrescos parece estar relacionado con el trastorno depresivo mayor (TDM), y la bacteria intestinal Eggerthella podría estar implicada al afectar al equilibrio de la microbiota.
Este hallazgo es especialmente preocupante dado que el consumo de estas bebidas está aumentando en todo el mundo, especialmente entre los niños y adolescentes. Estos resultados también aportan más pruebas a favor del eje intestino-cerebro y la relación entre la microbiota intestinal y las enfermedades mentales.
Pero hay buenas noticias. Ciertos enfoques dietéticos también pueden favorecer una microbiota más equilibrada y ayudar a regular el estado de ánimo.
Descubra cómo ciertos alimentos pueden desempeñar un papel protector leyendo nuestro artículo:

 Prácticas que ponen en riesgo la microbiota vaginal
Prácticas que ponen en riesgo la microbiota vaginal
 Cerveza y roquefort: la microbiota revela lo que comían nuestros antepasados
Cerveza y roquefort: la microbiota revela lo que comían nuestros antepasados