Exposoma: comprender cómo nuestro entorno moldea nuestra microbiota
¿Qué es el exposoma y cómo interactúa con el microbiota humano? En esta serie de videos con la Dra. Véronique Mondain, descubra cómo el exposoma conecta el microbiota, el cuerpo y el entorno, y por qué es esencial para el futuro de la atención sanitaria.

¿Qué pasaría si la salud fuera más que genética? ¿Y si fuera todo aquello a lo que estamos expuestos? El exposoma representa la suma de todos los factores ambientales, conductuales y sociales que influyen en nuestra biología desde la concepción hasta la muerte. IEn esta serie, expertos exploran cómo el exposoma conecta nuestra microbiota, el entorno, el estilo de vida y las emociones, ofreciendo una nueva manera de comprender y prevenir las enfermedades crónicas. Desde disruptores endocrinos y estrés, hasta nutrición, medicina integrativa y exposiciones en los primeros años de vida, descubra cómo estos factores interactúan para moldear la salud a lo largo de la vida. understand and prevent chronic diseases.
Sumérjase en esta serie para comprender mejor la ciencia detrás del exposoma y cómo pequeños cambios informados pueden marcar una gran diferencia para la salud global.
Exposoma: microbiota expuesta, salud en peligro
¿Cómo podemos evitar exposiciones perjudiciales para nuestra salud?

La vida moderna es conveniente, pero no siempre saludable. En este video, descubra cómo las elecciones cotidianas relacionadas con la alimentación, el estilo de vida y el entorno moldean nuestro bienestar a largo plazo y la salud de las generaciones futuras.
A través del lente del exposoma, esta charla nos recuerda que la verdadera prevención comienza con hábitos sencillos y con sentido común: comer alimentos reales y mínimamente procesados; moverse cada día; proteger la salud mental; y vivir de manera más consciente, tanto para nosotros como para el planeta.
Aprenderá:
- Cómo los hábitos modernos y los alimentos ultraprocesados afectan la salud y la inflamación
- Por qué el equilibrio, la simplicidad y el consumo consciente son importantes
- Cómo la primera infancia y la crianza moldean la resiliencia a lo largo de la vida
Medicina ambiental e integrativa: ¿una nueva forma de sanar?

La atención sanitaria moderna está evolucionando: más allá de los síntomas, explora cómo nuestro entorno, estilo de vida y equilibrio mente-cuerpo influyen en las enfermedades crónicas.
Este video explica cómo la medicina ambiental (comprender nuestras exposiciones) y la medicina integrativa (combinar enfoques no farmacológicos basados en evidencia) trabajan juntas para mejorar la prevención y los resultados en los pacientes.
Aprenderá:
- Qué significan la medicina ambiental e integrativa en la salud actual
- La ciencia detrás de prácticas no farmacológicas validadas: nutrición, actividad física, hipnosis, meditación y acupuntura
- Cómo estos enfoques apoyan el manejo del cáncer, la diabetes, la obesidad y otras enfermedades crónicas
Exposoma y salud: ¿el género marca la diferencia?

Desde los disruptores hormonales hasta las exposiciones laborales, el género influye en cómo interactuamos con nuestro entorno y en cómo este impacta nuestra salud.
En este video, descubra cómo los disruptores endocrinos pueden influir en el desarrollo de cánceres hormono-dependientes, la pubertad precoz y los trastornos reproductivos, y por qué comprender las exposiciones específicas por género es clave para proteger a las generaciones futuras.
Aprenderá:
- Cómo los disruptores endocrinos afectan de manera diferente a mujeres, hombres y niños
- Ejemplos reales: cosméticos, construcción, agricultura y más
- Por qué el exposoma debe incluir el género para avanzar en la prevención de precisión
Genoma, epigenética, exposoma: ¿en qué se diferencian?

Tus genes no son tu destino. Este video explica cómo el genoma (tu ADN), la epigenética (cómo se activan o desactivan los genes) y el exposoma (el conjunto de exposiciones a lo largo de la vida) interactúan para moldear la salud.
Desde la metilación del ADN y las histonas, hasta los disruptores endocrinos, la microbiota y las ventanas de vulnerabilidad —como los primeros 1.000 días—, descubra cómo el entorno y el estilo de vida orquestan la biología y por qué la prevención comienza entendiendo las exposiciones.
Aprenderá:
- Definiciones claras: genoma vs. epigenética vs. exposoma
- Cómo las exposiciones modulan los genes y promueven la inflamación de bajo grado
- Recomendaciones prácticas para reducir exposiciones nocivas
¿Cómo introducir el exposoma en la consulta?

¿Qué pasaría si la clave para comprender las enfermedades crónicas residiera en todo aquello a lo que estamos expuestos, desde el estrés y la alimentación hasta la contaminación y el estilo de vida?
En este video, la Dra. Véronique Mondain, especialista en enfermedades infecciosas, explica cómo el estudio del exposoma —la suma de todas las exposiciones ambientales y conductuales— transforma la forma en que abordamos la prevención y la medicina integrativa.
Yogur de coco con probióticos vivos ¿merece la pena recomendarlo?
Por la Dr. Hanna Stolińska
Clínica Dietética, Varsovia, Polonia

Numerosos influencers de la salud en redes sociales están entusiasmados con un yogur de coco probiótico de gama alta que afirma revolucionar la salud intestinal. Se comercializa como un superalimento repleto de miles de millones de probióticos, y ha ganado un gran número de adeptos entre los entusiastas del bienestar. Los fans alaban sus supuestos beneficios, desde una mejor digestión hasta una piel más sana, pero ¿qué dice la ciencia en comparación con los probióticos tradicionales? ¿Es esta fórmula rica en probióticos derivados del coco un auténtico potenciador del microbioma o solo una exagerada moda de bienestar?
¿Qué contiene el yogur probiótico a base de coco?
El yogur de coco está elaborado con pulpa y agua de coco ecológico, fermentado con 16 cepas probióticas personalizadas,
entre ellas Lactobacillus acidophilus, Bifidobacterium breve y Streptococcus thermophilus.
¿Qué beneficios para la salud afirma ofrecer? ¿Es realmente beneficioso para la salud?
Según su página oficial en Internet, el consumo de este yogur puede mejorar la digestión, reducir la hinchazón, favorecer una piel más sana y fortalecer el sistema inmunitario. Aunque los probióticos pueden ofrecer beneficios para la salud, las pruebas científicas que respaldan específicamente las propiedades de este yogur siguen siendo limitadas.
Sabemos que la pulpa de coco se compone principalmente de lípidos, y que el yogur de este tipo aporta muy pocas proteínas. Además, el aceite de coco se utiliza como remedio para todo tipo de dolencias, como luchar contra virus y bacterias, reforzar la inmunidad, reducir el colesterol, ayudar a la función tiroidea e incluso a la pérdida de peso 1-4.
El aceite de coco contiene ácidos grasos TCM de cadena media, que se digieren más fácilmente y se absorben menos que los ácidos grasos de cadena más larga. Sin embargo, de todos los ácidos grasos saturados del aceite de coco, los TCM solo constituyen la mitad. Algunos TCM, como el ácido láurico y el ácido cáprico, tienen propiedades antifúngicas y antivíricas 1-3, pero la finalidad del consumo
de alimentos es aportar componentes que refuercen el sistema inmunitario, que a su vez combate los microbios 4.
¿Cómo afecta a la microbiota intestinal?
Este yogur enriquecido con probióticos contiene bacterias vivas que pueden influir en la microbiota intestinal. Sin embargo, la efectividad de los probióticos depende de numerosos factores, como las cepas concretas utilizadas, su capacidad para sobrevivir al ácido estomacal y la composición del microbioma intestinal de cada persona.
Algunos estudios sugieren que los triglicéridos de cadena media (TCM) presentes en el coco pueden influir en la composición del microbioma. Sin embargo, la investigación sobre productos probióticos a base de coco todavía está en las primeras fases. Además, aunque el aceite de coco contiene compuestos antimicrobianos como el ácido láurico (que se convierte en monolaurina en el cuerpo),
esto no se traduce necesariamente en beneficios generales para la salud intestinal 1-3.
En un interesante estudio con ratas para investigar los efectos de diferentes aceites alimentarios en la microbiota intestinal se observó que el consumo de aceite de coco provocaba una reducción de la diversidad bacteriana, un aumento de los marcadores de endotoxemia metabólica, esteatosis hepática y niveles más altos de colesterol LDL 5. Aunque los estudios en animales proporcionan información valiosa, se necesitan más ensayos clínicos en humanos para determinar los efectos reales de este yogur enriquecido con probióticos sobre la salud intestinal.
Desde su perspectiva nutricional, ¿merece la pena tener en cuenta estos nuevos productos probióticos?
Es importante recordar que los alimentos están destinados principalmente a proporcionarnos nutrientes, vitaminas y minerales. Los productos lácteos de coco, al igual que el yogur, no tienen una alta densidad nutricional 1, 3.
Aunque este yogur rico en probióticos presenta un enfoque innovador para aportar bacterias beneficiosas, hay que tener en cuenta su alto contenido en grasas, su bajo nivel de proteínas y su coste a la hora de recomendarlo como opción dietética 2, 6. Los alimentos tradicionales ricos en probióticos, como el yogur, el kéfir y las verduras fermentadas, aportan beneficios similares con un perfil nutricional más equilibrado. Una alimentación variada y equilibrada, baja en alimentos procesados y rica en verduras, frutas, cereales integrales y legumbres, favorece la diversidad del microbioma.
- Boateng L, Ansong R, Owusu WB. Coconut oil and palm oil’s role in nutrition, health and national development: A review. Ghana Med J 2016; 50: 189-96.
- Eyres L, Eyres MF, Chisholm A, Brown RC. Coconut oil consumption and cardiovascular risk factors in humans. Nutr Rev 2016; 74: 267-80.
- Lockyer S, Stanner S. Coconut oil – a nutty idea? British Nutrition Foundation Nutrition Bulletin 2016; 41: 42-54.
- Joshi S, Kaushik V, Gode V, Mhaskar S. Coconut Oil and Immunity: What do we really know about it so far? J Assoc Physicians India 2020; 68: 67-72.
- López-Salazar V, Tapia MS, Tobón-Cornejo S, Díaz D, Alemán-Escondrillas G, Granados-Portillo O, Noriega L, Tovar AR, Torres N. Consumption of soybean or olive oil at recommended concentrations increased the intestinal microbiota diversity and insulin sensitivity and prevented fatty liver compared to the effects of coconut oil. J Nutr Biochem. 2021; 94: 108751.
- Sacks FM, Lichtenstein AH, Wu JHY, et al.; American Heart Association. Dietary Fats and Cardiovascular Disease: A Presidential Advisory From the American Heart Association. Circulation 2017; 136: e1-e23.
Microbiota vaginal #23
Por la Pr. Satu. Pekkala
Becaria de investigación de la Academia de Finlandia, Facultad de Ciencias
del Deporte y la Salud, Universidad de Jyväskylä, Finlandia

Mujeres transgénero: una flora neovaginal específica
Algunas mujeres transgénero corrigen la incongruencia de género de sentirse mujer en lo más profundo de su ser a pesar de la presencia física de genitales masculinos -y de que se refieran a ellas como hombre- sometiéndose a una “vaginoplastia por inversión peneana”. En otras palabras, transformando quirúrgicamente el pene en vagina. Independientemente del éxito de la intervención, la piel de esta vagina recién construida combinará piel del pene y un injerto de piel del escroto y/o de otra(s) zona(s) (estómago, ingle,
etc.). ¿Cómo afecta esto a la salud? La microbiota vaginal es clave para la buena salud vaginal de las mujeres cisgénero. Los investigadores estadounidenses han centrado ahora su atención en la flora íntima de las mujeres transgénero sometidas a cirugía: ¿la composición de la microbiota neovaginal podría explicar ciertos problemas, entre ellos el frecuentemente referido del flujo vaginal?
Es una pregunta que merece la pena plantearse, y que ahora se ha respondido gracias a un estudio que compara la microbiota vaginal de mujeres transgénero que se han realizado una vaginoplastia con la de mujeres cisgénero. ¿Los resultados? Tienen una microbiota muy diferente. La flora vaginal de las mujeres cisgénero no es muy diversa y está dominada en gran medida por los lactobacilos, que crean un entorno ácido que repele a los patógenos. La de las mujeres transgénero tiene menos de un 3 % de estos
valiosos aliados y es mucho más diversa. En la vagina, la diversidad no es signo de buena salud, sino todo lo contrario. Se ha observado en mujeres cisgénero que padecen vaginosis bacteriana, lo que aumenta el riesgo de infecciones de transmisión sexual (incluido el VIH/SIDA) y de aborto espontáneo.
¿Cómo se crea este nuevo ecosistema microbiano? O más concretamente, ¿qué bacterias componen la microbiota neovaginal de mujeres transgénero operadas? Sin duda, resultan de la flora de la piel (pene, escroto, etc.) utilizada durante la cirugía. Sin embargo, parece ser que la transmisión oral-genital y genital-genital también está implicada. De hecho, se ha demostrado que la flora neovaginal de las mujeres transexuales operadas incluye especies bacterianas típicas no solo de la piel y el tubo digestivo, sino también de la boca. Puesto que las relaciones sexuales influyen en la probabilidad de presencia de una bacteria llamada E. faecalis, también hay transferencia genital.
Por otro lado, mientras que la proliferación de lactobacilos protectores en las mujeres cisgénero se puede explicar por las hormonas, el estado hormonal de las mujeres transgénero (comparable al de las mujeres cisgénero debido al tratamiento) no parecía tener ningún cambio. Se necesitarán más estudios con un mayor número de mujeres transgénero para comprender mejor su salud neovaginal.
Microbiota intestinal #23
Por la Pr. Satu. Pekkala
Becaria de investigación de la Academia de Finlandia, Facultad de Ciencias
del Deporte y la Salud, Universidad de Jyväskylä, Finlandia

La microbiota intestinal regula comportamientos similares al insomnio a través del eje intestino-cerebro
Aunque se sabe que el sueño tiene una conexión bidireccional con la microbiota intestinal, los mecanismos subyacentes se desconocen en gran medida. Sin embargo, parece que ciertos metabolitos derivados del intestino pueden afectar a algunos comportamientos del anfitrión, como el comportamiento ansioso. Además, algunos estudios clínicos han observado alteraciones en la microbiota intestinal de personas con insomnio crónico.
Wang et al. trataron de aclarar cómo la microbiota intestinal podría afectar
al comportamiento del sueño. Para ello, estudiaron el comportamiento de sueño-vigilia en ratones carentes de patógenos específicos (CPE) y axénicos. Los ratones axénicos están libres de TODOS los microorganismos, incluidos los mientras que los ratones CPE están libres de una lista específica de patógenos mediante pruebas rutinarias. El registro de 24 horas de electroencefalograma (EEG) y electromiograma (EMG) ambulatorio mostró que los ratones axénicos tenían un menor tiempo de vigilia y sueño REM respecto de los ratones CPE. Para identificar los metabolitos específicos que intervienen en los cambios de comportamiento relacionados con el sueño en los que interviene la microbiota intestinal, los autores estudiaron muestras de heces y tejido del hipotálamo mediante metabolómica dirigida. Se observó que el butirato, el ácido graso de cadena corta derivado de la microbiota intestinal, era el modulador más significativo del comportamiento del sueño. Además, la administración oral de tributirina, un precursor de la administración de butirato, conllevó una reducción significativa del 39,50 % de la vigilia y un aumento del 77,99 % del sueño REM. Parece que el mecanismo subyacente es que la tributirina inhibe la actividad de la neurona orexina del hipotálamo lateral.
Mediante el estudio en seres humanos, los autores también observaron una disminución de 39 productores de butirato en pacientes con insomnio en comparación con los testigos. Por último, los autores también demostraron que los ratones axénicos que recibieron
microbiota de pacientes con insomnio presentaban alteraciones del sueño, que se recuperaban con una suplementación con butirato. En conclusión, el estudio pone de relieve las posibilidades del butirato como agente terapéutico para aliviar trastornos del sueño.
La toxina de distensión citoletal derivada de Campylobacter jejuni favorece la metástasis del cáncer colorrectal
Varias bacterias protumorigénicas, como la genotóxica Escherichia coli (E. coli) y la enterotoxigénica Bacteroides fragilis (B. fragilis), se han asociado con el avance de la metástasis del cáncer. Además, se ha observado que Campylobacter productoras de toxina de distensión citoletal (TDC) aumentan en tejidos tumorales en comparación con tejidos adyacentes normales. Sin embargo, aún no se tiene un buen conocimiento de la relación entre las bacterias productoras de genotoxinas y la metástasis del cáncer.
Los autores de este estudio obtuvieron tejidos de cáncer colorrectal (CCR) primario de 34 pacientes sin tratamiento previo de quimioterapia (estadios TNM I y IIA) con metástasis a distancia en un plazo de 3 años (grupo de metástasis) y 37 pacientes que no sufrieron metástasis (grupo sin metástasis) durante 3 años de seguimiento. Observaron un enriquecimiento significativo de Campylobacter en el grupo de metástasis, y que los pacientes con Campylobacter intratumoral tenían un pronóstico notablemente peor. Además, confirmaron sus hallazgos con una cohorte de validación y una base de datos de acceso público.
La TDC es el principal factor de virulencia responsable de la patogénesis producida por Campylobacter, y en las células anfitrionas provoca daños en el ADN y el cese del ciclo celular. El grupo de metástasis expresó más subunidad TDC bioactiva tdcB y antígeno de invasión B de Campylobacter (aiBC), un factor de virulencia específico de C. jejuni. In vitro, C. jejuni aumentó significativamente la
migración celular y la capacidad de invasión de varias líneas celulares de CCR. En un modelo murino, la administración de C. jejuni aumentó la capacidad de migración e invasión en comparación con los testigos, y en otro aumentó significativamente la metástasis hepática. En conjunto, estos hallazgos demuestran que C. jejuni intestinal promueve la metástasis del CCR. Curiosamente, la capacidad prometástasis se atenuó en ausencia de tdcB. Mecánicamente, parece que la TDC activó la vía de señalización JAK-STAT que conduce a la expresión de genes de MMP y a la metástasis tumoral.
Enfermedad de Crohn quiescente, microbios sulfidogénicos y vías metabólicas del azufre: consecuencias funcionales
En la enfermedad intestinal inflamatoria quiescente, no hay inflamación activa. Sin embargo, los pacientes refieren síntomas
persistentes, especialmente en la enfermedad de Crohn (EC). Se ha comprobado que el microbioma está alterado en pacientes con EC inactiva con síntomas persistentes (ECi + S). En concreto, se ha observado que los pacientes con ECi + S tienen más microbios sulfidogénicos y vías génicas microbianas de metabolismo del azufre. Sin embargo, se desconoce el significado funcional de estos
cambios. En este estudio observacional multicéntrico, se realizó una secuenciación metagenómica indiscriminada y un perfil metabolómico de las heces de los pacientes con ECi + S. Además, se incluyeron pacientes con enfermedad de Crohn activa (ECa), con enfermedad de Crohn inactiva sin síntomas gastrointestinales persistentes (ECi-S) y con síndrome del intestino irritable con diarrea predominante (SII-D), y se compararon con los pacientes Eci + S.
Los autores observaron que los metabolitos fecales de las vías de la cisteína/metionina, los ácidos biliares y los ácidos grasos se encontraban entre los más abundantes en los pacientes con ECi + S en comparación con los otros grupos. Las diferencias
persistían incluso cuando la inflamación, es decir los niveles de calprotectina, eran inferiores. La glicina, la serina y la treonina, el glutatión, la cisteína y la metionina fueron las vías más incrementadas en el grupo ECi + S. Todas ellas son importantes vías metabólicas del azufre en el intestino humano. Además de los metabolitos, muchos genes bacterianos metabólicos del azufre estaban desregulados en el grupo ECi + S. Al integrar los conjuntos de datos metagenómicos y metabolómicos, los autores descubrieron además que la taurina y la hipotaurina, el nicotinato y la nicotinamida, la cisteína y la metionina, y la glicina, la serina y la treonina eran las principales vías metabólicas asociadas con los microbios enriquecidos en el grupo ECi + S. Dado que altas concentraciones de H2S inhiben las funciones mitocondriales del anfitrión, los resultados sugieren una relación entre los metabolitos de origen microbiano y la función mitocondrial del anfitrión en pacientes con ECi + S. En conjunto, los resultados de este estudio sugieren que las estrategias para disminuir los microbios sulfidogénicos y las vías metabólicas del azufre asociadas podrían suponer una estrategia novedosa para mejorar la calidad de vida en la enfermedad de Crohn inactiva con síntomas persistentes.
ESPGHAN 2025: enfoque en las interacciones microbiota-fármacos
Por la Dr. Thị Việt Hà
Subdirectora del Departamento de Pediatría, Universidad
Médica de Hanói. Directora del Departamento de Gastroenterología,
Hospital Nacional Infantil, Hanói, Vietnam
Por la Dr. Thị Diệu Thúy
Jefa del Departamento de Pediatría - Hanoi Universidad Médica.
Subdirectora del Departamento de Inmunología - Alergia -
Reumatología, Hospital Nacional Infantil de Hanoi, Vietnam

Reumatología, Hospital Nacional Infantil. La 57.ª reunión anual del ESPGHAN se centró en las interacciones bidireccionales entre la microbiota intestinal y los medicamentos en el contexto de la gastroenterología pediátrica, la nutrición y la farmacomicrobiómica. Un tema recurrente en las presentaciones fue el creciente reconocimiento del microbioma intestinal como factor clave en el tratamiento farmacológico, la modulación inmunitaria y el tratamiento de enfermedades en niños.
Mecanismos
La microbiota se compone de una amplia variedad de bacterias, virus, hongos y otros microorganismos que son fundamentales para la homeostasis inmunológica, hormonal y metabólica del anfitrión. A menudo nos referimos a ella como un “órgano oculto”.
Cuando este ecosistema está alterado (disbiosis) puede contribuir a una gran variedad de enfermedades, desde enfermedades
gastrointestinales hasta trastornos metabólicos y neurológicos generalizados 1.
Al nacer, el intestino del recién nacido es estéril, pero los microorganismos del entorno, como enterobacterias, enterococos, lactobacilos y bifidobacterias lo colonizan rápidamente. La microbiota intestinal pasa por cambios dinámicos y progresivos desde la infancia hasta la
edad adulta, y se moldea por distintos factores internos y externos. Estos cambios microbianos son fundamentales para formar un microbioma estable y resistente que favorezca la salud a lo largo de toda la vida. Se calcula que, en adultos sanos, la microbiota intestinal se compone de más de 1000 especies de bacterias. Es importante señalar que esta comunidad microbiana puede afectar a la farmacodinámica de los medicamentos, bien metabolizándolos directamente o bien modificando las respuestas metabólicas e inmunitarias del anfitrión.
Los fármacos por vía oral recorren el tubo digestivo, y su absorción y metabolismo se ven afectados en cada etapa. Los fármacos que no se absorben completamente en la porción alta del tubo digestivo pueden llegar al colon. A su vez, el microbioma intestinal participa activamente en la transformación química de estos fármacos, lo que repercute en su farmacocinética, su bioactividad y su posible toxicidad.
Son varios los mecanismos por los que los fármacos influyen en la microbiota intestinal, como:
1 / efectos directos (los antibióticos pueden matar algunas especies de la microbiota, las nocivas pero también las beneficiosas, lo que provoca desequilibrios en la microbiota intestinal);
2 / alteración de la motilidad intestinal (ciertos fármacos pueden ralentizar la motilidad intestinal, lo que a su vez puede provocar una hiperproliferación de bacterias patógenas);
3 / modulación de la función inmunitaria (hay varios fármacos que pueden interactuar con la inmunidad intestinal, lo que a su vez puede repercutir en la microbiota intestinal);
4 / cambios en el pH del intestino (el equilibrio del pH desempeña una función importante en el tubo digestivo, que afecta al crecimiento y la supervivencia de distintos tipos de especies de la microbiota intestinal. Algunos fármacos pueden modificar el valor del pH del intestino, lo que afecta a la proliferación de diferentes microbios y repercute en la composición general de la microbiota intestinal);
5 / interferencia con el metabolismo microbiano (existen distintos fármacos que pueden interferir con el metabolismo microbiano, lo que puede afectar a la microbiota intestinal);
6 / cambios en la alimentación (algunos fármacos pueden cambiar el entorno dietético del intestino. Esto puede influir en la microbiota intestinal modificando la disponibilidad de nutrientes y otros compuestos que la microbiota intestinal utiliza para crecer y sobrevivir) 2-4.
Las interacciones entre el microbioma intestinal y los fármacos no solo están determinadas por la actividad microbiana, sino también por la genética del anfitrión, la exposición ambiental y su interacción, lo que representa un desafío complejo para conseguir una terapia personalizada. Los estudios de asociación del genoma completo (EAGC) han identificado variantes genéticas humanas, especialmente en genes relacionados con la inmunidad, el metabolismo y la digestión (por ejemplo, lectinas de tipo C y lactasa) que repercuten en la composición de la microbiota intestinal.
Los ejemplos del irinotecán y del citocromo p450
El irinotecán -un medicamento contra el cáncer- se reactiva en el intestino por las enzimas microbianas y provoca diarrea grave, un efecto secundario importante de la quimioterapia. Algunas bacterias intestinales, en concreto las especies productoras de beta-glucuronidasa como Escherichia coli, Clostridium y Bacteroides producen enzimas que transforman nuevamente la SN-38G en su forma
activa SN-38 en el intestino. Esta reactivación es tóxica para las células epiteliales intestinales, lo que provoca lesiones en la mucosa, inflamación y diarrea grave de aparición tardía 3.
El microbioma intestinal puede afectar profundamente a las enzimas metabolizadoras de fármacos del anfitrión, un factor emergente en la medicina personalizada. Las enzimas del citocromo P450, en concreto la CYP3A4, están moduladas por compuestos de origen intestinal. Los ácidos grasos de cadena corta (AGCC) pueden modular la expresión de genes enzimáticos mediante mecanismos epigenéticos. Mientras tanto, los ácidos biliares secundarios interactúan con receptores nucleares como FXR, CAR y PXR, lo que altera el metabolismo de los fármacos 3.
Estrategias para reducir los daños colaterales de los fármacos en el microbioma 5
Para proteger el microbioma intestinal, una estrategia clave consiste en evitar, en la medida de lo posible, fármacos que sabemos que alteran el equilibrio microbiano. Minimizar la interacción directa entre los fármacos y la microbiota intestinal puede reducir los efectos negativos. Por el contrario, las estrategias restaurativas buscan reparar las comunidades microbianas tras una alteración. Entre ellas
se encuentran las modificaciones de la alimentación, los probióticos, los productos bioterapéuticos vivos y el trasplante de microbiota fecal. Las modificaciones de la alimentación actúan como terapias dirigidas a la microbiota. Por ejemplo, la fibra alimentaria favorece la proliferación de bacterias productoras de AGCC, fundamentales para la función inmunitaria, el desarrollo epitelial y el mantenimiento de un entorno intestinal anaeróbico. Los probióticos como Saccharomyces boulardii CNCM I-745, Lactobacillus reuteri y Bifidobacterium spp. favorecen una colonización resistente, una modulación inmunitaria y la integridad de la barrera intestinal. Los postbióticos, compuestos por microbios inactivados o sus componentes, también presentan beneficios para la salud sin necesitar organismos vivos. Por otro lado, los productos bioterapéuticos vivos representan una nueva categoría de intervenciones médicas que utilizan microbios vivos específicamente diseñados para tratar o prevenir enfermedades, a diferencia de los complementos tradicionales 5.
Reparar la comunidad microbiana es algo más que recolonizar bacterias. Requiere restablecer un ecosistema equilibrado que favorezca las funciones inmunitarias, metabólicas y de barrera. Las estrategias para proteger el microbioma durante el tratamiento farmacológico se dividen en dos categorías principales: estrategias preventivas que minimizan las alteraciones causadas por los fármacos, y estrategias restauradoras que buscan reconstruir la diversidad y la función microbianas una vez producido el daño 5.
Seleccionar la estrategia adecuada necesita de un enfoque centrado en la precisión, adaptado al fármaco, al contexto de la enfermedad y al paciente. El éxito depende de una comprensión profunda de los principios ecológicos y bioquímicos que rigen las interacciones entra la microbiota y los fármacos. La investigación continua es fundamental para orientar la recuperación eficaz y la protección del microbioma intestinal durante y después del tratamiento farmacológico.
- Hou K, Wu ZX, Chen XY, et al. Microbiota in health and diseases. Signal Transduct Target Ther 2022; 7: 135.
- Zhao Q, Chen Y, HuangW, et al. Drug-microbiota interactions: an emerging priority for precision medicine. Signal Transduct Target Ther 2023; 8: 386.
- Wang S, Ju D, Zeng X. Mechanisms and clinical implications of human gut microbiota-drug interactions in the precision medicine era. Biomedicines 2024; 16: 194.
- Patangia D, Ryan CA, Dempsey E, et al. Impact of antibiotics on the human microbiome and consequences for host health. Microbiologyopen 2022; 13: e1260.
- de la Cuesta-Zuluaga J, Müller P, Maier L. Balancing act: counteracting adverse drug effects on the microbiome. Trends Microbiol 2025; 33: 268-76.
¿Podemos actuar sobre la microbiota en el abordaje de niños con trastornos funcionales de dolor abdominal?
Por Iulia Florentina Tincu, Roxana Elena Matran, Cristina Adriana Becheanu
Universidad de Medicina y Farmacia Carol Davila, Rumanía
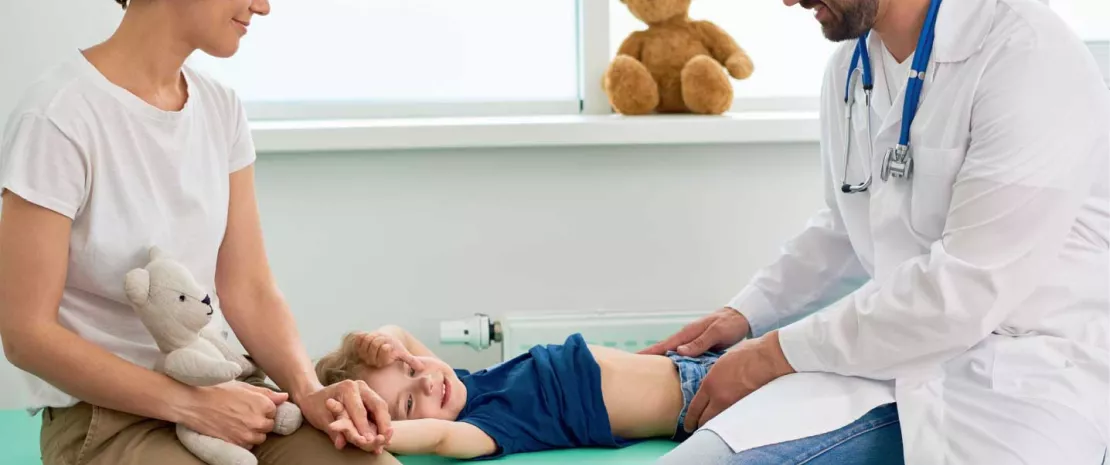
El intestino disbiótico en los trastornos funcionales de dolor abdominal en niños
Los trastornos funcionales de dolor abdominal (TFDA), también conocidos como trastornos funcionales gastrointestinales (TFGI), representan una de las principales etiologías de dolor abdominal crónico en la población pediátrica e implican la interacción entre factores de regulación del sistema nervioso entérico y del sistema nervioso central [1]. El sistema de clasificación actual, ROMA IV, distingue varios TFGI con predominio del dolor a partir de patrones de síntomas reconocibles, como la dispepsia funcional (DF), el síndrome del intestino irritable (SII), la migraña abdominal y el dolor abdominal funcional no especificado (DAF-NOS) 2. Durante las
dos últimas décadas, numerosos estudios han investigado las posibles causas y mecanismos subyacentes de aparición, pero aún no se ha descubierto con detalle la fisiopatología, a pesar de los hallazgos de la neurogastroenterología pediátrica en términos de motilidad intestinal, moléculas de señalización, cambios en la microbiota o mecanismos epigenéticos 3.
Es posible que las modificaciones de la microbiota intestinal, conocidas como intestino disbiótico, desempeñen una función en los trastornos funcionales de dolor abdominal a través de la alteración de la inmunidad y de la integridad intestinales 4, 5. En numerosos estudios se describe un nivel inferior de diversidad microbiana en los pacientes con trastornos funcionales de dolor abdominal 6, 7 y especies como Lactobacilli y Bifidobacteria se encuentran considerablemente alteradas 8. Por lo tanto, disponemos de cada vez más datos clínicos sobre el uso de probióticos en el abordaje de los trastornos funcionales, aunque faltan datos de estudios en niños 9.
Perspectivas de investigación
El análisis de la microbiota en 18 pacientes con TFGI proporcionó datos sobre la disbiosis intestinal en el momento del diagnóstico y sus cambios durante de un período de tres meses de tratamiento con cepas específicas de probióticos y prebióticos
(figura 1).
Pacientes. Entre 4 y 14 años de edad y con un diagnóstico de trastornos funcionales de dolor abdominal (dispepsia funcional y síndrome del intestino irritable) de acuerdo con los criterios de ROMA IV.
Intervención. Seis cepas bacterianas (Lactobacillus rhamnosus R0011, Lactibacillus casei R0215, Bifidobacterium lactis BI-04, Lactobacillus acidophilus La-14, Bifidobacterium longum BB536, Lactobacillus plantarum R1012) y 210 mg de fructooligosacáridos-inulina. Se administró una cápsula por vía oral, a diario, durante 12 semanas, y la medicación fue suministrada por profesionales sanitarios.
Resultado clínico. Se puntuó la gravedad de las molestias abdominales, la dispepsia, la flatulencia y el dolor epigástrico en una escala ordinal (calificación numérica) de diez puntos.
Se recogieron muestras fecales de los participantes antes y después del tratamiento con un kit especial de laboratorio con dos recipientes estériles, que se llevaron al laboratorio en condiciones que dependían del tiempo transcurrido desde la recogida hasta la entrega al laboratorio: si el intervalo era inferior a 24 horas, se almacenaban ambos recipientes y se transportaban en condiciones refrigeradas a 4 °C; si el período entre la deposición de las heces y la entrega al laboratorio superaba las 24 h, se almacenaba uno de
los recipientes congelado a -80 °C hasta el análisis, y el otro se refrigeraba a 4 °C. Las muestras de heces se analizaron mediante la prueba Colonic dysbiosis-basic profile (SBY 1) realizada por Synlab-Alemania. La composición de la microbiota se expresó como número de unidades formadoras de colonias (UFC) de diversas especies bacterianas y fúngicas aerobias/ anaerobias. El análisis proporcionó datos sobre pH fecal, IgA en μg/mL (rangos normales 510-2040 μg/mL), lactoferrina en μg/mL (rangos normales <7,2), calprotectina en mg/kg (rangos normales <50,0 negativo, 50-99 intermedio, >100 positivo).
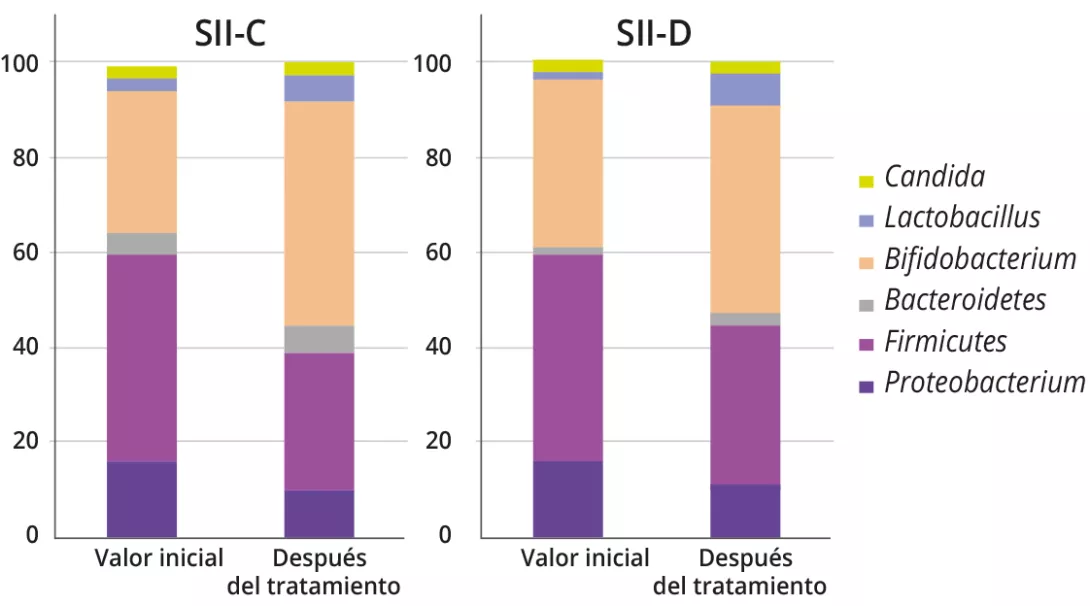
En el análisis microbiano fecal se observó un aumento de la proporción de géneros bacterianos asociados a beneficios para la salud (por ejemplo, Bifidobacterium y Lactobacillus), tanto para el SII-C como para el SII-D (SII-C: 31,1 ± 16,7 % frente a 47,7 ± 13,5 %, p = 0,01; SII-D: 35,8 ± 16,2 % frente a 44,1 ± 15,1 %, p = 0,01). Por otro lado, se comprobó que los géneros de bacterias nocivas como
Escherichia, Clostridium, y Klebsiella disminuían después del tratamiento (21,3 ± 16,9 % frente a 16,3 ± 9,6 %, p = 0,02). No se observaron particularidades en los niños con DF.
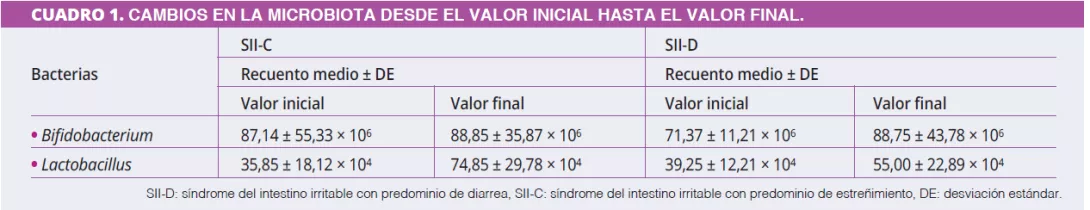
Al inicio, antes de que se produjera cualquier intervención simbiótica, los perfiles de Bifidobacterium eran significativamente diferentes entre SII-C y SII-D (87,14 ± 23,19 frente a 71,37 ± 12,24; p = 0,02), con recuentos más bajos en SII-D. La administración simbiótica tuvo
un efecto significativo en los perfiles bacterianos desde el inicio hasta el final del tratamiento, tanto en el grupo SII-C como en el SII-D (cuadro 1).
Consecuencias prácticas
Los síntomas clínicos en la población del estudio disminuyeron más tras el tratamiento, con significación estadística, lo que sugiere que influir en la disbiosis intestinal también puede reducir la carga de los pacientes además de mejorar las puntuaciones clínicas.
En total, 14 (el 78 %) pacientes afirmaron que el tratamiento había funcionado (definido como ausencia de dolor). La proporción de pacientes con un alivio adecuado de los síntomas fue mayor en el grupo SII-D que en el grupo SII-C; sin embargo, la diferencia no fue estadísticamente significativa (74,4 % frente al 61,9 %, p = 0,230). Tanto en el grupo SII-C como en el SII-D, las puntuaciones en la escala de Bristol mejoraron significativamente tras la intervención (valor inicial frente a después del tratamiento; 2,8 ± 0,6 frente a 3,9 ± 0,9, p = 0,03, 6,1 ± 0,9 frente a 4,1 ± 1,0, p = 0,01, respectivamente). Tanto la distensión abdominal como la flatulencia mejoraron significativamente en los grupos SII-C y SII-D (SII-C: 6,5 ± 2,8 frente a 3,7 ± 1,8, P = 0,01; SII-D: 5,9 ± 2,2 frente a 2,9 ± 1,8, P = 0,01).
- La exploración del microbioma humano ha revelado a lo largo del tiempo que la disbiosis desempeña una importante función en la patogénesis de los trastornos funcionales de dolor
abdominal, aunque los perfiles específicos como biomarcadores tempranos están aún lejos de tener un uso práctico en la actualidad. - Hay una necesidad real de futuros estudios unitarios en términos de intervenciones modificadoras de la microbiota para obtener un contexto más amplio de los trastornos pediátricos.
- Podemos concluir que una perspectiva novedosa en el campo en desarrollo de las terapias que modifican la microbiota en niños con TFGI puede aportar valiosos conocimientos sobre los mecanismos de la enfermedad, con lo que las estrategias terapéuticas personalizadas podrían mejorar los síntomas de los pacientes.
CONCLUSIÓN
Puede que la intervención centrada en la microbiota sea capaz de producir cambios significativos en la disbiosis gastrointestinal y este hallazgo está relacionado con el alivio de los síntomas gastrointestinales en pacientes con trastornos funcionales de dolor abdominal.
- Royle JT, Hamel-Lambert J. Biopsychosocial issues in functional abdominal pain. Pediatr Ann 2001; 30: 32-40.
- Hyams JS, Di Lorenzo C, Saps M, Shulman RJ, Staiano A, van Tilburg M. Functional Disorders: Children and Adolescents. Gastroenterology 2016: S0016-5085.
- Oświęcimska J, Szymlak A, Roczniak W, Girczys-Połedniok K, Kwiecień J. New insights into the pathogenesis and treatment of irritable bowel syndrome. Adv Med Sci 2017; 62: 17-30.
- Chong PP, Chin VK, Looi CY, Wong WF, Madhavan P, Yong VC. The Microbiome and Irritable Bowel Syndrome - A Review on the Pathophysiology, Current Research and Future Therapy. Front Microbiol 2019; 10: 1136. Erratum in: Front Microbiol 2019; 10: 1870.
- Pantazi AC, Mihai CM, Lupu A, et al. Gut Microbiota Profile and Functional Gastrointestinal Disorders in Infants: A Longitudinal Study. Nutrients 2025; 17: 701.
- Carroll IM, Ringel-Kulka T, Keku TO, et al. Molecular analysis of the luminal- and mucosal-associated intestinal microbiota in diarrhea-predominant irritable bowel syndrome. Am J Physiol Gastrointest Liver Physiol 2011; 301: G799-807.
- Rosa D, Zablah RA, Vazquez-Frias R. Unraveling the complexity of Disorders of the Gut-Brain Interaction: the gut microbiota connection in children. Front Pediatr 2024; 11: 1283389.
- Bellini M, Gambaccini D, Stasi C, Urbano MT, Marchi S, Usai-Satta P. Irritable bowel syndrome: a disease still searching for pathogenesis, diagnosis and therapy. World J Gastroenterol 2014; 20: 8807-20.
- Klem F, Wadhwa A, Prokop LJ, et al. Prevalence, Risk Factors, and Outcomes of Irritable Bowel Syndrome After Infectious Enteritis: A Systematic Review and Meta-analysis. Gastroenterology 2017; 152: 1042-54.
Vías interconectadas relacionan los lípidos plasmáticos, la microbiota fecal y la actividad cerebral con la cognición asociada a la desnutrición infantil
ARTÍCULO COMENTADO - Niño
Por el Prof. Emmanuel Mas
Gastroenterología y nutrición, Hospital de Niños, Toulouse, Francia
Comentario del artículo de Portlock et al., Nat Commun 1

La desnutrición afecta a más de 30 millones de niños cada año, con profundas repercusiones inmediatas y duraderas. Los niños que sobreviven suelen presentar secuelas neurocognitivas duraderas, que afectan al rendimiento escolar y su situación socioeconómica. Aún no se conocen bien los mecanismos que provocan estos efectos. Mediante modelos SHAP interpretados por análisis multisistémicos de bosques aleatorios y redes, los autores muestran que la desnutrición aguda moderada (DAM) se asocia a un aumento de la presencia de Rothia mucilaginosa y Streptococcus salivarius en las heces y a una disminución de Bacteroides fragilis en un grupo de niños de un año de Dacca, (Bangladés). Estas modificaciones del microbioma forman vías interconectadas que implican una reducción de los niveles plasmáticos de ácidos grasos de cadena impar, una reducción de la potencia de las onda gamma y beta del encefalograma en las regiones temporales y frontales del cerebro, y una reducción de la vocalización. Estos resultados confirman la hipótesis según la cual una colonización prolongada por especies comensales orales retrasa el desarrollo del microbioma intestinal y del cerebro. Aunque hay que confirmar los vínculos causales con datos empíricos, este estudio aporta información útil para mejorar las intervenciones dirigidas a los déficits del neurodesarrollo asociados a la DAM.
¿Qué se sabe ya sobre este tema?
La desnutrición infantil es un grave problema de salud pública y una de las principales causas de mortalidad antes de los cinco años de edad. La desnutrición aguda moderada (DAM) se asocia a un retraso del desarrollo neurocognitivo, pero aún se desconoce la relación. Se asocia también a una disbiosis de la microbiota intestinal (MI), cuyo desarrollo se ralentiza y está marcado por un enriquecimiento en especies de Bifidobacterium y Escherichia. Es posible que estas alteraciones de la MI repercutan en el desarrollo cerebral a través del eje intestino-cerebro, debido a una absorción defectuosa de nutrientes o a la acumulación de metabolitos tóxicos. En esta comunicación entre órganos podrían intervenir indirectamente los lípidos plasmáticos, ya que los lípidos son el constituyente esencial del cerebro y están modulados por metabolitos de la MI, como los ácidos biliares.
¿Cuáles son los principales resultados aportados por este estudio?
Este estudio se realizó en la región de Mirpur (Bangladés) y comparó a 159 niños con DAM con 75 testigos bien nutridos a la edad de 12 meses. La DAM se definió por una relación peso/altura entre - 2 y – 3 puntuaciones Z. El grupo DAM se asoció significativamente con factores sociodemográficos (tipo de parto, inodoros y agua tratada–hervidor).
La DAM se asoció con una disminución de la diversidad alfa bacteriana (Shannon), un aumento de la prevalencia y abundancia de Rothia mucilaginosa y Streptococcus salivarius (figura 1), y con un aumento de la relación Bacteroidetes/ Firmicutes. No se observaron diferencias en los análisis funcionales de la MI.
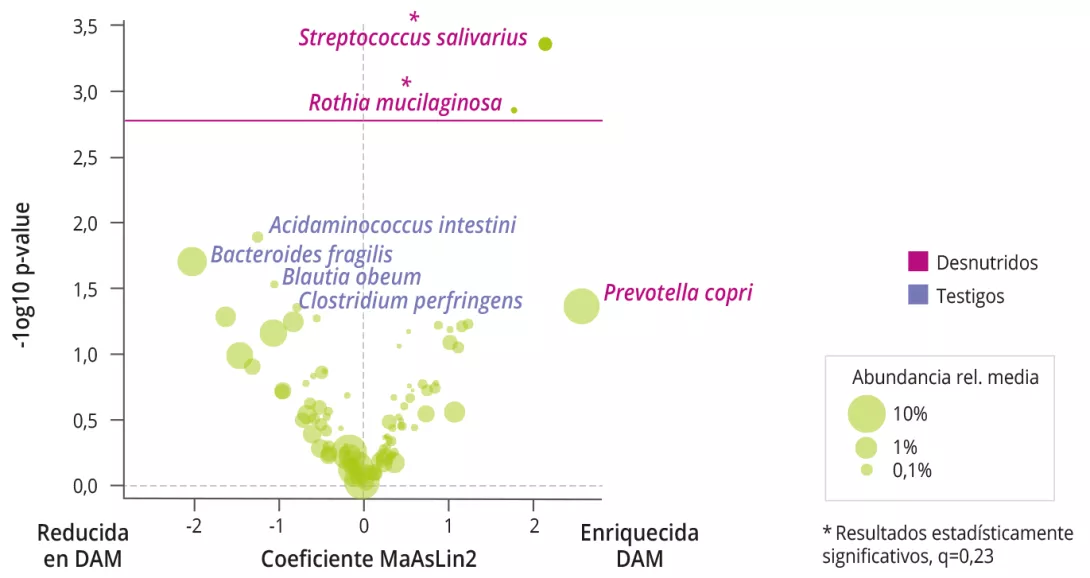
En el electroencefalograma (EEG) se observó una disminución significativa de las frecuencias beta (12-30 Hz) y gamma (30-45 Hz) en la región temporal y frontal en los niños con DAM. Además, se detectó una reducción significativa de las puntuaciones de comunicación expresiva, motricidad fina y gruesa y vocalización.
Después de ajustar por tipo de parto, sexo y duración de la lactancia materna exclusiva, la DAM se asoció con cambios en el lipidoma plasmático, con un aumento de la abundancia relativa de 128 (16 %) compuestos y una disminución de 189 (24 %) (figura 2).
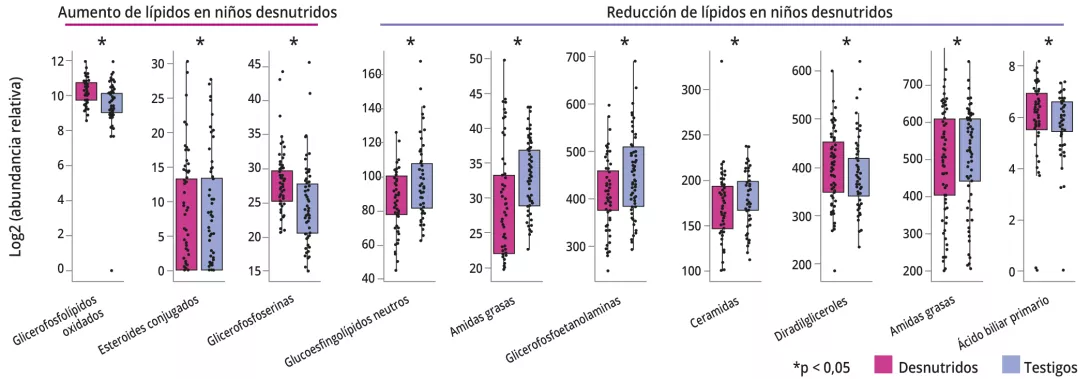
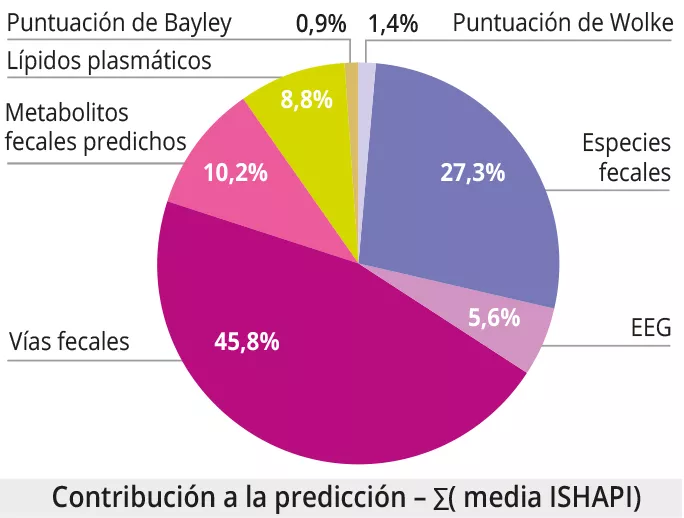
La integración de datos multimodales demostró que los mejores predictores de DAM a los 12 meses eran: 1) los lípidos plasmáticos (AUROC = 0,95 0,05); 2) las mediciones cerebrales y conductuales (puntuación de Wolke, EEG, puntuación de Bayley) (AUROC = 0,73 0,05, 0,71 0,10, 0,68 0,07 respectivamente); 3) el perfil taxonómico, funcional y de metabolitos predichos del microbioma fecal (AUROC = 0,56 0,07, 0,53 0,07, 0,52 0,06). Hay que señalar que el microbioma fecal desempeña una función importante en la predicción de la DAM en el análisis multimodal, a pesar de los malos resultados del microbioma fecal (figura 3).
El análisis de redes multimodales permitió predecir que una agrupación de B. fragilis, de vías de fermentación del piruvato, de ceramidas plasmáticas, de EEG y de comunicación expresiva estaba estrechamente correlacionada con un buen estado nutricional a los 12 meses. Por último, el efecto más fuerte como interacción entre especies se observó entre R. mucilaginosa y S. salivarius, cuya presencia combinada amplificó la predicción de DAM a los 12 meses.
¿Cuáles son las consecuencias en la práctica?
Este estudio demuestra la importancia de la MI en el estado nutricional del lactante. La presencia de bacterias orales grampositivas comensales y anaerobias facultativas como R. mucilaginosa y S. salivarius podría ser la causa de la desregulación de los ácidos biliares. Esto a su vez podría provocar modificaciones lipídicas, importantes para el desarrollo cerebral.
Además, es importante destacar el beneficio de B. fragilis en relación con las vías de fermentación sobre el estado nutricional a los 12 meses.
- La persistencia de las bacterias comensales Rothia mucilaginosa y Streptococcus salivarius en el intestino de los niños del grupo DAM reemplaza la colonización por Bacteroides fragilis. Esto interfiere en la síntesis de ácidos grasos, fundamentales para el desarrollo del cerebro
CONCLUSIÓN
Este estudio demuestra que la disbiosis de la microbiota intestinal se asocia con anomalías en el desarrollo cerebral de niños
con DAM, mediante modificaciones de los lípidos plasmáticos.
Hacia un índice de especies clave asociado a la salud para la microbiota intestinal humana
ARTÍCULO COMENTADO - Adulto
Por el Pr. Harry Sokol
Gastroenterología y nutrición, Hospital Saint-Antoine, París, Francia
Comentario del artículo de Goel et al., Cell Reports 2025 1

Un índice sólido de taxones del microbioma intestinal, que incluyera su asociación con la salud del anfitrión y la resiliencia del microbioma, sería muy valioso para el desarrollo y la optimización de tratamientos basados en el microbiota. Los autores presentan aquí una clasificación única de 201 taxones, el índice Health-Associated Core Keystone (HACK), elaborado a partir de su prevalencia/asociación comunitaria en personas no enfermas, su estabilidad temporal y su asociación con la salud del anfitrión. Este índice se ha elaborado a partir de 127 cohortes de descubrimiento y de 14 conjuntos de datos de validación (que agrupan un total de 45 424 microbiotas intestinales procedentes de personas mayores de 18 años, y que abarcan 42 países, 28 categorías de enfermedades y 10 021 muestras longitudinales). Los autores demuestran que este índice es reproducible, independientemente de las estrategias de análisis del microbioma y de los estilos de vida de las cohortes. Ciertos grupos de taxones con un elevado índice HACK responden de forma positiva a intervenciones basadas en una alimentación mediterránea y se asocian a una mejor respuesta a los inhibidores de puntos de control inmunitario y a los perfiles funcionales específicos a nivel genómico. La disponibilidad de los índices HACK proporciona así una base racional para comparar microbiomas y facilitar la selección y el diseño de tratamientos basados en el microbiota.
¿Qué se sabe ya sobre este tema?
Los tratamientos basados en el microbioma intestinal (probióticos, productos bioterapéuticos vivos, pre/simbióticos, trasplantes fecales) buscan restablecer una microbiota sana, pero su éxito varía según las distintas poblaciones. Para optimizar estos enfoques, se necesitaría una definición consensuada del microbioma “sano”, difícil tarea debido a la gran variabilidad entre individuos. Sin embargo, los metaanálisis muestran a taxones sistemáticamente empobrecidos o enriquecidos en numerosas enfermedades, lo que sugiere
que los microbios pueden situarse a lo largo de un continuo de vínculos con la salud del anfitrión 2, 3. Las especies que encabezan esta clasificación son las que presentan un mayor potencial: i) como agentes terapéuticos directos o para incrementar su concentración; ii) como marcadores de eficacia clínica. Así, los autores proponen crear un índice de priorida que se componga de tres criterios: asociación positiva con la salud, contribución a la estabilidad de la microbiota y gran “interacción” comunitaria. Este índice, explotable en amplios conjuntos de datos públicos, podría servir para seleccionar y evaluar de forma racional las futuras estrategias terapéuticas microbianas.
¿Cuáles son los principales resultados aportados por este estudio?
A partir de una cohorte de descubrimiento compuesta por 39 926 microbiomas intestinales procedentes de 127 cohortes (datos transversales y longitudinales que abarcan 42 países y 28 patologías diferentes), los autores elaboraron una clasificación de 201 taxones prevalentes de microbiota intestinal (detectados en un ≥5 % de las muestras en ≥50 % de las cohortes estudiadas), el “índice HACK” (Health-Associated Core Keystone Index), asignándoles una puntuación basada en tres propiedades cuantificables: i) prevalencia/asociación comunitaria en personas no enfermas; ii) estabilidad temporal; y iii) asociación negativa con la enfermedad.
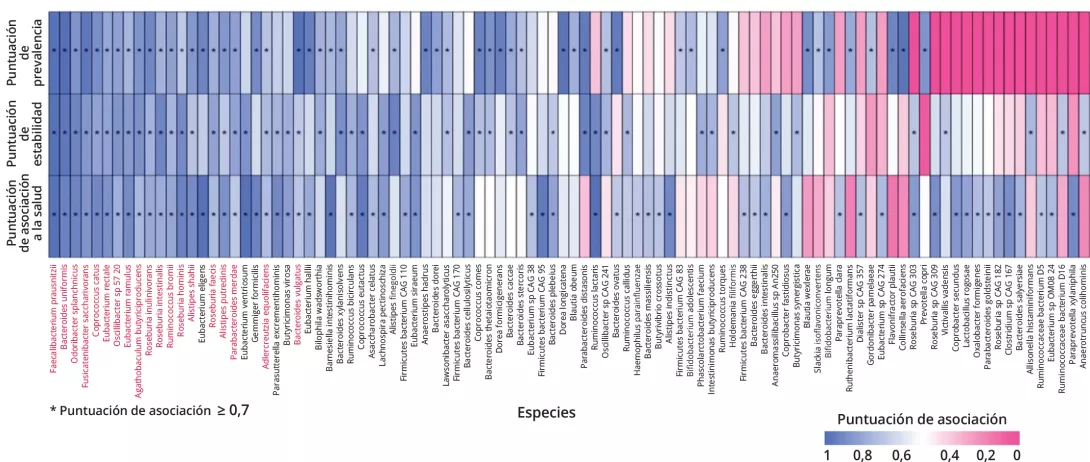
El índice HACK se calculó como el producto de dos puntuaciones: i) la media de las puntuaciones de asociación de un taxón para cada una de las tres propiedades; y ii) una puntuación de recompensa que evalúa la similitud (o la distribución equilibrada) de estas tres puntuaciones entre sí. El análisis de los taxones con mejor clasificación según este orden reveló 17 taxones con un índice HACK de ≥75 % (figura 1). Todos estos taxones obtuvieron puntuaciones de ≥70 % en las tres propiedades. Entre ellos había Faecalibacterium
prausnitzii, un conocido marcador de salud del microbioma 4, seguido de Bacteroides uniformis. En esta lista también se encontraban varias especies de los géneros Roseburia, Alistipes y Eubacterium, además de Coprococcus catus.
A continuación, los autores demostraron la reproducibilidad de las puntuaciones individuales y del índice HACK en su conjunto volviendo a calcular las puntuaciones de asociación individualmente en cada cohorte, utilizando diferentes métodos de secuenciación (secuenciación indiscriminada o shotgun o 16S) y diferentes tipos de población (urbana industrializada en comparación con otras), y después en un conjunto de validación adicional compuesto por 14 cohortes adicionales con un total de 5498 microbiomas.
Más allá de su estrecha relación con la salud y la estabilidad de la microbiota, algunos taxones que presentan un índice HACK elevado se asocian a una respuesta favorable a distintas intervenciones terapéuticas relacionadas con la microbiota, como la alimentación mediterránea o la inmunoterapia contra el cáncer.
Con el análisis de las anotaciones funcionales de todo el genoma obtenidas a partir de 32 005 genomas que abarcaban 122 de los 201 taxones, los autores identificaron 150 familias de funciones específicamente enriquecidas y conservadas en los genomas de los taxones con un índice HACK elevado. Esto representa una amplia gama de funciones: producción de butirato/propionato con propiedades
antinflamatorias, síntesis de numerosas vitaminas, biosíntesis de aminoácidos neuroactivos como el triptófano, así como de sus derivados antinflamatorios beneficiosos como los indoles y los sulfatos de condroitina. Se pueden explorar estas funciones para comprender los mecanismos subyacentes.
¿Cuáles son las consecuencias en la práctica?
Los índices HACK se calcularon a partir de una cohorte mundial de 45 000 microbiomas intestinales que abarcaban los seis continentes, en uno de los estudios más exhaustivos hasta la fecha. Estos índices representan un avance hacia la priorización racional
de especies microbianas intestinales como herramientas terapéuticas basadas en el microbioma. Además, las funcionalidades asociadas a los índices HACK podrían ayudar a identificar las vías y las capacidades metabólicas vinculadas a la salud general y a la estabilidad del microbioma.
- A partir de 45 454 microbiomas procedentes de 141 cohortes (42 países, 28 grupos de enfermedades), este estudio clasificó 201 taxones según sus modos de asociación con tres características fundamentales de la salud del anfitrión y el microbioma: i) prevalencia en personas no enfermas; ii) estabilidad temporal; y iii) asociación negativa con la enfermedad
- Entre las 17 bacterias con las puntuaciones más altas se encuentran Faecalibacterium prausnitzii y Bacteroides uniformis, en primer y segundo lugar.
- La clasificación fue reproducible independientemente del tipo de secuenciación y del estilo de vida de las cohortes.
- Los taxones con mejor clasificación están relacionados con respuestas positivas a distintas intervenciones terapéuticas relacionadas con la microbiota.
CONCLUSIÓN
Partiendo de una base de datos muy extensa, este estudio permite identificar un grupo de 17 taxones particularmente prevalentes, estables a lo largo del tiempo y asociados a la salud. Además de avanzar hacia la definición de los componentes
clave de la microbiota humana en términos de taxonomía y de funciones, este trabajo ofrece una base racional para la definición de nuevos tratamientos basados en la microbiota intestinal o dirigidos a ella.
- Goel A, Shete O, Goswami S, et al. Toward a health-associated core keystone index for the human gut microbiome. Cell Rep 2025 ; 44 : 115378.
- Shanahan F, Ghosh TS, O’Toole PW. The Healthy Microbiome—What Is the Definition of a Healthy Gut Microbiome? Gastroenterology 2021 ; 160 : 483-94.
- Pasolli E, Asnicar F, Manara S, et al. Extensive Unexplored Human Microbiome Diversity Revealed by Over 150,000 Genomes from Metagenomes Spanning Age, Geography, and Lifestyle. Cell 2019 ; 176 : 649-62.
- Martín R, Rios-Covian D, Huillet E, et al. Faecalibacterium: a bacterial genus with promising human health applications. FEMS Microbiol Rev 2023 ; 47.
Cuando los fármacos se encuentran con los microbios: un diálogo bidireccional con consecuencias terapéuticas
Por el Prof. Emmanuel Montassier
Urgencia, Cuidados Intensivos, Reanimación, Medicina Interna y Enfermedades Infecciosas, Universidad de Nantes, Francia

Las interacciones bidireccionales entre fármacos orales y microbioma intestinal se consideran cada vez más importantes para la eficacia, seguridad y tolerancia de los medicamentos. Aunque es bien sabido que los antibióticos alteran las comunidades microbianas, en torno al 24 % de los fármacos no antibióticos también inhiben al menos a una especie comensal. Además, entre el 10 y el 15 % de los medicamentos ora les son transformados por los microbios intestinales in vivo, lo que influye en su eficacia o toxicidad. Los medicamentos habituales como los inhibidores de la bomba de protones (IBP), los antinflamatorios no esteroideos (AINE), la metformina y las estatinas, pueden alterar la composición y la función de la microbiota, influyendo en el metabolismo y en la inmunidad del anfitrión. A pesar de estos hallazgos, es frecuente no tener en cuenta el microbioma en el momento de recetar y desarrollar medicamentos. Esta revisión resume los principales conocimientos clínicos y farmacodinámicos, destaca las notables interacciones entre fármacos y microbiota y explora las estrategias emergentes para mejorar los desenlaces clínicos. La integración de la farmacomicrobiómica en la atención clínica puede reducir los efectos y ayudar a la medicina de precisión.
La microbiota intestinal actúa como un órgano metabólico, favoreciendo la digestión, la inmunidad y la homeostasis [1]. Sin embargo, su interacción con los fármacos es bidireccional: los medicamentos pueden alterar el equilibrio microbiano, mientras que los microbios pueden alterar la actividad de los fármacos. Esto hace que el microbioma sea un factor importante, aunque a menudo descuidado, en el riesgo de reacciones adversas a medicamentos (RAM) 2, 3. Las enzimas microbianas intestinales pueden transformar los fármacos en formas más tóxicas, aumentando la exposición de los tejidos y sus efectos nocivos. Hay cada vez más pruebas de que la variabilidad microbiana es un factor clave de las diferencias individuales en la respuesta a los fármacos y las reacciones adversas 2, 4. La integración de la farmacomicrobiómica en la evaluación del riesgo junto con los datos genéticos y clínicos podría ayudar a predecir la predisposición a los daños relacionados con los medicamentos y a orientar estrategias de prevención personalizadas.
Alteración de la microbiota provocada por fármacos: antibióticos y más allá
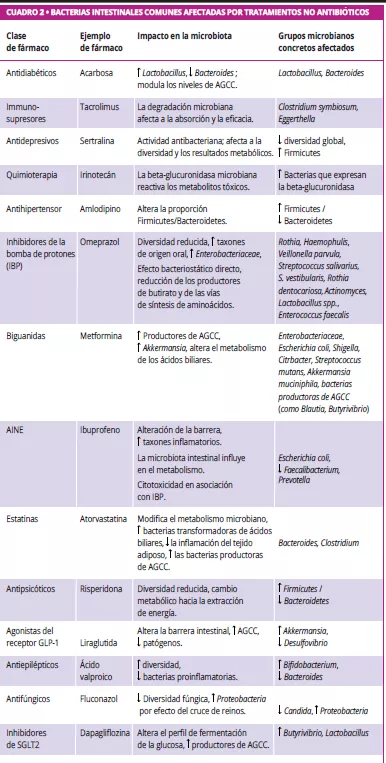
Es bien sabido que los antibióticos alteran la microbiota intestinal reduciendo la diversidad, alterando la composición y promoviendo cepas resistentes (cuadro 1) 5, 6. Van Zyl et al. descubrieron que los antibióticos especialmente las quinolonas y los betalactámicos, alteran sistemáticamente las comunidades microbianas en todas las zonas del cuerpo, y que los tratamientos combinados provocaban una disbiosis prolongada y un aumento de la carga patógena 5. Del mismo modo, Maier et al. demostraron que las diferentes clases de antibióticos tienen efectos distintos en las bacterias intestinales, los macrólidos y las tetraciclinas provocan pérdidas constantes de anaerobios, y fármacos como la amoxicilina y la ceftriaxona desplazan las poblaciones hacia las Proteobacterias. A pesar de la variabilidad individual, se observó una tendencia común: el agotamiento de anaerobios estrictos (por ejemplo, Firmicutes) y el enriquecimiento de microbios facultativos y potencialmente patógenos 6.
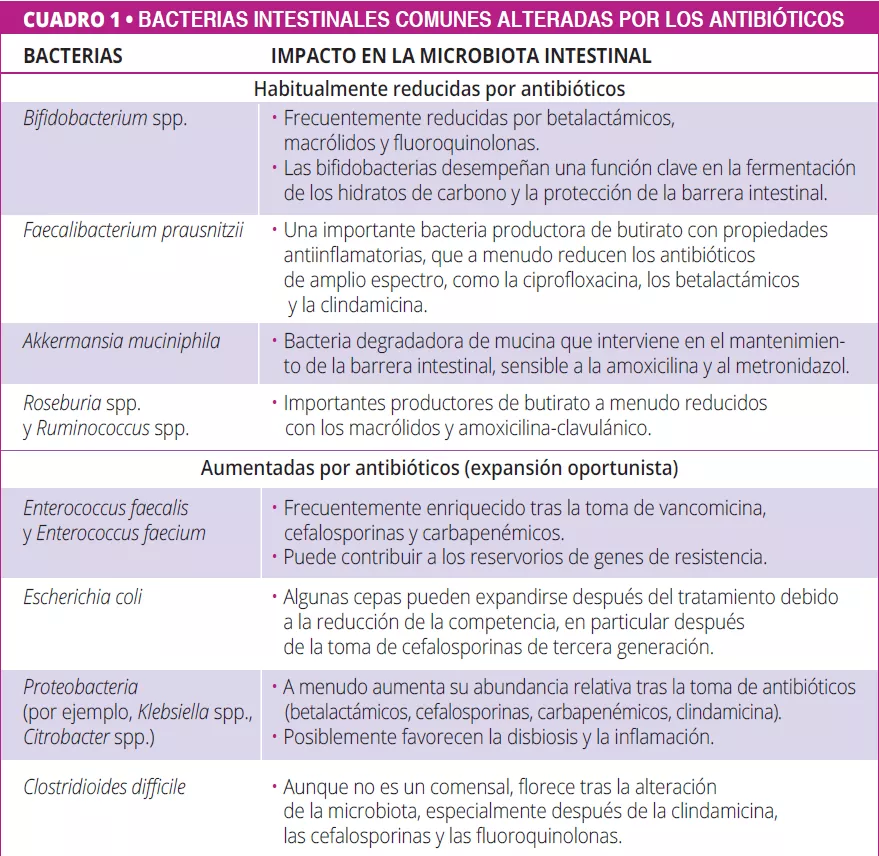
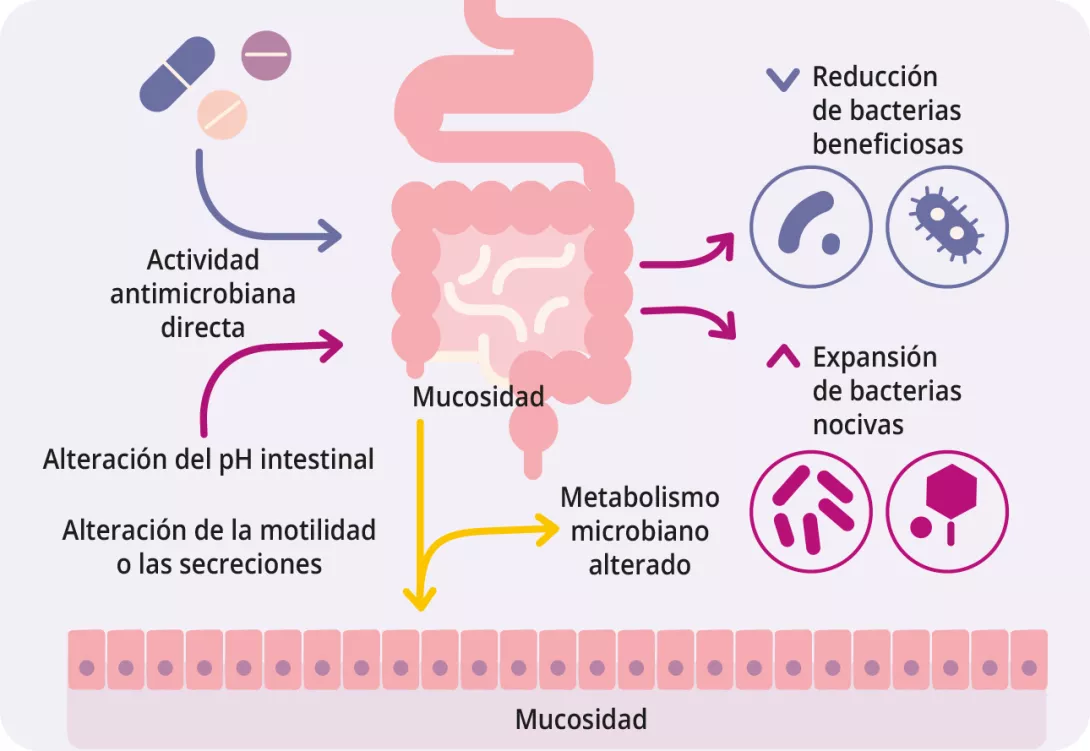
Más allá de los antibióticos, existen muchos fármacos no antibióticos como los IBP, la metformina, los AINE, los antipsicóticos y las estatinas que también alteran la microbiota intestinal (figura 1, cuadro 2) 7, 8. Los fármacos influyen en la microbiota intestinal a través de varios mecanismos: la acción antimicrobiana directa, la alteración del pH, la modulación de los ácidos biliares, los cambios en la motilidad intestinal y la secreción de moco 9.
La microbiota intestinal modifica el metabolismo de los fármacos
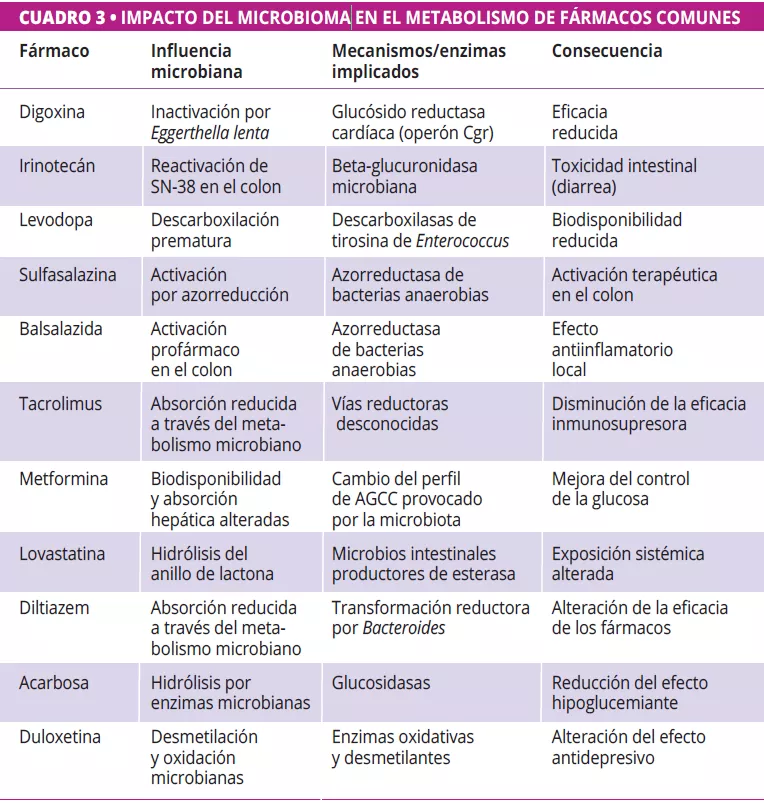
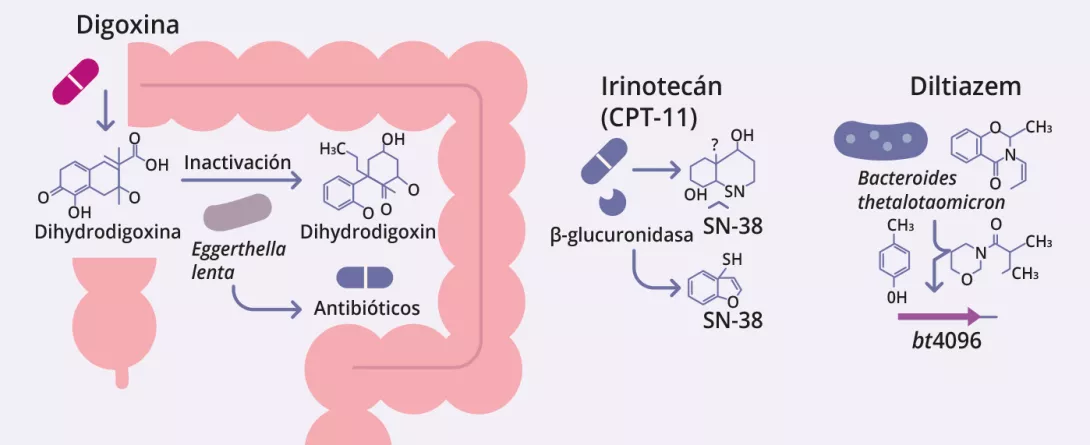
La microbiota intestinal puede biotransformar los fármacos terapéuticos, alterando su actividad, eficacia y toxicidad (figura 2, cuadro 3) 12-14. Zimmermann et al. trazaron un mapa del metabolismo microbiano mediante el cribado de 271 fármacos orales frente a 76 cepas bacterianas intestinales, y descubrieron que 176 eran metabolizados por al menos una cepa. En concreto, Bacteroides dorei y B. uniformis metabolizaron casi 100 fármacos. Se identificaron más de 40 enzimas microbianas que intervienen en una amplia gama de reacciones, como la reducción, la hidrólisis, la descarboxilación, la desalquilación y la desmetilación 12.
Javdan et al. desarrollaron una plataforma personalizada (MDM-Screen) para evaluar el metabolismo microbiano de los fármacos utilizando microbiota ex vivo de determinados donantes. Después de analizar 575 fármacos, descubrieron que el 13 % eran metabolizados por los microbios intestinales, incluidas muchas interacciones que no se habían reconocido anteriormente. Estas transformaciones, como la hidrólisis, la reducción y la desacetilación, pueden activar, inactivar o aumentar la toxicidad de los fármacos. El estudio reveló además una variabilidad significativa entre las personas, e identificó genes microbianos clave (por ejemplo, uridina fosforilasa, beta-glucuronidasa) vinculados a vías metabólicas específicas 15.
La eficacia de algunos fármacos puede depender más de la composición de la microbiota que de la genética del anfitrión.
Consecuencias clínicas: hacia una medicina personalizada
Las interacciones microbiota-fármaco tienen importantes implicaciones clínicas, ya que las diferencias individuales en la microbiota intestinal pueden explicar la variabilidad en la respuesta a los fármacos y sus efectos secundarios. Hay que señalar que lo que influye en los resultados del tratamiento no es únicamente la composición de la microbiota, sino también su estabilidad funcional.
En el melanoma avanzado, los pacientes que respondían bien al tratamiento anti-PD-1 presentaron funciones microbianas estables y
linfocitos CD8+ reactivos a los péptidos bacterianos de Lachnospiraceae, que imitan antígenos tumorales, lo que pone de relieve la funcionalidad microbiana como posible marcador pronóstico y complemento terapéutico en la inmunoterapia contra el cáncer 16.
Estos datos ponen de relieve la necesdad de integrar la genómica humana y microbiana en las evaluaciones farmacológicas. En el desarrollo de fármacos, la simulación informática de las interacciones microbiota-fármaco ha pasado a ser un elemento clave. Dodd y Cane propusieron un marco detallado que combina sistemas in vitro (como bibliotecas de cepas, comunidades derivadas de heces), herramientas
genéticas (ensayos de ganancia/ pérdida de función) y metagenómica para identificar genes microbianos implicados en el metabolismo de fármacos. Los modelos murinos gnotobióticos ayudan a diferenciar los efectos microbianos de los de los anfitriones en la farmacocinética.
A medida que avanza este campo, se perfila que una manera de personalizar los tratamientos y de reducir los efectos adversos será la prescripción teniendo en cuenta a la microbiota. En el futuro, la farmacomicrobiómica podría orientar las elecciones de fármacos y su posología según los biomarcadores microbianos, para dar paso a una medicina verdaderamente personalizada 17.
Es posible que, en el futuro, la personalización del tratamiento necesite de un perfil de la microbiota.
Preservar y restablecer la microbiota: Una frontera terapéutica
Proteger la microbiota intestinal durante el tratamiento farmacológico es una estrategia prometedora para reducir los efectos adversos y preservar la eficacia. Aunque se ha observado que los probióticos y los prebióticos presentan algunos beneficios contra la disbiosis inducida por fármacos, su eficacia varía. Los probióticos específicos adaptados a efectos farmacológicos concretos y el trasplante de microbiota fecal (TMF), en concreto para la infección recurrente por C. difficile, ofrecen opciones más fiables.
Se están investigando herramientas de precisión como inhibidores de enzimas microbianas (por ejemplo, bloqueadores de la beta glucuronidasa para frenar la toxicidad del irinotecán), probióticos de bioingeniería, el desarrollo de fármacos que no afecten a la microbiota e intervenciones basadas en la alimentación. Los ensayos clínicos están explorando los simbióticos adaptados a la farmacoterapia para mejorar los resultados con la mínima alteración de la microbiota. También se están evaluando los postbióticos, como el butirato, por sus efectos antiinflamatorios y de refuerzo de la barrera intestinal.
La integración de estrategias dirigidas a la microbiota en la farmacología necesitará herramientas avanzadas —multiómica, aprendizaje automático y modelización de sistemas del microbioma— para predecir y gestionar eficazmente las interacciones microbiota-fármaco.
La manipulación de la microbiota intestinal puede mejorar el éxito del tratamiento y reducir las complicaciones.
CONCLUSIÓN
Las interacciones microbiota-fármaco son un aspecto emergente y a menudo ignorado de la medicina, que tiene importantes repercusiones en los resultados de los tratamientos. La integración de estos conocimientos en la práctica clínica es fundamental para desarrollar tratamientos más seguros, más precisos y respetuosos con la microbiota. A medida que aumentan las pruebas, surgen nuevas oportunidades de modular el microbioma y así potenciar la eficacia, reducir la toxicidad y recuperar las respuestas
a los fármacos.
Los planteamientos innovadores como los bioterapéuticos vivos, los microbios genomanipulados y los metabolitos derivados de la microbiota (“farmabióticos”) están remodelando la farmacoterapia. Aunque el interés normativo es cada vez mayor, los protocolos clínicos normalizados se encuentran aún en fase de desarrollo. En un futuro cercano, la ingeniería del microbioma podría convertirse en un componente habitual de la atención médica personalizada basada en sistemas.
- Valdes AM, Walter J, Segal E, Spector TD. Role of the gut microbiota in nutrition and health. BMJ 2018; 361: k2179.
- Zhao Q, Chen Y, Huang W, Zhou H, Zhang W. Drug-microbiota interactions: an emerging priority for precision medicine. Signal Transduct Target Ther 2023; 8: 386.
- Wallace BD, Wang H, Lane KT, et al. Alleviating cancer drug toxicity by inhibiting a bacterial enzyme. Science 2010; 330: 831-5.
- Bolte LA, Björk JR, Gacesa R, Weersma RK. Pharmacomicrobiomics: The Role of the Gut Microbiome in Immunomodulation and Cancer Therapy. Gastroenterology 2025 Online publication ahead of print.
- Nel Van Zyl K, Matukane SR, Hamman BL, Whitelaw AC, Newton-Foot M. Effect of antibiotics on the human microbiome: a systematic review. Int J Antimicrob Agents 2022; 59: 106502.
- Maier L, Goemans CV, Wirbel J, et al. Unravelling the collateral damage of antibiotics on gut bacteria. Nature 2021; 599: 120-4.
- Vich Vila A, Collij V, Sanna S, et al. Impact of commonly used drugs on the composition and metabolic function of the gut microbiota. Nat Commun 2020; 11: 362.
- Macke L, Schulz C, Koletzko L, Malfertheiner P. Systematic review: the effects of proton pump inhibitors on the microbiome of the digestive tract-evidence from next-generation sequencing studies. Aliment Pharmacol Ther 2020; 51: 505-26.
- Le Bastard Q, Berthelot L, Soulillou JP, Montassier E. Impact of non-antibiotic drugs on the human intestinal microbiome. Expert Rev Mol Diagn 2021; 21: 911-24.
- Maier L, Pruteanu M, Kuhn M, et al. Extensive impact of non-antibiotic drugs on human gut bacteria. Nature 2018; 555: 623-8.
- Weersma RK, Zhernakova A, Fu J. Interaction between drugs and the gut microbiome. Gut 2020; 69: 1510-9.
- Zimmermann M, Zimmermann-Kogadeeva M, Wegmann R, Goodman AL. Mapping human microbiome drug metabolism by gut bacteria and their genes. Nature 2019; 570: 462-7. •
- Haiser HJ, Gootenberg DB, Chatman K, Sirasani G, Balskus EP, Turnbaugh PJ. Predicting and manipulating cardiac drug inactivation by the human gut bacterium Eggerthella lenta. Science 2013; 341: 295-8.
- Takasuna K, Hagiwara T, Hirohashi M, et al. Involvement of beta-glucuronidase in intestinal microflora in the intestinal toxicity of the antitumor camptothecin derivative irinotecan hydrochloride (CPT-11) in rats. Cancer Res 1996; 56: 3752-7.
- Javdan B, Lopez JG, Chankhamjon P, et al. Personalized mapping of drug metabolism by the human gut microbiome. Cell 2020; 181: 1661-79.e22.
- Macandog ADG, Catozzi C, Capone M, et al. Longitudinal analysis of the gut microbiota during anti-PD-1 therapy reveals stable microbial features of response in melanoma patients. Cell Host Microbe 2024; 32: 2004-18.e9.
- Dodd D, Cann I. Tutorial: Microbiome studies in drug metabolism. Clin Transl Sci 2022; 15: 2812-37.








