Los cambios de la microbiota en la mujer
¿Qué pasa con tu microbiota en la edad adulta y por qué es importante? Desde las variaciones hormonales hasta las enfermedades crónicas, pasando por el riesgo de cáncer, la salud mental o incluso la libido, la investigación científica muestra que los desequilibrios en la microbiota intestinal, vaginal, cutánea e incluso seminal pueden tener un impacto profundo en la salud de las mujeres. ¿Cómo influyen las hormonas, los anticonceptivos, el estrés o el envejecimiento en tus ecosistemas microbianos? ¿Tus hábitos diarios o tu alimentación pueden ayudar a restablecer el equilibrio?
Explora el eje intestino-cerebro, las microbiotas íntimas, la fertilidad y la inflamación para comprender cómo cuidar tu microbiota puede fomentar el bienestar, prevenir ciertos trastornos y mejorar la calidad de vida en cada etapa de la vida adulta de las mujeres.

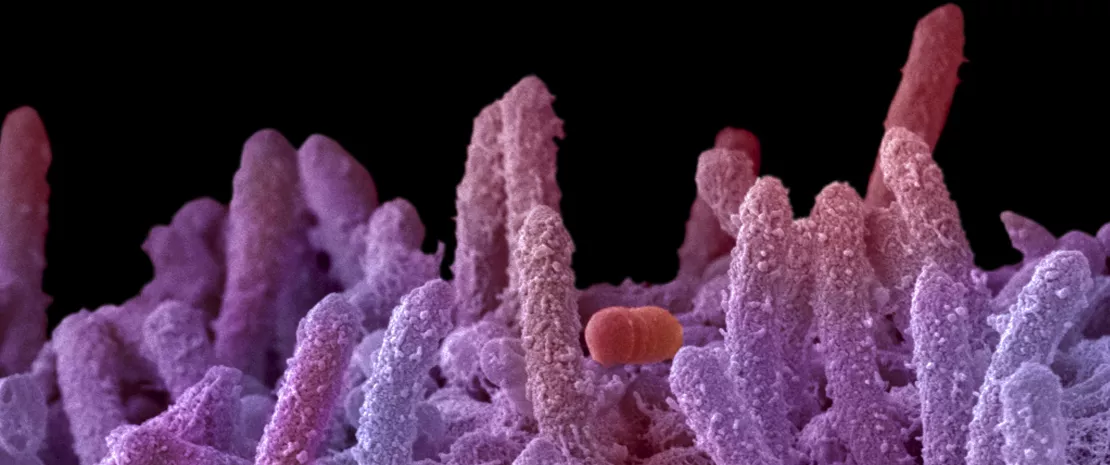
Microbiota vaginal y equilibrio íntimo
La microbiota femenina desempeña un papel esencial en la salud sexual, la salud menstrual, la fertilidad y las enfermedades vaginales.
¿Cómo influyen las hormonas, los anticonceptivos y los desequilibrios microbianos en estos distintos aspectos? Descubre los avances científicos más recientes sobre los vínculos entre la microbiota y la salud íntima.
Salud sexual, ITS y microbiota
Durante mucho tiempo pasados por alto, los vínculos entre la salud sexual, las infecciones de transmisión sexual (ITS) y la microbiota vaginal generan hoy un interés creciente en la investigación. Estos estudios destacan el papel de los ecosistemas microbianos en el riesgo de infección, los mecanismos de protección y el equilibrio íntimo en general.
Anticoncepción y microbiota
Estudios emergentes sugieren que los anticonceptivos pueden alterar la microbiota vaginal e intestinal, lo que podría influir en el riesgo de infecciones, la inflamación y la salud reproductiva. ¿Cómo afectan las hormonas, los dispositivos intrauterinos (DIU) o las píldoras a nuestros ecosistemas microbianos íntimos?
Salud menstrual y microbiota
La menstruación provoca cambios en las hormonas, la inmunidad y el equilibrio microbiano. Investigaciones emergentes revelan cómo la microbiota vaginal e intestinal podría influir en el dolor, la endometriosis y las infecciones. ¿Podrían los microbios ayudarnos a comprender mejor la salud menstrual?
Fertilidad, embarazo y microbiota
El papel de la microbiota en la fertilidad y el embarazo despierta un interés creciente en la investigación. ¿Podría una microbiota vaginal e intestinal equilibrada favorecer la concepción y reducir los riesgos de aborto espontáneo o de complicaciones durante el embarazo?
Enfermedades vaginales y microbiota
La salud vaginal está fuertemente influenciada por la microbiota. Los desequilibrios pueden conducir a patologías como la vaginosis bacteriana, las infecciones por hongos o la cistitis. ¿Qué papel juegan estas alteraciones microbianas en el desarrollo y el tratamiento de las enfermedades vaginales?

Hormonas femeninas y microbiota
Las variaciones hormonales a lo largo de la vida de una mujer, especialmente durante la menopausia, pueden tener un impacto importante en las microbiotas vaginal, intestinal y cutánea.
¿Cómo influyen estos cambios en la salud? ¿Actuar sobre la microbiota podría ayudar a regular las hormonas y a promover el bienestar? Descubre los avances científicos más recientes sobre el tema.
Equilibrio hormonal y microbiota
Las variaciones hormonales, como las que se observan durante la menopausia, influyen en la microbiota, con repercusiones en la salud vaginal, intestinal y cutánea. ¿Cómo afectan estos cambios al bienestar general y es posible actuar sobre la microbiota para preservar el equilibrio hormonal?
Menopausia y microbiota
La menopausia provoca cambios hormonales profundos que modifican la microbiota, especialmente a nivel vaginal e intestinal.
¿Cómo influyen estos cambios en la inflamación, la salud urinaria y el bienestar general? ¿Cuáles son las nuevas soluciones emergentes para acompañar esta etapa?
Enfermedades crónicas, cánceres y microbiota femenina
¿Puede un desequilibrio de la microbiota intestinal aumentar el riesgo de cáncer, de inflamación crónica o de infertilidad?
Las alteraciones en la microbiota intestinal, vaginal o seminal podrían influir en las enfermedades inflamatorias intestinales crónicas (EII), los resultados de la fecundación in vitro (FIV) y la progresión tumoral, abriendo así nuevas perspectivas en cuanto a prevención, diagnóstico e innovación terapéutica. Mantener el equilibrio microbiano podría convertirse en un pilar esencial de la salud femenina a lo largo de toda la vida.
Microbiota y cáncer: de los factores de riesgo a los tratamientos
¿Cómo influyen las microbiotas intestinal, mamaria o vaginal en el riesgo de cáncer y en su tratamiento? Descubre cómo el equilibrio microbiano puede impactar en los cánceres de mama y de cuello uterino, desde el manejo del dolor hasta la eficacia de la inmunoterapia.
La ciencia está revelando nuevos aliados poderosos en el abordaje del cáncer.
Infertilidad y microbiota
¿Puede un desequilibrio de la microbiota ser la causa de la infertilidad? Descubre cómo una disbiosis intestinal, vaginal o seminal puede afectar la fertilidad, los resultados de la fecundación in vitro (FIV) y la salud embrionaria. Investigaciones recientes destacan nuevas dianas microbianas para apoyar la concepción y la salud reproductiva de las parejas.
Inflamación y microbiota
¿Puede una microbiota desequilibrada desencadenar inflamación? Desde las enfermedades inflamatorias intestinales (EII) hasta la psoriasis, pasando por la artritis o los trastornos vaginales y urinarios, explora cómo las microbiotas intestinal, cutánea y vaginal influyen en la inflamación crónica y cómo podrían tener la clave para anticipar y mejorar los tratamientos.
Prevención y microbiota
¿Puede la microbiota contribuir a prevenir el cáncer, la infertilidad o las enfermedades inflamatorias intestinales (EII)? Descubre cómo los desequilibrios de la microbiota intestinal, vaginal y seminal conocidos como disbiosis pueden afectar la salud de las mujeres, y cómo restablecer este equilibrio microbiano podría favorecer la prevención de enfermedades e incluso ayudar en el diagnóstico.
Conexión intestino-cerebro y salud de las mujeres
¿Puede tu microbiota intestinal influir en tu estado de ánimo, tu nivel de estrés o incluso en tu libido? Muchas mujeres se preguntan por qué se sienten ansiosas, deprimidas o desconectadas, y la ciencia está revelando el papel clave del eje intestino-cerebro. Descubre cómo los desequilibrios en la microbiota intestinal y vaginal pueden alterar la salud mental y hormonal, y qué hábitos cotidianos pueden ayudar de forma natural a restablecer el equilibrio y el bienestar.
Efectos de la microbiota en la salud mental
¿Pueden las bacterias intestinales influir en la salud mental de las mujeres? En la edad adulta, la ansiedad, la depresión o los cambios de humor podrían estar relacionados con un desequilibrio en la microbiota intestinal. Descubre cómo el eje intestino-cerebro moldea el equilibrio emocional y abre nuevas vías para la prevención y el abordaje terapéutico.
Efectos de la microbiota en la libido
¿Puede la microbiota intestinal influir en la libido femenina? En mujeres adultas, una disminución del deseo sexual podría estar relacionada con una disbiosis intestinal, trastornos del estado de ánimo o con el eje intestino-cerebro. Explora cómo los desequilibrios microbianos pueden afectar la salud sexual y qué revela la ciencia sobre las formas de reavivar el deseo.
Microbiota: hábitos cotidianos que marcan la diferencia
¿Qué hábitos diarios ayudan a mantener una microbiota saludable? Desde una alimentación favorable para la flora intestinal hasta una higiene íntima adecuada, descubre consejos prácticos, accesibles y respaldados por la ciencia para apoyar el equilibrio de la microbiota intestinal y vaginal, y fortalecer la salud y el bienestar de las mujeres adultas.

Lo que las mujeres saben (y lo que no)
sobre su microbiota vaginal
¿Cuál es la relación entre la microbiota y la salud de las mujeres? El Observatorio Internacional de la Microbiota, basado en una encuesta realizada a 7,500 personas en 11 países, explora los conocimientos, percepciones y comportamientos de las mujeres con respecto a su microbiota intestinal, vaginal y urinaria. La edición 2024 revela una falta de sensibilización a nivel mundial, un interés creciente por el papel de la microbiota en la salud hormonal, digestiva e íntima, así como una fuerte demanda en términos de prevención, educación y acompañamiento. Sumérgete en el informe completo para descubrir los hallazgos clave, las cifras más destacadas y lo que realmente saben o desconocen las mujeres de todo el mundo sobre su microbiota.
Descubre la encuesta del Observatorio Internacional de la Microbiota 2024
BMI 25.13
 Anatomía femenina, microbiota e higiene íntima
Anatomía femenina, microbiota e higiene íntima
 ¿Cuál es el papel de la microbiota en la infertilidad?
¿Cuál es el papel de la microbiota en la infertilidad?