El impacto de la microbiota genital masculina en la salud femenina
Por el Prof. Jean-Mar Bohbot
Director del Institut Fournier, París, Francia
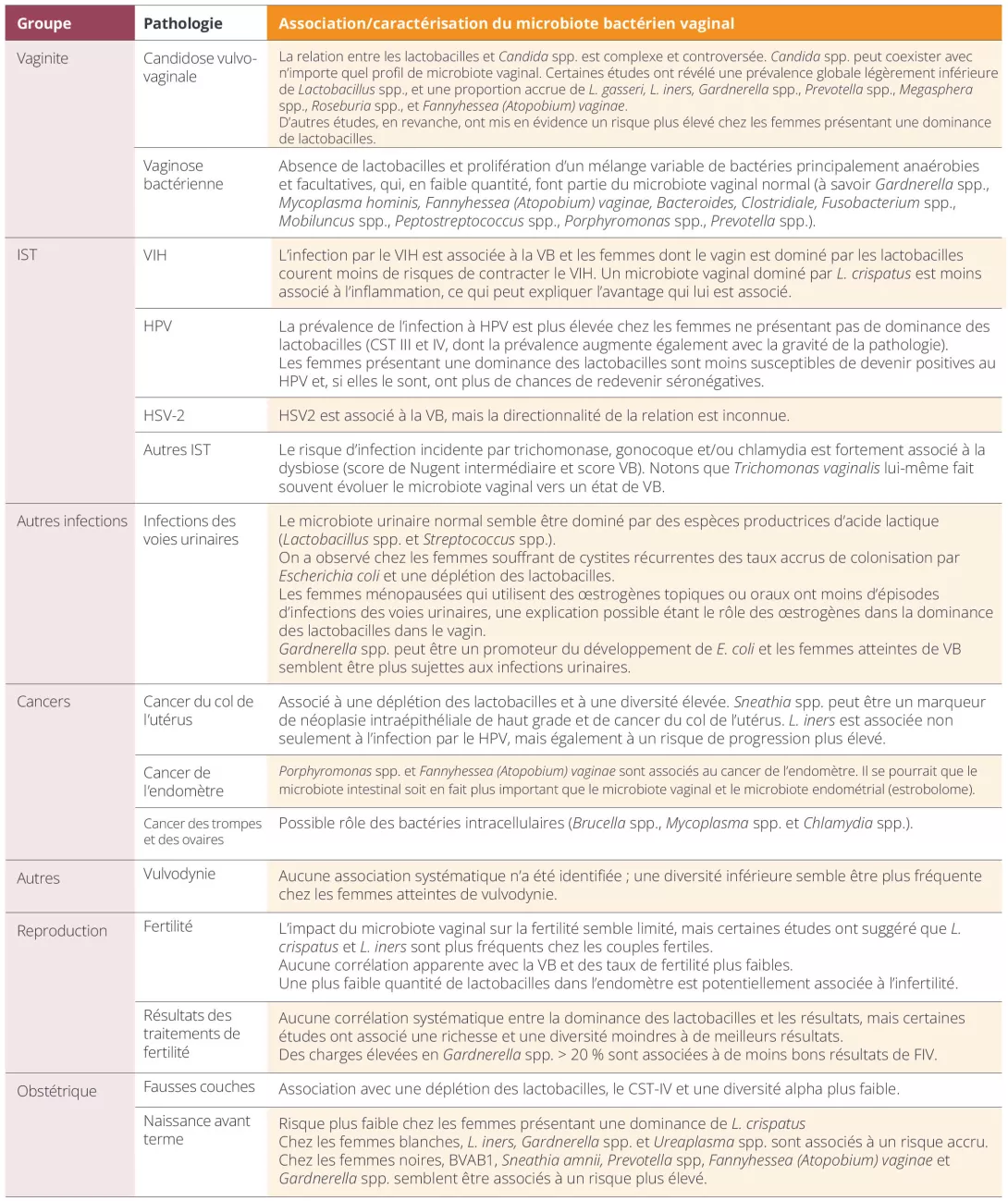
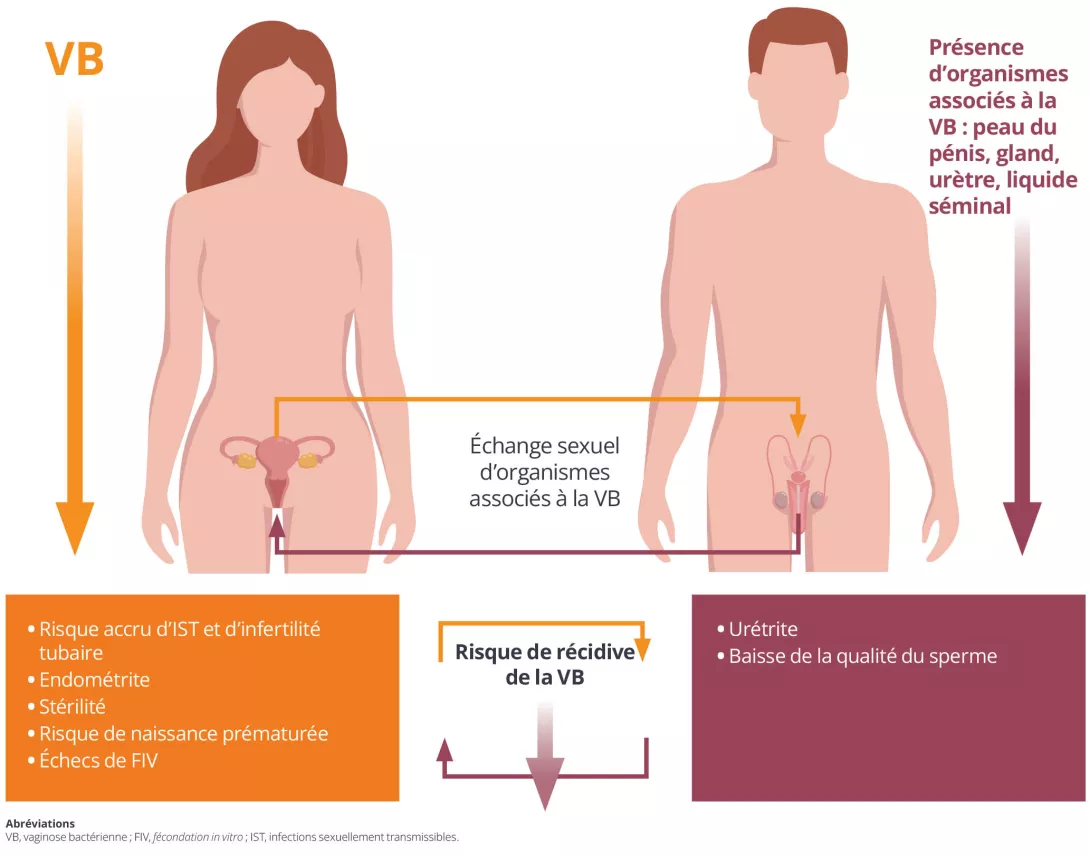
Las conversaciones sobre infecciones vaginales, fertilidad o complicaciones durante el embarazo suelen centrarse solamente en las mujeres. Pero hay otra pieza clave: el aparato urogenital masculino (AUGM) La gran variedad de microbios que existen en el AUGM pueden afectar significativamente la salud reproductiva y vaginal femenina (Figura 1). Comprender estas influencias puede mejorar los resultados para las mujeres, especialmente para aquellas con infecciones vaginales persistentes, problemas de fertilidad y complicaciones en el embarazo.
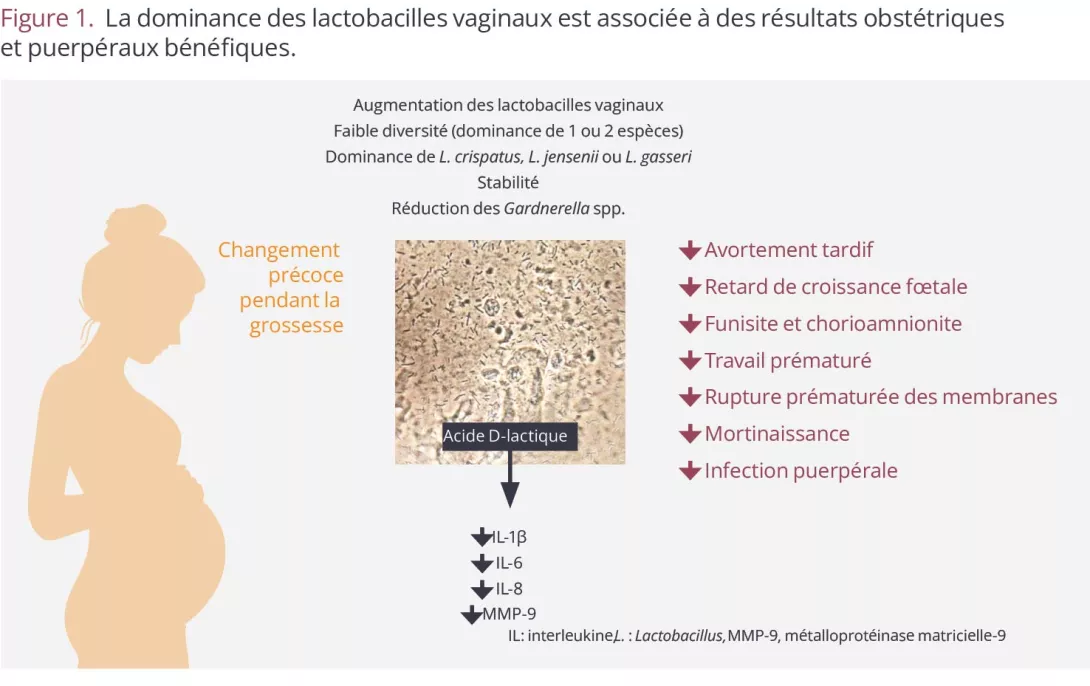
Figura 1. Consecuencias de los intercambios de bacterias asociadas con la vaginosis durante el contacto sexual entre hombres y mujeres
¿Qué conocemos de la microbiota genital masculina?
El AUGM alberga varios ambientes microbianos diferentes: la piel del pene, la uretra, el semen y el tracto urinario. Cada uno tiene una comunidad bacteriana única, influenciada por factores como la circuncisión, las prácticas sexuales, la higiene y el estilo de vida.
La piel del pene alberga bacterias similares a las que podemos encontrar en otras superficies cutáneas (piel), principalmente Corynebacterium y Staphylococcus genera1, 2. En hombres sin circuncidar, el área bajo el prepucio (el sulco balanoprepucial) se encuentra dominado por bacterias anaerobias, como Anaerococcus, Peptoniphilus, Finegoldia, y Prevotella, algunas de las cuales también se pueden encontrar en mujeres con vaginosis bacteriana (VB)1, 2. La circuncisión reduce significativamente estos anaerobios, lo que explicaría por qué las mujeres con parejas circuncidadas tienen menor riesgo de VB2 .
Tomar muestras directamente de la uretra es doloroso, por eso la mayoría de estudios usan la primera orina de la mañana como indicador para estudiar la microbiota de la uretra. Este fluido contiene una mezcla de bacterias como Lactobacillus, Streptococcus, Sneathia, Veillonella, Corynebacteria, y Prevotella3. Es interesante que algunas de ellas están relacionadas con la VB (por ejemplo, Gardnerella vaginalis) y la vaginitis aerobia (S. agalactiae) 4.
El semen no solo es esperma, sino que también contiene fluidos de la próstata y de las vesículas seminales. Los estudios demuestran que una microbiota seminal dominada por Lactobacillus está relacionada a un esperma de mejor calidad, mientras que otras bacterias (como por ejemplo, Ureaplasma, Mycoplasma, Prevotella, y Klebsiella pneumoniae) se asocian a una baja fertilidad5.
La microbiota urinaria masculina tiene menos estudios, pero se han encontrado niveles más bajos de géneros de Streptococcus, Lactobacillus, Pseudomonas, y Enterococcus en hombres con una concentración anómala de esperma comparados con aquellos con una concentración de esperma normal6. Los hombres con una motilidad espermática anormal pueden tener altos niveles de la bacteria Dialister micraerophilus, que contribuye a un microambiente proinflamatorio espermático6.
La microbiota del AUGM varía según la persona esté circuncidada o no, las prácticas sexuales y la composición de la microbiota vaginal femenina de su pareja7. Es interesante que la microbiota de la uretra de los hombres homosexuales no se ve modificada por el tipo de relaciones sexuales (oral o anal)8. Los intercambios de bacterias entre parejas durante el contacto sexual son la norma; no está claro el motivo por el que estos intercambios provocan disbiosis vaginal en algunos casos y en otros no.
La microbiota seminal también se ve influenciada por múltiples funciones fisiológicas (edad, cambios hormonales) y por el estilo de vida o factores epigenéticos (tabaco, alcohol, obesidad, dietas altas en grasa, exposición a toxinas)5. Estos factores modificables son objetivos potenciales de intervención.
¿Cómo impacta el AUGM a la salud femenina?
La transmisión de microorganismos responsables de las infecciones de transmisión sexual bacteriales y virales (ETS), incluida la infección del VIH y del herpes simple durante el contacto sexual, es la consecuencia más obvia del impacto del AUGM en la salud femenina. Las complicaciones de ETS bacterianas (gonorrea, infecciones por Chlamydia trachomatis o M. genitalium) son bien conocidas (inflamación e infección del tracto genital superior, riesgo de infertilidad tubárica).
Muchos estudios han demostrado que el perfil epidemiológico de mujeres con VB es comparable al de mujeres con ETS, lo que sugiere que la transmisión sexual de bacterias estaría implicada en la VB. La presencia de bacterias asociadas a la VB en el prepucio y la uretra de las parejas de las mujeres con VB y la coincidencia de cepas bacterianas vaginal y de la uretra masculina respaldan la idea de que las cepas de VB se comparten o se transmiten sexualmente
Tratar a la pareja masculina con antibióticos orales (metronidazol) ha tenido un impacto muy limitado en las tasas de reaparición en mujeres con VB recurrente, aunque combinar el metronidazol con un antibiótico tópico a la piel del pene en parejas de mujeres con VB reduciría el riesgo de reaparición9.
La influencia del AUGM en la salud uterovaginal no está limitada a la transmisión pasiva de bacterias. Los fluidos seminales contienen substancias proinflamatorias (como prostaglandinas) que pueden interferir con respuestas inmunes e inflamación en el tracto genital femenino10.
PUNTOS CLAVE
- La microbiota genital masculina tiene un papel importante pero poco reconocido en la salud reproductiva femenina, concretamente en las infecciones genitales recurrentes y los problemas de fertilidad.
- La revisión rutinaria de ETS puede no detectar bacterias importantes que no se clasifican normalmente como patógenos, pero que alteran la microbiota genital femenina.
- El tratamiento para la VB de las parejas masculinas necesitaría más que antibióticos orales, incorporando terapias tópicas y tratar factores de riesgo compartidos.
CONCLUSIÓN
La microbiota urogenital masculina es importante, no solo para la salud masculina, sino también para la de las mujeres. Mientras las investigaciones continúan evolucionando, es evidente que la dinámica, el estilo de vida y el intercambio microbiano de la pareja masculina influyen en la salud urogenital femenina. La evidencia respalda cada vez más un enfoque más holístico basado en parejas para tratar problemas de fertilidad, incorporando al hombre en el tratamiento con estrategias de rutinas sexuales y de salud reproductiva para mejores resultados para ambas partes, especialmente en casos de infecciones vaginales persistentes o recurrentes. Incentivar hábitos más saludables entre los hombres, como dejar de fumar o mejorar la dieta, pueden mejorar la salud microbiana seminal y reducir el riesgo de consecuencias negativas para sus parejas mujeres.