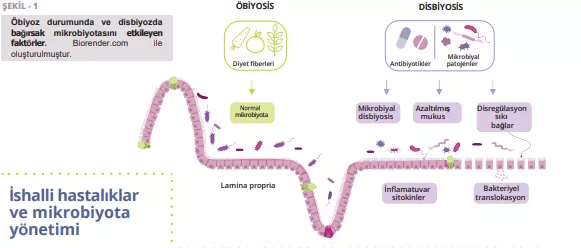
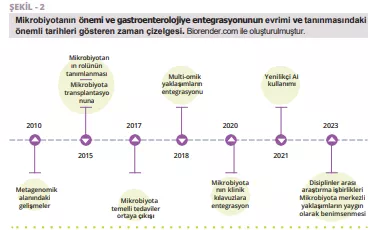
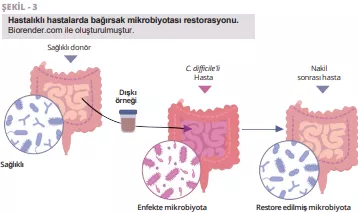
Fekal mikrobiyota transplantasyonu anti-PD-1 immünoterapi ile birlikte ileri melanomda: Faz I çalışması
YORUMLANMIŞ MAKALE
Yazan: Pr. Harry Sokol
Gastroenteroloji ve Beslenme Bölümü, SaintAntoine Hastanesi, Paris, Fransa
Routy ve diğerlerinin makalesine ilişkin yorumlar, Nature Medicine 2023 [1]
Fekal mikrobiyota transplantasyonu (FMT), refrakter melanomlu hastalarda immün kontrol noktası inhibitörlerine karşı direncin üstesinden gelmek için potansiyel bir stratejiyi temsil etmektedir; ancak FMT'nin birinci basamak tedavi ortamlarındaki rolü değerlendirilmemiştir. Yazarlar, sağlıklı donör FMT'yi PD-1 inhibitörleri nivolumab veya pembrolizumab ile birleştiren çok merkezli bir Faz I çalışması yürütmüştür. Daha önce tedavi edilmemiş 20 ileri melanom hastası. Güvenlik birincil sonlanım noktasıydı. FMT sırasında hiçbir 3. derece olay bildirilmemiştir. Beş hastada (%25) kombinasyon tedavisinden kaynaklanan 3. derece immün ilişkili advers olaylar görülmüştür. Temel ikincil sonlanım noktaları objektif yanıt oranı, bağırsak mikrobiyom bileşimindeki değişiklikler ve sistemik immün ve metabolomik analizler olmuştur. Objektif yanıt oranı, dördü (%20) tam yanıt olmak üzere %65 (20'de 13) olmuştur. Boylamsal mikrobiyom profili, tüm hastaların kendi donörlerinden gelen suşları aşıladığını ortaya koymuştur. Bununla birlikte, donör ve hasta mikrobiyomları arasındaki kazanılmış benzerlik yalnızca yanıt alanlarda zaman içinde artmıştır. Yanıt verenlerde FMT sonrası immünojenik bakterilerde bir zenginleşme yaşadı ve zararlı bakteriler azaldı. Sonuçlar, sağlıklı donörlerden alınan FMT'nin birinci basamakta güvenli olduğunu göstermiştir ve immün kontrol noktası inhibitörleri ile birlikte kullanıldığında daha fazla araştırmaya ihtiyaç duyulmaktadır.
Bu konu hakkında halihazırda ne biliyoruz?
- Anti-PD-1 monoterapisi alan ileri evre melanom hastalarının neredeyse yarısında primer direnç gelişmesi, immün kontrol noktası inhibitörlerine (ICI'ler) yanıtı iyileştirmek için yeni terapötik stratejiler geliştirme ihtiyacını vurgulamaktadır. Anti-PD-1 ve anti-CTLA4 (cytotoxic T-lymphocyte-associated antigen-4) kombinasyonu yanıt oranını artırsa da, bu tedavi yüksek sayıda bağışıklıkla ilişkili advers olay (IR-AE) ile sınırlıdır. Bağırsak mikrobiyomu, lokal ve sistemik bağışıklık yanıtlarının önemli bir düzenleyicisi olarak ortaya çıkmıştır. ICI'larla tedavi edilen kanser hastalarında yapılan deneysel çalışmalar, spesifik bağırsak bakterilerinin hem bağışıklık sistemi yanıtı hem de advers olaylarla ilişkili olduğunu göstermiştir [1]. Daha spesifik olarak, Ruminococcus, Faecalibacterium ve Eubacterium gibi belirli kommensal cinslerin varlığı melanom hastalarında olumlu sonuçlarla ilişkilendirilmiştir [2]. Bağırsak mikrobiyomunun terapötik potansiyeli ilk olarak, ICI direnci ile ilişkili yanıt vermeyen (NR) hastalardan alınan dışkı kullanılarak ICI'leri FMT ile birleştiren fare modellerinde gösterilmiştir [1]. İki çalışma, ICI tedavisine uzun süreli yanıt veren hastalarda FMT'nin, ICI'ye dirençli melanomlu hastaların en fazla %30'unda anti-PD-1 direncini önlediğini göstermiştir [3, 4]. Bu çalışmalarda, FMT sonrasında hastaların mikrobiyotasındaki değişmiş ve yanıt veren (R) hastalarda Ruminococcaceae ve Bifidobacteriaceae'de artış, ayrıca CD8+ T hücresi infiltrasyonu ve interferon-γ sinyalizasyonunda artış ile tümör mikroçevresinde yeniden programlama gözlenmiştir. Bu klinik bulgular, melanomda ICI direncinin üstesinden gelmek için mikrobiyom temelli müdahalelerin potansiyelini doğrulamaktadır.
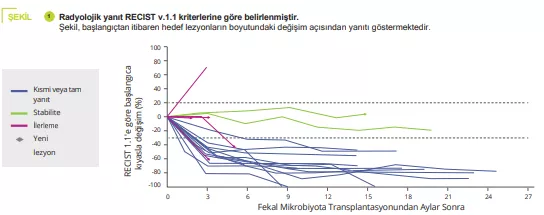
Bu çalışmadan elde edilen temel bilgiler?
Bu makalede yazarlar, ilerlemiş melanomlu tedavi naif hastalarda sağlıklı donörlerden elde edilen FMT'yi PD-1 inhibitörleri nivolumab veya pembrolizumab ile birleştiren bir Faz I çalışmasının (NCT03772899) klinik ve translasyonel bulgularını bildirmişlerdir (Şekil 1). Gözlemlenen toksisite (%25'i derece 3 toksisite ve sıfır derece 4 veya 5 toksisite olmak üzere %85 IR-AE) anti-PD-1 için Faz III çalışmalarında bildirilene benzerdi. Gözlenen klinik etkinlik (objektif yanıt %65), Faz III çalışmalarında (objektif yanıt %42-45) ve gerçek dünya verilerinde (objektif yanıt %17,2-51,6) nivolumab ve pembrolizumab monoterapisinden daha yüksektir. Bununla birlikte, kontrol kolunun olmaması ve çalışmanın küçük boyutu sonuçların yorumlanmasını engellemiştir.
Önceki çalışmalardan [3, 4] farklı olarak, birinci basamak tedavi alan hastalar dahil edilmiş, oral kapsül ile tek bir FMT gerçekleştirilmiş, donörler sağlıklı bireyler (ve ICI yanıt vermeyenler) olmuş ve son olarak hazırlık için sadece PEG (antibiyotik kullanılmadan) kullanılmıştır. Donörlerin ve alıcıların mikrobiyotasını inceleyen yazarlar, donörlerin mikrobiyotasının yanıt verenler Ruminococcus SGB15234 ve SGB15229, Alistipes communis, Eubacterium ramuleus ve Faecalibacterium SGB15346 bakımından zenginleşirken Enterocloster aldensis ve Enterocloster clostridioformis'in bolluğu azalmıştır. Önceki çalışmalarda da Faecalibacterium'daki artış ICI'ya verilen yanıtla ilişkilendirilmiştir [3, 4].
Yazarlar daha sonra insan mikrobiyotası ile kolonize edilmiş fareler üzerinde deneyler yapmış ve bu bağlamda sağlıklı bireylerden alınan dışkı transplantasyonunun benzer bir etkinliğe sahip olduğunu gözlemlemişlerdir; bu etki tümör mikroortamında CD8+ T bellek lenfositlerinin infiltrasyonundaki artışla ilişkilidir.
Uygulamadaki sonuçları nelerdir?
Kısıtlamalarına rağmen, bu çalışma FMT yoluyla mikrobiyota modülasyonunun metastatik melanom için birinci basamakta uygulandığında ICI etkinliğini artırabileceğini göstermiştir. FMT'nin geniş ölçekli kullanımı mevcut uygulamada zor görünse de, mikrobiyotanın özellikle yeni nesil probiyotiklerle modüle edilmesi, ICI ile birlikte standart bir tedavi haline gelebilir.
- Bağırsak mikrobiyotası ICI yanıtında rol oynar
- Metastatik melanom için birinci basamakta ICI ile tedavi edilen hastalarda sağlıklı donörlerden FMT uygulanabilir ve güvenlidir
- Bir kontrol kolunun olmaması ve çalışmanın küçük boyutuyla ilişkili sınırlamalara rağmen, ICI ile birlikte FMT alan hastalarda gözlenen klinik etkinlik, Faz III çalışmalarında ve gerçek dünya verilerinde ICI monoterapisinden daha yüksektir.
SONUÇ
Bu çalışma, metastatik melanom için birinci basamakta ICI ile tedavi edilen hastalarda sağlıklı donörlerden FMT'nin uygulanabilir ve güvenli olduğunu göstermiştir. Mikrobiyotanın FMT veya diğer yöntemlerle modüle edilmesi yönteminin ICI etkinliğini artırabileceği, ancak verilerin doğrulanması için daha büyük kontrollü çalışmalara ihtiyaç olduğu belirtilmiştir.
1. Routy B, Lenehan JG, Miller WH Jr, et al. Fecal microbiota transplantation plus anti-PD-1 immunotherapy in advanced melanoma: a phase I trial. Nat Med 2023; 29: 2121-32.
2. Gopalakrishnan V, Spencer CN, Nezi L, et al. Gut microbiome modulates response to anti-PD-1 immunotherapy in melanoma patients. Science 2018 ; 359 : 97–103.
3. Baruch EN, Youngster I, Ben-Betzalel G, et al. Fecal microbiota transplant promotes response in immunotherapy-refractory melanoma patients. Science 2021 ; 371 : 602–9.
4. Davar D, Dzutsev AK, McCulloch JA, et al. Fecal microbiota transplant overcomes resistance to anti-PD-1 therapy in melanoma patients. Science 2021 ; 371 : 595–602.