Bu konu hakkında halihazırda ne biliyoruz?
Dikkat eksikliği hiperaktivite bozuklu-ğu (DEHB) ve otizm spektrum bozukluğu (OSB) nörogelişimsel bozukluklardır. DEHB ve OSB olan bu çocuklarda sıklık-la karın ağrısı ve kabızlık gibi gastrointes-tinal bozukluklar görülür. Bu bozuklukla-rın ortaya çıkmasında genetik anormallik-lerin yanı sıra çevresel risk faktörleri ve özellikle de beslenme rol oynamaktadır. Bu nedenle, ilaç tedavilerine paralel ola-rak, bağırsak-beyin ekseninin düzenlen-mesinde esas olan bağırsak mikrobiyo-munun kompozisyonuna bağlı olarak di-yet yönetimi önerilmektedir. Dahası, OSB'li mikrobiyotasındaki bir değişimi açıklayabilecek nitelikte seçici beslenen kişiler olduğunu biliyoruz. Disbiyozise ek olarak, hem DEHB hem de OSB'de dü-şük dereceli sistemik inflamasyona ek olarak bağırsak geçirgenliğinde bir artış tanımlanmıştır. Bu çalışmanın amacı, sağlıklı kardeşler ve akraba olmayan kontrollerle karşılaştı-rıldığında DEHB, OSB ve hem DEHB hem de OSB olan gruplarda bağırsak mikrobiyotasındaki değişiklikleri analiz etmektir. İkincil hedefler ise bağırsak geçirgenliğini ve bağışıklık sistemini değerlendirmektir.
Bu çalışmadan elde edilen temel bilgiler nelerdir?
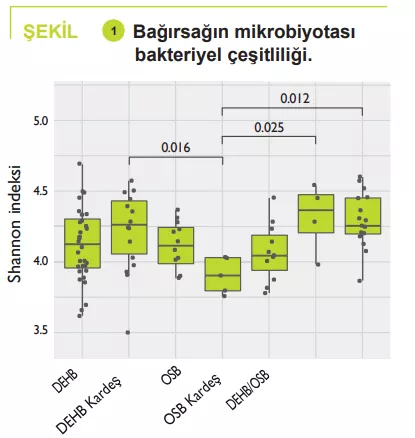
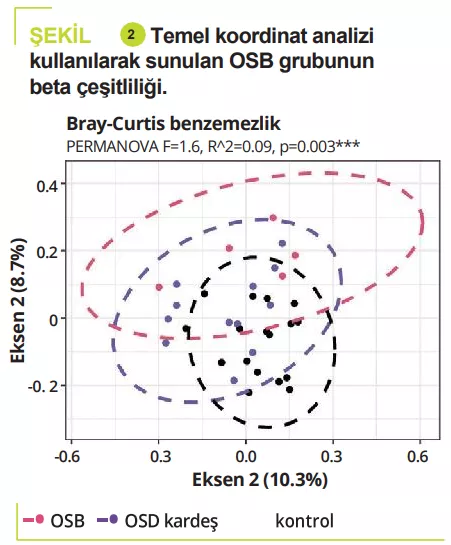
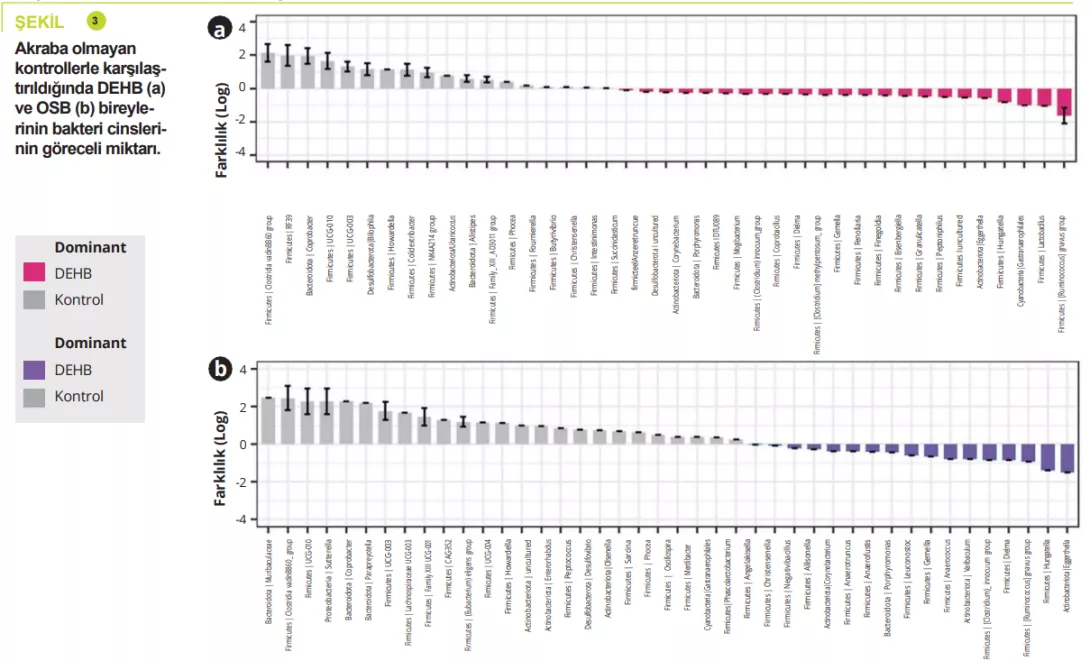
32 DEHB, 12 OSB, 11 DEHB/ASD, 14, 5, 4 kardeş ve 17 akraba olmayan kontrol olmak üzere 5-17 yaş arası top-lam 95 çocuk. Gastrointestinal bozukluk-lar kabızlık şeklindeydi: DEHB %15,6 (kardeşler %7,1), OSB %8,3 (kardeşler %0), DEHB/ASD %18,2 (kardeşler %0), kontroller %5,9; karın ağrısı: DEHB %3,1 (kardeşler %0), OSB %16,7 (kardeşler %0), DEHB/ASD %18,2 (kardeşler %0), kontroller %0; ve daha az sıklıkla gastro-özofageal reflü. Atipik diyetin en yaygın olarak OSB'li çocuklar arasında (%50) görüldüğü, esasen gıda alımında çeşitlilik olmadığı tespit edilmiştir. Bağırsak mikrobiyotasının analizi DEHB, OSB, DEHB/ASD ve akraba olan ya da olmayan kontroller arasında alfa çeşitli-liğinde herhangi bir farklılık bulamamıştır; aksine, OSB'li kardeşlerde alfa çeşitliliği önemli ölçüde düşüktür (şekil 1). Bağır-sak mikrobiyota bileşimi, beta çeşitliliği-nin gösterdiği gibi DEHB ve OSB arasın-da çok benzerdi, ancak bu, akraba olma-yan kontrollere kıyasla DEHB ve OSB a-rasında önemli ölçüde farklılık vardı (şekil 2). Bağırsak mikrobiyota bileşimi-nin analizi, bazı DEHB, OSB veya DEHB /ASD'li çocukların Bacteroidetes filumun-da nispeten daha düşük bir miktar ve Ac-tinetobacteria'da daha fazla miktarda ol-duğunu göstermiştir. Tüm gruplarda Bac-teroides, Faecalibacterium, Blautia ve Bifidobacterium cinsleri baskındır; bazı çocuklar yüksek düzeyde Prevotella sergi-lemiştir. Bakteri cinslerinin bolluğundaki farklılıklar DEHB, OSB ve kontroller arasın-da bulunmuştur (şekil 3). ancak DEHB ve OSB arasında bulunmamıştır.
Fekal kalprotektin veya lipopolisakkarit bağlayıcı protein (LBP) seviyeleri açısın-dan ne çeşitli gruplar arasında ne de ak-raba olan veya olmayan kontroller ara-sında bir fark gözlenmemiştir. Bununla birlikte, fekal kalprotektin ve LBP ile bakteriyel alfa ve beta çeşitlilikleri arasın-da herhangi bir korelasyon bulunma-mıştır. Çeşitli sitokinlerin ve kemokinlerin ölçümü çeşitli gruplar arasında anlamlı farklılıklar göstermemiştir; ancak, birkaç DEHB ve OSB bireyinde akraba olmayan kontrollere kıyasla daha yüksek IL1-RA seviyeleri ve beş DEHB çocuğu ile bir OSB çocuğunda akraba olmayan control-lere kıyasla daha yüksek IFN-g konsant-rasyonları görülmüştür. Son olarak, LBP ile IL-8 (p=0,023), IL-12 (p=0,018), IL-13 (p=0,035) ve PlGF (p=0,045) arasında zayıf pozitif korelasyonlar bulunmuştur; bu da bağırsak bariyer fonksiyonunun bozulmasının immün düzensizliğe yol açabileceğini düşündürmektedir.
Pratikteki etkileri ne olacaktır?
Bu çalışma, ilgili kontrol grubuyla ilgili olarak, az sayıda birey üzerinde gerçekleştirilmiştir. Bağırsak mikrobiyo-tasının yanı sıra bağırsak geçirgenliği, DEHB ve OSB'li çocuk ve ergenlerin tedavisi için uygun hedefler olabilir.