Je vais commencer par vous parler de la situation que nous connaissons actuellement. Aujourd'hui, au niveau mondial, nous sommes confrontés à une épidémie de maladies chroniques dont l'augmentation est incontrôlée depuis 70 ans, des maladies qui touchent le système cardiovasculaire, le cardiométabolisme, l'obésité, le diabète, mais aussi les maladies inflammatoires, articulaires ou intestinales, les maladies du foie, puis les maladies qui touchent le système nerveux, neurodégénératives ou neuropsychiatriques, par exemple.
Cela représente 41 millions de décès en 2019.
74 % des décès sont liés à une maladie chronique. Cela signifie qu'en 2025, une personne sur quatre sera touchée par au moins l'une de ces maladies et, souvent, nous avons plusieurs problèmes de santé, des maladies chroniques cumulées. Selon les prévisions de l'Organisation, une personne sur deux dans le monde sera obèse d'ici 2035.
Nous pouvons donc constater que les choses évoluent vraiment d'une certaine manière. C'est assez impressionnant, mais pas dans le bon sens.
Qu'est-ce que cela signifie ?
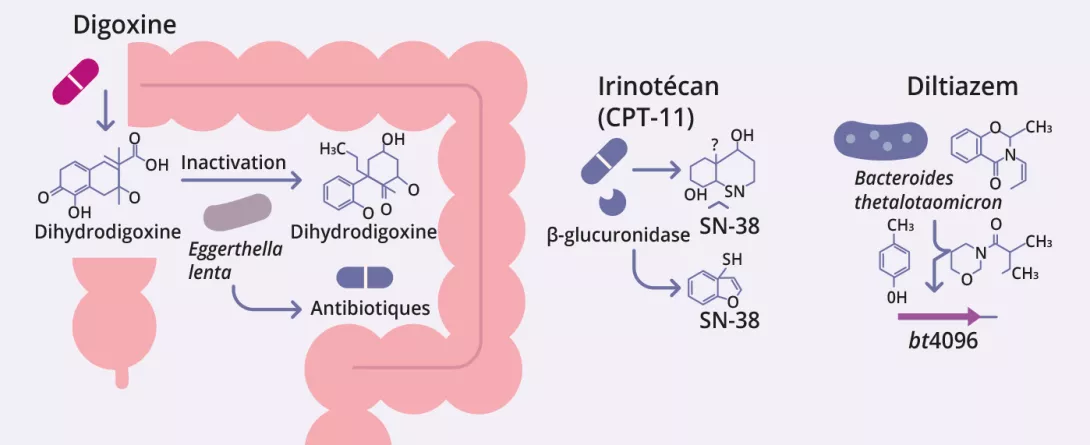
Cela signifie que nous n'avons pas compris à quoi nous avons affaire. Nous avons affaire à un être humain microbien, nous avons affaire à une symbiose, et cela n'est pas encore pris en compte dans nos comportements qui ont été mentionnés, mais aussi dans la pratique médicale actuelle. Nous avons pu caractériser le microbiote, nous avons pu tester le microbiote dans un sens quelque peu générique du terme et caractériser les variations ou les variabilités du microbiote dans différents contextes.
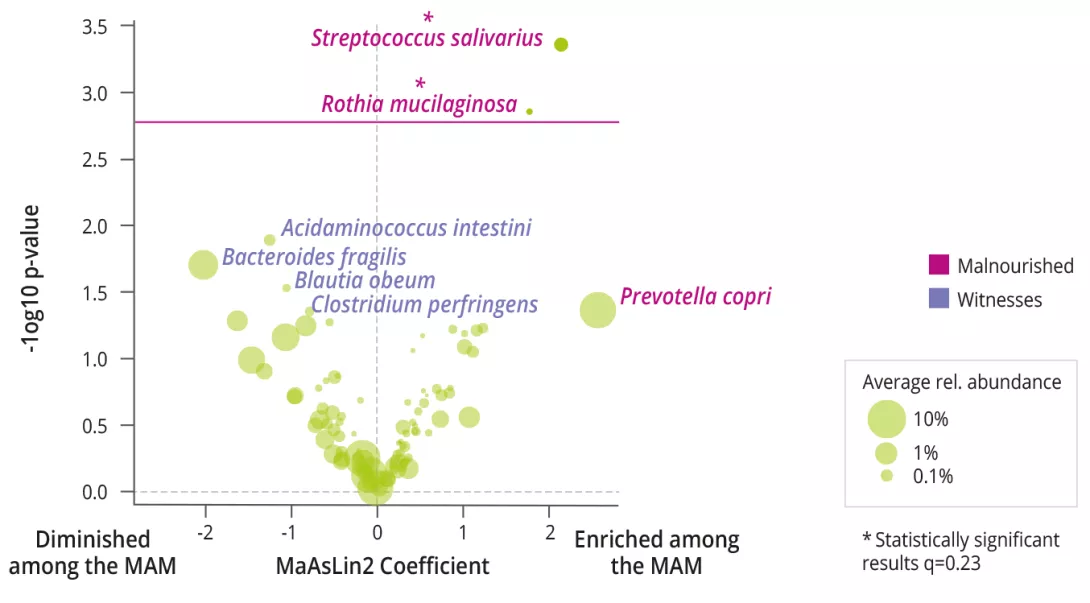
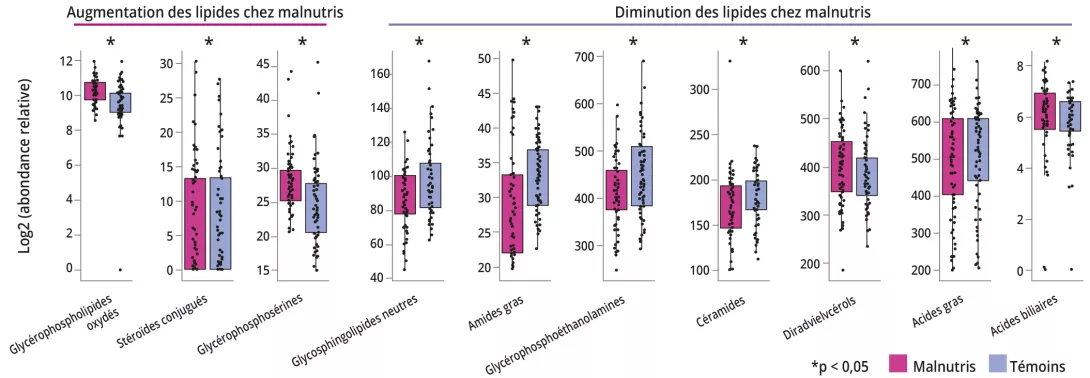
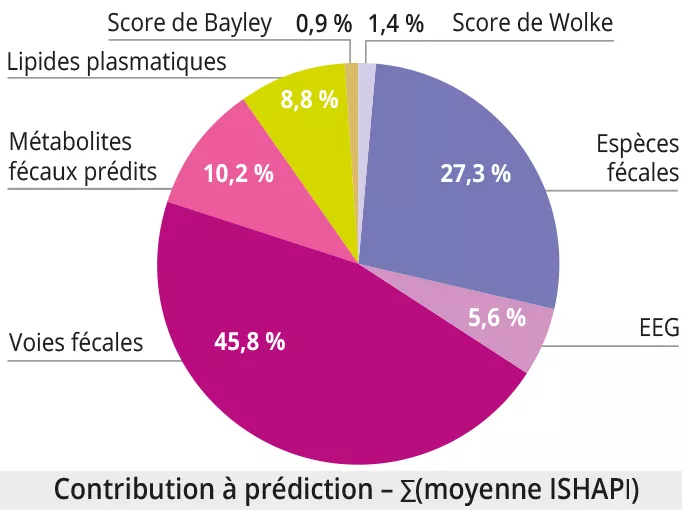
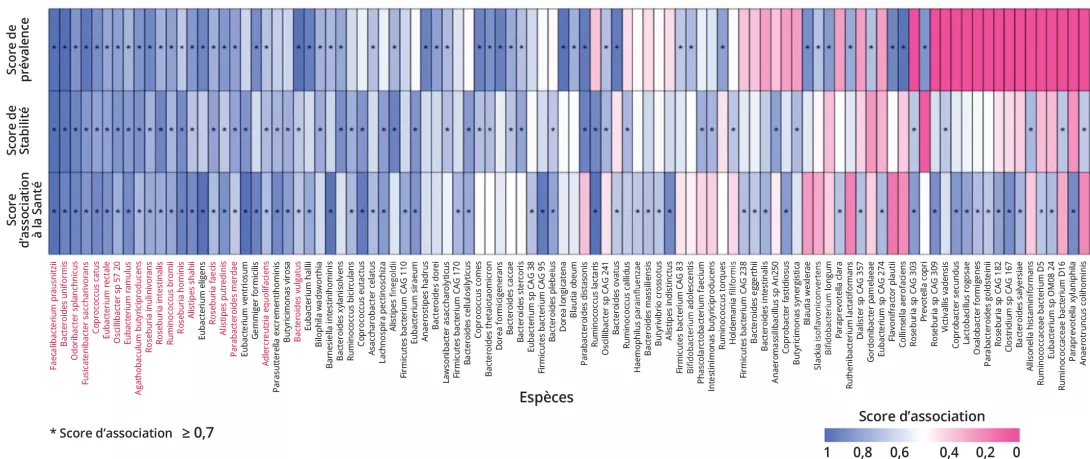
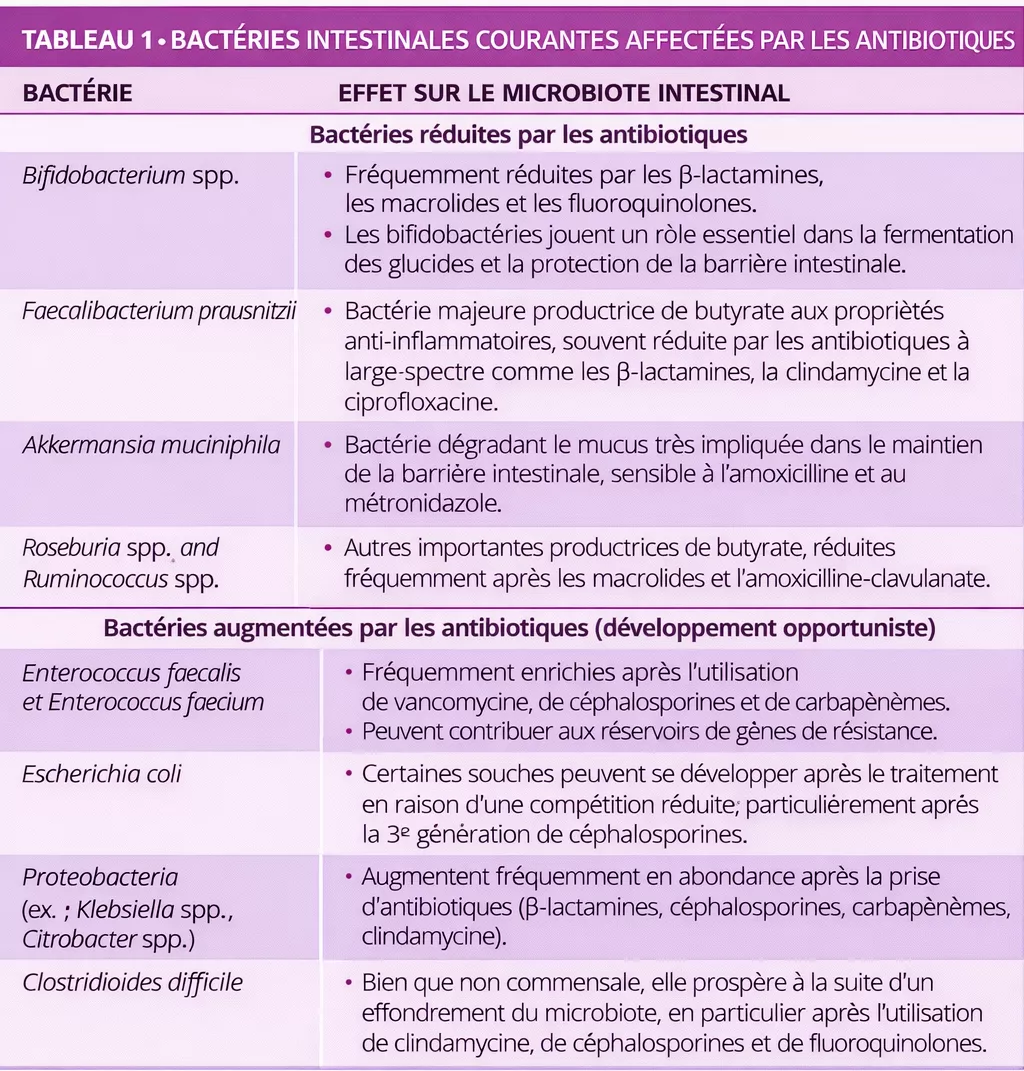
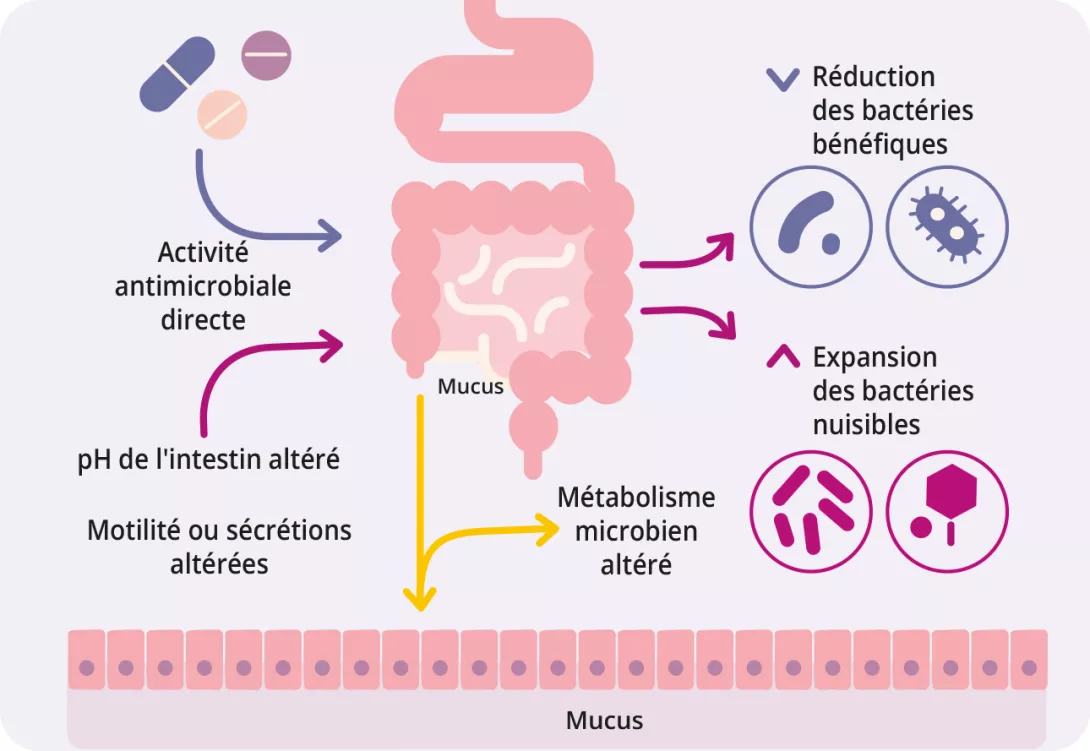
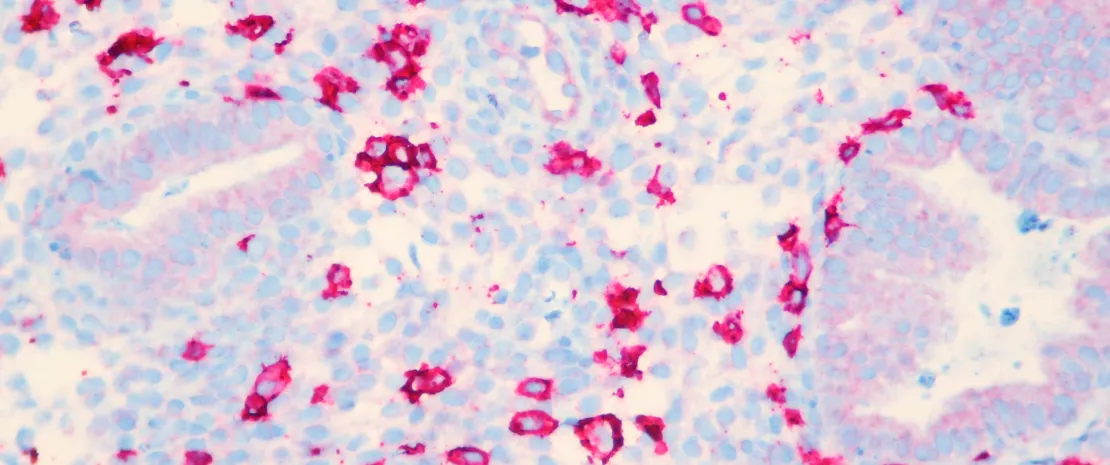
À gauche, ici, nous avons cette image d'une différenciation des microbiomes des personnes vivant dans un environnement industrialisé ou non industrialisé. Et puis, au milieu, ce que nous représentons ici, c'est cette histoire qui nous dit que le microbiote est important, que le microbiote joue un rôle dans un grand nombre de pathologies pour lesquelles une altération du microbiote a été documentée par rapport à des individus qui sont restés en bonne santé. Et ces maladies sont assez nombreuses, elles concernent en fin de compte les pathologies majeures de la société moderne, dont l'incidence est en augmentation, comme nous l'avons vu. Mais cela concerne également des paramètres humains, notamment la perméabilité intestinale, l'inflammation, le stress oxydatif, qui font vieillir nos cellules un peu plus vite que nous le souhaiterions, en fait, et qui peuvent également altérer davantage le microbiote intestinal.
On voit bien comment cette situation peut devenir un peu un cercle vicieux qui s'installe sous la forme d'un cercle vicieux. Et c'est ce que l'on documente aujourd'hui dans les maladies chroniques. Peut-être est-ce lié à cette idée que nous n'avons pas tout à fait compris ce que nous devons faire lorsque nous nous adressons au microbien humain. Donc, quand on zoome un peu sur la perception actuelle de cela qui concerne le test du microbiote intestinal.
Il y a une sorte de colère grandissante. Une petite colère, qui se traduit par des articles d'opinion dans les journaux ou dans la littérature scientifique. Ce sont des commentaires de collègues nord-américains, qui nous parlent ici du DTC, le Direct to Consumer, la caractérisation du microbiote à la demande de M. Tout-le-monde, qui devrait vraiment être un peu mieux réglementée qu'elle ne l'est aujourd'hui. Cela pourrait donc être un sujet de discussion. Mais nous partons de là.
Aujourd'hui, il existe de nombreuses petites entreprises qui proposent des analyses du microbiote, parfois pour quelques centaines d'euros, et qui fournissent un rapport de quarante pages avec de belles images qui vous montrent à quoi vous ressemblez lorsque vous prenez un selfie de l'intérieur. Cela pose problème, car ces personnes consulteront leur médecin avec une bonne relation que la médecine ne peut pas gérer aujourd'hui. Et nous aimerions en effet parvenir à ce cercle vertueux qui permettrait aux médecins de prescrire l'analyse du microbiote en même temps que les analyses biologiques classiques, comme les analyses de sang ou d'urine, par le biais des laboratoires de biologie médicale, qui sont l'interface naturelle dans ce schéma, dans ce circuit.
Dans quel but ?
Enfin, intégrer ces données sur le microbiote dans la pratique médicale. Il s'agit de diagnostiquer les altérations du microbiote et de la symbiose. Il s'agit de suivre l'évolution de la symbiose tout au long du parcours du patient, en particulier pendant le traitement. Et puis, il s'agit d'intégrer les données sur le microbiote et la symbiose dans les recommandations nutritionnelles, par exemple, ou dans les soins médicaux. Pour que ce cercle vertueux s'établisse,
de quoi avons-nous besoin ?
Il faut des normes. Je vais vous expliquer que nous les avons déjà. Il faut des grands nombres et, bien sûr, Le French gut joue un rôle dans ce schéma en apportant des grands nombres pour construire la référence. Et ensuite, il faudra le démontrer avec des preuves, avec des preuves scientifiques qu'il y a un bénéfice clinique, un bénéfice à l'apport. Si bien sûr le médecin est formé au microbiote intestinal. L'éducation et la formation des patients seront également nécessaires pour les professionnels de santé. En réalité, nous constatons assez souvent aujourd'hui que l'éducation des patients se fait presque entièrement en ligne, un peu plus rapidement que l'adaptation de la formation des professionnels de santé aux connaissances scientifiques qui, elles-mêmes, évoluent très rapidement.
Comme je le disais, nous avons les normes. En ce qui nous concerne, nous avons publié en 2017 les normes qui permettent d'analyser le microbiote intestinal de manière totalement standardisée, à tel point que si cela était fait de la même manière aux États-Unis, en Europe et en Australie, nous obtiendrions le même résultat.
C'est ce qui est vraiment nécessaire pour une application clinique. Et puis, nous avons également vu apparaître des équipements de référence qui nous permettent de calibrer les processus que nous mettons en œuvre pour effectuer cette analyse. Et nous avons des collègues scientifiques aux États-Unis ou en Angleterre, par exemple, qui nous proposent des outils qui vont dans ce sens. Cet aspect est réglé.
Ce qui reste à fournir pour ce schéma, c'est le grand nombre et le microbiote français. Le French Gut vise à accélérer la recherche sur le microbiote et donc à fournir ces informations supplémentaires. Il s'agit d'un projet d'intérêt public visant à améliorer la prévention pour dépister, diagnostiquer et traiter les maladies chroniques de demain. Et l'objectif que nous nous sommes fixé est, d'ici 2029, de collecter et de caractériser ceux de 100 000 volontaires en France, adultes, résidents français et également des personnes en bonne santé par rapport à des personnes malades.
Dans quel but ?
Définir la référence, les normes du microbiote, les plages de variation des paramètres classiques, habituels et dominants du microbiote intestinal chez l'individu sain et mieux comprendre son altération dans la maladie. Il s'agit également de jeter les bases d'un véritable développement de recommandations nutritionnelles, éventuellement préventives et personnalisées, afin d'ouvrir la voie à de nouvelles thérapies, notamment dans le contexte des maladies chroniques, mais aussi de sensibiliser le grand public, les adultes et les enfants qui sont ou seront demain les gardiens de leur santé. Il s'agit d'un projet mené par l'INRAE, qui est réalisé en très étroite collaboration avec l'Assistance publique et les hôpitaux parisiens, au PHP, et qui rassemble des partenaires publics et privés, des institutions publiques telles que Agro ParisTech, l'Inserm, le CEA, l'Institut Pasteur et l'INRIA, ainsi que des entreprises privées telles que Biocodex, depuis le début, comme cela a été mentionné, pour le secteur pharmaceutique, mais aussi des partenaires qui couvrent davantage l'aspect nutritionnel ou les ingrédients et GMT pour l'analyse du microbiote intestinal à des fins médicales.
Il s'agit d'un projet soutenu par de nombreux partenaires en matière de communication. Je voudrais dire que vous pouvez tous être comme ça, mais nous avons des ambassadeurs, notamment Michel Cymes, Marine Lorphelin, Jimmy Mohamed et Julien Scanzi, qui prendront la parole après moi et qui communiquent avec des millions de personnes via Internet, en particulier.
Comment procédons-nous ?
Nous travaillons depuis des années, je dirais, à simplifier autant que possible le parcours des bénévoles. Ainsi, en tant que bénévole, vous devrez vous inscrire sur Internet et créer une page personnelle. Ensuite, vous devrez bien sûr vérifier que vous remplissez les conditions requises. L'éligibilité repose sur plusieurs critères. Il faut être âgé de plus de 18 ans, ne pas être sous tutelle ou curatelle, résider en France métropolitaine et ne pas avoir pris d'antibiotiques ni subi de coloscopie au cours des trois mois précédant le don. Enfin, si vous recevez votre kit de prélèvement et que vous devez prendre un antibiotique pour une raison quelconque.
Si vous ne vous sentez pas bien, revenez nous voir dans trois mois et tout ira bien. Il n'y a aucun problème. Le processus est le suivant : je m'inscris, je signe un formulaire de consentement. Il s'agit d'un exemple classique d'éthique dans les études de cohorte. Un consentement éclairé qui vous informera que vous participez à l'étude. Et puis aussi un deuxième consentement qui nous dira si vous acceptez d'être recontacté à l'avenir pour explorer la relation entre l'alimentation, la santé et les microbiomes à travers des questionnaires supplémentaires, par exemple, ou bien si vous proposez de participer à des études spécifiques sur des questions complexes dans la science des microbiomes. Vous remplissez quelques questionnaires, le questionnaire de base obligatoire est rempli en environ une cinquantaine de questions, donc cela prend 15 à 20 minutes.
Cependant, vous disposez également de questionnaires facultatifs que vous pouvez remplir dans ce formulaire, qui nous en apprendront davantage sur vous, vos habitudes alimentaires, votre mode de vie ou votre état de santé. Le kit présenté ici dans le coin supérieur droit est un kit similaire à celui utilisé pour le dépistage du cancer colorectal. En fait, nous l'avons simplifié autant que possible. Vous placez une selle sur un petit hamac en papier dans les toilettes et vous disposez d'un coton-tige ou d'un équivalent à placer dans la selle, puis vous placez ce morceau de coton dans un tube qui stabilise complètement votre échantillon pendant une semaine et qui est envoyé par la poste. L'impact est vraiment minimisé.
Néanmoins, certaines personnes ont du mal à faire ce geste. Nous le comprenons. Devenez l'un de nos bénévoles, rejoignez notre équipe de communication. J'en parlerai plus tard.
Où en sommes-nous aujourd'hui ?
Nous avons un peu plus de 25 000 participants qui sont effectivement venus vers nous en tant que bénévoles. Cela représente un quart de notre objectif. Nous allons donc continuer à travailler, à communiquer et à recruter de nouveaux bénévoles. En termes d'âge, il s'agit principalement de personnes d'âge moyen, entre 40 et 60 ans. C'est là que nous avons le plus de monde.
Nous avons un peu moins de personnes âgées ou très âgées que nous le souhaiterions. Un peu moins de jeunes adultes que nous le souhaiterions. 70 % sont des femmes. Messieurs, à vos tablettes ou à vos toilettes. Et puis, la répartition nationale correspond de manière impressionnante à la démographie de la population française. Nous sommes donc très heureux de pouvoir compter sur des bénévoles dans tout le pays. Un peu moins dans le Nord, un peu moins en Corse. Évidemment, je tiens à le dire, mais malgré tout, nous avons une très bonne représentation.
Et puis, un tiers de nos bénévoles sont... des patients qui consultent pour une pathologie, principalement des maladies respiratoires ou cardiométaboliques. En fait, l'hypertension, par exemple, vient après les maladies digestives. Évidemment, il y a ensuite les maladies systémiques ou auto-immunes. Et puis, enfin, les maladies neurologiques. Le système nerveux est impliqué.
Je ne vois pas les chiffres car c'est un peu loin pour moi, mais nous avons un peu plus de 80 % de personnes qui n'ont jamais fumé parmi nos volontaires. Environ 80 % des personnes sont omnivores. Bien sûr, nous nous intéressons également aux habitudes alimentaires. Et puis, nous avons une forte proportion de personnes qui déclarent avoir une activité physique régulière, à savoir au moins 30 minutes par jour de marche dynamique.
Voilà, vous pouvez tous communiquer. Idéalement, vous devriez contacter frenchgut-press@inrae.fr pour obtenir les outils de communication qui vous sont confiés, par exemple une affiche à imprimer et à apposer dans votre pharmacie ou votre supermarché. Et puis, éventuellement, des kits, des dépliants à distribuer autour de vous. Impliquez également les membres de votre famille. C'est important pour nous.

 Les bons réflexes alimentaires pour chouchouter sa flore vaginale
Les bons réflexes alimentaires pour chouchouter sa flore vaginale
 Microbiote vaginal et papillomavirus humains (HPV) : des bactéries qui font le ménage !
Microbiote vaginal et papillomavirus humains (HPV) : des bactéries qui font le ménage !