Bien dans sa peau… et son microbiote cutané
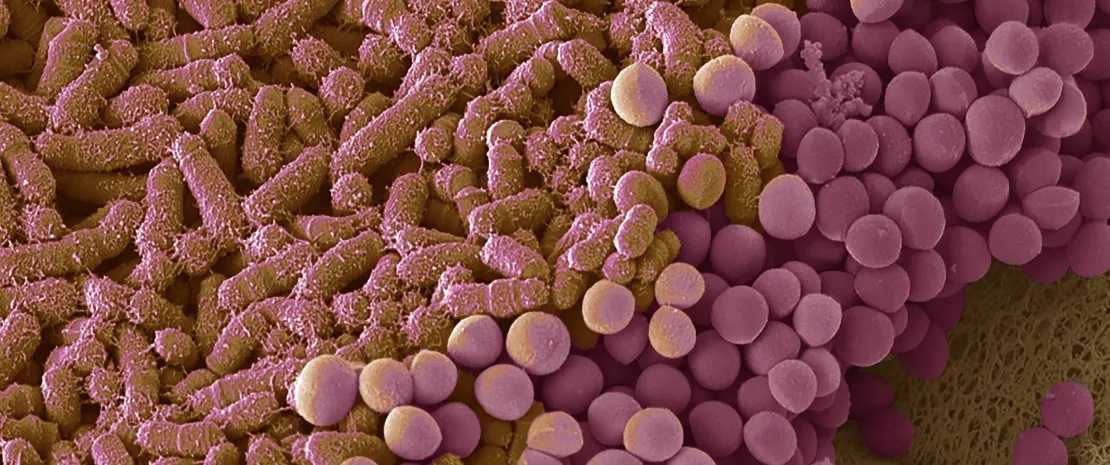
Et si le secret de notre bien-être se cachait sur notre peau ? Une étude britannique pionnière dans le genre, suggère un lien entre microbiote cutanée et équilibre émotionnel :les personnes ayant plus de Cutibacterium seraient moins stressées et plus heureuses.
Le microbiote cutané La dépression Eczéma Psoriasis et microbiote Acné et microbiote
Faudra-t-il désormais dire « bien dans son microbiote cutané ” plutôt que « bien dans sa peau » ?
C’est en substance ce que suggère une étude britannique qui tisse un lien entre le bien-être psychologique et les microorganismes qui peuplent notre peau, plus précisément de la peau du visage, du cuir chevelu, de l’avant-bras et aisselles, sur la base de l’étude de 53 Britanniques âgés en moyenne de 63 ans.
Cette recherche met en lumière un système d’interactions entre peau et cerveau, en écho aux dynamiques déjà connues dans l’axe intestin-cerveau.
Davantage de Cutibacterium, davantage de bien-être ?
L’étude montre pour la première foisune présence accrue de certains genres bactériens chez les participants les mieux dans leur peau, que ce soit en termes de bien-être général ou de bien-être de la zone cutanée incriminée. La bactérie cutanée la plus souvent présente chez les Britanniques les mieux dans leurs corps : (sidenote: Cutibacterium Genre de bactéries dont le classement a été beaucoup remanié ces dernières années (jusqu’en 2016, on parlait de Propionibacterium). Ce genre bactérien comprend plusieurs espèces donc la célèbre C. acnes (pathogène opportuniste impliqué dans l’acné et dans des infections de prothèses mammaires, d’épaule, etc.,) mais aussi C. avidum, C. granulosum, C. namnetense et C. humerusii. Ahle CM, Feidenhansl C, Brüggemann H. Cutibacterium acnes. Trends Microbiol. 2023 Apr;31(4):419-420. ; CTCB ) . Vous en avez davantage sur le visage ? Vous devez être peu stressé(e). Vos aisselles en regorgent : votre humeur a de fortes chances d’être au beau fixe et votre niveau de stress au plus bas. À l’inverse, une moindre présence de cette bactérie pourrait contribuer à des troubles comme le stress, l’anxiété ou la dépression.
A noter que cette trouvaille a de quoi surprendre : quand on parle de Cutibacterium, c’est surtout l’image de C. acnes et de cauchemars pubertaires qui viennent à l’esprit. Et non celle de la zénitude des seniors britanniques. Ainsi cette bactérie pourrait aussi participer à notre santé cutanée en repoussant les pathogènes et en régulant l’acidité de la peau, grâce à sa capacité à transformer le sébum en acides gras libres.
Effets de Cutibacterium selon la zone du corps
- Visage : les personnes qui hébergent davantage de Cutibacterium sur leur visage ressentent moins de stress.
- Aisselles : une plus grande présence de cette bactérie est liée à une meilleure humeur et à un stress réduit.
- Avant-bras : plus de Cutibacterium sur cette zone est associé à une meilleure satisfaction vis-à-vis de sa peau.
Cause ou conséquence ?
Reste la question centrale : la présence de Cutibacterium est-elle une cause ou une conséquence du bien-être ? Autrement dit, est-ce la présence de Cutibacterium qui nous rend heureux ou est-ce notre bien-être qui les attire sur notre peau ? A moins que les deux résultent d’un autre dénominateur commun (le style de vie, le sport, l’alimentation par exemple)
Impossible de trancher à ce stade. On sait que la peau et son microbiote cutané offrent une barrière protectrice à notre corps, repoussant les pathogènes... et donc nous offrant sécurité et tranquillité. Inversement, il a été montré que le stress, l’anxiété ou la dépression peuvent impacter notre peau, en entraînant l’apparition de troubles cutanés notamment l’eczéma (ou dermatite atopique), le psoriasis, l'acné, ou les odeurs au niveau des aisselles.
17% Seulement 17% des personnes sondées déclarent savoir précisément ce qu’est le microbiote cutané. ²
Nous avons entendu parler de l’axe intestin-cerveau, maintenant, il existe l’axe peau-cerveau bidirectionnel, le premier influençant le second et vice-versa. Et pour la première fois, une relation entre microbiote cutané et bien-être psychologique est mise en évidence. De quoi inviter la recherche en (sidenote: Psychodermatologie La psychodermatologie est un domaine relativement nouveau de la médecine, qui se concentre sur les interactions entre l'esprit et la peau. Le traitement des troubles psychodermatologiques se concentre sur l'amélioration de la fonction, la réduction de la détresse physique, le diagnostic et le traitement de la dépression et de l'anxiété associés aux maladies de la peau, la gestion de l'isolement social et l'amélioration de l'estime de soi du patient. Les interventions pharmacologiques et psychologiques sont utilisées dans le traitement des troubles psychocutanés. Approfondir Jafferany M, Franca K. Psychodermatology: Basics Concepts. Acta Derm Venereol. … ) à étudier plus avant les bactéries impliquées et leur influence potentielle sur notre santé cutané et général.
Sèche, humide ou grasse : à chaque zone sur le corps, son microbiote
Souvent trop sèche au niveau des mains – au point que l’on passe l’hiver à l’hydrater – la peau est tout au contraire humide au niveau des aisselles, des plis (coude, arrière du genou) ou de l‘aine.
S’y ajoute une troisième variante : la peau grasse, typique de certaines zones du visage, de la poitrine ou du dos. Trois environnements donc (sec, humide, gras), dans lesquels vivent trois microbiotes différents, adaptés aux spécificités de ces trois milieux.
A noter : le microbiote cutané varie également tout au long de l’épaisseur de la peau, de l’épiderme (en surface) à l’hypoderme (sous le derme) : plus on s’enfonce profondément, moins les bactéries sont nombreuses et plus elles sont comparables d’un individu à l’autre.