ВАГИНАЛЬНАЯ МИКРОБИОТА #22
Проф. Сату Пеккала (Satu Pekkala)
Научный сотрудник Академии Финляндии, Факультет спорта и здравоохранения, Университет Ювяскюля, Финляндия



Проф. Сату Пеккала (Satu Pekkala)
Научный сотрудник Академии Финляндии, Факультет спорта и здравоохранения, Университет Ювяскюля, Финляндия

В пременопаузе (период до полного прек-ращения менструаций) снижение уровня эстрогенов приводит к уменьшению со-держания гликогена в клетках слизистой оболочки влагалища. В свою очередь, гликоген является основным источником питания для Lactobacillus. В условиях недостатка питания коли-чество Lactobacillus уменьшается и они теряют свое доминирующее положение в микрофлоре, что может привести к дисбалансу вагинальной микробиоты.
Снижение уровней половых гормонов так-же связано с неблагоприятным увеличе-нием микробного разнообразия. Нес-колько исследований показали, что утрата доминирования Lactobacillus и увеличение бактериального разнообразия связаны с воспалением слизистой влагалища. Вос-паление повышает риск инфекций, осо-бенно инфекций, передаваемых половым путем (ИППП), и предраковых поражений шейки матки.
Хотя связь между изменениями ваги-нальной микробиоты и воспалением была продемонстрирована у женщин в преме-нопаузе, до сих пор не проводилось ис-следований, чтобы определить, сохраня-ется ли эта связь в постменопаузе. Чтобы изучить этот вопрос, группа американских исследователей использовала данные 119 женщин в постменопаузе (средний возраст 61 год), которые участвовали в клиническом исследовании, сравниваю-щем влияние эстрогена или увлажняю-щего крема на вагинальную флору. Они проанализировали бактериальные попу-ляции и маркеры воспаления (цитокины) в вагинальном секрете женщин-доброволь-цев, чтобы определить возможные связи между этими двумя параметрами.
Оказалось, что у женщин с наиболее разнообразной вагинальной микробиотой или с наименьшим количеством Lactoba-cillus наблюдался самый высокий уровень цитокинов. Таким образом, эти две харак-теристики вагинальной микробиоты свя-заны с воспалением, как и у женщин в пременопаузе.
Эти результаты заслуживают внимания, так как указывают на потенциальную воз-можность в будущем предотвращать воспаление влагалища у женщин в пост-менопаузе путем регулирования ваги-нальной микробиоты.
Проф. Сату Пеккала (Satu Pekkala)
Научный сотрудник Академии Финляндии, Факультет спорта и здравоохранения, Университет Ювяскюля, Финляндия

Нарушения нервно-психического раз-вития (ННПР), включая расстройства аутистического спектра (РАС), оказы-вают значительное воздействие на центральную нервную систему. У людей с РАС часто встречаются желудочно-кишечные симптомы, возможно, из-за дисфункции оси кишечник — головной мозг. Однако, механизм влияния микро-биома на развитие ННПР до конца не ясен. В шведском когортном исследовании рождений (n=16,440) с периодом наблюдения более 20 лет изучали связь различных биомаркеров, включая микробиоту, с развитием ННПР. Инфекции и воздействие антибиотиков в раннем возрасте, особенно у лиц с РАС, являются факторами риска ННПР. Некоторые виды кишечной микробиоты, особенно Firmicutes, ассоциированы с проблемами со стороны ЖКТ.
Дети, часто болеющие отитом, чаще заболевали РАС, тогда как воздействие вредных химических веществ предрас-полагало к синдрому дефицита внима-ния и гиперактивности (СДВГ). При РАС исследовали метаболом и липидом сы-воротки пуповинной крови при рождении и метаболом стула в возрасте 1 года. У новорожденных, у которых впослед-ствии было диагностировано РАС, наб-людалось снижение уровня α-лино-леновой и желчных кислот, что может указывать на воспаление. Дисбиоз кишечника начинался в ран-нем возрасте и был связан, например, с жирными кислотами и предшествен-никами нейротрансмиттеров. Отсутствие Akkermansia muciniphila, по-лезной для здоровья и иммуномодули-рующей бактерии, в младенчестве было связано с последующим развитием РАС, но не СДВГ. У младенцев с последующими ННПР уровни Akkermansia и Coprococcus были снижены, но положительно коррелирова-ли с фекальными предшественниками нейротрансмиттеров и незаменимыми витаминами.
Результаты исследования указывают на то, что кишечная микробиота опосредует возникновение ННПР в раннем возрасте. Это создает основу для разработки ран-них вмешательств при ННПР и прогнози-рования ННПР в раннем возрасте.
Ингибиторы контрольных точек иммуните-та (ИКТ) увеличивают выживаемость па-циентов с распространенными опухолями. Однако лишь часть пациентов отвечает на ИКТ, возможно, из-за влияния кишечного микробиома, хотя поперечные исследова-ния показывают противоречивые резуль-таты. Поэтому необходимы продольные исследования.
В исследовании с использованием сек-венирования методом дробовика анали-зировали микробиом 175 пациентов с распространенной меланомой, получав-ших ИКТ, в течение первых 12 недель лечения. Выживаемость без прогресси-рования (ВБП) определяли как время от начала иммунотерапии до прогрессиро-вания заболевания или смерти. Пациен-тов с ВБП ≥12 месяцев сравнивали с пациентами с ВБП <12 месяцев.
Результаты показали, что у пациентов с ВБП <12 месяцев наблюдалось большее количество таксонов, связанных с воспа-лением. Напротив, у пациентов с ВБП ≥12 месяцев наблюдалось повышенное содер-жание нескольких таксонов, считающихся «провоспалительными».
Примечательно, что у пациентов с ВБП ≥12 месяцев были стабильно повышены пять таксонов. У пациентов с ВБП ≥12 ме-сяцев стабильно преобладали A. Butyrici-producens, I. bartlettii, Dorea sp. AF24 7LB, группа L. gasseri и L. celerecrescens, а у пациентов с ВБП <12 месяцев — R. lactatiformans, R. Неклассифицирован-ная группа SGB15265, P. copri clade A и неопознанный вид из филума Bacteroide-tes. Затем авторы подтвердили обобщае-мость результатов на шести независимых когортах меланомы. Различить пациентов с ВБП ≥12 и ВБП <12 месяцев удалось только в когорте с достаточно большим числом участников (N = 112).
Авторы считают, что их исследование подчёркивает динамичность кишечного микробиома и важность продольного про-филирования для оптимизации микро-биом-ориентированных вмешательств с целью улучшения результатов лечения распространенной меланомы.
Растет число исследований, связываю-щих кожные заболевания с общим состо-янием организма, включая гомеостаз ки-шечной микробиоты. Псориаз (ПСО), ато-пический дерматит (АД), акне и красный плоский лишай — самые распространён-ные кожные заболевания. ПСО и АД свя-заны с состоянием желудочно-кишечного тракта, а многие исследования указыва-ют на связь акне и дисбаланса кишечной микробиоты. Однако неясно, отражают ли наблюдаемые ассоциации истинную причинно-следственную связь.
В этом исследовании из общедоступных баз данных были получены полные дан-ные генетических ассоциаций для кишеч-ной микробиоты, псориаза, атопического дерматита, акне и красного плоского лишая. Для изучения причинно-следственной свя-зи между кишечной микробиотой и кож-ными заболеваниями авторы применили двунаправленный двухвыборочный менде-левский рандомизационный анализ (MR). В исследование были включены 18340 человек, и идентифицированы значимые для всего генома однонуклеотидные поли-морфизмы (SNP), связанные с таксонами GM. Исследование выявило пять ассоцииро-ванных родов в группе ПСО, семь в группе АД, десять в группе акне и четыре в группе красного плоского лишая. После коррекции на ложноположительные ре-зультаты, значимой осталась лишь связь между Eubacterium fissicatena и ПСО. Обратный MR-анализ не подтвердил результаты прямого анализа, полученные с использованием перекрестной проверки.
Авторы приходят к заключению, что ре-зультаты демонстрируют причинно-след-ственную связь между кишечной микро-биотой и иммунными заболеваниями кожи, открывая новые возможности для терапии и изучения последних. Только род Eubacterium fissicatena был значимо связан с одним из изученных кожных заболеваний.
Д-р Марта Ардила Хименес (Marta Ardila Jimenez)
Координатор отделения педиатрии и неонатологии, Клиника Марли Хорхе Кавалье Гавирия, Богота, Колумбия

На 56-м конгрессе ESPGHAN в Милане микробиота стала одной из центральных тем, что обусловлено увеличением числа перспективных исследований и постоянной потребностью в углублении знаний в этой области. В новую эпоху микробиота играет ключевую роль в снижении заболеваемости будущих поколений. Как врачам эффективно информировать пациентов о профилактике заболеваний?
Исследования показывают, что первые 1000 дней жизни — критический период для вмешательств, предотвращающих не-инфекционные заболевания и улучшаю-щих здоровье населения в долгосрочной перспективе. Почему это так значимо? Этот период критически важен для коло-низации кишечника и, как следствие, фор-мирования микробиоты. Таким образом, он существенно влияет на созревание кишеч-ника, а также метаболическое и иммуно-логическое программирование. Микробная колонизация желудочно-кишечного тракта играет ключевую роль в метаболическом программировании и иммунном созре-вании; нарушение колонизации в младен-честве повышает риск развития бронхи-альной астмы, атопического дерматита, пищевой аллергии, сахарного диабета, воспалительных заболеваний кишечника и ожирения. 1
С самого начала эмбрионального развития рост и темпы развития определяются как генетикой, так и факторами окружающей среды. Эпигенетические механизмы, вклю-чая модификацию гистонов, некодирую-щие РНК и метилирование ДНК, подвер-жены влиянию различных факторов, вклю-чая воздействие определенных веществ, питание и стресс.Каждый этап роста и развития критически важен для положительного влияния микро-биоты, подобно пазлу, где необходимы все элементы.

Исследования микробиоты во время бере-менности выявляют изменения в ее соста-ве у матери в эндометрии, влагалище и ки-шечнике, что иногда приводит к ослож-нениям. В первом триместре беремен-ности кишечная микробиота схожа с мик-робиотой здоровых небеременных женщин 2. В третьем триместре наблюдается экс-поненциальное увеличение разнообразия микробиоты, приводящее к набору веса, инсулинорезистентности и повышенному содержанию фекальных цитокинов, что свидетельствует о воспалении. У беремен-ных женщин с избыточной массой тела в фекалиях наблюдается повышенный уро-вень Bacteroides и Staphylococcus по срав-нению с беременными женщинами со здо-ровым весом. Вертикальный перенос бак-терий от матери к новорожденному спо-собствует формированию кишечной мик-робиоты и может влиять на развитие и функционирование иммунной системы. Микробиота новорожденных, рожденных естественным путем, заметно отличается от микробиоты новорожденных, рожденных путем кесарева сечения, и микробиоты их матерей. Некоторые исследования связывают кесарево сечение с повышенным риском иммунных нарушений, таких как аллергия и астма, у детей. Контакт «кожа к коже» инициирует грудное вскармливание, критически важное для иммунитета новорожденного благодаря поступлению необходимых питательных веществ 3, 4.
Сроки введения твердой пищи также влияют на состав кишечной микробиоты. На развитие кишечной микробиоты у недоношенных детей влияют различные факторы, включая время, прошедшее с момента рождения, и грудное вскармливание. Применение про- и пребиотиков демонстрирует потенциал в снижении заболеваемости и смертности в этой группе.
Осознавая влияние первых 1000 дней жизни на здоровье взрослого человека, мы стремимся формировать государственную политику для укрепления микробиоты. Для достижения этой цели необходимо поддерживать кормящих матерей, стимулировать грудное вскармливание и распространять информацию о здоровом питании среди всех пациентов.
Д-р Пурна С. Кашьяп (Purna C. Kashyap)
Отделение гастроэнтерологии и гепатологии, Программа микробиомики имени Бернарда и Эдит Уотерман, Центр персонализированной медицины, Медицинский колледж клиники Майо, Рочестер, США

В мае 2024 года более 13 000 специалистов, интересующихся заболеваниями органов пищеварения, из более чем 100 стран приняли участие в ежегодной Неделе заболеваний органов пищеварения (Digestive Disease Week). В рамках встречи, спонсируемой Американской гастроэнтерологической ассоциацией (AGA), Американской ассоциацией по изучению заболеваний печени (AASLD), Американским обществом гастроинтестинальной эндоскопии (ASGE) и Обществом хирургии пищеварительного тракта (SSAT), было проведено более 400 оригинальных лекций и 4300 сессий устных и стендовых докладов, охватывающих инновации и передовые исследования в области заболеваний желудочно-кишечного тракта и печени. Специализированная секция «Микробиом и микробная терапия» и Центр образования и исследований кишечного микробиома в рамках AGA провели 11 научных сессий с 33 приглашенными докладами ведущих международных экспертов и 52 устными докладами, освещающими передовые исследования и инновации в области науки о микробиоме. Ниже краткий обзор ключевых презентаций.
Первую лекцию имени Гейл Хехт и Дэвида Хехта, посвященную микробиому, прочи-тала доктор Дженнифер Варго (Jennifer Wargo). Она представила данные о микро-окружении опухоли, кишечной микробиоте при раке, микробных биомаркерах ответа на терапию и новых стратегиях профилак-тики и лечения рака, воздействующих на ткани, опухоль и кишечную микробиоту. Доктор Варго показала, что разнообразие и состав микробиома кишечника и опухоли — важные прогностические мар-керы исходов рака, особенно после трансплантации стволовых клеток и иммунотерапии.

Данные доктора Варго показали, что определенные пробиотики могут быть связаны с ухудшением исходов рака у некоторых пациентов, что подтверждается исследованиями на животных моделях 1 (Spencer et al., Science, 2021). CBM588 в сочетании с блокадой CTLA4 и PD1 продемонстрировал преимущества в лечении метастатического почечно-клеточ-ного рака 2. Комменсальные бактерии, например Bifidobacterium, усиливают про-тивоопухолевый иммунитет и эффек-тивность блокады PD-L1/CTLA4, указывая на важность персонализированных и тар-гетных пробиотиков.
Как и в случае с пробиотиками, примене-ние антибиотиков перед терапией инги-биторами иммунных контрольных точек ас-социировалось с ухудшением результатов лечения 3. И наоборот, целенаправлен-ное применение антибиотиков, например, ципрофлоксацина или метронидазола, для воздействия на интратуморальные бак-терии, вызывающие резистентность к тера-пии рака 4, 5 может усилить противо-опухолевый иммунитет и улучшить ответ на лечение.
Трансплантация фекальной микробиоты (ТФМ) — перспективный метод в контексте лечения рака. Небольшие открытые кли-нические исследования показали способ-ность ТФМ преодолевать резистентность к иммунотерапии у пациентов с метастати-ческой меланомой [6, 7]. У ранее нелечен-ных пациентов с метастатической мела-номой, ТФМ от здоровых доноров в соче-тании с анти-PD1 терапией показала высо-кие показатели ответа.
Питание существенно влияет на микроби-ом кишечника и результаты лечения рака. Потребление более 20 граммов клетчатки в день улучшало результаты блокады им-мунных контрольных точек 1. Современ-ные исследования диеты с высоким содер-жанием клетчатки и других персонали-зированных подходов к питанию демонст-рируют многообещающие перспективы улучшения ответа на терапию рака.

Доктор Варго представила обнадеживаю-щие результаты исследования BEGONE по применению диеты PreFED, богатой пре-биотиками (например, бобами), демонст-рирующие способность пребиотиков моду-лировать кишечную микробиоту и снижать системное воспаление. Доктор Тесса Андерман также представила уроки, извле-чённые из исследования пребиотиков у па-циентов после аллогенной трансплантации гемопоэтических стволовых клеток (алло-ТГСК). Эффективность пребиотиков и вы-работка короткоцепочечных жирных кислот зависят от типа пребиотика и состава микробиоты, поэтому комбинирование раз-личных пребиотиков может быть более полезным для здоровья.
Д-р Коллин Келли (Colleen Kelly) изложила рекомендации, разработанные Американ-ской гастроэнтерологической ассоциацией (AGA) по применению фекальной микро-биоты для лечения заболеваний желудоч-но-кишечного тракта. AGA рекомендует те-рапию фекальной микробиотой после стан-дартного курса антибиотиков у иммуноком-петентных взрослых, а также у взрослых с легким/умеренным иммунодефицитом и рецидивирующей C. difficile или у госпи-тализированных с тяжелой/молниеносной C. difficile, не отвечающей на стандартное лечение. Кроме того, AGA рекомендует использовать традиционную транспланта-цию фекальной микробиоты после завер-шения стандартного курса антибиотиков. У взрослых с язвенным колитом, болезнью Крона, резервуарным илеитом или синд-ромом раздраженного кишечника AGA не рекомендует использовать традиционную трансплантацию фекальной микробиоты, за исключением случаев клинических исс-ледований. Д-р Джессика Аллегретти сооб-щила об актуальных изменениях в терапии на основе фекальной микробиоты, особо отметив новые требования FDA: обяза-тельную заявку на исследование нового лекарственного средства для продуктов из банка стула и расширенный скрининг доноров, включая тесты на Sars-Cov-2 и бактерии, продуцирующие бета-лактамазы расширенного спектра (ESBL), в связи с зарегистрированными случаями системной инфекции ESBL после ТФМ у иммуноде-фицитных пациентов.
рапия инфекции C. difficile (CDI) быстро прогрессирует. FDA одобрило REBYOTA (фекальная микробиота, живая — jslm) для однократной ректальной инстилляции и VOWST (споры фекальной микробиоты, живые-brpk) — 4 капсулы перорально один раз в день в течение 3 дней, через 3-4 дня после антибиотикотерапии, для предотв-ращения рецидивов CDI. Также продолжа-ется III фаза исследований рационально определенного консорциума живых бактерий, не полученного из донорского кала.
Модерируемая дискуссия всесторонне ох-ватила роль пробиотиков при заболевани-ях ЖКТ у взрослых и детей. Обсуждение касалось дальнейших перспектив. Хотя общие данные не подтверждают эффек-тивность пробиотиков при желудочно-ки-шечных заболеваниях у взрослых, их дей-ствие зависит от вида и штамма, и неко-торым пациентам они могут быть полезны. Кроме того, обсуждались домашние фер-ментированные продукты, такие как йогурт, кимчи и кефир, как экономически эффек-тивные альтернативы. Различия в реко-мендациях по пробиотикам, вероятно, обусловлены различиями в методологиях и типах клинических исследований, учиты-ваемых разными научными обществами. Тесты микробиома для потребителей, осо-бенно для выбора пробиотиков, популяр-ны, однако эксперты считают, что их кли-ническая польза не доказана и рекомен-довать их не следует. Однако, это может быть перспективно для мониторинга изме-нений микробиоты человека после вмеша-тельств. Основной темой обсуждений стала необходимость персонализации те-рапии микробиома.
КОММЕНТАРИИ К СТАТЬЕ Раздел, посвященный детям
Проф. Эммануэль Мас (Emmanuel Mas)
Отделение гастроэнтерологии и диетологии, Детская больница, Тулуза, Франция

В статье рассматривается взаимосвязь микробиоты кишечника и неалкогольной жировой болезни печени (НАЖБП) у детей с ожирением, учитывая глобальный рост распространенности обоих заболеваний. Методология основана на мультиомном анализе и исследованиях когорт детей в сочетании с экспериментами in vitro и in vivo. Выделенный у детей Enterococcus faecium B6 способствовал развитию НАЖБП через выработку тирамина, вызывая накопление липидов, воспаление и фиброз печени. Эти результаты подтверждают причинно-следственную связь между бактерией и прогрессированием НАЖБП, открывая возможности для микробно- или метаболит-ориентированной терапии.
В условиях пандемии ожирения мета-болически обусловленные заболевания пе-чени, такие как неалкогольная жировая бо-лезнь печени (НАЖБП), стали преоблада-ющей патологией, прогрессирующей от стеатоза до неалкогольного стеатогепатита (НАСГ) и цирроза. НАЖБП все чаще встречается у детей.
Патофизиология НАЖБП сложна, и важную роль в ней, вероятно, играет кишечная микробиота. Эффекты кишечной микроби-оты могут быть опосредованы различными метаболитами, включая тирамин.
В первой части исследования участ-вовали 156 детей с ожирением в возрасте от 6 до 18 лет, в том числе 78 с НАЖБП и 78 с изолированным ожирением. Две груп-пы различались по печеночным и метабо-лическим параметрам. Альфа-разнообра-зие микробиоты было ниже в группе НАЖБП. При НАЖБП наблюдалось увели-чение численности Enterococcus, Escherichia, Klebsiella, Dialister и Enterobacter и уменьшение численности Faecalibacterium, Eubacterium_eligens_group, Roseburia, Fusicatenibacter, Clostridium, Coprococcus и Parasutterella. Численность Enterococcus кор-релировала с уровнями АЛТ, АСТ, тригли-церидов и общего холестерина в сыво-ротке.
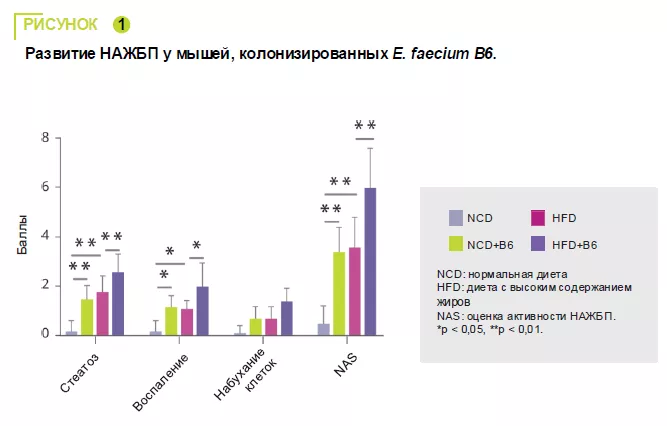
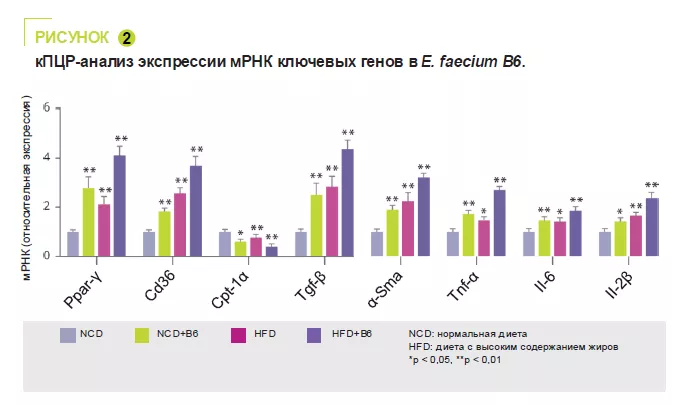
E. faecium B6, выделенный из кишечника детей с НАЖБП и ожирением, продемонс-трировал способность накапливать липиды в клеточной культуре. В 12-недельном исс-ледовании на мышах сравнивали нор-мальную (NCD) или обогащенную жирами (HFD) диету с витамином B6 или без него. E. faecium B6 усугублял повреждение пе-чени, вызванное перегрузкой, на биоло-гическом и гистологическом уровнях, не влияя на массу тела. (рисунок 1). Транс-криптомный анализ выявил, что E. faecium B6 модулирует экспрессию генов, свя-занных с метаболизмом липидов, воспа-лением, фиброзом и метаболизмом лино-левой кислоты, включая сигнальные пути PPAP, хемокинов, NF-kB и TGF-β. В мета-болизме липидов наблюдалось увеличе-ние экспрессии мРНК, белков PPARγ и CD36, и снижение экспрессии CPT-1a. За-фиксировано усиление экспрессии прово-спалительных цитокинов (TNF-α, IL-6, IL-1β) и фибротических белков (TGF-β, α-SMA) (рисунок 2).
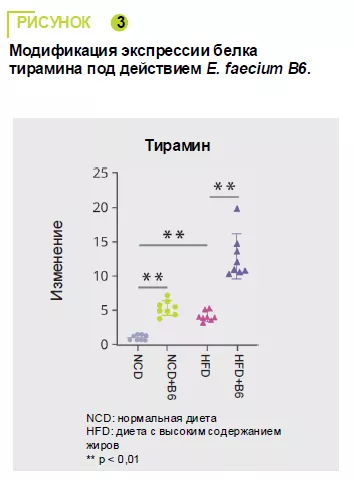
Нецелевой тандемный масс-спектрометри-ческий анализ сыворотки мышей показал, что E. faecium B6 изменял уровни метаболитов при нормальной диете (30 увели-чений и 85 уменьшений) и диете с высоким содержанием жиров (18 увеличений и 45 уменьшений). Наиболее заметным измене-нием было увеличение тирамина (рисунок 3).
Дальнейшие анализы показали, что E. faecium B6 способен продуцировать тирамин. Кроме того, введение мышам на диете NCD или HFD тирамина воспро-изводило развитие НАЖБП без влияния на массу тела, аналогично тому, как это наблюдалось с E. faecium B6, а также изменяло экспрессию генов, кодирующих PPARγ, CD36, CPT-1a, TNF-α, IL-6, IL-1β, TGF-β и α-SMA.
Наконец, авторы подтвердили эти ре-зультаты у 123 детей с НАЖБП и ожи-рением и у 123 человек из контрольной группы. Содержание E. faecium B6 и экс-прессия гена, кодирующего тирамин (mfnA), были выше в группе НАЖБП и кор-релировали с биологическими маркерами НАЖБП (АСТ, АЛАТ, тригли-цериды, об-щий холестерин и ЛПНП) и провоспали-тельными цитокинами (TNF-α, IL-6, IL-1β).
Данное исследование подчеркивает роль кишечной микробиоты в развитии НАЖБП и предполагает новые терапев-тические возможности. Помимо Enterococcus faecium B6 и тирамина, PPARγ может играть центральную роль в связывании накопления липидов, воспалении и фиб-розе.
E. faecium B6, выделенная у детей с НАЖБП и ожирением, усугубляет заболевание посредством продукции биоактивного метаболита тирамина
E. faecium B6 и тирамин вызывают сходное развитие НАЖБП у мышей, как на нормальной, так и на высокожировой диете
Enterococcus faecium B6 идентифицирован как штамм, усугубляющий НАЖБП у детей с ожирением. Эта бактерия продуцирует тирамин, биоактивный метаболит, активирующий сигнальный путь PPARγ и опосредующий наблюдаемые эффекты.
КОММЕНТАРИИ К СТАТЬЕ - Раздел, посвященный взрослым
Проф. Гарри Сокол (Harry Sokol)
Отделение гастроэнтерологии и диетологии, Больница Сент-Антуан (Saint-Antoine Hospital), Париж, Франция

Материнский микробиом играет важную роль в здоровье во время беременности, однако его влияние на плаценту, связующее звено между матерью и плодом, остается малоизученным. В этой статье авторы показали, что микробиота кишечника матери способствует развитию плаценты у мышей. Истощение кишечной микробиоты матери снижает рост плаценты и нарушает васкуляризацию плода и плаценты. Материнская кишечная микробиота влияет на метаболиты в кровотоке матери и плода. Короткоцепочечные жирные кислоты (КЦЖК) стимулируют тубулогенез эндотелиальных клеток in vitro и предотвращают нарушения васкуляризации плаценты у мышей с дефицитом микробиоты. В модели материнского недоедания добавление КЦЖК предотвращает ограничение роста плаценты и сосудистую недостаточность. Эти результаты подчеркивают важность симбиоза хозяина и микробов в период беременности, демонстрируя вклад материнского кишечной микробиоты в рост и васкуляризацию плаценты у мышей.
Несмотря на недавние исследования, подчеркивающие влияние материнского микробиома на пренатальное развитие потомства 2, механизмы его воздейст-вия на здоровье матери и плода во время беременности остаются неясны-ми. Сильно васкуляризированная пла-цента обеспечивает обмен питатель-ными веществами и газами между ма-терью и плодом, поддерживая развитие плода на стыке двух организмов 3. Авторы изучили влияние кишечного мик-робиома матери на развитие плаценты у мышей, учитывая ее ключевую роль в формировании долгосрочного здоровья потомства.
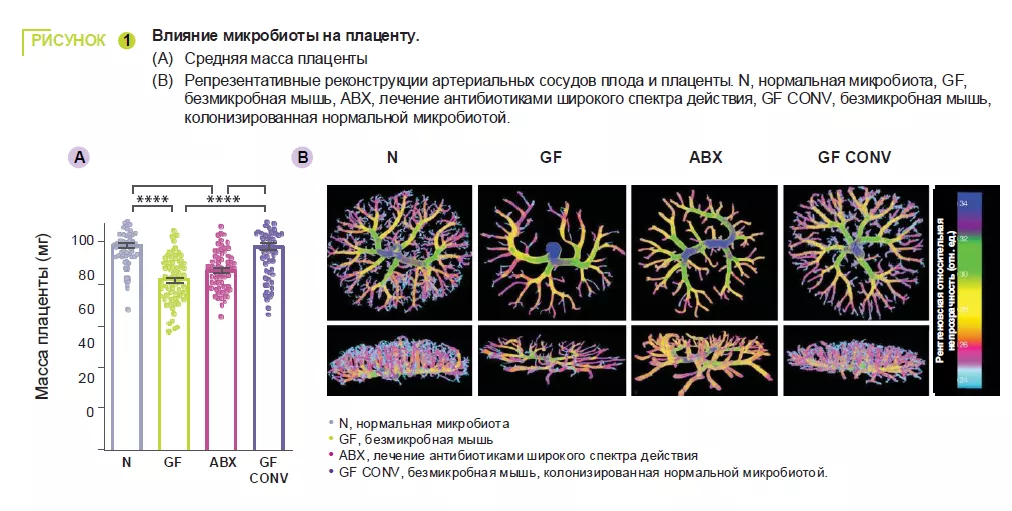
Для изучения влияния материнского кишечного микробиома на развитие пла-центы беременных мышей выращивали либо в безмикробных условиях (GF), либо с истощенным антибиотиками широкого спектра действия (ABX) кишечным мик-робиомом. Отсутствие или истощение материнского микробиома снижало вес плаценты по сравнению с контрольной группой (CONV) с нормальной микро-фло-рой (рисунок 1). Дефицит материнского микробиома, приводя к снижению веса плаценты, также уменьшал общий объем плаценты и снижал объем и плотность тка-ни в плацентарном лабиринте, основном месте обмена веществ между матерью и плодом. Авторы наблюдали снижение веса и объема плода, сопутствующее плацен-тарной патофизиологии, вызванной ABX. Дефицит микробиоты у матерей ассоци-ировался со снижением объема и площади фетоплацентарных сосудов, а также с уменьшением их ветвления (рисунок 1). Это указывает на роль материнского мик-робиома в регуляции развития сосудов во время беременности. Поскольку материн-ский микробиом регулирует циркулирую-щие метаболиты, авторы предположили, что фетоплацентарная сосудистая недо-статочность может быть связана с микро-биотой и вызвана изменениями ключевых метаболитов в кровообращении плода.
Авторы специально рассмотрели роль ко-роткоцепочечных жирных кислот (КЦЖК). КЦЖК, образующиеся при бактериальной ферментации углеводов, значительно сни-жены в сыворотке крови матерей и плода при дефиците микробиоты у матерей.
Опираясь на предыдущие данные о пере-носе КЦЖК от матери к плоду, вызванном добавлением КЦЖК в рацион матери, авторы давали получавшим ABX матерям воду, обогащенную КЦЖК, или контроль-ную воду. Стратегия добавок значимо по-высила концентрации бутирата и пропио-ната в крови плода. Воздействие КЦЖК увеличивало вес плаценты и устраняло вызванные ABX изменения в росте плацен-ты, приближая показатели к контрольным значениям, с сопутствующим увеличением общего объема плаценты и лабиринта. Затем эндотелиальные клетки пупочной вены человека (HUVEC) обрабатывали КЦЖК в физиологических концентрациях. Ацетат и пропионат КЦЖК значительно увеличивали длину ветвления HUVEC по сравнению с контролем, в то время как влияние бутирата было менее выражен-ным. Этот эффект зависел от рецепторов свободных жирных кислот 2 и 3 (FFAR2 и FFAR3). У матерей с белковой недостаточ-ностью добавление КЦЖК восстанавли-вало вес и объем плаценты и усиливало фетоплацентарную васкуляризацию.
Данное исследование показывает физи-ологические роли материнской кишечной микробиоты, в частности, влияние на вас-куляризацию плаценты. Плацентарная не-достаточность ассоциирована с низким ве-сом плода, преэклампсией и повышенным риском заболеваний во взрослом возрасте. Стимуляция выработки КЦЖК микроби-отой, особенно с помощью питания, может оказывать защитное действие.
В целом, данные подчеркивают ключевую роль материнской кишечной микробиоты в стимуляции роста и развития плаценты
Материнский микробиом важен для оптимального развития сосудов плаценты
КЦЖК способствуют росту и развитию сосудов плаценты, даже в условиях недоедания матери
Материнская кишечная микробиота во время беременности критически важна для роста и васкуляризации плаценты у мышей.
Понимание влияния микробиома кишечника матери на структуру и функцию плаценты может открыть новые возможности для улучшения здоровья матери и плода и снижения риска хронических заболеваний.
Проф. Юозас Купчинскас (Juozas Kupcinskas)
Кафедра гастроэнтерологии и Институт исследований пищеварения, Литовский университет медицинских наук, Каунас, Литва
Helicobacter pylori (H. pylori) поражает около 50% населения земного шара, это самая распространенная бактериальная инфекция в мире. Согласно данным ВОЗ, H. pylori является канцерогеном группы 1, способным вызывать предраковые состояния и рак желудка, включая аденокарциному. Несмотря на прежние представления об H. pylori как единственном обитателе желудка, современные методы исследования расширили понимание желудочного микробиома.
H. pylori играет ключевую роль в формировании микробной среды желудка. Тем не менее, активно исследуется и не-хеликобактерный микробиом желудка. H. pylori — основной модулятор микробиома желудка, но другие виды также могут участвовать в канцерогенезе. Также изучается влияние ингибиторов протонной помпы (ИПП) и эрадикации H. pylori на микробиом. В данном обзоре обобщены современные данные о микробиоме желудка, роли H. pylori в его формировании и влиянии эрадикации H. pylori и ингибиторов протонной помпы (ИПП) на микробиом человека.
Микробиом желудка привлекает все боль-ше внимания, а факторы, определяющие его состав, вызывают растущий интерес. Vilchez-Vargas и соавт. исследовали микробный состав различных отделов же-лудочно-кишечного тракта (ЖКТ). В иссле-довании проанализировали биоптаты мик-робиома желудка слизистой оболочки 108 пар близнецов. Разнообразие микробиома оценили путем амплификации и секвени-рования областей V1-V2 гена 16S рРНК. Результаты подтвердили ключевую роль H. pylori в составе микробиоты желудка, согласуясь с предыдущими данными. 1
Hua и соавт. изучили влияние H. pylori на богатство и разнообразие микробиоты же-лудка у 193 пациентов с хроническим гаст-ритом. Анализ V3-V4 области гена 16S рРНК выявил значительные изменения в микробиоте желудка, вызванные инфек-цией H. pylori. В частности, H. pylori подавляла доминирующую микробиоту желудка на уровне рода, включая Aliidio-marina, Reyranella, Halomonas, Pseudomo-nas и Acidovorax. Результаты показали сильную связь между вирулентными штам-мами H. pylori, хроническим атрофическим гастритом и снижением разнообразия микробиоты желудка. 2
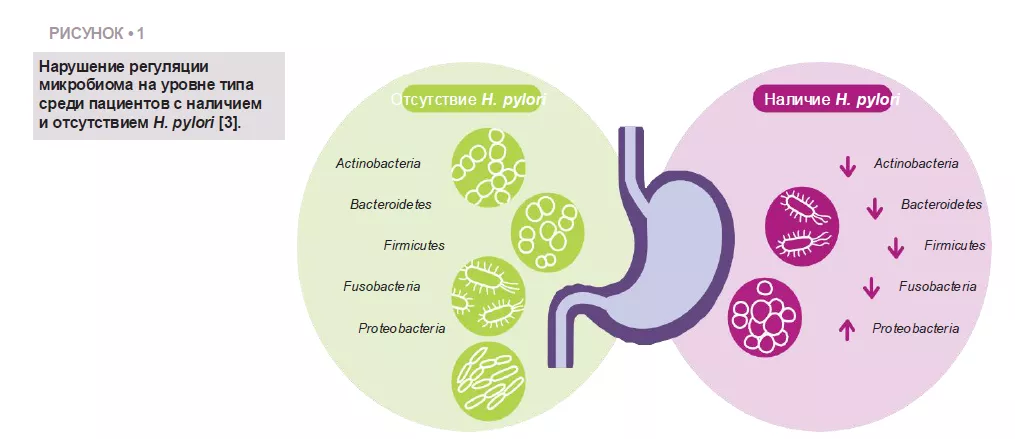
Schulz и соавт. проанализировали различия в микробиоте у пациентов с и без H. pylori. Относительная численность Proteobacteria была значимо выше в аспиратах пациентов, инфицированных H. pylori. Другие типы имели меньшую относительную численность (рисунок 1). 3
Miftahussurur и соавт. изучили различия в микробиоте желудка между H. pylori-положительными и H. pylori-отрицательными пациентами в индонезийской когорте из 137 человек. Микробное β-разнообразие и богатство были значимо выше в H. pylori-положительных образцах, чем в H. pylori-отрицательных. Результаты также показали ведущую роль H. pylori в формировании микробного сообщества желудка у данной этнической группы. 4
В совокупности эти исследования подчеркивают ключевую роль H. pylori в формировании разнообразия и богатства микробиома желудка, несмотря на его агрессивную среду.
В желудке крайне неблагоприятная среда для микроорганизмов. Несколько десяти-летий назад было установлено, что H. pylori — бактерия, способная выживать в этой агрессивной среде. Это открытие вызвало интерес и стиму-лировало дальнейшее изучение микро-биома желудка. Неясно, являются ли не-Helicobacter бактерии желудка транзитор-ными контаминантами или частью рези-дентной микробиоты. Spiegelhauer и со-авт. исследовали 22 пациентов с диспеп-сией и 12 пациентов с аденокарциномой желудка. 5
Их биоптаты слизистой же-лудка были исследованы путем культиви-рования микроорганизмов и анализа V3-V4 области гена 16S рРНК. Авторы пред-положили, что H. pylori, как истинный ре-зидент желудка, сохранится в промытых биоптатах. Результаты показали снижение бактериальной нагрузки в промытых биоп-татах, что указывает на транзиторное заг-рязнение из ротовой полости. Однако, раз-нообразие микроорганизмов не отлича-лось между промытыми и непромытыми биоптатами.
Неясно, являются ли микроорганизмы, отличные от H. pylori, в желудке транзиторными или постоянными обитателями.
Вероятно, слюна с микроорганизмами спо-собна некоторое время выживать в кислой среде желудка. При гастроскопии и взятии проб следует учитывать контаминацию из ротоглотки 6. Эти результаты указывают на необходимость дальнейших исследо-ваний собственного микробиома желудка.
H. pylori — одна из наиболее распростра-ненных инфекций в мире, поражающая более половины населения. Большинство схем лечения H. pylori, включающих два и более антибиотика, могут негативно вли-ять на микробиом желудочно-кишечного тракта. Liou и соавт. исследовали долго-срочные изменения кишечной микробиоты после эрадикации H. pylori. Их много-центровое рандомизированное исследова-ние включало 1620 участников, случайным образом распределенных по трем группам лечения. Бактериальное разнообразие оценивали в динамике после эрадикации по анализу образцов кала. Результаты показали сни-жение альфа- и бета-разнообразия в те-чение двух недель после эрадикации, с последующим возвратом к исходному уровню к 8-й неделе и через год. Эти данные свидетельствуют о кратковремен-ных нарушениях микробиома желудочно-кишечного тракта после эрадикации H. pylori и предполагают ее общую безо-пасность в долгосрочной перспективе. 7
Не и соавт. изучили изменения микро-биома желудочно-кишечного тракта после эрадикации H. pylori, проанализировав ген 16S рРНК в образцах слизистой желудка и кала. После эрадикации, через 24 недели, альфа-разнообразие микробиома желудка увеличилось, а бета-разнообразие кишеч-ного микробиома значимо изменилось, приближаясь к показателям здоровых контрольных субъектов. 8
Guo и соавт. обобщили данные об изме-нениях микробиома желудка после эради-кации H. pylori. Их систематический обзор и метаанализ включал девять исследова-ний с участием 546 пациентов. Этот мета-анализ впервые детально описывает из-менения альфа-разнообразия после эра-дикации H. pylori. Результаты не выявили значимых различий в разнообразии микро-биоты между четырех- и трехкомпонен-тной терапией. Авторы выявили увели-чение альфа-разнообразия, сохраняюще-еся в долгосрочной перспективе, с умень-шением таксонов, связанных с H. pylori, и увеличением комменсалов желудка 9. Для оценки влияния эрадикации H. pylori на кишечный микробиом, Yap и соавт. про-вели исследование на 17 молодых людях. Они секвенировали область V3-V4 гена 16S рРНК и проанализировали ки-шечный микробиом до и через 18 месяцев после эрадикации H. pylori с использо-ванием кларитромицина и метронидазола. Микробное разнообразие существенно не изменилось за 18 месяцев после эради-кации по сравнению с исходным уровнеm10.
Глобальное потребление ингибиторов протонной помпы (ИПП) растет, выводя их в число 10 самых назначаемых лекарст-венных препаратов в мире 11. Это пре-параты первой линии при гастроэзофаге-альной рефлюксной болезни, язвенной бо-лезни, диспепсии и, в сочетании с антиби-отиками, для эрадикации H. pylori 12. Необоснованное или длительное при-менение ИПП связано с повышенным рис-ком кишечных инфекций, включая Clostridium difficile, Salmonella spp., Shigella spp., Campylobacter spp. и другие кишечные патогены 11.
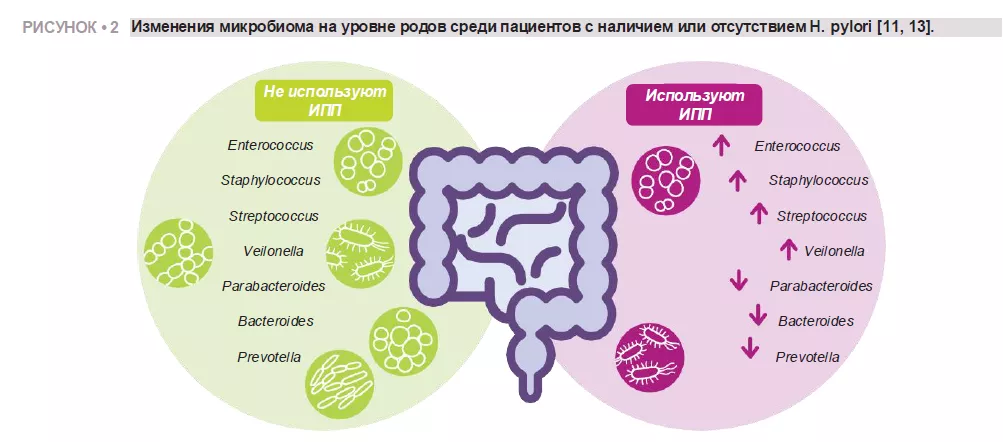
Imhann и соавт. проанализировали мик-робиом 211 пациентов, принимающих ИПП, секвенируя V4-область гена 16S рРНК. Применение ИПП было связано со значимым снижением альфа-разнообра-зия и увеличением численности бактерий родов Enterococcus, Streptococcus, Staphy-lococcus и Veillonella. (рисунок 2). Роды Enterococcus и Veillonella были связаны с повышенной восприимчивостью к инфек-циям Clostridium difficile 11. Несмотря на общепризнанную безопасность ИПП и редкие побочные эффекты, данные указы-вают на их негативное воздействие на ки-шечный микробиом.
Zhang и соавт. провели метаанализ вли-яния ИПП на кишечную микробиоту чело-века, проанализировав данные четырех исследований с секвенированием ампли-конов гена 16S рРНК. Их результаты продемонстрировали зна-чимое влияние использования ИПП на микробное разнообразие, при этом у пользователей ИПП наблюдалось более низкое альфа-разнообразие по сравнению с контрольной группой. Они обнаружили снижение численности родов Parabacteroides, Veillonella, Bacteroides и Prevotella, а также семейств Ruminococcaceae и Lachnospiraceae (рисунок 2) 13.
В исследовании Weitsman и соавт. 177 участников были разделены на группу пользователей ИПП и контрольную группу в соотношении 1:2. Они проанализи-ровали образцы стула и, впервые, мик-робиом двенадцатиперстной кишки. Зна-чимых различий в альфа- или бета-разнообразии между пользователями ИПП и контрольной группой обнаружено не было. Тем не менее, у принимающих ИПП наблюдалось увеличение относительной численности Campylobacteraceae (филум Proteobacteria) и снижение Clostridiaceae (филум Firmicutes) на уровне семейства. Анализ стула также выявил снижение Clostridiaceae и увеличение Streptococcaceae14.
В целом, эти исследования показывают, что ИПП влияют на микробиом человека. Клиническая значимость этих результатов требует дальнейшего изучения в будущих исследованиях.

Желудок — агрессивная среда для микроорганизмов, продолжающиеся исследования изучают, является ли его микробиота постоянной или транзиторной. Несмотря на клиническую значимость, H. pylori играет заметную роль в формировании микробиома желудка. Эрадикация H. pylori оказывает временное и обратимое влияние на микробиом желудка и кишечника. Ингибиторы протонной помпы (ИПП) — одни из самых часто используемых лекарственных средств. Научные исследования показывают, что ИПП изменяют структуру кишечного микробиома; однако клиническая значимость этих изменений требует дальнейшего изучения.
Сколько пациентов с постоянным дискомфортом в верхних отделах желудочно-кишечного тракта вы встречаете каждую неделю? Сколько из них остаются недиагностированными с функциональной диспепсией (ФД)?
ФД страдает около 7 % взрослых3 , но ее часто неправильно диагностируют из-за совпадения симптомов с рефлюксом, гастропарезом и СРК. Будучи нарушением взаимодействия кишечника и мозга, она включает в себя изменения моторики, дисбаланс микробиоты и психологические факторы, что затрудняет диагностику.
Чтобы помочь, профессор Маура Корсетти, профессор Николас Тэлли и профессор Лукас Ваутерс в сотрудничестве с Институтом микробиоты Biocodex разработали контрольный список для диагностики функциональной диспепсии. Этот инструмент способствует более точной диагностике и более четкому общению с пациентами, улучшая управление и уход.

Часто называемое несварением желудка, это распространенное расстройство взаимодействия кишечника и мозга (DGBI), характеризующееся постоянными симптомами в верхней части живота без признаков структурного заболевания.
Функциональной диспепсии - это хроническое и ремиттирующее расстройство, возникающее в верхнем гастродуоденальном отделе и характеризующееся одним или несколькими из следующих симптомов2:

БОЛЬ В ЭПИГАСТРИИ
«Это как будто тебя пронзают изнутри наружу.»

ЖЖЕНИЕ В ЭПИГАСТРИИ
«у меня горит желудок, будто он в огне.»

БЫСТРОЕ НАСЫЩЕНИЕ
(сокращение обычного объема пищи)
«я чувствую сытость, даже если почти ничего не съел(а).»

ОЩУЩЕНИЕ ПЕРЕПОЛНЕНИЯ В ЖЕЛУДКЕ ПОСЛЕ ЕДЫ
(при нормальном размере порции)
«у меня ощущение, будто в желудке лежит камень.»
Функциональной диспепсии - высоко распространенное заболевание ДГПЖ, основанное на строгих критериях Рима IV:
7% распространенность функциональной диспепсии в мире
Однако оценки распространенности варьируются в зависимости от диагностических критериев и географических регионов.
Функциональной диспепсии несколько чаще встречается у женщин, чем у мужчин, и может поражать людей всех возрастов. Это состояние часто недодиагностируется, поскольку симптомы могут накладываться на другие желудочно-кишечные расстройства, такие как гастроэзофагеальная рефлюксная болезнь (ГЭРБ) и синдром раздраженного кишечника (СРК). Несмотря на высокую распространенность, функциональная диспепсия остается сложным состоянием для лечения из-за ее сложной и многофакторной патофизиологии.

Существует два подтипа Функциональной диспепсии:
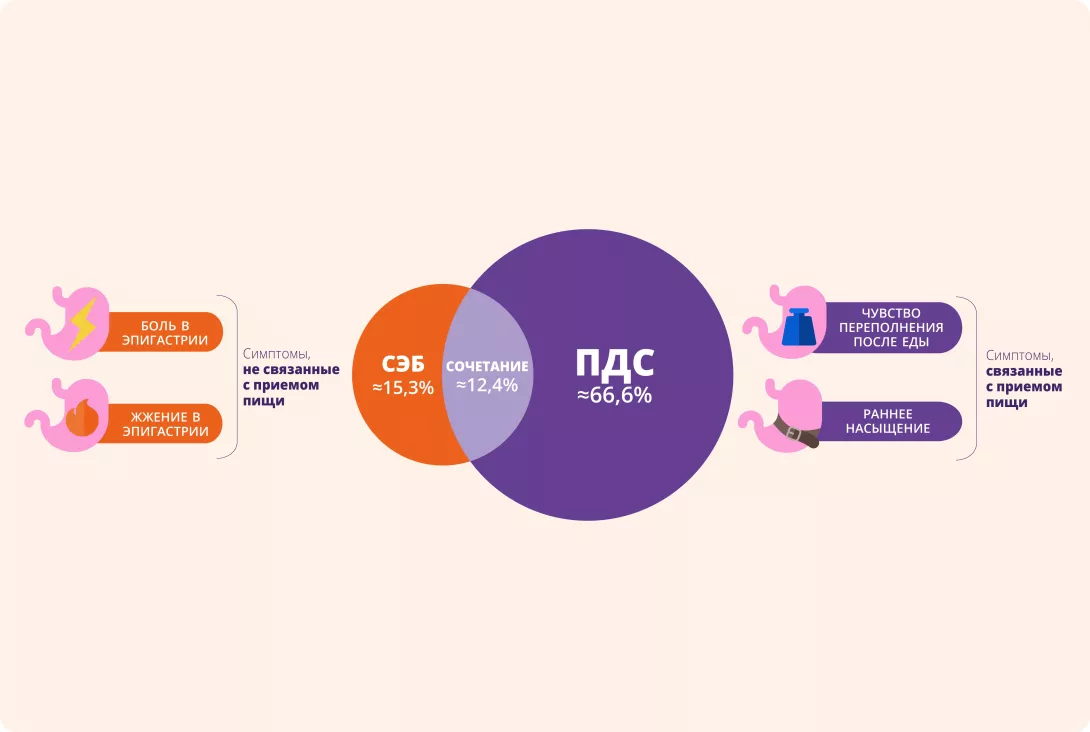
При отсутствии биомаркеров диагностика основывается на симптоматических критериях, среди которых наиболее современными и валидизированными являются Римские критерии IV пересмотра.
Согласно Римским критериям IV, пациенты с Функциональной диспепсией классифицируются на два подтипа:
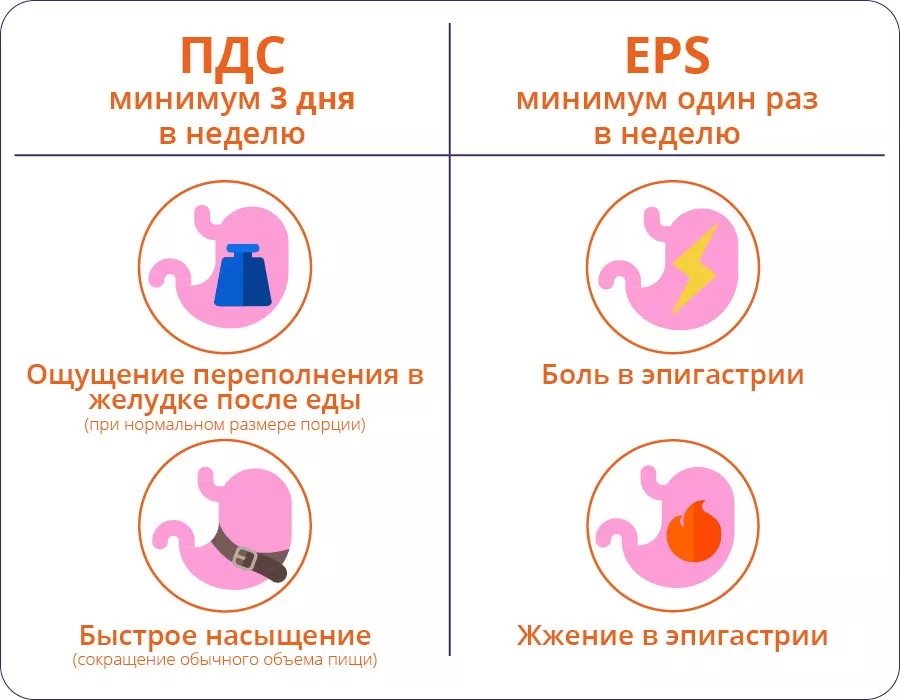
- Постпрандиальный дистресс-синдром (PDS) — характеризуется симптомами, вызванными приёмом пищи.
- Синдром эпигастральной боли (EPS) — включает эпигастральную боль или жжение, которые возникают не исключительно после еды и могут даже облегчаться после приёма пищи.

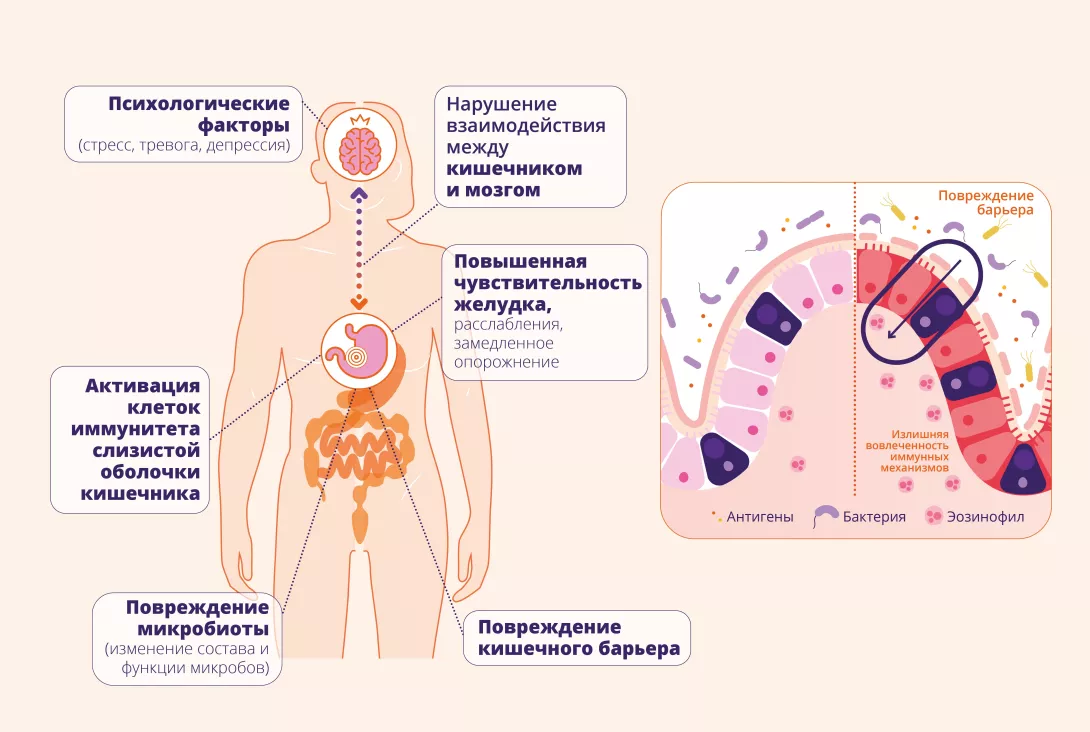
Хотя точные патофизиологические механизмы, лежащие в основе Функциональной диспепсии, пока полностью не изучены, и её этиология остаётся неясной, последние исследования выявили следующие патофизиологические механизмы¹:
Психологические факторы: Нарушенное взаимодействие между кишечником и мозгом — стресс и тревожность влияют на функцию ЖКТ и могут усиливать симптомы.
Гиперчувствительность и нарушенная моторика желудка: Повышенная чувствительность сенсорных нейронов желудка и двенадцатиперстной кишки приводит к усиленному восприятию боли и дискомфорта при обычных стимуляциях; нарушение моторики, включая замедленное опорожнение желудка и ухудшение фундального расслабления.
Активация кишечного иммунного ответа: Вялотекущие воспалительные процессы, особенно увеличение количества тучных клеток и эозинофилов в двенадцатиперстной кишке, способствуют появлению симптомов.
Нарушение кишечного барьера: Повреждение слизистого барьера позволяет пищевым антигенам и микробным продуктам проникать в слизистую, что может инициировать иммунную активацию.
Изменения микробиоты двенадцатиперстной кишки: Нарушения в составе микробиоты могут способствовать иммунной активации, висцеральной гиперчувствительности и нарушению моторики.
Эти механизмы взаимодействуют между собой в сложной сети, что делает Функциональную диспепсию многофакторным расстройством, требующим персонализированного подхода к лечению.

Диагноз ставится на основании симптомов в соответствии с Римскими критериями²:

*В регионах Юго-Восточной Азии и других местностях с высокой заболеваемостью раком желудка следует учитывать более низкий возрастной порог.
Следует направить пациента на консультацию к гастроэнтерологу

Лечение Функциональной диспепсии предполагает комплексный подход, направленный на облегчение симптомов и улучшение качества жизни³,⁶,⁷

Изменения образа жизни, включая:
могут способствовать снижению выраженности симптомов.
Медикаментозный подход предполагает преимущественное использование препаратов, подавляющих кислотность (ингибиторы протонной помпы — ИПП, применяются наиболее часто), а также прокинетиков.
Нейромодуляторы, такие как трициклические антидепрессанты, применяются для модуляции висцеральной гиперчувствительности, изменения восприятия боли и улучшения симптомов в резистентных случаях.
Когнитивно-поведенческая терапия, гипнотерапия, управление стрессом, может играть ключевую роль в долгосрочном контроле симптомов.
Наиболее частые вопросы o Функциональной диспепсии
Функциональной диспепсии можно лечить, но нельзя полностью излечить. Возможно самостоятельное выздоровление
Функциональной диспепсии не увеличивает риск развития рака любой локализации
Функциональной диспепсии— это многофакторное нарушение, вызванное изменением чувствительности кишечника, моторики, микробиоты и связи между кишечником и мозгом
Диета эффективна и полезна
Вода не улучшает состояние при Функциональной диспепсии
Функциональной диспепсии не увеличивает риск смерти.

Подход к последующему наблюдению зависит от ответа на лечение (многие пациенты не отвечают на терапию).
Интервал в 2–3 месяца является оптимальным для контроля, с возможностью увеличения интервалов при положительной динамике, в зависимости от инициативы пациента.
Чувствительность к добавкам, различная у каждого человека, во многом определяется кишечной микробиотой. Можно ли по анализу кала предсказать эту чувствительность?

Хотя пищевые добавки улучшают текстуру и продлевают срок хранения многих продуктов, они также вызывают опасения относительно здоровья. Предполагается, что некоторые из них способствуют развитию хронических воспалительных заболеваний, воздействуя на кишечную микробиоту.
Однако эффекты могут в значительной степени различаться у разных людей, как показало недавнее клиническое рандомизированное контролируемое исследование (исследование FRESH [Functional Research on Emulsifiers in Humans]). Используемая добавка: карбоксиметилцеллюлоза (или E466).
Как можно объяснить или даже предсказать повышенную чувствительность? Группа исследователей 1 продолжила ранее начатую работу, фокусируя внимание на микробиоте. Для демонстрации экспериментов in vitro был использован лабораторный реактор, способный имитировать микробиоту кишечника человека
2500 Объединенный комитет экспертов ФАО/ВОЗ по пищевым добавкам (JECFA) провел оценку более 2500 пищевых добавок, около 40 загрязнителей и природных токсикантов, а также компонентов примерно 90 ветеринарных препаратов. ²
Когда исследователи подвергли микробиоту, собранную у добровольцев в рамках исследования FRESH, воздействию карбоксиметилцеллюлозы в биореакторе, они обнаружили ту же разницу в чувствительности, что наблюдалась in vivo в исследовании FRESH: микробиота тех же 2 из 7 добровольцев, получавших E466, была нарушена при контакте с эмульгатором.
Микрореактор точно воспроизводит индивидуальные различия, наблюдаемые в исследовании FRESH, что позволяет предсказать, чувствительна ли данная микробиота к E466, без необходимости проведения исследований in vivo.
Чтобы подтвердить связь между изменением кишечной флоры и воспалением кишечника, наблюдаемым у некоторых участников исследования FRESH, получавших E466, микробиоту 2 «чувствительных» к E466 индивидуумов и 2 нечувствительных индивидуумов трансплантировали мышам, лишенным собственной флоры.
Только у мышей, получивших «чувствительную» флору и получавших добавку, развилось кишечное воспаление и тяжелый колит с укорочением толстой кишки, повреждением слизистой оболочки и инфильтрацией макрофагами.
С этим воспалением были связаны определенные бактерии, включая Adlercreutzia equolifaciens и Frisingicoccus caecimuris.
Pending a possible signature, this study highlights new links between the gut microbiota and healthy eating. It also points to the need to consume fewer ultra-processed products (which, like some sweeteners, appear to be detrimental to the health of the gut microbiota).
Оставалось выяснить, могла ли
(sidenote:
метагеномику
Метод изучения генетического материала в образцах, взятых непосредственно из природной экосистемы (кишечник, океан, почва, воздух и т. д.), а не в образцах, полученных в лаборатории. Она позволяет описать гены, содержащиеся в образце, а также понять функциональные возможности микробного сообщества
источник: Riesenfeld CS, Schloss PD, Handelsman J. Metagenomics: genomic analysis of microbial communities. Annu Rev Genet. 2004;38:525-52.)
)
сигнатура в образцах кала предсказать исход. Обучение алгоритма (на образцах кала 7 добровольцев из исследования FRESH, получавших E466) выявило 78 функциональных маркеров чувствительности.
Эта сигнатура позволила предсказать чувствительность к добавке в контрольной группе того же исследования (среди тех, кто не получал E466). Однако ее применение в других когортах не дало убедительных результатов.
В ожидании возможного подтверждения, исследование указывает на новые связи между кишечной микробиотой и здоровым питанием. Оно также указывает на необходимость потреблять меньше ультраобработанных продуктов (которые, подобно некоторым подсластителям, могут быть вредны для здоровья кишечной микробиоты)
 Зеленая средиземноморская диета: каковы связи между кардио-метаболическим здоровьем и микробиотой кишечника?
Зеленая средиземноморская диета: каковы связи между кардио-метаболическим здоровьем и микробиотой кишечника?
 С грядки в кишечник: удивительное влияние фруктов и овощей на кишечную микробиоту
С грядки в кишечник: удивительное влияние фруктов и овощей на кишечную микробиоту
Новый консенсус 69 мировых экспертов переопределяет правила анализа микробиома, подчеркивая необходимость строгого контроля, комплексных методов и учета важнейших данных о пациентах, чтобы предоставить клиницистам надежную информацию о здоровье кишечника.

В последние годы идея использования кишечной микробиоты в качестве диагностического инструмента захватила воображение медицинского сообщества. Несмотря на растущий интерес, клиническая польза анализа микробиома остается в значительной степени недоказанной.
Недавний международный консенсусный 1 отчет осветил эту актуальную проблему. Международная инициатива, объединившая 69 экспертов из 18 стран, разработала научно обоснованные стандарты для анализа микробиома, предназначенные для клиницистов и лабораторий.
69 эксперты
18 страны
группы руппа, включающая клиницистов, микробиологов, микробных экологов, вычислительных биологов и биоинформатиков, использовала метод Дельфи для выработки рекомендаций. Эксперты в пяти группах изучили общие принципы, процедуры пробоподготовки, анализ микробиома, стандарты отчетности и клиническую значимость. Каждое положение тщательно проверялось и оценивалось по шкале Лайкерта. В финальную версию включались только рекомендации, достигшие 80% согласия
Этот тщательный процесс выявил необходимость мер контроля качества, междисциплинарного сотрудничества и четкого информирования об ограничениях анализов микробиома. Также было подчеркнуто, что анализы должны назначаться только по медицинским показаниям, а не по инициативе пациентов.
Ниже приведены четыре рекомендации, ОБЯЗАТЕЛЬНЫЕ для каждого клинициста, заинтересованного в использовании микробиома в своей клинической практике.
Признавая перспективность анализа микробиома для определенных состояний, группа заключила, что его рутинное клиническое применение пока недостаточно обосновано. Необходимы дальнейшие исследования, включая надежные исследования диагностической точности. Для будущей интеграции необходимо обучение клиницистов основам микробиомики и интерпретации отчетов. Этот консенсус является важной дорожной картой для ответственной разработки и клинического внедрения.

