Revista da Imprensa #1: Microbiota Vaginal
Dra. Nguyễn Bá Mỹ Nhi
Diretora do Centro de Ginecologia e Obstetrícia do Hospital Tam Anh, Cidade de Ho Chi Minh, Vietname



Dra. Nguyễn Bá Mỹ Nhi
Diretora do Centro de Ginecologia e Obstetrícia do Hospital Tam Anh, Cidade de Ho Chi Minh, Vietname

O corpo humano hospeda biliões de microrganismos, designados coletivamente por microbioma, que residem em vários locais e coexistem numa complexa parceria simbiótica. É importante referir que a microbiota vaginal influencia a saúde reprodutiva e a saúde geral das mulheres. A compreensão deste ecossistema tem o potencial de revolucionar a prevenção e o tratamento destas afeções.
Esta análise destaca as relações entre a disbiose da microbiota vaginal e as doenças ginecológicas, bem como as complicações relacionadas com a gravidez. Especificamente, a redução dos lactobacilos e o aumento da diversidade da microbiota vaginal estão associados à infeção pelo vírus do papiloma humano (VPH), à formação de lesões no colo do útero e ao cancro do colo do útero. A perda da predominância vaginal de Lactobacillus pode criar um ambiente pró-inflamatório que compromete o sucesso da implantação embrionária, levando à infertilidade. Um desequilíbrio no microbioma vaginal pode desencadear uma inflamação que leva a complicações na gravidez. Ter menos espécies de Lactobacillus no microbioma vaginal aumenta os riscos de rotura prematura de membranas, parto pré-termo, abortamento espontâneo e gravidez ectópica. A disbiose vaginal pode contribuir para a resistência à insulina, algo caraterístico da diabetes mellitus gestacional. Foi também encontrada uma maior diversidade na composição bacteriana na pré-eclampsia grave. O exame para a deteção de colonização por Prevotella bivia durante a gravidez pode ajudar a prever e a mitigar as afeções hipertensivas durante a gravidez.
Esta análise destaca a importância fundamental do microbioma vaginal na saúde reprodutiva e geral das mulheres. A composição deste microbioma pode ter impacto em tudo, desde a fertilidade e desfechos da gravidez à suscetibilidade a infeções. O artigo engloba diversos aspetos da microbiota vaginal, incluindo a sua relação com o funcionamento do sistema imunitário, a inflamação e a defesa contra agentes patogénicos, proporcionando assim uma compreensão ampla e holística do seu papel, com informações úteis generalizáveis sobre a saúde da mulher em geral. Um melhor conhecimento sobre a forma como o microbioma vaginal influencia a saúde representa um avanço importante para a deteção precoce e a prevenção de doenças, em vez de apenas se centrar em tratar infeções ou doenças depois de estas surgirem. No entanto, são necessários dados de estudos a longo prazo para esclarecer os efeitos a longo prazo dos desequilíbrios do microbioma vaginal. Embora os probióticos e outras intervenções que têm por base o microbioma se mostrem promissoras para a manutenção de um microbioma vaginal saudável, as estirpes probióticas, as dosagens e os mecanismos de administração ainda não foram padronizados para aplicação clínica. Há ainda muito trabalho a fazer.
Em suma, ter menos espécies de Lactobacillus vaginais e maior diversidade microbiana vaginal está associado a complicações obstétricas e ginecológicas. Esta análise destaca a possibilidade de utilizar diagnósticos baseados no microbioma para detetar desequilíbrios na flora vaginal, potencialmente antes da manifestação dos sintomas. A intervenção precoce pode evitar consequências adversas.
Dra. Nguyễn Bá Mỹ Nhi
Diretora do Centro de Ginecologia e Obstetrícia do Hospital Tam Anh, Cidade de Ho Chi Minh, Vietname

As alterações provocadas pela menopausa diminuem a diversidade do microbioma intestinal e causam uma mudança para um microbioma que se assemelha mais a um microbioma intestinal masculino. Esta análise descreve em pormenor as consequências destas alterações para a saúde. Durante a perimenopausa, uma diminuição gradual dos níveis hormonais perturba o equilíbrio do microbioma intestinal e contribui para resultados adversos para a saúde, incluindo doenças cardiometabólicas e alterações no metabolismo do estrogénio. As flutuações hormonais durante a menopausa alteram o microbioma oral, aumentando o risco de cáries dentárias, de periodontite e de infeções orais como a candidíase. As alterações da microbiota vaginal provocadas pela menopausa aumentam a suscetibilidade à vaginose bacteriana, à atrofia vulvovaginal e às infeções recorrentes do trato urinário. A menopausa também altera a diversidade e a abundância da microbiota intestinal que tem sido associada à inflamação. A inflamação crónica provocada pela disbiose predispõe as mulheres na menopausa a distúrbios metabólicos e doenças autoimunes.
Este artigo faz a ponte entre a endocrinologia e a microbiologia e destaca o impacto sistémico da menopausa para além da saúde reprodutiva. Um ponto forte da revisão é a sua análise holística das flutuações hormonais relacionadas com a menopausa, com as correspondentes alterações na composição e diversidade microbiana intestinal e vaginal. Isto permite explorar biomarcadores baseados no microbioma para gerir os sintomas da menopausa, como a síndrome geniturinária, as alterações metabólicas ou a inflamação. A interpretação deste artigo relativamente às alterações relacionadas com a idade na saúde das mulheres enriquece o interesse crescente sobre o papel do microbioma humano na doença. Embora a terapia de substituição hormonal se tenha revelado promissora na atenuação de alguns dos efeitos adversos da deficiência de estrogénio, a sua aplicação mais generalizada é limitada pelos seus riscos sistémicos. A utilização direcionada de probióticos específicos para restabelecer o equilíbrio microbiano intestinal, associada a modificações na dieta e no estilo de vida, pode facultar alternativas mais seguras e individualizadas que atenuem os efeitos adversos da menopausa na saúde.
A investigação científica relativamente ao microbioma na menopausa está sobrerrepresentada com dados provenientes de populações ocidentais e apresenta uma lacuna de conhecimentos mecanísticos pormenorizados. Uma vez que a dieta, o estilo de vida e os fatores ambientais influenciam significativamente o microbioma, necessitamos de investigação étnica e geograficamente diversificada que incorpore abordagens “ómicas” avançadas para elucidar completamente estas influências. Surgirão então estratégias de tratamento mais eficazes e personalizadas que poderão melhorar a qualidade de vida das mulheres na menopausa.
Em suma, a menopausa é uma transição de todo o organismo que envolve mudanças significativas no ecossistema microbiano. A compreensão e a resposta a estas alterações podem melhorar os desfechos para os pacientes e promover um envelhecimento mais saudável nas mulheres.
Dra. Nguyễn Bá Mỹ Nhi
Diretora do Centro de Ginecologia e Obstetrícia do Hospital Tam Anh, Cidade de Ho Chi Minh, Vietname

A microbiota intestinal é cada vez mais encarada como um sistema invisível, semelhante a um órgão, que para além de desempenhar um papel importante no bemestar da mulher, também afeta a fisiopatologia de algumas doenças, como a síndrome do ovário poliquístico (SOP). O conhecimento das vias dos metabolitos microbianos pode dar origem a tratamentos eficazes.
Uma meta-análise recente que incluiu 948 mulheres com SOP de 14 estudos explorou as relações entre a microbiota intestinal de mulheres de diferentes regiões e com diferentes níveis de testosterona. As principais conclusões revelaram composições distintas da microbiota intestinal em pacientes com SOP em comparação com os seus pares saudáveis, e uma microbiota intestinal significativamente diferente entre pacientes com SOP com níveis de testosterona mais elevados e pacientes com níveis de testosterona mais baixos. Além disso, os géneros de bactérias intestinais diferiam entre as pacientes com SOP de diferentes regiões; as pacientes europeias tinham elevados níveis de Alistipes, enquanto que as pacientes chinesas tinham níveis elevados de Blautia e Roseburia.
Estas conclusões apoiam a evidência científica atual que mostra que as pacientes com SOP têm menos tipos diferentes de bactérias e uma comunidade microbiana menos equilibrada em comparação com as mulheres saudáveis. Os dados também confirmam a abundância de géneros bacterianos específicos, tais como Escherichia/ Shigella e Alistipes, em pacientes com SOP, géneros associados à resistência à insulina e à inflamação. Este estudo sugere que o microbioma intestinal está associado a vários distúrbios metabólicos e hormonais associados à SOP, o que está em linha com estudos anteriores. É importante salientar que demonstra diferenças nas taxa bacterianas entre mulheres chinesas e europeias com SOP, o que pode auxiliar na personalização de estratégias de tratamento. Mais investigação para identificar as estirpes bacterianas associadas à SOP poderá melhorar as terapêuticas microbianas anti-SOP, e estudos realizados em diversas regiões geográficas contribuiriam para o tratamento global da SOP.
Em suma, a caracterização da microbiota intestinal em pacientes com SOP de diferentes países pode permitir que a microbiota intestinal funcione como um biomarcador para distinguir diferentes subtipos de SOP, melhorando assim o diagnóstico clínico e o tratamento da SOP.
Prof. Assoc. Ina Schuppe Koistinen
Departamento de Microbiologia, e Biologia Tumoral e Celular, Karolinska Institutet, Estocolmo, Suécia
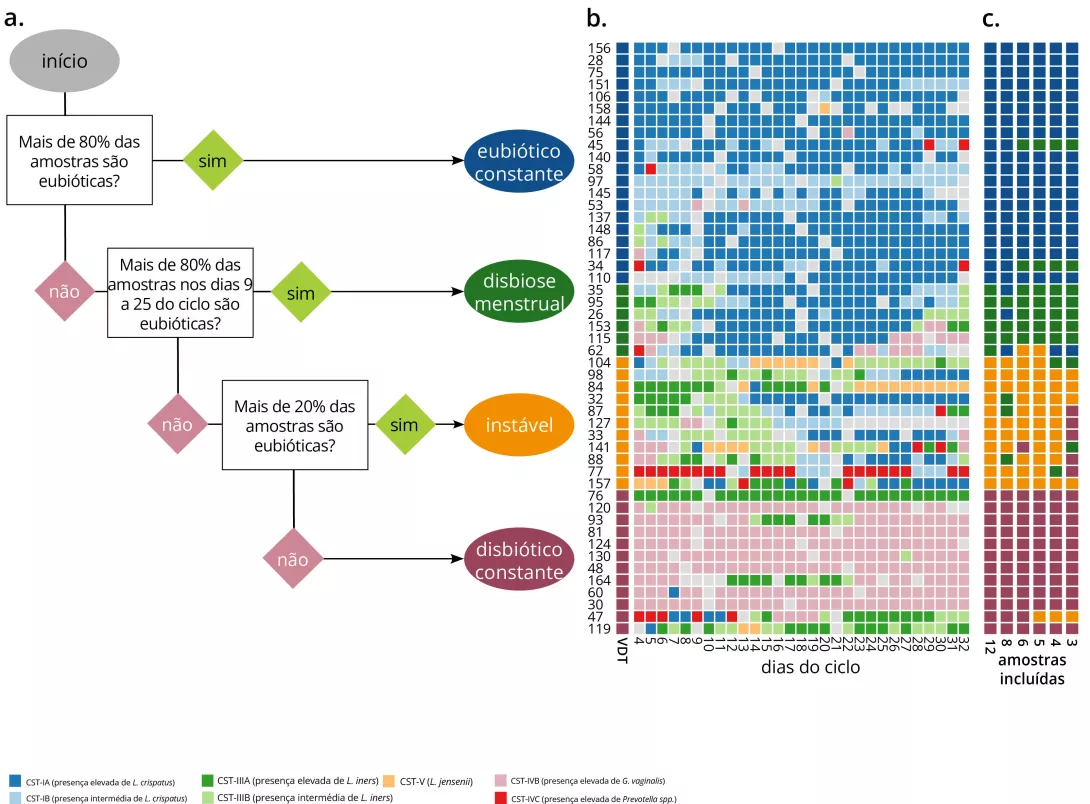
Este estudo metagenómico de alta resolução investiga as transições diárias no microbioma vaginal ao longo de um ciclo menstrual em 49 mulheres jovens saudáveis. Através da análise de dados taxonómicos, virais e de genes funcionais de amostras diárias, os autores apresentam um sistema de classificação dinâmico denominado Dinâmicas da Comunidade Microbiana Vaginal (DCMV), que classifica as mulheres em quatro grupos: eubiótica constante, disbiótica constante, disbiose relacionada com a menstruação, e disbiótica instável. Estes padrões refletem a forma como os microbiomas individuais respondem à menstruação, à atividade sexual e a outras exposições, e demonstram que a saúde vaginal não pode ser adequadamente avaliada apenas a partir de amostras estáticas. Em especial, a abundância de bacteriófagos e o conteúdo de genes bacterianos — como as bacteriocinas — podem contribuir para a estabilidade ou instabilidade das comunidades microbianas. Este trabalho destaca a complexidade e a individualidade do comportamento do microbioma vaginal e tem implicações para a melhoria do diagnóstico e dos cuidados personalizados em ginecologia.
A microbiota vaginal desempenha um papel fundamental na defesa contra agentes patogénicos, na manutenção da imunidade das mucosas e no apoio à saúde reprodutiva. A predominância de espécies de Lactobacillus, em especial L. crispatus, mantém um pH baixo e inibe a colonização patogénica2 . A disbiose, definida por uma perda de lactobacilos e crescimento excessivo de espécies anaeróbias, tais como Gardnerella ou Prevotella, está associada a um risco acrescido de vaginose bacteriana (VB), parto pré-termo3 , infertilidade4, infeções sexualmente transmissíveis, infeções pelo vírus do papiloma humano (VPH) e cancros ginecológicos5 . . Estudos anteriores demonstraram que as alterações hormonais, a menstruação e as relações sexuais podem influenciar a composição do microbioma vaginal6.Muitos destes estudos basearam-se em amostragens pouco frequentes e careciam de resolução para avaliar as flutuações a curto prazo ou determinar os fatores de transição entre a eubiose e a disbiose. As contribuições da dinâmica viral e dos genes bacterianos funcionais têm permanecido largamente inexploradas.
Este estudo introduz o conceito de DCMV, proporcionando uma nova estrutura para classificar o comportamento do microbioma ao longo do ciclo menstrual. Ao contrário dos tipos de estado de comunidade microbiana (CST), que descrevem composições estáticas do microbioma, os DCMV captam padrões temporais que podem refletir melhor a resiliência e a vulnerabilidade do microbioma. Os quatro DCMV — eubiótico constante, disbiótico constante, disbiose relacionada com a menstruação, e disbiótico instável — constituem perfis distintos de estabilidade microbiana. As mulheres do grupo eubiótico constante mantiveram predominância de Lactobacillus ao longo do ciclo, enquanto que as mulheres com disbiose constante tinham comunidades microbianas persistentes associadas à VB. A disbiose relacionada com a menstruação foi caracterizada por mudanças temporárias durante a menstruação, revertendose frequentemente a meio do ciclo, enquanto o grupo instável registou flutuações abruptas após exposições como relações sexuais, sugerindo uma maior fragilidade ecológica.
Uma das principais conclusões foi que a instabilidade no microbioma vaginal está associada a um aumento da atividade dos bacteriófagos e a uma maior prevalência de L. iners. Esta espécie está frequentemente associada a estados de transição ou menos estáveis, e a abundância de fagos pode refletir ciclos líticos ativos que desestabilizam as bactérias dominantes através de uma dinâmica de “eliminar o vencedor”. Além disso, as mulheres com disbiose transitória apresentaram uma maior abundância de potenciais agentes patogénicos, tais como Sneathia spp. durante e após a menstruação, o que sugere períodos específicos de vulnerabilidade.
A análise ao nível das estirpes revelou diferenças no conteúdo genético bacteriano, incluindo bacteriocinas produzidas por Gardnerella leopoldii que podem inibir os lactobacilos. Estes genes eram mais prevalentes nas DCMV instáveis e disbióticas, o que sugere um possível papel mecanicista na formação da estrutura da comunidade microbiana. Embora estes resultados genéticos exijam uma validação mais aprofundada, destacam a importância de ir além da classificação ao nível das espécies para compreender a função microbiana e o seu impacto na saúde do hospedeiro.
Este estudo destaca a necessidade de repensar a forma como a saúde vaginal é avaliada e acompanhada na prática clínica. O reconhecimento de que a microbiota vaginal é dinâmica — e de que os padrões de estabilidade diferem acentuadamente entre as mulheres — tem implicações para o diagnóstico, a avaliação de riscos e as estratégias terapêuticas. A colheita de amostras num único ponto no tempo, especialmente durante a menstruação, pode não captar flutuações significativas ou pode dar a ideia errada do estado microbiano de referência de uma mulher. Os médicos devem considerar a colheita de amostras em vários pontos do ciclo para avaliar melhor o comportamento do microbioma, particularmente em pacientes com sintomas recorrentes ou preocupações reprodutivas.
As limitações da classificação baseada nas CST são evidentes neste estudo. Duas mulheres com a mesma CST podem apresentar DCMV completamente diferentes, uma com eubiose estável e a outra com disbiose frequente. A incorporação da avaliação de DCMV poderia possibilitar intervenções mais personalizadas, como a recomendação de apoio profilático ao microbioma para mulheres com padrões instáveis ou a seleção de janelas de tempo de alto risco (por exemplo, pós-menstruação) para o rastreio de infeções.
A identificação da instabilidade provocada por fagos e das caraterísticas bacterianas ao nível das estirpes abre caminho para a medicina de precisão. As futuras terapêuticas poderão dar resposta ao nível da função microbiana — como a formação de biofilmes ou a produção de bacteriocinas — em vez de se limitarem à composição. A compreensão da dinâmica dos bacteriófagos vaginais pode também servir de base para novas estratégias de estabilização do microbioma.
Este estudo representa um avanço significativo na nossa compreensão do comportamento do microbioma vaginal, deslocando o foco dos CST estáticos para os padrões dinâmicos da comunidade microbiótica. Ao classificar as mulheres em quatro categorias de DCMV, o estudo proporciona uma nova perspetiva para avaliar a saúde do microbioma e as suas consequências clínicas. Estas informações exigem abordagens mais personalizadas e sensíveis ao tempo para a amostragem, o diagnóstico e a intervenção. A incorporação de dados do viroma e de caraterísticas bacterianas funcionais pode aperfeiçoar ainda mais as estratégias preditivas do risco e de tratamento. Em última análise, uma compreensão ecológica mais profunda do microbioma vaginal poderia ajudar a reduzir complicações como a vaginose bacteriana, o parto pré-termo e a infertilidade e apoiar um padrão mais individualizado de cuidados de saúde reprodutiva das mulheres.
Prof. Jean-Marc Bohbot
Diretor, Instituto Fournier, Paris, França
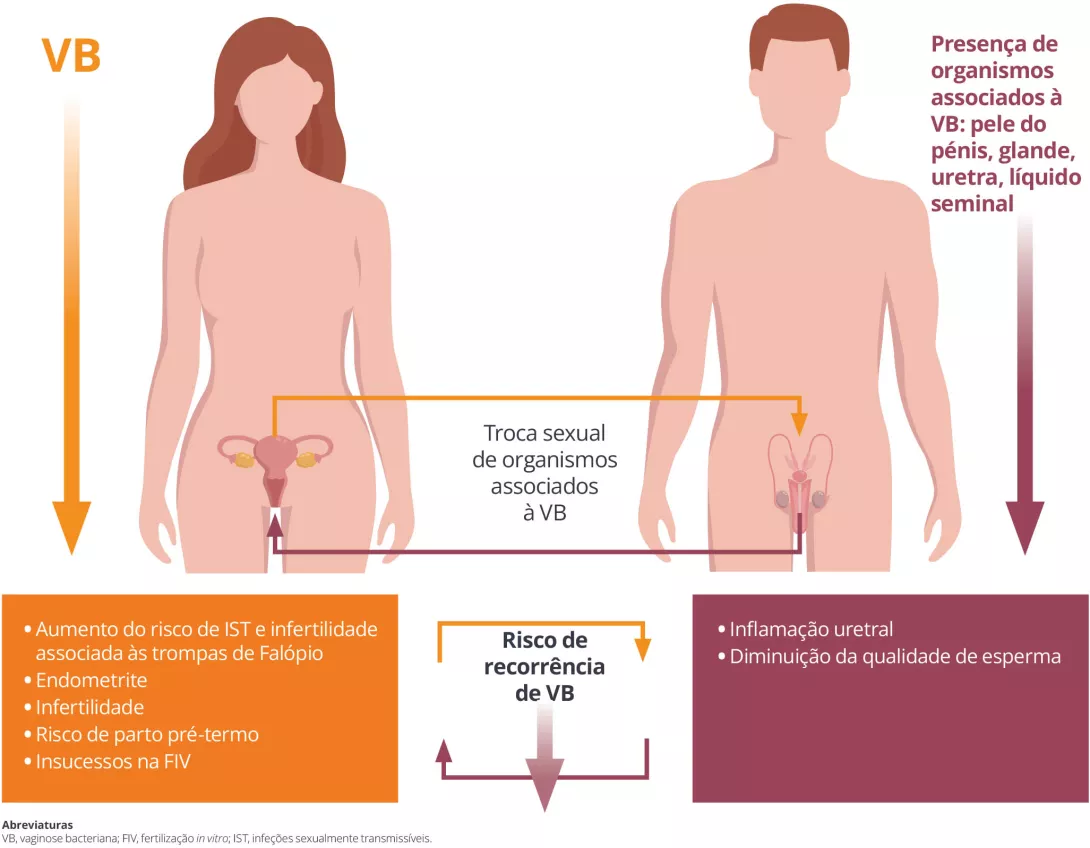
Os temas relativos a infeções vaginais, fertilidade ou complicações na gravidez centram-se frequentemente apenas nas mulheres. Mas há outro interveniente importante: o trato urogenital masculino (TUGM). A grande variedade de micróbios no TUGM pode afetar significativamente a saúde reprodutiva e vaginal feminina (Figura 1). A compreensão destas influências pode melhorar os desfechos para as mulheres, especialmente as que sofrem de infeções vaginais persistentes, problemas de fertilidade e complicações na gravidez.
O TUGM inclui diversos ambientes microbianos distintos: a pele do pénis, a uretra, o sémen e o trato urinário. Cada um tem uma comunidade microbiana única, influenciada por fatores como a circuncisão, as práticas sexuais, a higiene e o estilo de vida.
A pele do pénis tem bactérias semelhantes às que se encontram noutras superfícies cutâneas (pele) — principalmente Corynebacterium e Staphylococcus genera1, 2. Nos homens não circuncidados, a área sob o prepúcio (o sulco balanoprepucial) é predominada por bactérias anaeróbias, tais como Anaerococcus, Peptoniphilus, Finegoldia, e Prevotella, algumas das quais também se encontram em mulheres com vaginose bacteriana (VB)1, 2. A circuncisão reduz significativamente estes organismos anaeróbios, o que pode explicar o facto de as mulheres com parceiros circuncidados terem um menor risco de VB2.
A amostragem direta da uretra é dolorosa, pelo que a maioria dos estudos utiliza a urina da primeira micção como substituto para estudar a microbiota uretral. Este fluido contém uma mistura de bactérias como Lactobacillus, Streptococcus, Sneathia, Veillonella, Corynebacteria, e Prevotella3. Curiosamente, algumas delas estão ligadas à VB (ex.: Gardnerella vaginalis) e vaginite aeróbica (S. agalactiae)4.
O sémen não é apenas o esperma, inclui também os fluidos da próstata e das glândulas seminais. Estudos mostram que uma microbiota seminal predominada por Lactobacillus está associada a melhor qualidade espermática, enquanto outras bactérias (ex.: Ureaplasma, Mycoplasma, Prevotella, e Klebsiella pneumoniae) estão associadas a uma menor fertilidade5.
A microbiota urinária masculina é menos estudada, mas níveis mais baixos de géneros de Streptococcus, Lactobacillus, Pseudomonas, e Enterococcus foram encontrados em homens com concentração anormal de espermatozoides em comparação com homens com concentração normal de espermatozoides6. Os homens com motilidade anormal dos espermatozoides podem ter níveis elevados da bactéria Dialister micraerophilus, que contribuem para um microambiente pró-inflamatório do esperma6.
A microbiota do TUGM varia consoante o estado de circuncisão, as práticas sexuais e a composição da microbiota vaginal da parceira7.
Curiosamente, a microbiota uretral dos homens homossexuais não aparenta ser modificada pelo tipo de relação sexual (oral ou anal)8. As trocas bacterianas entre parceiros durante o contacto sexual são a regra. A razão pela qual estas trocas levam à disbiose vaginal em alguns casos e não noutros não é clara.
A microbiota seminal também é influenciada por várias funções fisiológicas (idade, alterações hormonais) e pelo estilo de vida ou fatores epigenéticos (tabagismo, consumo de álcool, obesidade, dieta rica em gordura, exposição a toxinas)5. Estes fatores modificáveis são potenciais alvos de intervenção.
A transmissão de microrganismos responsáveis por infeções bacterianas e virais sexualmente transmissíveis (IST), incluindo o VIH e o vírus Herpes simplex, durante o contacto sexual é a consequência mais óbvia do impacto do TUGM na saúde feminina. As complicações femininas ao nível de IST bacterianas (gonorreia, infeções por Chlamydia trachomatis ou M. genitalium) são amplamente conhecidas (inflamação e infeção do trato genital superior, risco de infertilidade associada às trompas de Falópio).
Diversos estudos mostraram que o perfil epidemiológico das mulheres com VB é comparável ao das mulheres com IST, sugerindo uma possível transmissão sexual das bactérias envolvidas na VB. A presença de bactérias associadas à VB no prepúcio e na uretra de parceiros de mulheres com VB e uma correspondência de estirpes bacterianas vaginais e uretrais masculinas sustentam a partilha destas estirpes ou a transmissão sexual da VB.
O tratamento do parceiro do sexo masculino com antibióticos orais (metronidazol) teve um impacto muito limitado nas taxas de recorrência em mulheres com VB recorrente, embora a combinação de metronidazol com um antibiótico tópico aplicado na pele do pénis em parceiros de mulheres com VB possa reduzir o risco de recorrência9.
O impacto do TUGM na saúde uterovaginal não se limita à transferência passiva de bactérias. O líquido seminal contém substâncias próinflamatórias (como as prostaglandinas) que podem ter impacto nas respostas imunitárias e na inflamação no trato genital feminino10.
A microbiota urogenital masculina é importante, não só para a saúde dos homens, mas também para a das mulheres. Embora a investigação ainda esteja a evoluir, é evidente que a dinâmica do parceiro do sexo masculino, o estilo de vida e a troca microbiana influenciam a saúde urogenital feminina. A evidência científica apoia cada vez mais uma abordagem mais holística e baseada no casal no que toca a gerir as preocupações reprodutivas, incorporando os cuidados do parceiro do sexo masculino nas estratégias de saúde sexual e reprodutiva de rotina para melhorar os desfechos para ambos os parceiros, especialmente em casos de infeções vaginais persistentes ou recorrentes. Incentivar hábitos mais saudáveis nos homens, incluindo deixar de fumar ou melhorar a dieta, pode melhorar a saúde microbiana do sémen e reduzir o risco de desfechos negativos para as suas parceiras.
Prof. Andrew Horne
Professor de Ginecologia e Diretor do Centro de Saúde Reprodutiva da Universidade de Edimburgo, no Reino Unido, com especialização na gestão da endometriose.
Dr. William Fusco
Gastroenterologista e investigador clínico do microbioma na Policlínica Agostino Gemelli, Roma, Itália.

A.H.: A endometriose é surpreendentemente comum, é tão comum quanto a asma e a diabetes. Estima-se que afete 1 em cada 10 mulheres.
W.F.: Na minha clínica dedicada à síndrome do intestino irritável (SII), é ainda mais comum, certamente mais de 25%.
A.H.: Os sinais são diversos e o diagnóstico pode ser difícil. O principal sintoma é a dor pélvica crónica, que, muitas vezes, pode ser debilitante, afetando a vida pessoal e profissional. No entanto, as pacientes podem também relatar relações sexuais dolorosas, fadiga crónica, diarreia e/ou obstipação e sintomas urinários. Qualquer sintoma cíclico pode ser um sinal de alerta para a endometriose.
W.F.: O aumento do peristaltismo e fezes mais moles durante a menstruação são normais, mas a diarreia significativa e cíclica pode não o ser. É expectável que se sinta dor, mas não ao ponto de deixar alguém de cama.
A.H.: Outro sintoma que causa alarme é a infertilidade. Mas eu tranquilizo as pacientes com endometriose: dois terços delas não terão problemas para engravidar, e as que têm geralmente respondem bem à cirurgia ou à FIV.
W.F.: Gostaria de acrescentar que a endometriose é crónica, mas isso não significa que não possa ser tratada. É importante que qualquer especialista envolvido no tratamento destas pacientes reforce esta informação.
A.H.: Não se conhece a verdadeira prevalência, mas quase todos as minhas pacientes têm sintomas digestivos: sensação de inchaço, alterações intestinais, azia. As lesões na parede intestinal explicam alguns sintomas, mas muitas pacientes têm doença peritoneal superficial, o que torna a ligação mais difícil de estabelecer.
W.F.: Fiz uma observação semelhante e diria que a doença inflamatória intestinal (DII) é quatro vezes mais comum nas mulheres com endometriose do que na população em geral (4% vs. 1%). A DII e a endometriose são ambas doenças autoimunes, sofrer de uma delas aumenta o risco de desenvolver a outra.
A.H.: A endometriose é uma doença inflamatória sistémica. Como ginecologistas, não estamos preparados para gerir os sintomas digestivos. Em Edimburgo, criei recentemente uma clínica conjunta de ginecologia e gastroenterologia.
W.F.: Quando a dor abdominal está estritamente relacionada com a menstruação, o gastroenterologista pode ter dificuldade em contribuir. Quando a relação é mais vaga, devemos investigar. Devemos investigar. A persistência de sintomas digestivos apesar do tratamento pode indicar a coexistência de SII. Além disso, é necessário ter em atenção os medicamentos, nomeadamente os antiinflamatórios não esteroides (AINE). O uso esporádico em pacientes jovens é aceitável, mas o uso crónico pode levar à necessidade de tomar um inibidor da bomba de protões (IBP), o que pode causar disbiose. Não existe uma regra universal, temos de adaptar os cuidados a cada paciente.
A.H.: Há um interesse crescente no papel dos microbiomas intestinal e vaginal na endometriose. Alguns estudos sugerem associações, mas são estudos pequenos e com falhas. Precisamos de grandes estudos de coortes. Acredito que o microbioma desempenha um papel importante, mas ainda não é claro o que vem primeiro: as alterações do microbioma ou a endometriose. Se a microbiota for responsável pelos sintomas, tal poderá abrir caminho para novos tratamentos.
W.F.: É uma área entusiasmante. Em pacientes com endometriose, observamos uma disbiose intestinal com ácidos gordos de cadeia curta reduzidos, como o acetato, o propionato e o butirato, que protegem a permeabilidade intestinal. O mesmo padrão pode ser observado noutras doenças gastroenterológicas, como a SII ou a DII, mas ainda não compreendemos a sua relação. Talvez um dia possamos personalizar os cuidados de saúde, restaurando de forma precisa as estirpes em falta. Para já, não sabemos o que causa o quê, pelo que são necessários estudos mecanísticos.
W.F.: Não existe uma dieta universal para a endometriose e não devemos criar falsas esperanças. Podem entrar aqui fatores como alergias, intolerância à lactose e doença celíaca. O melhor passo é referenciar as pacientes para um nutricionista.
A.H.: Não existe uma “dieta para a endometriose” específica, mas muitas pacientes relatam um alívio dos sintomas após alterações na dieta. Na minha clínica, as pacientes colaboram com um nutricionista para ajustar cuidadosamente as suas dietas. No nosso inquérito internacional a 2500 pacientes com endometriose, algumas obtiveram alívio ao deixar de consumir álcool e cafeína, ou alimentos com glúten. No entanto, sem orientação, a restrição alimentar pode ser prejudicial.
O Biocodex Microbiota Institute tem parcerias com diversas organizações profissionais, incluindo sociedades médicas, associações de pacientes e fundações de investigação envolvidas na saúde da mulher. Nesta edição, analisamos o trabalho realizado pela Fundação para a Investigação da Endometriose e conversamos com os seus especialistas que se debruçam sobre a importância da microbiota feminina na investigação e na prática clínica.

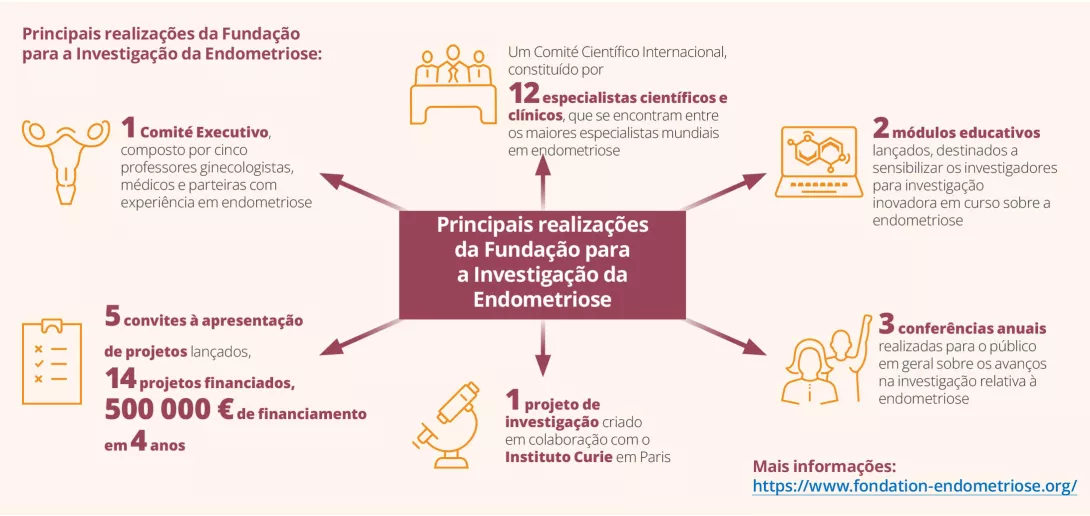
Fundada em França, em 2021, pela Associação ENDOmind sob a égide da Fundação para a Investigação Médica, a Fundação para a Investigação da Endometriose procura acelerar a investigação sobre uma doença que afeta uma em cada 10 mulheres: a endometriose. Todos os anos, a Fundação financia projetos de investigação destinados a compreender a patologia da endometriose, a melhorar o diagnóstico e a desenvolver tratamentos mais eficazes.
Em 2024, o Comité Executivo da Fundação para a Investigação da Endometriose decidiu definir mais claramente as suas prioridades de investigação relativamente à endometriose e maximizar o seu impacto na investigação. Com este objetivo, a Fundação codesenvolveu e cofinanciou uma colaboração inovadora com o Instituto Curie de Paris, que visa comparar os microambientes celulares das lesões da endometriose e do cancro do ovário. Este ambicioso projeto terá início em 2025 e ilustra o desejo da Fundação de incentivar abordagens de investigação interdisciplinares e inovadoras.
Além disso, a Fundação para a Investigação da Endometriose iniciou uma investigação científica multidisciplinar com especialistas europeus relativamente à associação entre a microbiota e a endometriose. A Fundação lançará um convite a manifestações de interesse no final de 2025, com o objetivo de iniciar novos trabalhos de investigação no início de 2026, com apoio financeiro.
Ao concentrar os seus esforços em temas estratégicos, a Fundação para a Investigação da Endometriose cimenta o seu papel na aceleração da investigação e, em última análise, contribui para melhorar a qualidade de vida dos milhões de mulheres afetadas por esta doença ainda pouco conhecida.
Dr. Pedro Vieira Baptista
Hospital Lusíadas Porto, Porto, Portugal; Departamento de Ginecologia-Obstetrícia e Pediatria, Faculdade de Medicina da Universidade do Porto; Faculdade de Medicina e Ciências da Saúde, Universidade de Gante, Gante, Bélgica
O mundo do microbioma vaginal humano é fascinante, apesar da existência do conhecimento limitado sobre o mesmo. A evolução levou a um cenário único, em que a predominância de espécies específicas de lactobacilos constitui o estado ideal durante os anos reprodutivos, apesar das enormes variações entre indivíduos — e mesmo a variação que se verifica na mesma mulher ao longo do tempo. Compreender o microbioma vaginal e o seu potencial é a chave para melhorar a saúde das mulheres em áreas como as infeções sexualmente transmissíveis e as vaginites recorrentes. Além disso, e este ponto é de suma importância, pode ser a resposta a um problema para o qual até ao momento não existem respostas satisfatórias: o parto pré-termo. Neste artigo, abordamos o microbioma vaginal através de uma perspetiva evolutiva, destacando a aparente ausência de um continuum entre espécies. Discutimos o conhecimento atual, mas também nos focamos nas possibilidades futuras.
O início do longo percurso rumo à compreensão do microbioma vaginal pode ser atribuído a Albert Döderlein, no final do século XIX. No seu livro Das Scheidensekret und seine Bedeutung für das Puerperalfieber salientou que as mulheres “normais” e saudáveis têm predominância de bacilos Gram-positivos na vagina, a que chamou Lactobacillus acidophilus.
Este conceito ainda molda as interpretações contemporâneas do microbioma vaginal, mas a realidade é provavelmente muito mais complexa.
A compreensão das vaginites ainda é incompleta e o seu tratamento é na grande maioria dos casos empírico, apesar de ser uma das causas mais comuns para as mulheres procurarem atendimento médico1.
Em 2011, Ravel et al. publicaram um dos artigos mais importantes e que mudou o paradigma em termos de compreensão do microbioma vaginal humano. Nesse artigo, demonstraram que assintomático não é sinónimo de "normal" (o que leva também à questão do que seria um microbioma vaginal "normal" ou, mais precisamente, "ideal") e que existem diferenças significativas entre etnias2.
A diversidade é a regra na natureza, mas a vagina humana parece ser uma exceção: o microbioma vaginal “ideal” aceite consiste na prevalência de uma ou duas espécies de lactobacilos (baixa diversidade alfa). Se pensarmos noutros órgãos ou regiões anatómicas, a predominância de uma espécie é geralmente sinónimo de doença (infeção). Se realizarmos o mesmo exercício considerando qualquer sistema ecológico, tal representa o último passo antes do colapso (ex.: nunca ocorrem monoculturas de plantas na natureza e, quando realizadas artificialmente, devem ser limitadas no tempo). Podemos procurar outras explicações para esta aparente "anormalidade" (ou "exceção") na natureza, mas tal parece levar a um beco sem saída.
Deveríamos, em vez disso, passar a investigar os conjuntos de genes em vez das espécies ou géneros para ultrapassar esta aparente anormalidade biológica?
O objetivo final dos seres vivos parece ser a transmissão dos genes para as gerações seguintes e a evolução parece ser muito impulsionada por este “instinto” primordial. Como tal, podemos facilmente supor que o microbioma vaginal humano deve ser uma parte fulcral do produto final da evolução para otimizar o processo reprodutivo. Se esta premissa estiver correta, podemos esperar:
Surpreendentemente, nenhuma das três premissas é satisfeita. Na natureza, a filogenia não pode ser relacionada com o pH vaginal (um marcador muito indireto da composição do microbioma vaginal), e a predominância dos lactobacilos é exclusiva da espécie humana. Mesmo quando se comparam os seres humanos com outros primatas, as diferenças são enormes e, atualmente, não são facilmente explicáveis3,4. O que é que tornou a vagina humana tão única? Terá sido fruto do acaso ou o corolário evolutivo do ciclo ovárico contínuo, do elevado risco de lacerações e infeções à nascença, ou da agricultura e consequente elevado consumo de amido3?
Uma questão parece não suscitar dúvidas: os lactobacilos são fundamentais para o sucesso da gravidez, mas não é assim tão claro se o mesmo se aplica a conseguir engravidar5.
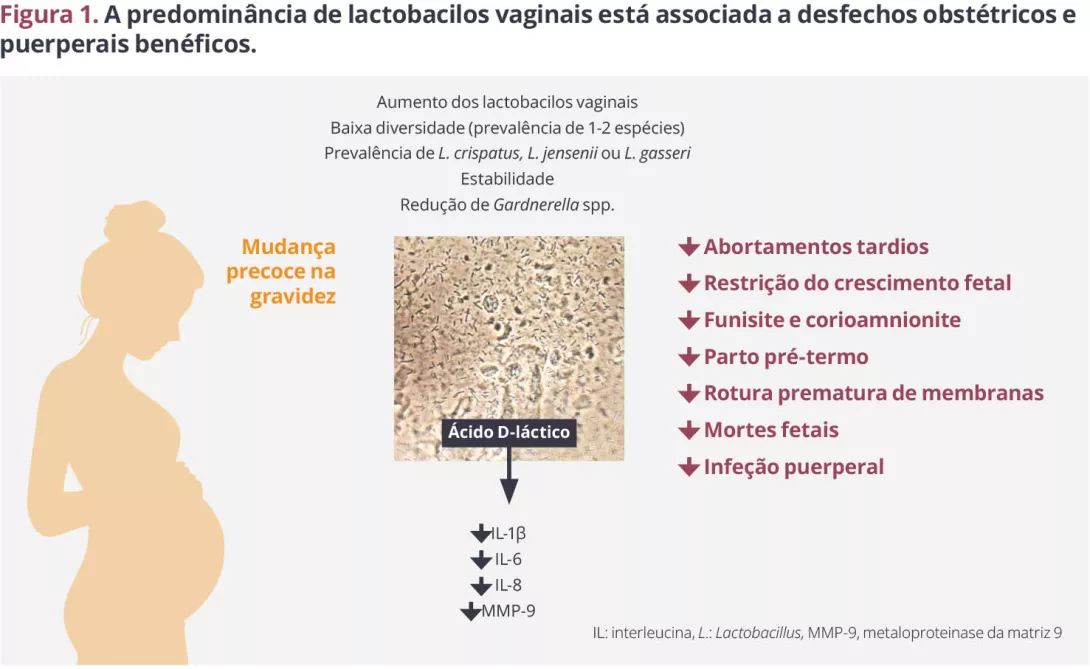
Os dados disponíveis mostram claramente que uma vagina sem predominância de lactobacilos durante a gravidez está associada a desfechos obstétricos e puerperais negativos, incluindo parto pré-termo, rotura prematura de membranas e infeções puerperais (Figura 1). É de salientar que um milhão de bebés morrem todos os anos devido a complicações relacionadas com a prematuridade6.
Temos o hábito de repetir que os lactobacilos têm um papel protetor e que a sua presença é desejável, porém, supor isso significa que temos de ignorar alguns factos óbvios, como o facto de esta predominância não ocorrer em crianças, durante a amamentação, nem em mulheres pós-menopáusicas. Assim, podemos teorizar que a nossa relação simbiótica com os lactobacilos tem um propósito durante a idade reprodutiva. Podemos considerar que este propósito inclui uma redução do risco de infeções sexualmente transmissíveis (IST) (que constituem um risco para o sucesso reprodutivo e para a prole), de infeções genitais ascendentes (e consequentes abortamentos, mortes fetais e partos pré-termo), bem como de complicações puerperais. O papel do microbioma na concretização de uma gravidez parece ser mais limitado. Por exemplo, as populações com elevadas taxas de disbiose vaginal não parecem ser menos férteis7.
Da mesma forma, o impacto do microbioma cervicovaginal no desfecho dos tratamentos de fertilidade também não é claro5.
Uma das maiores diferenças evolutivas entre os seres humanos e os outros mamíferos tem a ver com o parto: o difícil equilíbrio entre nascer com um grande perímetro cefálico e compatibilizar esse perímetro com uma pélvis que teve de se adaptar ao bipedismo. Os humanos têm os partos mais difíceis — talvez só ultrapassados pelos das hienas. Poderá residir aqui a chave para compreender a singularidade do microbioma vaginal humano? Qualquer que tenha sido o propósito evolutivo, para a maioria das mulheres em idade reprodutiva, mesmo não estando grávidas, a predominância de lactobacilos na vagina é desejável. No entanto, a falta de lactobacilos, apesar de representar um estado disbiótico, não é sinónimo de doença.
A nossa compreensão do papel da microbiota vaginal é ainda muito limitada. Mesmo questões aparentemente simples, como a forma como os lactobacilos colonizam a vagina, ainda carecem de uma resposta clara.
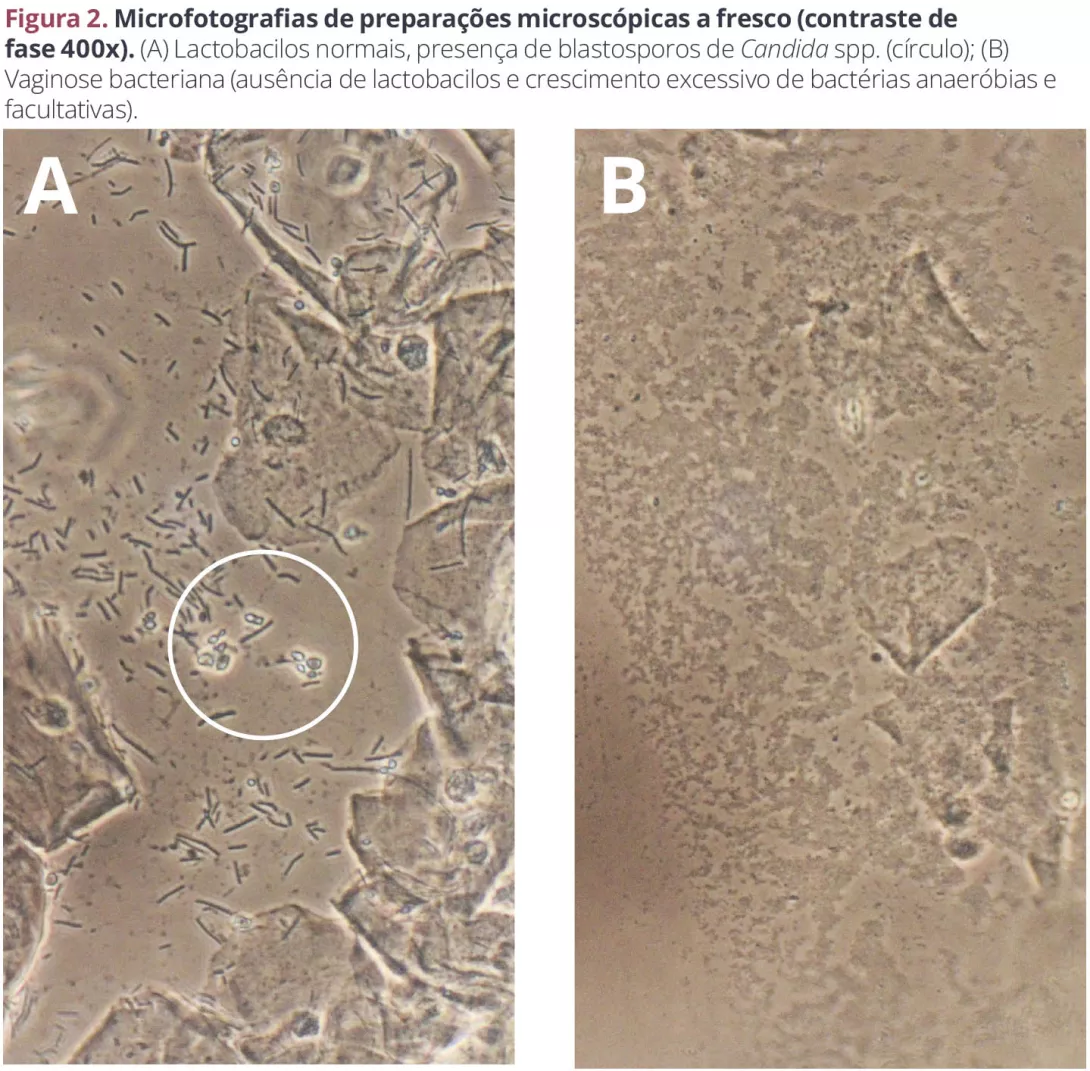
O efeito mais visível de um microbioma alterado é a vaginite. A maioria das mulheres sofrerá pelo menos um episódio de candidíase e, em algumas populações, mais de metade das mulheres em idade reprodutiva têm vaginose bacteriana (VB), assintomática na maioria das vezes (figura 2A e 2B). Temos uma compreensão limitada do que está na origem destas alterações (“normal” — colonização/ estado assintomático — sintomático)8.
O microbioma vaginal pode proporcionar diferentes perfis de risco ou de proteção.
O perfil bacteriano da vagina, independentemente dos sintomas, pode proporcionar diferentes perfis de risco ou de proteção. Em geral, considera-se que os Lactobacillus spp. tendem a proporcionar benefícios para a saúde. No entanto, nem todas as espécies são iguais e apenas um número limitado das espécies existentes é normalmente encontrado em estados de predominância na vagina. O L. iners, com um genoma significativamente menor e um perfil metabólico diferente, está geralmente associado a estados disbióticos ou de transição9.
Pouco se conhece sobre a relação entre Candida spp. e o microbioma vaginal
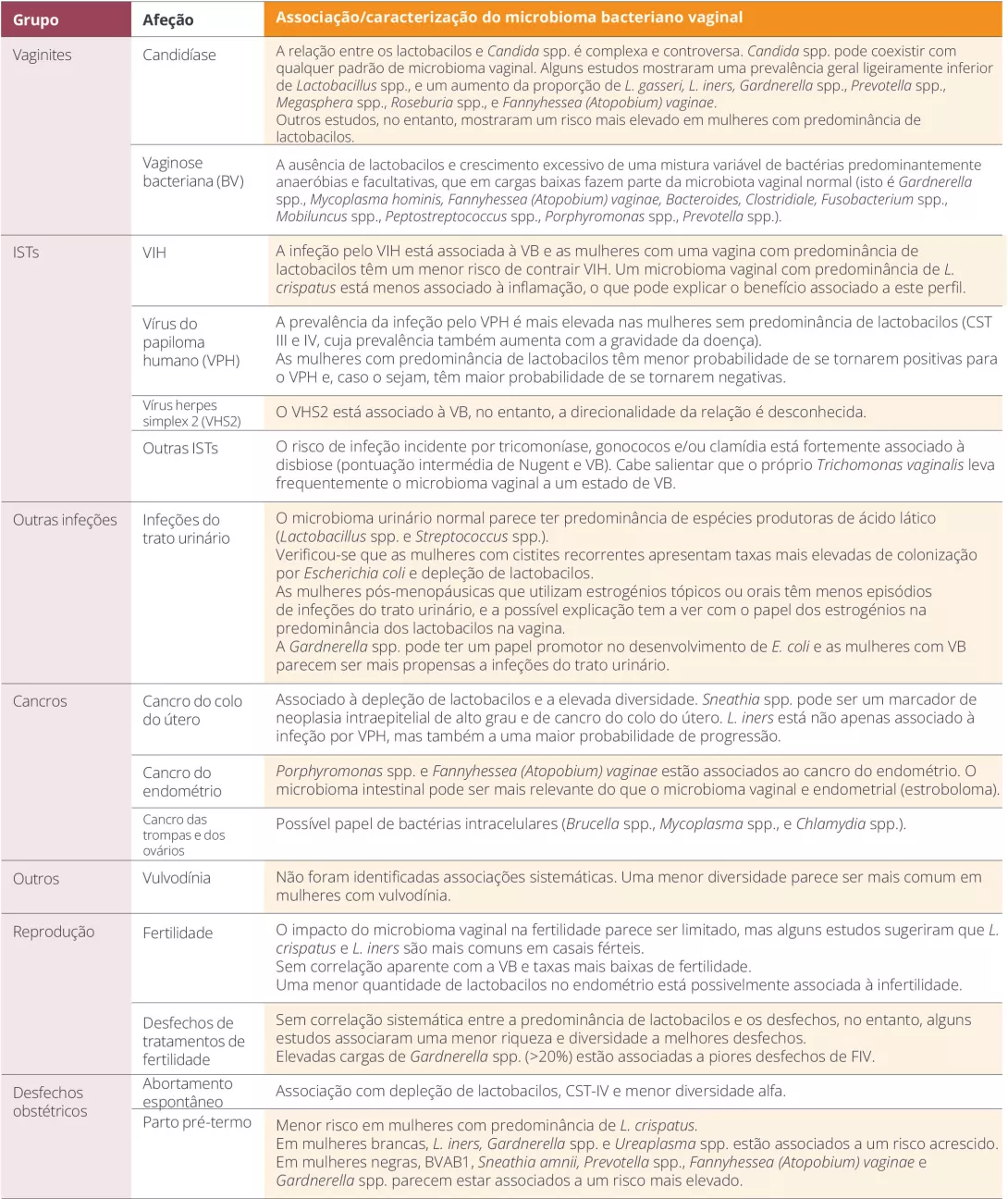
Embora não existam atualmente recomendações para tratar a disbiose assintomática (por exemplo, VB), esta tem sido associada a complicações obstétricas e não obstétricas (incluindo o risco de contrair ISTs [VPH, VIH])8 (Tabela 1).
Quando estiverem disponíveis estratégias eficazes (de preferência sem recurso a antibióticos), poderá ser aconselhável rastrear e tratar a disbiose em mulheres com risco acrescido de ISTs ou mesmo em mulheres infetadas pelo VPH. No entanto, isto pode revelar-se mais complexo do que aparenta. O comportamento semelhante a uma IST que a VB apresenta é reconhecido há já bastante tempo, no entanto, dados recentes confirmamno e sugerem que a redução das recorrências pode necessitar do tratamento dos parceiros, o que poderá constituir um grande obstáculo às estratégias de prevenção10.
BA VB é uma síndrome comum, na qual existe uma depleção de lactobacilos e um crescimento excessivo de várias bactérias anaeróbias estritas e facultativas, associada à formação de um biofilme que parece contribuir para as frequentes recorrências após o tratamento. A composição da VB varia de mulher para mulher, e provavelmente varia até na mesma mulher ao longo do tempo11. Atualmente, é possível diagnosticar a VB através de exames moleculares, mas espera-se que, com o aumento do conhecimento do microbioma vaginal, estes exames permitam traçar o “perfil” da VB, avaliar o resistoma e escolher tratamentos mais adequados8.
A relação entre Candida spp. e o microbioma vaginal é muito complexa e está longe de ser totalmente compreendida. Embora a candidíase possa existir em qualquer microbioma vaginal, tende a ser mais comum com a predominância de lactobacilos (e o consequente pH reduzido)12.
Várias patologias ginecológicas foram associadas a caraterísticas específicas do microbioma e, quase sistematicamente, uma redução dos lactobacilos constitui um risco acrescido de ISTs e cancros ginecológicos (mesmo do trato genital superior). No entanto, nem sempre é fácil estabelecer uma relação causal entre os desvios do microbioma e patologias específicas. Podemos, no entanto, esperar um dia conseguir avaliar ou modular o risco de cancro através da avaliação do microbioma vaginal, especialmente no caso do cancro do colo do útero13.
TO interesse e o conhecimento relativo ao microbioma vulvar são mais recentes e a quantidade de dados é escassa, no entanto, o seu papel em afeções como a vulvodínia, as dermatoses vulvares, a neoplasia intraepitelial vulvar e o cancro está a ser estudado14-16.
Estão a ser dados grandes passos para a compreensão do microbioma vulvovaginal. Até compreendermos totalmente o microbioma, podemos começar por respeitá-lo e ao seu papel funcional, reconhecendo que cada mulher é única (e que esta singularidade é mutável), evitando o uso desnecessário de antibióticos e antissépticos e diagnosticando corretamente as ISTs e as vaginites, em vez de confiarmos no empirismo. Um diagnóstico preciso minimizará tratamentos incorretos, com um potencial impacto a longo prazo.
Nesta fase, é essencial distinguir o que é experimental e o que é clinicamente relevante. Estamos num processo de aprendizagem e de tentativa de utilização de técnicas e conceitos experimentais na prática clínica que, muitas vezes, levam a exames, despesas e tratamentos desnecessários. Por exemplo, a metagenómica é uma ferramenta de investigação muito útil, mas atualmente não tem lugar na avaliação clínica das vaginites.
Nas últimas duas décadas, acumulámos uma enorme quantidade de informação, que em breve se traduzirá em melhores cuidados de saúde para as mulheres, incluindo recomendações dietéticas específicas, bem como em prebióticos e probióticos. É expectável que este conhecimento reduza substancialmente os partos pré-termo e cancros ginecológicos, bem como a recorrência das vaginites e cistites.
Os próximos capítulos serão, sem dúvida, os mais entusiasmantes!
O microbioma vaginal humano ainda não é totalmente compreendido e alguns dos nossos pressupostos atuais poderão ter de ser atualizados ou adaptados à medida surgem novos dados. A sua plena compreensão e o potencial para o manipular poderão ser desvendados quando a aparente ausência de lógica evolutiva for totalmente compreendida.
No entanto, podemos estar certos que os lactobacilos são benéficos para a maioria das mulheres em idade reprodutiva e que são fundamentais para o sucesso da gravidez, independentemente da localização geográfica ou etnia.
O conhecimento crescente nesta área está a levar a progressos no diagnóstico e tratamento das vaginites e, num futuro próximo, permitirá reduzir o risco de problemas graves como ISTs e partos pré-termo.
Por que a constipação de um bebé mantém-se amena enquanto a de outro leva à bronquiolite? Um novo estudo revela que a resposta não se encontra apenas no vírus, mas no ecossistema microbiano do nariz que atua como a primeira linha de defesa do sistema imunológico.
A microbiota pulmonar
Todos os pais conhecem a cascata de eventos: uma tosse simples e o nariz a escorrer podem progredir rapidamente e levar a uma infeção no ouvido, ou pior, a uma bronquiolite. Há muito tempo culpamos os vírus, mas um novo estudo crítico publicado na Nature Communications 1 revela que os vírus são muitas vezes apenas o ato de abertura. O verdadeiro drama se desenrola dentro da (sidenote: Microbiota otorrinolaringológica Comunidade específica de microrganismos (bactérias, fungos, vírus) que residem nas regiões interligadas do ouvido, nariz e garganta. Este ecossistema é distinto da microbiota intestinal e desempenha um papel crucial direto na imunidade local e na saúde respiratória. ) , do seu bebé, a complexa comunidade de bactérias do nariz e da garganta que serve como linha de frente do sistema imunológico. Esta investigação fornece uma nova estrutura para entender a saúde respiratória durante o crucial primeiro ano de vida.
Os investigadores acompanharam 300 bebés desde o nascimento, observando meticulosamente a sua saúde e analisando mais de 2400 amostras nasais. Os dados revelam um mecanismo claro: uma infeção viral, seja de um Rinovírus comum ou do vírus sincicial respiratório (VSR), altera profundamente a paisagem do sistema respiratório
Causa 3,6 milhões de hospitalizações por ano e cerca de 100 000 mortes em crianças com menos de 5 anos. ²
A presença de um vírus mostrou aumentar as chances de (sidenote: Colonização bacteriana É a presença persistente e o crescimento de bactérias em uma superfície do hospedeiro, como os canais nasais, sem causar sinais clínicos de doença. É um pré-requisito necessário porém distinto da infeção, e representa um estado de portador assintomático. ) com o Haemophilus influenzae em 44% e o Streptococcus pneumoniae a um impressionante índice de 83%.
Para lactentes já portadores de S. pneumoniae, uma infeção viral amplificou a sua (sidenote: Densidade de colonização Medida quantitativa da carga bacteriana ou o número de uma bactéria específica presente em uma amostra, em vez de um simples resultado de presença/ausência. A alta densidade de colonização pode aumentar o risco de transição de um patógeno de um colonizador inofensivo para uma infeção ativa. ) em quase quatro vezes, criando um ambiente de alto risco para doenças invasivas.
Esi está a descoberta mais significativa do estudo: o vírus não ajuda apenas as bactérias nocivas, mas sabota também ativamente os micróbios benéficos que as mantêm sob controlo.
A análise identificou espécies protetoras específicas, como a Corynebacterium, que normalmente impedem que os patógenos possam estabelecer-se. Os dados mostraram que uma infeção viral leva a uma perda direta dessas bactérias benéficas. É este esgotamento que abre as portas para a colonização dos patógenos.
Em uma reviravolta contraintuitiva, as mesmas infeções virais foram associadas a uma probabilidade 55% mais baixa de adquirir o Staphylococcus aureus, revelando o quão específicas e complexas são estas interações microbianas.
Este trabalho enfatiza que uma microbiota otorrinolaringológica saudável não é opcional. É sobretudo um componente fundamental da imunidade no início da vida.
Na verdade, a composição da microbiota nasal de uma criança foi um preditor mais preciso da aquisição bacteriana futura do que os fatores de risco clínicos padrão. O desenvolvimento deste ecossistema é moldado pelo
(sidenote:
Expossoma
Foi em 2005, num artigo publicado na revista Cancer Epidemiology, Biomarkers & Prevention, que o Dr. Christopher Wild definiu pela primeira vez o expossoma como “a totalidade das exposições a que um indivíduo está sujeito desde a conceção até à morte. Trata-se de uma representação complexa e dinâmica das exposições a que uma pessoa está sujeita ao longo da vida, integrando os ambientes químico, microbiológico, físico, recreativo, medicinal, o estilo de vida e a alimentação, bem como as infeções”
Fonte
)
, com fatores como a amamentação a desempenhar um papel fundamental na propagação e nutrição de espécies benéficas.
Compreender estas dinâmicas microbianas precoces é essencial, pois estabelecem as bases para a saúde respiratória a longo prazo e podem influenciar o risco futuro de infeções recorrentes e asma.
 Antibióticos durante o primeiro ano de vida aumentam risco de desenvolver doença celíaca
Antibióticos durante o primeiro ano de vida aumentam risco de desenvolver doença celíaca
 Microbiota do bebé: pai, é a tua vez!
Microbiota do bebé: pai, é a tua vez!
A resistência aos antibióticos (RAM) ameaça a eficácia dos cuidados de saúde. É hora de agir: esta página fornece ferramentas concretas para você se equipar e sensibilizar seus pacientes sobre este desafio global.

Os antibióticos revolucionaram a medicina moderna, salvando inúmeras vidas. Mas seu uso repetido ou inadequado perturba profundamente a microbiota intestinal, reduzindo sua diversidade e capacidade de proteção. Essa dupla faceta entre o progresso terapêutico e o desequilíbrio microbiano lembra a necessidade de um uso racional.
70 % dos entrevistados afirmam saber que os antibióticos têm impacto sobre a microbiota
35 % Apenas 1 em cada 3 pessoas foi informada por um profissional de saúde que o uso de antibióticos pode ter consequências negativas para o equilíbrio da sua microbiota.
Desde 2015, a OMS organiza anualmente a Semana Mundial de Conscientização sobre a Resistência aos Antimicrobianos (WAAW), que tem como objetivo aumentar a conscientização sobre o fenômeno global da resistência aos antimicrobianos.
Organizada de 18 a 24 de novembro, esta campanha convida o público em geral, os profissionais de saúde e os decisores políticos a fazerem um uso racional de antibióticos, antivirais, antifúngicos e antiparasitários, a fim de prevenir o aumento da resistência aos antimicrobianos.
A exposição repetida a antibióticos pode desequilibrar profundamente a microbiota, causando disbiose com várias consequências clínicas. Essas alterações na microbiota são hoje reconhecidas como um fator de risco em muitas doenças. Compreendê-las melhor significa reforçar a prevenção e a personalização dos cuidados de saúde.
O uso generalizado e, por vezes, inadequado de antibióticos torna-os cada vez menos eficazes no tratamento de infecções, uma vez que muitas bactérias são agora resistentes aos antibióticos. A vigilância, a investigação e a sensibilização continuam a ser essenciais para controlar este importante problema de saúde.
Esta conferência Microbiotalk tem como objetivo destacar os múltiplos desafios da RAM, explorando as complexas ligações entre a microbiota intestinal, os fatores ambientais e a saúde pública. Com a participação de especialistas internacionais e representantes de pacientes, o evento abordará temas como o impacto dos antibióticos na microbiota intestinal, o surgimento de resistências desde a primeira infância, os reservatórios ambientais de bactérias resistentes e o papel crucial do envolvimento dos pacientes e do público em geral.

Cada iniciativa é importante na luta contra a resistência aos antimicrobianos. Visualizar os dados, compartilhar conhecimentos e fortalecer a colaboração entre profissionais de saúde são alavancas essenciais. A conscientização coletiva está no centro da estratégia global de prevenção.
Confira a primeira colagem que ilustra os desafios da resistência aos antimicrobianos.
Após um tratamento com antibióticos, a microbiota leva tempo para recuperar o equilíbrio. Abordagens baseadas na compreensão das interações entre antibióticos e flora intestinal abrem caminho para novas abordagens de apoio. Esses conhecimentos abrem perspectivas promissoras para a manutenção de uma microbiota saudável e a prevenção de disbiose pós-tratamento.
Como falar sobre saúde intestinal: conselhos do Prof. Sokol. Esta série de vídeos educativos foi concebida para ajudar os profissionais de saúde a comunicarem melhor com os seus pacientes sobre a microbiota intestinal.

Os efeitos da resistência aos antibióticos vão além da esfera clínica: eles também afetam o meio ambiente, a microbiota e a saúde planetária. Esse fenômeno global exige uma abordagem integrada de “saúde única” para agir de forma eficaz. É hora de compreender, prevenir e colaborar.
Confira nossos artigos para explorar todos os impactos da resistência e as soluções previstas em escala global:
 11.01.2024
Quando as viagens criam a resistência aos antibióticos
Mais informação
11.01.2024
Quando as viagens criam a resistência aos antibióticos
Mais informação
 07.09.2023
Genes da resistência aos antibióticos encontrados em grandes quantidades nas nuvens
Mais informação
07.09.2023
Genes da resistência aos antibióticos encontrados em grandes quantidades nas nuvens
Mais informação
 22.02.2022
Os fagos que vêm em socorro das infeções multirresistentes?
Mais informação
22.02.2022
Os fagos que vêm em socorro das infeções multirresistentes?
Mais informação
 10.04.2024
À boleia do intestino: Como as viagens moldam a nossa paisagem interior
Mais informação
10.04.2024
À boleia do intestino: Como as viagens moldam a nossa paisagem interior
Mais informação

