За кулисами инфекционной диареи: роль микробиоты
Инфекционная диарея — это распространенное и часто мучительное состояние, которое может нарушить привычный образ жизни. Ключ к пониманию и преодолению этой проблемы может находиться в нашем собственном организме. Узнайте, как вирусные, паразитарные, бактериальные инфекции, в том числе при диарее путешественников, могут нарушать тонкий баланс кишечной микробиоты, вызывая расстройства пищеварения.
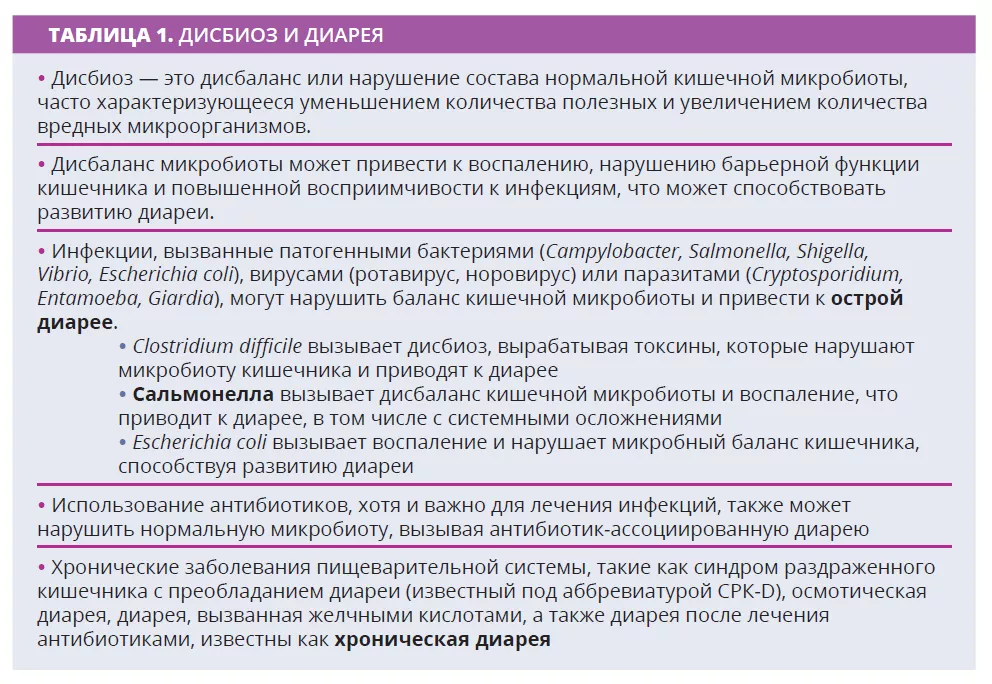
Кишечная микробиота