Что мы уже знаем?
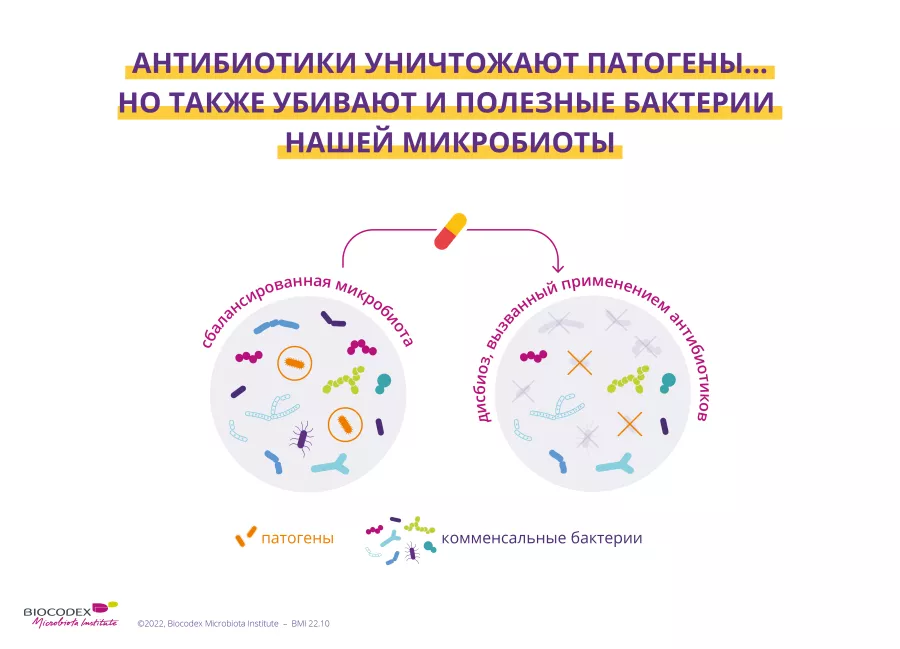
Микробиота кишечника человека образует сложную и сбалансированную экосистему. Нарушения этой экосистемы могут играть роль в развитии инфекций, ожирения, сахарного диабета, а также неврологических и воспалительных заболеваний. Антибиотики добавили от 2 до 10 лет к ожидаемой продолжительности жизни, но воздействие этих препаратов в раннем возрасте связано с неблагоприятными метаболическими, воспалительными и неврологическими эффектами как у животных, так и у человека. Когда микробные сообщества подвергаются воздействию антибиотиков, они не только реагируют, изменяя свой состав, но и эволюционируют, оптимизируя и распространяя гены устойчивости к антибиотикам (гены ABR), в совокупности образующие резистом.[2] Микробиота кишечника человека является резервуаром генов ABR, которые обмениваются между резидентными штаммами, распространяя устойчивость.[3] Появление и распространение антибиотикорезистентных бактерий представляет серьезную угрозу для общественного здравоохранения. Только в нескольких исследованиях изучали влияние конкретных антибиотиков на кишечные экосистемы и связанные с ними резистомы. Показано, что применение антибиотиков вызывает уменьшение разнообразия микробиоты и увеличение носительства генов ABR.[4, 5] Однако влияние комбинации антибиотиков на микробиоту и роль генов ABR в микробной персистенции еще не изучены. В этом исследовании 12 здоровых мужчин в возрасте от 18 до 40 лет получали коктейль из трех антибиотиков последней инстанции (ванкомицин, гентамицин и меропенем). Авторы проанализировали влияние такого «лечения» на микробиоту кишечника путем секвенирования образцов кала, взятых до и в четыре временных точки на протяжении 6-месячного периода после приема антибиотиков.
Каковы основные результаты исследования?
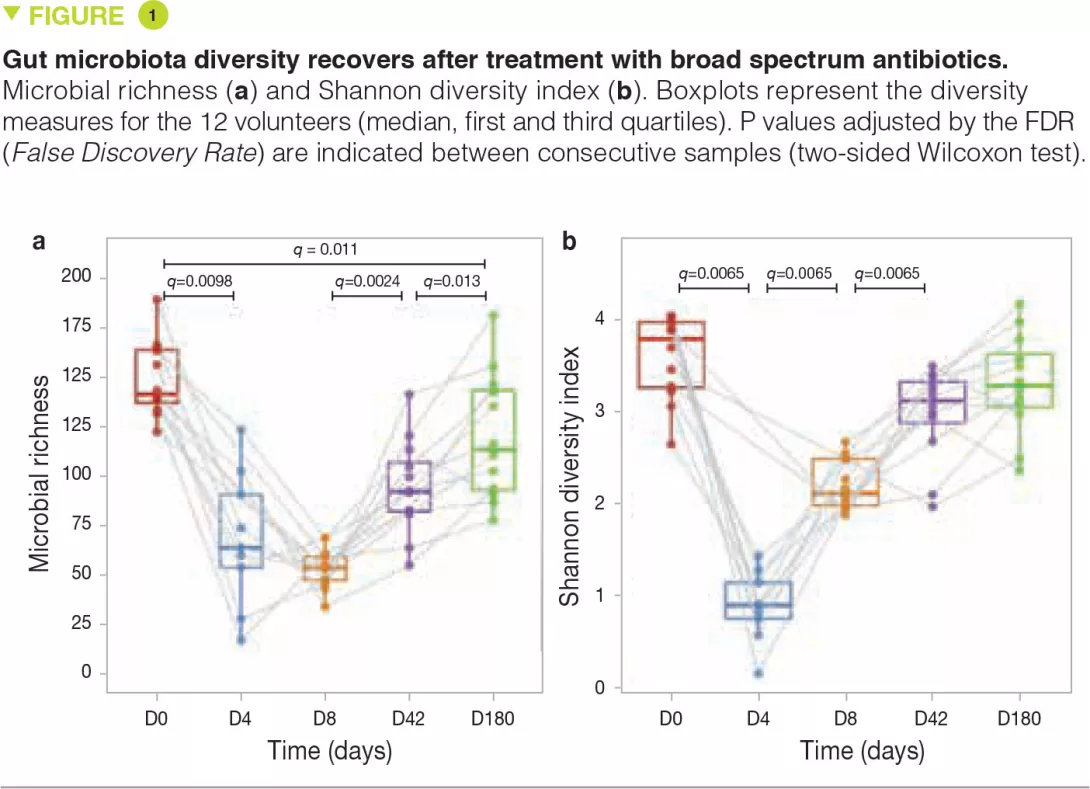
На 4-й день после вмешательства разнообразие и богатство микробиоты заметно снизились по сравнению с исходным уровнем. Однако, несмотря на воздействие антибиотиков очень широкого спектра действия, многие виды все еще обнаруживались на 4-й день (рисунок 1a). На 8-й день разнообразие микробиоты (измеренное по индексу Шеннона) значительно увеличилось, свидетельствуя о начале восстановления сохранившихся микроорганизмов (рисунок 1b). Через 6 месяцев разнообразие микробиоты почти полностью восстановилось до исходного уровня, но это не относилось к богатству, указывая на то, что некоторые штаммы были полностью (или, по крайней мере, в течение длительного времени) уничтожены.
Некоторые ранние изменения включали бурный рост обычно субдоминантных комменсалов, таких как Escherichia coli, Veillonella spp., Klebsiella spp., Enterococcus faecalis и Fusobacterium nucleatum, а также резкое истощение продуцентов бутирата, таких как Faecalibacterium prausnitzii, Roseburia hominis, Anaerostipes hadrus, Coprococcus spp. и Eubacterium spp. Эти сдвиги в составе микробиоты уже не были значимыми на 42-й день.
Затем авторы изучили роль генов ABR в восстановлении микробиоты. В частности, они обнаружили, что метагеномные виды, несущие β-лактамазы, имели значимо более высокие шансы на выживание (ОШ = 1,64 [1,24-2,17]) на 8-й день. Кроме того, метагеномные виды, не выявляемые на исходном уровне, имели лучшие шансы на последующую колонизацию de novo, если несли гены ABR против одного из трех используемых классов антибиотиков.
Что все это значит на практике?
Эти данные показывают, что микробиота кишечника здоровых молодых людей устойчива к 4-дневному курсу антибиотиков широкого спектра действия, однако на восстановление большинства микробных сообществ требуется около 6 месяцев. Восстановление отдельных видов модулируется переносом генов ABR. Необходимы дальнейшие исследования для оценки влияния повторяющейся и/или продолжительной антибиотикотерапии, в том числе у детей с незрелой иммунной системой и микробиотой. Возможно, что повторное использование антибиотиков в течение длительного времени приводит к отбору бактерий, несущих гены ABR, за счет других комменсалов, что может оказывать длительное или постоянное воздействие на микробиоту. В таких случаях может оказаться полезным корректирующее вмешательство с введением экзогенных микроорганизмов. Антибиотики оказывают значимое влияние на кишечную микробиоту, поэтому их следует использовать рационально.
 Анализ характеристик мекония для прогнозирования развития аллергии
Анализ характеристик мекония для прогнозирования развития аллергии
 Микробиота кишечника: защита от пищевой аллергии?
Микробиота кишечника: защита от пищевой аллергии?