Кишечный микробиом и резистентность к противомикробным препаратам
Д-р Джозеф Несме (Joseph Nesme)
Доцент кафедры микробиологии биологического факультета Копенгагенского университета, Дания
Устойчивость к антибиотикам — древний и распространенный феномен. Резистом окружающей среды напоминает большое хранилище генов резистентности, подпитывающее тихую пандемию антибиотикорезистентности. Горизонтальный перенос генов, динамика популяций и совместный отбор ускоряют появление и распространение резистома. К 2050 году более 10 миллионов смертей ежегодно будут вызваны устойчивостью к антибиотикам. В раннем возрасте кишечный микробиом склонен к дисбиозу, что может способствовать увеличению количества и разнообразия кишечного резистома у младенцев. Принятие подхода единого здоровья с учетом взаимосвязи здоровья человека, животных и окружающей среды имеет важное значение для решения сложных проблем, связанных с антибиотикорезистентностью».
Устойчивость к антибиотикам в окружающей среде: давняя проблема
Антибиотикорезистентность (АР) — древний и распространенный феномен, существовавший задолго до начала использования антибиотиков в качестве лекарственных средств. Окружающая среда служит огромным резервуаром генов антибиотикорезистентности, где различные микробные сообщества имеют свои механизмы резистентности. Феномен АР можно обнаружить в различных условиях окружающей среды, включая почву, воду, растений, животных и даже в арктической вечной мерзлоте возрастом 30 000 лет [1, 2]. Экологическая роль молекул антибиотиков и связанной с ними резистентности в природных условиях не до конца изучена, однако неоспорим тот факт, что легкодоступный пул генов существовал еще до начала клинического использования антибиотиков и объясняет быстрое появление патогенов. Нынешний кризис антибиотиков является эволюционным событием, а стратегии его преодоления должны учитывать микробную экологию. Проблема заключается в быстром приобретении резистентности еще недавно чувствительными патогенами, что ведет к неудачам терапии, особенно на фоне очень ограниченного поступления новых противомикробных препаратов на рынок [3].
Механизмы появления и распространения резистома
Резистомом называют весь набор генов, кодирующих связанные с АР белки, или белки, потенциально способные эволюционировать в мощные инструменты АР [4] (рисунок 1). Он включает известные гены АР у патогенных (проблемные) и антибиотикпродуцирующих организмов (например, Streptomyces spp. , производящий стрептомицин), ассоциированные гены резистентности [5], скрытые гены АР (т. е. гены, способные обеспечить резистентность в определенных условиях, например, эффлюксные насосы или порины), предшественники генов АР, кодирующие белки с минимальным уровнем аффинности или резистентности к антибиотическим соединениям.
Примечательно, что большая часть этих генов имеет гомологичные последовательности, что может указывать на их общее эволюционное происхождение.
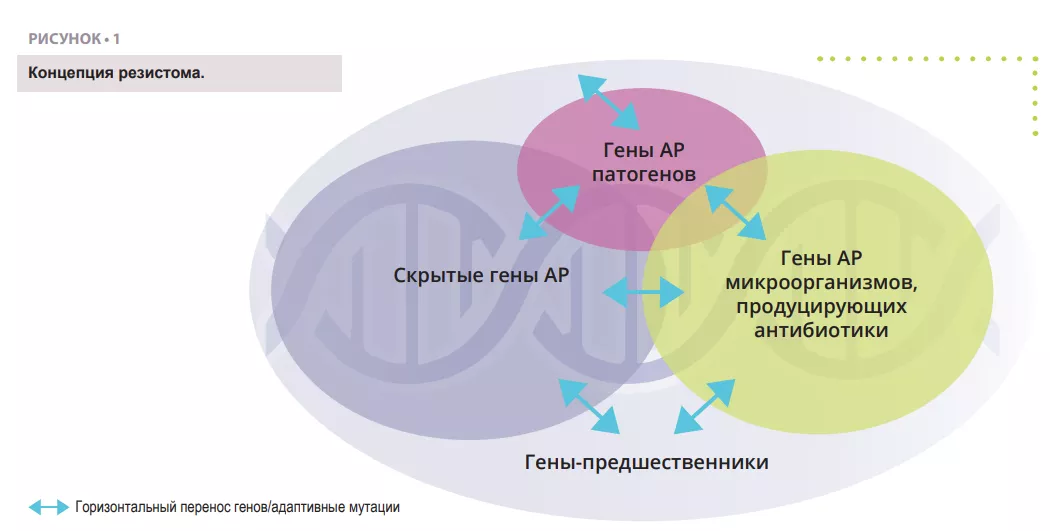
Важно отметить, что понятие резистома не означает «функциональную и клинически значимую АР» . Гены резистома могут переходить между различными состояниями, описанными выше, посредством горизонтального переноса генов (ГПГ) , точечны х мутаций или рекомбинации, которые приводят к появлению новых хозяев или генетического контекста, в котором создаются условия для реализации клинически значимого фенотипа АР. Фото: Shutterstock. Таким образом, гены резистентности сами по себе не являются проблемой, поскольку зависят от хозяин а и генетического контекста, однако все гены резистома представляют потенциальную угрозу и риски для здоровья населения. Обнаружение гена резистентности к клинически значимой молекуле в мобильном элементе патогена человека является серьезным риском, однако наличие того же гена или его близких гомологов, не связанных с мобильными генетическими элементами, у непатогенной почвенной бактерии ассоциируется с очень низким риском АР. Поэтому определение степени риска АР в исследованиях резистома имеет первостепенное значение.
Горизонтальный перенос генов (ГПГ) является важнейшим механизмом быстрого распространения генов АР среди бактерий, даже не родственных друг другу. Например, Bacteroides spp., преобладающая в кишечной микробиоте человека, обладает геном устойчивости к макролидам ermB, иде нтичным обнаруженным в нескольких изолятах Clostridium perfringens, Streptococcus pneumoniae и Enterococcus faecalis из различных географических регионов, что указывает на генетическую связь между Bacteroides и некоторыми грамположительными бактериями, которые не распространены в кишечнике человека [6]. Генетические элементы, такие как плазмиды, облегчают передачу генов резистентности между различными видами микроорганизмов [7].
ГПГ позволяет распространять гены в различных средах и популяциях бактерий, способствуя обще й распространенности и разнообразию АР.
Совместный отбор является еще одним значимым фактором распространения АР. Использование неантибиотических соединений, таких как тяжелые металлы и биоциды, помогает отбору генов АР благодаря избирательному давлению на микробные популяции, совместному приобретению резистентности (появление различных факторо в резистентности в одном генетическом элементе) или перекрестной резистентности (появление общего фактора устойчивости к антибиотикам и металлам) [8]. Воздействие природных антимикробных соединений, например, продуцируемых конкурирующими микроорганизмами, или любыхко-селективных молекул может стимулировать отбор резистентных штаммов [9]. Присутствие в окружающей среде антибиотиков, как природных, так ипроизводимых человеком, также способствует селективному давлению на резистентность. Кроме того, использование антибиотиков в сельском хозяйстве и ветеринарной практике может привести к попаданию их в окружающую среду, способствуя появлению и распространению генов АР [10].
Понимание барьеров и тенденций передачи генетических векторов, несущих гены резистентности, имеет решающее значение для разработки эко-эволюционных стратегий, направленных на ограничение распространения АР в клинических условиях в целом и у детей - в частности.
Дисбиоз и кишечный резистом у младенцев: тонкий баланс
Разнообразие экологического резервуара генов АР и возможности их передачи представляют угрозу для кишечного микробиома человека враннем возрасте. Такие стратегии, как улучшение очистки сточных вод, ответственное использование антибиотиков в сельском хозяйстве и ветеринарии, а также снижение загрязнения окружающей среды антибиотиками и антибиотикорезистентными бактериями могут помочь в борьбе с распространением АР [11]. Кроме того, наблюдение за экологическими резервуарами может дать ценную информацию овозникновении и сохранении АР, а также послужить основой для мероприятий в области общественного здравоохранения.
Принятие подхода «Единого здоровья», с учетом взаимосвязи здоровья человека, животных и окружающей среды, имеет важное значение для решения сложных проблем, связанных с антибиотикорезистентностью
После рождения наш кишечник быстро колонизируется микроорганизмами, полученными от матери и из окружающей среды. Именно в первые годы жизни изменения микробиома — более резкие и медленнее восстанавливаются по сравнению с более стабильным микробиомом кишечника здорового взрослого человека. Поэто м у новорожденные и младенцы более подвержены нарушениям со стороны микробных сообществ, известным как дисбиоз. В течение этого периода многие факторы могут влиять, в том ч и с л е н егативно, насозревани е кишечника, что потенциально может иметь долгосрочные последствия для здоровья [12]. Исследования на мышах показали, что в этом критическом периоде развития, не столько прямое воздействие молекул антибиотиков, сколько изменение состава кишечной микробиоты вызывает неблагоприятные метаболические последствия, например, ожирение [13].
Обнаружение резистома в кишечнике младенцев: результаты крупного когортного исследования
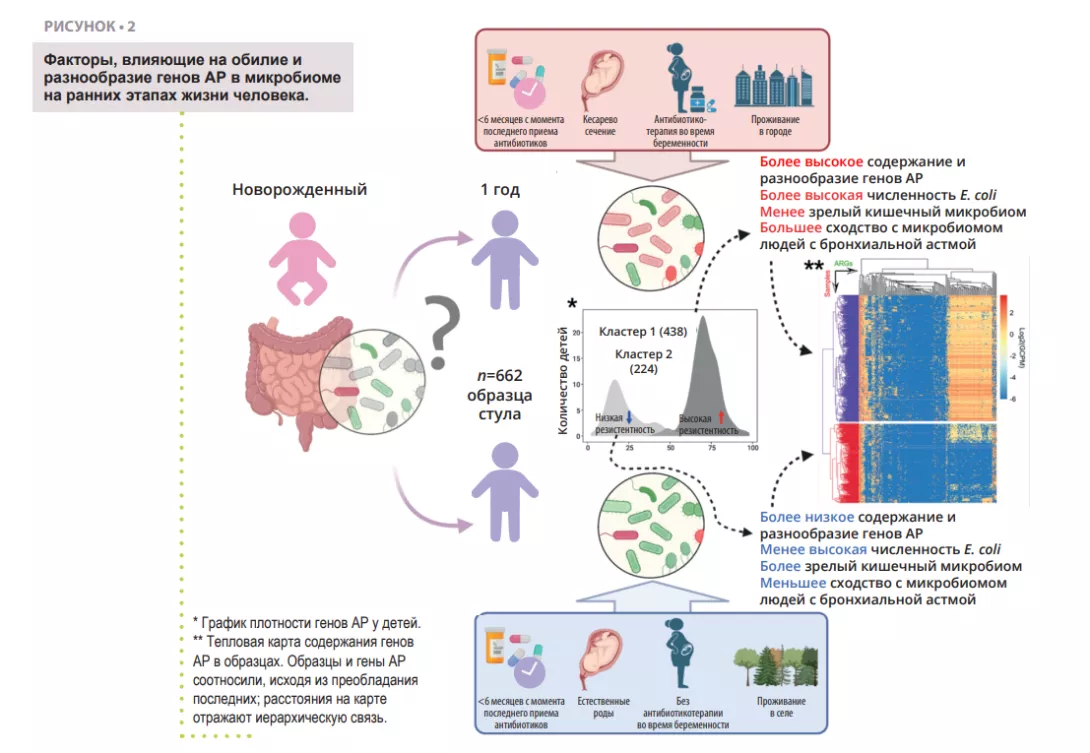
В то время как АР является проблемой в любом возрасте, созревание кишечного микробиома в раннем возрасте представляет собой окно возможностей для уменьшения резервуара генов АР в кишечнике. Поэтому важно выявить различные факторы, увеличивающие или уменьшающие количество генов А Р ,которые могут передаваться инфекционным патогенам и приводить к неэффективности антибиотикотерапии на протяжении всей жизни. Изучение резистома кишечника у человека основано на целостном подходе, учитывающем присутствие видов и функциональный потенциал их геномов, включая резистом. Ученые выделяют ДНК из окружающей среды косвенным путем (например, из фекалий), а затем используют метод неизбирательного в ы с о к о п р о и з в о д и т е л ь н о г о секвенирования (метод дробовика). Примерно 80% видов бактерий кишечника человека, обнаруженных с помощью молекулярных инструментов, не поддаются культивированию, особенно облигатные анаэробы. Вероятно, многие микробы организованы в многовидовые сообщества с общими метаболическими путями, что делает выделение чистого штамма трудным или невозможным. Однако с помощью вычислительных методовможно реконструировать квазиполные геномы из метагеномов и связать определенные гены с конкретными видами или даже штаммами бактерий. В недавнем исследовании ученые проанализировали образцы кала 662 детей, за которыми наблюдали от рождения до 7 лет [14]. Цель исследования заключалась в оценке резистома в возрасте 1 года и выявлении перинатальных и экологических факторов, ассоциированных с качественными и количественными характеристиками генов АР. С помощью секвенирования методом дробовика авторы изучили образцы, полученные у 662 детей в возрасте 1 года, для выявления генов АР и соответствующих бактериальных таксонов (рисунок 2). Используя большой набор данных, удалось проследить геномно-метагеномные ассоциации (MAG) и таксономически соотнести геномы конкретных микроорганизмов с генами АР.
Первой находкой оказалось то, что все дети имели минимум один ген множественной лекарственной устойчивости в своем кишечнике. Это значит, что даже при отсутствии лечения антибиотиками в организме человека существует резидентный резистом, ассоциированный с кишечным микробиомом. Далее оказалось, что большая часть генов множественной лекарственной устойчивости кодирует эффлюксные насосы. Эти белки являются нормальным компонентом каждой бактериальной клетки. Некоторые из них могут вызывать АР и сильно подвержены перекрестному отбору, например, в условиях воздействия тяжелых металлов или биоцидов, что потенциально объясняет их высокое содержание в кишечнике и в окружающей среде [8, 15]. Другим неожиданным результатом было четкое разделение когорты участников на две группы по профилю резистома. Первая группа характеризовалась более высоким разнообразием генов АР и относительным преобладанием Escherichiacoli в качестве основного переносчика генов АР (рисунок 2). Это согласуется с предыдущими наблюдениями, что Enterobacteriaceae преобладают в раннем возрасте, но затем их популяция быстро уменьшается по мере роста колонизации кишечника представителями Bacteroidetes. Задержка этих процессов у некоторых детей может быть связана с рядом факторов, таких как применение антибиотиков, способ родоразрешения, условия проживания (город или село). В результате происходит задержка сокращения популяции Escherichia coli и увеличение резистома в возрасте 1 года. Это подтверждается наблюдением, что более высокое содержание генов АР связано с более низкими показателями зрелости кишечного микробиома с точки зрения соотношений отдельных таксонов в том или ином возрасте [16].
Лечение антибиотиками во время беременности и на первом году жизни, конечно, оказывало значительное влияние на объем кишечного резистома у младенцев. Удалось проследить четкую тенденцию между временем (более или менее 6 месяцев) с момента получения последнего курса антибиотиков и обилием генов АР в кишечнике у детей.
Это указывает на некоторую пластичность микробиома в раннем возрасте, который потенциально может быть улучшен с помощью целенаправленного вмешательства, например, с помощью про- или пребиотиков. Эта гипотеза еще нуждается в проверке. Однако в когортном масштабе наибольшие различия в распространенности генов АР касались антибиотиков, никогда не назначавшихся детям, т. е. увеличение резистома кишечника зависит от перинатальных и экологических факторов, помимо антибиотикотерапии. Еще одно наблюдение, касающееся связей между окружающей средой и резистомом, в том числе кишечника, заключалось в том, что дети из городских районов имели значительно больше генов АР, чем их сельские сверстники. Существует множество потенциальных искажающих факторов, которые могут объяснить этот факт, однако нельзя спорить с тем, что окружающая среда вносит большой вклад в развитие микробиома на ранних этапах жизни.
Можно предположить, что городская жизнь связана с меньшим контактом с внешним миром и уменьшением разнообразия микробиома, или что тип жилья (частный дом или квартира) влияет на его внутренний микробиом (как видно на примере постельной пыли).
Заключение
Устойчивость к антибиотикам — древний и распространенный феномен. Резистом окружающей среды напоминает большое хранилище потенциальных генов резистентности. Такие механизмы, как горизонтальный перенос генов, сложная динамика популяции и совместный отбор значительно ускоряют эволюцию и распространение резистома, переводя ранее чувствительные патогены в разряд антибиотикорезистентных. Кишечный микробиом человека в ранней фазе своего развития подвержен дисбиозу и потенциальной инвазии, селекции и совместному отбору бактерий, несущих гены резистентности, что может иметь долгосрочные последствия для здоровья. Предсказать их связь с будущими неудачами антибиотикотерапии заранее невозможно. Чтобы подробно изучить динамику развития кишечного микробиома и наиболее вероятные пути горизонтального переноса генов АР необходимы долгосрочные мультиомные исследования с высокой частотой взятия и анализа образцов. Ожидается, что на основе полученных данных удастся разработать стратегии профилактики образования генов АР уже в раннем возрасте и ограничить их передачу возможным патогенам. Это позволит уменьшить бремя резистентности к противомикробным препаратам и улучшить здоровье людей во всем мире, благодаря сохранению эффективности некоторых антибиотиков, доступных для борьбы с инфекционными заболеваниями.
1. Nesme J, Cécillon S, Delmont TO, et al. Large-scale metagenomic-based study of antibiotic resistance in the environment. Curr Biol 2014; 24: 1096-100.
2. D’Costa VM, King CE, Kalan L, et al. Antibiotic resistance is ancient. Nature 2011; 477: 457-61.
3. Renwick MJ, Brogan DM, Mossialos E. A systematic review and critical assessment of incentive strategies for discovery and development of novel antibiotics. J Antibiot 2016; 69: 73-88.
4. Wright GD. The antibiotic resistome: the nexus of chemical and genetic diversity. Nat Rev Microbiol 2007; 5: 175-86.
5. Benveniste R, Davies J. Aminoglycoside antibiotic-inactivating enzymes in actinomycetes similar to those present in clinical isolates of antibiotic-resistant bacteria. Proc Natl Acad Sci USA 1973; 70: 2276-80.
6. Shoemaker NB, Vlamakis H, Hayes K, et al. Evidence for extensive resistance gene transfer among Bacteroides spp. and among Bacteroides and other genera in the human colon. Appl Environ Microbiol 2001; 67: 561-8.
7. Martínez JL, Coque TM, Baquero F. Prioritizing risks of antibiotic resistance genes in all metagenomes. Nat Rev Microbiol 2015; 13: 396.
8. Baker-Austin C, Wright MS, Stepanauskas R. Co-selection of antibiotic and metal resistance. Trends Microbiol 2006; 14: 176-82.
9. Wencewicz TA. Crossroads of Antibiotic Resistance and Biosynthesis. J Mol Biol 2019; 431: 3370-99.
10. Knapp CW, Dolfing J, Ehlert PA, et al. Evidence of increasing antibiotic resistance gene abundances in archived soils since 1940. Environ Sci Technol 2010; 44: 580-7.
11. Wolters B, Hauschild K, Blau K, et al. Biosolids for safe land application: does wastewater treatment plant size matters when considering antibiotics, pollutants, microbiome, mobile genetic elements and associated resistance genes? Environ Microbiol 2022; 24: 1573-89.
12. Dogra S, Sakwinska O, Soh SE, et al. Rate of establishing the gut microbiota in infancy has consequences for future health. Gut Microbes 2015; 6: 321-5.
13. Cox LM, Yamanishi S, Sohn J, et al. Altering the intestinal microbiota during a critical developmental window has lasting metabolic consequences. Cell 2014; 158: 705-21.
14. Li X, Stokholm J, Brejnrod A, et al. The infant gut resistome associates with E. coli, environmental exposures, gut microbiome maturity, and asthma-associated bacterial composition. Cell Host Microbe 2021; 29: 975-87.e4.
15. Mulder I, Siemens J, Sentek V, et al. Quaternary ammonium compounds in soil: implications for antibiotic resistance development. Rev Environ Sci Bio/Technology 2018; 17: 159-85.
16. Subramanian S, Huq S, Yatsunenko T, et al. Persistent gut microbiota immaturity in malnourished Bangladeshi children. Nature 2014; 510: 417-21.