Кишечный микробиом как отражение здорового питания
Анисса М. Армет (Anissa M. Armet) 1 , Жоао Ф. Мота (João F. Mota) 2 ,3 и Йенс Уолтер (Jens Walter) 3
1 Департамент сельского хозяйства, продовольствия и питания, Университет Альберты, Эдмонтон, Альберта, Канада
2 Факультет питания, Федеральный университет Гояс, Гояния, Гояс, Бразилия
3 APC Microbiome Ireland, Школа микробиологии, медицинский факультет и Институт микробиома APC, Университетский колледж Корк — Национальный университет Ирландии, Корк, Ирландия

Хронические неинфекционные заболевания (НИЗ) достигли масштабов эпидемии в промышленно развитых странах, что явно связано с изменениями в рационе питания по западному типу. НИЗ связаны и с кишечным микробиомом, а исследования на животных моделях показали наличие прямой связи между питанием и микробиомом при развитии некоторых заболеваний, а также лежащих в их основе механизмов. Авторы статьи рассуждают о здоровом питании с точки зрения науки о микробиоме, утверждая, что понимание механизмов взаимодействий между питанием и микробиотой может разрешить некоторые противоречия в области диетологии и помочь в разработке более здоровых диет.
Все больше данных указывает на то, что кишечный микробиом влияет на здоровье человека. Питание занимает центральное место в этих отношениях. Известно, что западный тип диеты сыграл важную роль в недавнем всплеске хронических неинфекционных заболеваний (НИЗ) в социоэкономически развитых обществах. Мы расскажем, что представляет собой здоровое питание с точки зрения науки о микробиоме, и используем эти данные для разрешения текущих противоречий в области диетологии и разработки стратегий питания, ориентированных на микробиом. Эта статья посвящена общим диетическим рекомендациям с целью профилактики заболеваний, но не рассчитана на пациентов с заболеваниями, которым необходимы особые рекомендации по питанию и которым следует проконсультироваться с квалифицированным врачом-диетологом.
Здоровое питание с точки зрения микробиома
Цельные продукты против обработанных продуктов
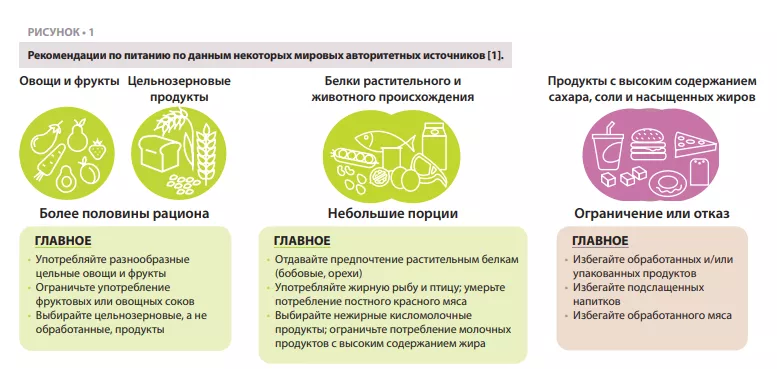
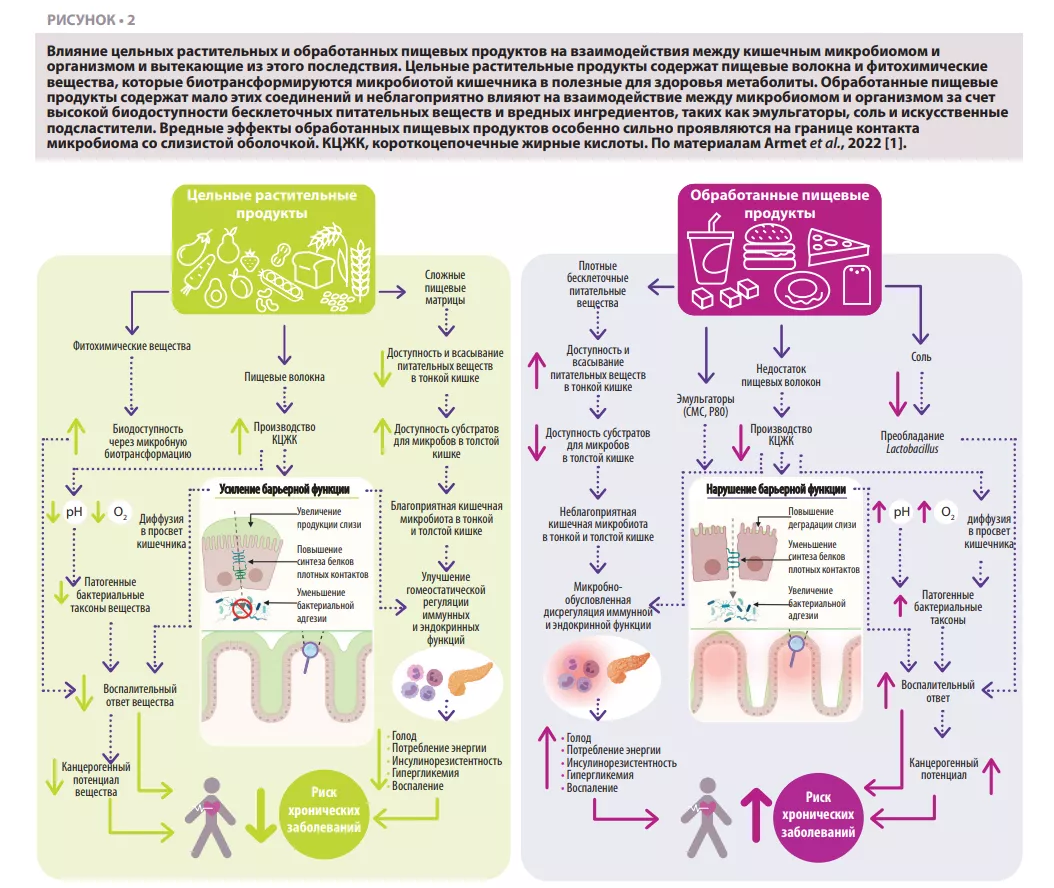
Согласно большинству рекомендаций по питанию [1], в ежедневном рационе должны доминировать цельные растительные продукты (овощи, фрукты, цельные зерна, бобовые и орехи), которые подверглись ограниченной обработке (рисунок 1). Эту рекомендацию хорошо подкрепляют наши знания о микробиоме (рисунок 2 и рисунок 3). Цельные растительные продукты — единственный естественный источник пищевых волокон, часть из которых являются ферментируемыми и обеспечивают рост микробов. Разнообразная растительная пища поддерживает разнообразие микробиома, а ферментация волокон приводит к образованию метаболитов, таких как короткоцепочечные жирные кислоты (КЦЖК), оказывающих широкий спектр метаболических (влияние на чувство насыщения и чувствительность к инсулину), физиологических (увеличение продукции слизи и экспрессия белков плотных контактов) и экологических (ингибирование роста патогенов) эффектов [2]. Кроме того, предоставление субстратов для роста бактерий предотвращает разрушение слизи, воспаление и возникновение инфекций у мышей [3]. Фитохимические вещества, присутствующие в цельных растительных продуктах, большая часть которых не всасывается в тонкой кишке, также подвергаются биотрансформации кишечной микробиотой, что повышает их биодоступность, всасываемость, антиоксидантное и иммуномодулирующее действие [4]. Однако, на данный момент значение этих взаимодействий для здоровья не полностью известно. Наконец, функциональные характеристики и питательные качества (например, состав и доступность) большинства цельных растительных продуктов значительно превосходят обработанные пищевые продукты, которые часто содержат пищевые добавки, ухудшающие состав микробиома и барьерную функцию кишечника (рисунок 2).
Цельнозерновые продукты
Внимание ученых все больше привлекает потенциальная роль кишечного микробиома в реализации хорошо известных положительных метаболических и иммунологических эффектов цельнозерновых продуктов. Например, отруби содержат пищевые волокна, такие как арабиноксиланы и β-глюканы, которые микробиота кишечника ферментирует в полезные метаболиты. Противовоспалительное действие цельных зерен связано со стимуляцией роста популяции продуцентов КЦЖК [5]. В эксперименте у безми кробных мышей, кишечник которых колонизировали фекальной микробиотой с Prevotella пациентов, употреблявших цельнозерновой ячменный хлеб, наблюдалось улучшение толерантности к глюкозе, отражающее подобный эффект у человека [6]. Кроме того, у пациентов с избыточной массой тела, в чьей микробиоте на исходном уровне содержалась Prevotella, наблюдалась ускоренная динамика снижения веса на диете, богатой цельнозерновыми продуктами [7]. Эти исследования показывают, что, как минимум, некоторые метаболические преимущества цельнозерновых продуктов опосредуются кишечным микробиомом (рисунок 3).

Источники белка
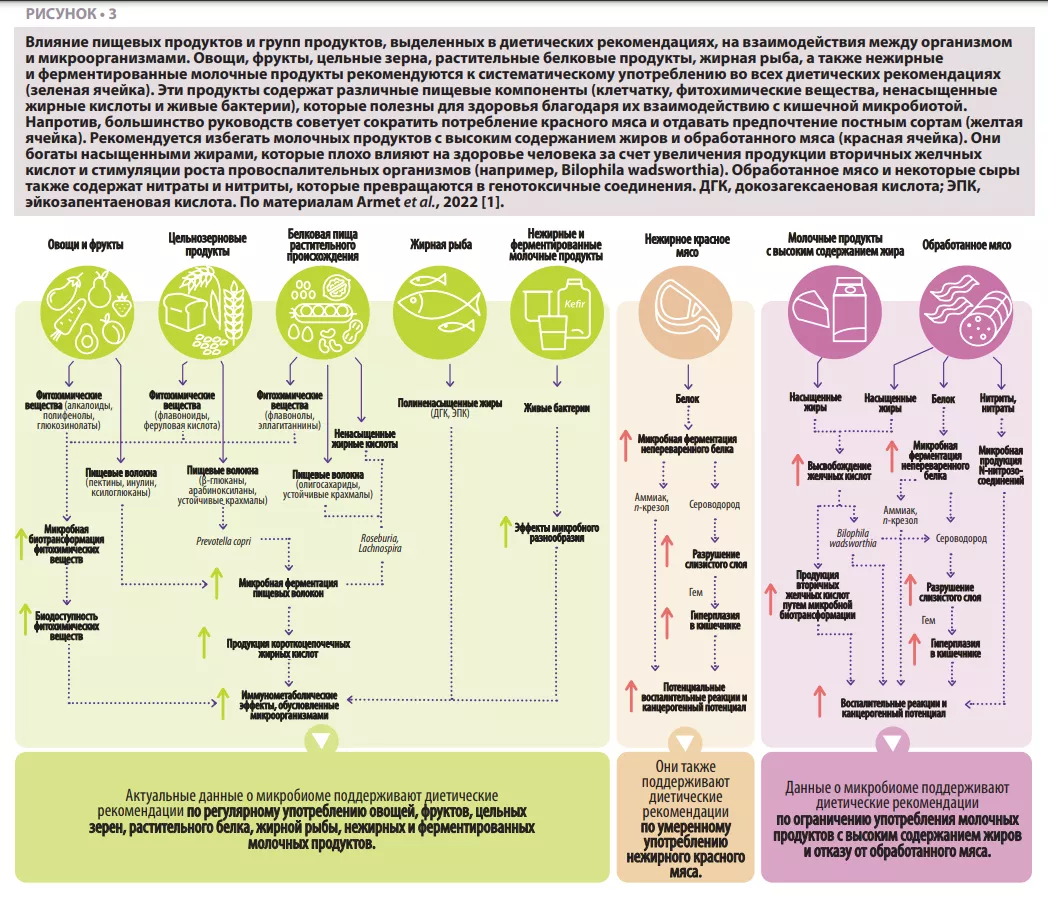
В большинстве рекомендаций по питанию советуют отдавать большее предпочтение растительным белкам (бобовые, орехи), рыбе (жирная рыба) и птице, чем другим источникам белка животного происхождения, в частности красному мясу (рисунок 1). Бобовые и орехи богаты клетчаткой, содержат фитохимические вещества и омега-3 жирные кислоты, которые влияют на взаимодействие между организмом и микроорганизмами (рисунок 3). Ежедневное употребление грецких орехов и миндаля увеличивает относительное преобладание продуцентов бутирата, в частности Roseburia [8]. Употребление бобов мунг снижало скорость набора массы тела и накопления жира у мышей на рационе с высоким содержанием жиров. Этого не наблюдалось у безмикробных мышей на том же рационе, что указывает на роль микробиома [9]. Среди всех белковых продуктов животного происхождения жирная рыба, вероятно, обладает наибольшими иммунологическими и метаболическими преимуществами, связанными с микробиомом [1].
Особенности питания
Осознание, что на здоровье в первую очередь влияют не отдельные продукты или питательные вещества, а их взаимосвязь и синергетический эффект, привело к тому, что в ряде недавно обновленных рекомендаций по питанию (например, «Рекомендации по питанию для американцев на 2020-2025 гг.» и «Руководство по питанию для Канады»), особое внимание было уделено особенностям питания. Средиземноморская диета объединяет многие группы продуктов, положительно влияющих на взаимодействие организма и населяющих его микробов. Для изучения этих взаимодействий было проведено несколько рандомизированных контролируемых исследований, которые показали, что метаболические, иммунологические и когнитивные преимущества средиземноморской диеты связаны с увеличением преобладания Faecalibacterium prausnitzii и Roseburia [10].
Кишечный микробиом в центре споров о здоровом питании
Красное и обработанное мясо
Большинство рекомендаций по питанию и несколько медицинских обществ рекомендуют сократить потребление красного мяса и не употреблять обработанное, хотя в серии систематических обзоров за 2019 год был сделан вывод о наличии лишь слабых доказательств их связи с негативными последствиями для здоровья [11].
Кишечный микробиом обеспечивает полезную перспективу в этом споре. Протеолитическая ферментация мясного белка кишечными микробами увеличивает количество токсичных метаболитов, таких как аммиак, п-крезол и сероводород [12]. За счет высокого содержания насыщенных жиров, обработанное мясо дополнительно стимулирует секрецию желчных кислот в тонкую кишку, которые затем трансформируются микробами во вторичные желчные кислоты. Кроме того, отверждающие агенты, нитраты и нитриты, содержащиеся в обработанном мясе, биотрансформируются микробами в N-нитрозосоединения. Таким образом, текущие рекомендации по питанию основаны также на токсикологических соображениях (рисунок 3).
Метаболиты, образующиеся в результате ферментации белка (например, сероводород, аммиак), имеют более низкую токсичность и в настоящее время не рассматриваются как канцерогены для человека, что подтверждается данными о том, что умеренное потребление постного красного мяса ассоциируется с ограниченным риском. Напротив, N-нитрозосоединения и вторичные желчные кислоты, образующиеся в результате потребления обработанного мяса, являются канцерогенами, поэтому рекомендации советуют избегать или сводить к минимуму его потребление.

Рекомендации по здоровому питанию, ориентированные на микробиом
- Следуйте рекомендациям по питанию (рисунок 1).
- Максимально увеличьте разнообразие потребляемых растительных продуктов, старайтесь употреблять клетчатку выше рекомендуемого в настоящее время уровня (25-38 г/сут).
- Минимизируйте потребление обработанных пищевых продуктов с высоким содержанием сахара, соли, насыщенных и трансжиров, а также обработанного мяса и молочных продуктов с высоким содержанием жира.
- Включите в рацион ферментированные продукты с живыми микробами (без термической обработки) с низким содержанием сахара, жира и соли (йогурт, ферментированные овощи, кефир и чайный гриб).
Молочные продукты
Большинство диетических рекомендаций советуют употреблять обезжиренные или нежирные (0-2%) молочные продукты и избегать молочных продуктов с высоким содержанием жира (>25%) (например, некоторые сыры, продукты на основе сливок, масло). Однако, нет единого мнения о молочных продуктах с естественным содержанием жира (~3,5%). Хотя вред от них сомнителен, их не советуют употреблять в некоторых диетических рекомендациях. В контексте этого обсуждения нельзя не упомянуть взаимодействия между молочным жиром и кишечным микробиомом. Насыщенные жиры молока индуцируют рост провоспалительной бактерии Bilophila wadsworthia, которая вызывает в мышиной модели такие заболевания, как колит [13]. Эти механистические данные согласуются с диетическими рекомендациями употреблять нежирные молочные продукты (рисунок 3).
Низкоуглеводная диета
Низкоуглеводные диеты популярны, так как позволяют за короткое время добиться заметного снижения массы тела и улучшения метаболизма, хотя их результаты могут быть неустойчивыми в долгосрочной перспективе. Эти диеты богаты жирами и/или белками и часто содержат мало клетчатки. Следовательно, они способствуют формированию неблагоприятного метаболического профиля (увеличение концентрации N-нитрозосоединений, снижение уровней бутирата и противовоспалительных фенольных соединений) [14]. Из-за воздействия на микробиоту кишечника, низкоуглеводные диеты могут быть вредными для здоровья, если придерживаться их длительное время.

Путь к здоровому питанию лежит через микробиом
Хотя международные рекомендации по питанию в высшей степени последовательны в плане того, что собой представляет здоровое питание, существуют возможности для улучшений и инноваций за счет смещения акцентов на микробиом.
Эволюционные соображения и восстановление микробиома
Симбиоз человека и микробиома развивался на протяжении миллионов лет при совершенно других окружающей среде и питании. Индустриализация, сместившая на первый план НИЗ, также привела к снижению разнообразия микробиомов, уменьшению их способности к утилиза ции углеводов, обогащению организмами и ферментами, разлагающими слизь, потере микробных симбионтов. Поэтому существует эволюционный аргумент в пользу увеличения потребления клетчатки сверх рекомендуемых ежедневных 25-38 г, что также подтверждают данные наблюдательных и интервенционных исследований [15]. Помимо увеличения потребления клетчатки в составе цельных продуктов научно обосновано снижение влияния факторов индустриализации на кишечный микробиом с помощью пребиотических, пробиотических и синбиотических стратегий. Продукты, потенциально способные восстановить и разнообразить микробиом, уже есть на рынке, однако исследования их клинической пользы только начинаются (см. ниже).
Пробиотики и пребиотики
Хотя многие исследования показали клиническую пользу пробиотиков и пребиотиков в конкретных медицинских ситуациях, лишь немногие показания к их применению были одобрены регулирующими органами. Кроме того, получено мало доказательств снижения риска НИЗ, и в подавляющем большинстве национальных диетических рекомендаций не содержится каких-либо рекомендаций об их включении в состав здорового питания. Есть большие возможности для разработки пробиотиков, пребиотиков и их комбинаций (синбиотиков) для более систематической профилактики хронических заболеваний. В текущих исследованиях изучается применение этих стратегий для устранения влияния факторов индустриализации на разнообразие и функционирование кишечного микробиома. Уже разработаны и присутствуют на рынке соответствующие продукты, которые ожидают клинической валидации в хорошо контролируемых РКИ, поскольку имеющихся данных недостаточно, чтобы давать общие рекомендации.
Живые микробы
Еще одним отличительным признаком индустриализации является снижение микробного воздействия. Гипотеза биоразнообразия гласит, что контакт с природной средой необходим для обогащения микробиома человека, поддержания иммунного баланса, защиты от аллергии и воспалительных заболеваний. Пробиотики являются источником живых микробов, изучаются и продаются в этом контексте на протяжении десятилетий (см. вставку «Пробиотики и пребиотики»). Кроме того, ферментированные продукты, такие как кефир, йогурт, чайный гриб и квашеная капуста, употребляемые в сыром виде, содержат большое количество живых микробов (бактерий и грибов). Хотя микробы, присутствующие в ферментированных пищевых продуктах, не колонизируют желудочно-кишечный тракт из-за несовместимости с кишечной экосистемой человека, они обнаруживаются в фекальной микробиоте и могут взаимодействовать с организмом.

Некоторые диетические рекомендации включают ферментированные продукты (йогурт и ферментированное молоко), а об их преимуществах все чаще сообщается в наблюдательных и небольших РКИ, однако все еще сохраняется потребность в больших хорошо контролируемых исследованиях с участием людей.
Прецизионное питание
Люди по-разному реагируют на диеты, что ставит под сомнение универсальный подход, применяемый в настоящее время в диетических рекомендациях. Прецизионное или персонализированное питание, в свою очередь, адаптировано к биологии человека (гены, метаболизм и т. д.). Измерения характеристик микробиома могут стать ключевым компонентом стратегий прецизионного питания. Несколько компаний уже предлагают персонализированные диетические рекомендации на основе фекального микробиома, однако, они не одобрены регулирующими органами, что заставляет сомневаться в их точности. Текущие национальные диетические рекомендации не предлагают прецизионные или персонализированные подходы, к тому же реализация последних может стать трудной задачей в масштабах населения. Хотя у персонализированного питания есть научное обоснование, важно подчеркнуть, что большинство людей выиграют от диетических рекомендаций, рассмотренных выше.
Заключение
Кишечный микробиом — это своего рода «черный ящик» для исследователей в области питания, поскольку многие физиологические эффекты диеты могут зависеть от взаимодействия между нею, микроорганизмами и организмом человека. Необходимы дополнительные исследования, чтобы понять, насколько микробиом влияет на физиологические эффекты диет и какие механизмы, открытые на животных моделях, применимы к людям. Тем не менее, данные подтверждают важный вклад кишечного микробиома в эффекты диеты, подчеркивая, что понимание механизмов взаимодействий между диетой и микробиомом может разрешить непрекращающиеся споры о «правильном» питании и способствовать разработке более здоровых диет.
1. Armet AM, Deehan EC, O’Sullivan AF, et al. Rethinking healthy eating in light of the gut microbiome. Cell Host Microbe 2022; 30: 764-85.
2. Blaak EE, Canfora EE, Theis S, et al. Short chain fatty acids in human gut and metabolic health. Benef Microbes 2020; 11: 411-55.
3. Desai MS, Seekatz AM, Koropatkin NM, et al. A dietary fiber-deprived gut microbiota degrades the colonic mucus barrier and enhances pathogen susceptibility. Cell 2016; 167: 1339-53 e21.
4. Chang SK, Alasalvar C, Shahidi F. Superfruits: phytochemicals, antioxidant efficacies, and health effects - a comprehensive review. Crit Rev Food Sci Nutr 2019; 59: 1580-604.
5. Martínez I, Lattimer JM, Hubach KL, et al. Gut microbiome composition is linked to whole grain-induced immunological improvements. ISME J 2013; 7: 269-80.
6. Kovatcheva-Datchary P, Nilsson A, Akrami R, et al. Dietary fiber-induced improvement in glucose metabolism is associated with increased abundance of Prevotella. Cell Metab 2015; 22: 971-82.
7. Roager HM, Christensen LH. Personal diet-microbiota interactions and weight loss. Proc Nutr Soc 2022: 1-28.
8. Creedon AC, Hung ES, Berry SE, Whelan K. Nuts and their effect on gut microbiota, gut function and symptoms in adults: a systematic review and meta-analysis of randomised controlled trials. Nutrients 2020; 12: 2347.
9. Nakatani A, Li X, Miyamoto J, et al. Dietary mung bean protein reduces high-fat diet-induced weight gain by modulating host bile acid metabolism in a gut microbiota-dependent manner. Biochem Biophys Res Commun 2018; 501: 955-61.
10. Kimble R, Gouinguenet P, Ashor A, et al. Effects of a mediterranean diet on the gut microbiota and microbial metabolites: a systematic review of randomized controlled trials and observational studies. Crit Rev Food Sci Nutr 2023; 63: 8698-719.
11. Johnston BC, Zeraatkar D, Han MA, et al. Unprocessed red meat and processed meat consumption: dietary guideline recommendations from the Nutritional Recommendations (NutriRECS) Consortium. Ann Intern Med 2019; 171: 756-64.
12. Louis P, Hold GL, Flint HJ. The gut microbiota, bacterial metabolites and colorectal cancer. Nat Rev Microbiol 2014; 12: 661-72.
13. Devkota S, Wang Y, Musch MW, et al. Dietary-fat-induced taurocholic acid promotes pathobiont expansion and colitis in Il10-/- mice. Nature 2012; 487: 104-8.
14. Russell WR, Gratz SW, Duncan SH, et al. High-protein, reduced-carbohydrate weight-loss diets promote metabolite profiles likely to be detrimental to colonic health. Am J Clin Nutr 2011; 93: 1062-72.
15. Reynolds A, Mann J, Cummings J, et al. Carbohydrate quality and human health: a series of systematic reviews and meta-analyses. Lancet 2019; 393: 434-45.
Микробиота и болезнь Альцгеймера
Проф. Паскаль Деркиндерен (Pascal Derkinderen)
Отделение неврологии, Нантский университет и INSERM U1235, Нант, Франция

Комментарий к статье Ferreiro et al. Gut microbiome composition may be an indicator of preclinical Alzheimer’s disease (Состав кишечного микробиома может помочь в доклинической диагностике болезни Альцгеймера). Sci Transl Med 2023; 15:eabo2984.
Ось кишечная микробиота — головной мозг является «модным» направлением в области нейродегенеративных заболеваний, соответственно болезнь Альцгеймера (БА), наиболее частое из них, не является исключением. Недавний метаанализ выявил 17 исследований этого типа (438 пациентов с БА и 672 контроля) [1]. Хотя результаты исследований иногда отличались, общее мнение заключается в том, что дисбиоз, наблюдаемый при БА, является результатом изменения в сторону «провоспалительного» профиля [1]. Все найденные исследования касаются симптоматической БА с когнитивными нарушениями, тогда как данные о доклинической стадии БА до сих пор отсутствуют. Эта фаза заболевания на несколько лет предшествует развитию когнитивных нарушений, и в это время новые биологические маркеры и методы визуализации могут обнаружить амилоидную нейропатологию, характерную для этого заболевания. Этот недостаток теперь устранен благодаря недавней работе, в которой авторы использовали оригинальный подход, изучив данные 164 человек, которые приняли участие в продольном исследовании по изучению когнитивных функций в сочетании с визуализацией головного мозга (позитронно-эмиссионная томография [ПЭТ] + люмбальная пункция), причем последние два исследования прямо или косвенно выявили отложения b-амилоидного пептида [2]. На момент анализа кишечной микробиоты (между 2019 и 2021 годами) возраст участников (164 человека) составлял от 68 до 94 лет (45% мужчин) и у 49 из них была выявлена доклиническая форма БА, т. е. у них имелись амилоидные маркеры по данным визуализации и/ или анализа спинномозговой жидкости при отсутствии клинически заметных когнитивных нарушений. Анализ микробиоты показал различия между здоровыми добровольцами и лицами с доклинической БА. Наиболее значимыми видами, связанными с доклинической БА, были Dorea formicigenerans, Faecalibacterium prausnitzii, Coprococcus catus и Anaerostipes hadrus. Метаболическими путями, связанными с доклинической формой БА, были пути деградации аргинина и орнитина, тогда как путь деградации глутамата наиболее сильно ассоциировался с отсутствием заболевания.
Считаете ли вы, что анализы образцов кала вскоре могут быть добавлены к тестам для выявления лиц с ранней стадией болезни Альцгеймера, чтобы быстрее направить их на подходящее лечение?
После прочтения этой статьи сразу возникает закономерный вопрос: можно ли использовать анализ микробиоты для выявления лиц с ранней или доклинической стадией БА. С точки зрения невролога ответ скорее отрицательный. Это связано с тем, что текущие данные, полученные у лиц с симптоматической и доклинической БА, не позволяют идентифицировать конкретную «стандартную» микробиоту, благодаря которой первых можно отличить от здоровых представителей общей популяции с помощью обычного анализа кала. Более того, в настоящее время существуют маркеры БА, надежные даже на доклинической стадии и легко применимые в условиях клиники. Оставляя в стороне ПЭТ-визуализацию, которая доступна не во всех центрах, и анализ спинномозговой жидкости, который включает люмбальную пункцию (инвазивная процедура), с помощью анализа плазмы (т. е. в простом образце крови) у пациентов с доклинической или симптоматической БА можно обнаружить изменения в экспрессии и/или фосфорилировании определенных белков, участвующих в нейродегенеративном процессе [3].
Стоит ли поделиться этой публикацией с пациентами, чтобы объяснить взаимосвязь между кишечной микробиотой и мозгом и подчеркнуть важное значение кишечной микробиоты для здоровья человека?
Несомненно, эта работа, впервые показавшая изменения состава микробиоты при доклинической БА, еще больше убеждает нас в том, что микробиота задействована уже на самых ранних этапах патогенеза БА. В этом контексте, краткое изложение работы можно представить широкой общественности или некоторым пациентам, чтобы подчеркнуть важную роль микробиоты для здоровья. Тем не менее, эти результаты требуют независимого подтверждения другими командами ученых.

1. Jemimah S, Chabib CMM, Hadjileontiadis L, et al. Gut microbiome dysbiosis in Alzheimer’s disease and mild cognitive impairment: A systematic review and meta-analysis. PLoS One 2023; 18: e0285346.
2. Ferreiro AL, Choi J, Ryou J, et al. Gut microbiome composition may be an indicator of preclinical Alzheimer’s disease. Sci Transl Med 2023; 15: eabo2984.
3. De Meyer S, Blujdea ER, Schaeverbeke J, et al. Longitudinal associations of serum biomarkers with early cognitive, amyloid and grey matter changes. Brain 2023: awad
ВАГИНАЛЬНАЯ МИКРОБИОТА #20
Проф. Сату Пеккала (Satu Pekkala)
Научный сотрудник Академии Финляндии, Факультет спорта и здравоохранения, Университет Ювяскюля, Финляндия
21% Only 1 in 5 women say they know exactly the meaning of the term “vaginal microbiota”
Привычное невынашивание: исследование случая трансплантации влагалищной микробиоты (ТВМ)
Данный случай, несомненно, представляет научный интерес. Женщине с поздними выкидышами и тяжелым дисбиозом влагалища была проведена трансплантация влагалищной микробиоты (ТВМ). Через пять месяцев она забеременела, имея здоровую микрофлору влагалища, и родила доношенного ребенка. Однако следует отметить ограничения исследования: в нем принимала участие одна пациентка с диагнозом «антифосфолипидный синдром» (АФЛС, тромбофилия, ассоциированная с выкидышами). Кроме того, полученные результаты могут быть частично или полностью объяснены терапией по поводу АФЛС, проводимой во время последней беременности. Перед трансплантацией 30-летняя мать одного ребенка перенесла серию выкидышей, часть из них на поздних сроках (неделя беременности 27 в 2019 г., недели 17 и 23 в 2020 г.). В течение последних 9 лет она жаловалась на зуд и выделения из влагалища, которые усиливались во время неудачных беременностей, несмотря на лечение. На то были причины: в июле 2021 г. при исследовании влагалищной микробиоты был выявлен тяжелый дисбиоз с преобладанием Gardnerella spp на 91,3%. В сентябре 2021 г., в рамках программы предоставления лечения в качестве благотворительной помощи, пациентке на 10-й день менструального цикла была проведена ТВМ от здорового донора без предварительной антибиотикотерапии. Хотя при пероральном или вагинальном применении антибиотиков (метронидазол или клиндамицин) частота излечения дисбиоза влагалища через месяц после начала терапии составляет 80-90%, вероятность рецидива через год может достигать 60%, при этом возникает дополнительный риск развития резистентности. ТВМ быстро скорректировала дисбиоз и его симптомы, и в течение нескольких месяцев в микрофлоре стали доминировать штаммы Lactobacillus (как и у донора). В феврале 2022 г. пациентка забеременела естественным путем. Во время этой беременности она получала терапию по поводу АФЛС. При регулярном мониторинге влагалищной микробиоты на шестой неделе беременности было выявлено присутствие Gardnerella spp. (41,8%). Вторая ТВМ была запланирована через две недели, но к этому дню L. crispatus вновь стала доминировать в микробиоте пациентки. В конце беременности женщине выполнили плановое кесарево сечение — родился совершенно здоровый мальчик. Хотя эти данные требуют подтверждения в других клинических исследованиях, но они позволяют прийти к заключению о том, что ТВМ может использоваться в качестве метода лечения пациенток с тяжелым дисбиозом влагалища, в том числе с риском осложнений после экстракорпорального оплодотворения. По мнению авторов, этот случай не только подтверждает концепцию, но и дает надежду на появление методов лечения, основанных на
КИШЕЧНАЯ МИКРОБИОТА #20
Проф. Сату Пеккала (Satu Pekkala)
Научный сотрудник Академии Финляндии, Факультет спорта и здравоохранения, Университет Ювяскюля, Финляндия

Персонализированная диета на основе микробиома для улучшения преддиабета
Исследователи из института Вейцмана были пионерами в разработке персонализированных диетических подходов на основе кишечного микробиома (КМ). В своей работе Бен-Яков (Ben-Yacov) и соавт. изучали влияние персонализированного постпрандиального таргетирования (ППТ) по сравнению со средиземноморской диетой (СЗД) на кардиометаболические факторы риска. Известно, что диета влияет на кардиометаболическое здоровье, но вопрос о том, модулирует ли КМ эти эффекты, не изучался в продольных условиях. В рамках 6-месячного исследования 225 взрослых пациентов с преддиабетом были рандомизированы в группы ППТ и СЗД. ППТ было основано на алгоритм, а СЗД — на выборе диетолога. ППТ представляло собой диету с низким содержанием углеводов и высоким содержанием жиров, поскольку углеводы пищи являются важным фактором, определяющим постпрандиальную реакцию на глюкозу. По сравнению с ССЗ, ППТ ассоциировалось с увеличением разнообразия и богатства КМ. Участники группы ППТ больше употребляли некоторые продукты, богатые катехином, включая темный шоколад и кешью. Такая диета ассоциировалась с обогащением флоры Flavonifractor plautii, который участвует в метаболизме флавоноидов и катехинов. Согласно статистической модели, изменения со стороны конкретных видов КМ частично опосредовали влияние диеты на клинические исходы. Например, изменение UBA11471 sp000434215 (порядок Bacteroidales) частично опосредовало влияние изменения потребления «жиров и масел» на уровень HbA1c. HbA1c представляет собой гликированный гемоглобин, который используется для оценки тяжести сахарного диабета. Оказалось, что три вида бактерий (Bacteroidales, Lachnospiraceae и Oscillospirales) опосредовали влияние ППТ на уровни HbA1c, холестерина липопротеинов высокой плотности (ЛПВП) и триглицеридов. Результаты исследования подтверждают роль КМ в опосредовании эффектов изменения диеты на кардиометаболические исходы, что свидетельствует об успешности концепции прецизионного питания для снижения бремени сопутствующих заболеваний при преддиабете.
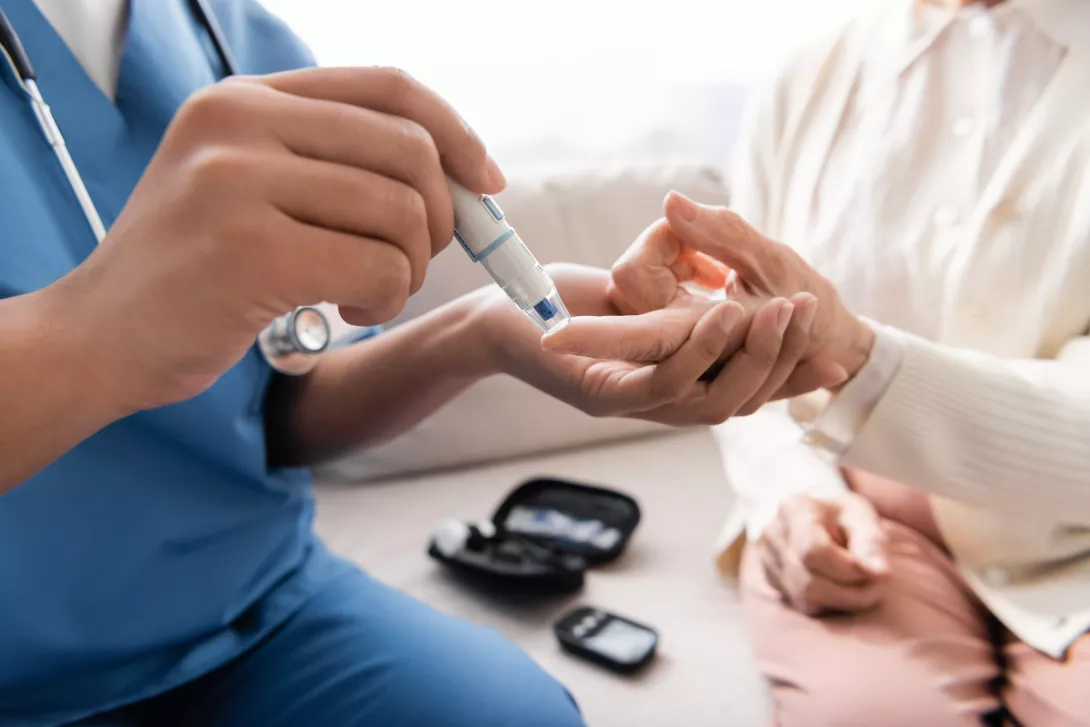
Фекальный метаболом при воспалительных заболеваниях кишечника
Воспалительные заболевания кишечника (ВЗК) включают в себя неспецифический язвенный колит (НЯК) и болезнь Крона (БК). Известно, что некоторые микробные метаболиты влияют на воспалительные реакции, которые являются важными звеньями патогенеза ВЗК. Однако исследований, посвященных изучению фекального метаболома у пациентов с ВЗК, очень мало. Чтобы восполнить этот пробел, ученые изучили ряд фекальных метаболитов в качестве биомаркеров ВЗК. В исследовании приняли участие 255 здоровых добровольцев (контрольная группа) и 424 пациента с ВЗК. Результаты анализа метаболома в обеих когортах сопоставляли с данными оценки состава кишечной микробиоты, секвенирования экзома и геномных данных. Метаболомы группы ВЗК характеризовались недостатком витаминов и молекул, связанных с жирными кислотами. Кроме того, у пациентов с ВЗК отмечались повышенные уровни фенольного соединения p-крезолсульфата, который образуется в результате ферментирования белков кишечными бактериями. У пациентов с ЯК были самые низкие уровни фекальных противовоспалительных короткоцепочечных жирных кислот. Для определения потенциальных биомаркеров и прогнозирования фенотипов заболеваний использовали метод машинного обучения. Отношение сфинголипида и L-уробилина различалось между группами ВЗК и не-ВЗК. У пациентов с ВЗК увеличение количества патобионтов сопровождалось повышением уровней сфинголипидов, этаноламина и первичных желчных кислот. У пациентов с БК резекция илеоцекального клапана ассоциировалась с изменениями уровней 212 метаболитов, таких как холевая кислота, а также уменьшением преобладания Faecalibacterium prausnitzii, что также отрицательно влияло на уровни противовоспалительных метаболитов. Результаты анализа показали, что наблюдаемые связи между образом жизни, клиническими факторами и фекальными метаболитами были обусловлены изменениями кишечной микробиоты. В целом, исследование показало возможности использования фекальных метаболитов в качестве биомаркеров ВЗК и что, несмотря на влияние образа жизни, генетики и заболеваний, кишечные микроорганизмы являются сильными предикторами уровней фекальных метаболитов.
Контрольные точки, модулируемые микробиотой, направляют иммуносупрессивные кишечные Т-клетки в опухоль
Устойчивость злокачественных опухолей к лечению ингибиторами контрольных точек иммунного ответа (ИКТ) может быть результатом применения антибиотиков (АБ), потенциального вовлекающего кишечную микробиоту. Однако эта взаимосвязь подробно не изучалась. Поэтому Фидель (Fidelle) и соавт. решили устранить этот пробел в знаниях, используя модель грызунов и реальных пациентов. Согласно данным литературы, кишечные бактерии могут влиять на дифференцировку лимфоцитов, примированных в брыжеечных лимфатических узлах или находящихся в собственной пластинке слизистой кишечника, а также экспрессию интегрина α4β7, который взаимодействует со своим рецептором, адгезионной молекулой слизистой по типу адрессина-1 (MAdCAM-1), расположенным в венулах с высоким эндотелием (ВВЭ). Это предотвращает миграцию клеток Treg17 в ткань опухолей кишечника, нарушая противоопухолевые эффекты ИКТ. Th17 — это разновидность провоспалительных Т-хелперов, которые продуцируют интерлейкин 17 (ИЛ-17). Эти клетки связаны с Т-регуляторными клетками и сигналами, которые заставляют Th17 ингибировать дифференцировку Treg. У грызунов введение АБ снижало экспрессию MAdCAM-1. Это можно объяснить реколонизацией кишечника родом Enterocloster. Далее, пероральное введение Enterocloster вызывало снижение экспрессии MAdCAM-1. Восстановление экспрессии MAdCAM-1 в ВВЭ подвздошной кишки путем трансплантации фекальной микробиоты или блокады ИЛ-17A устраняло ингибирующее действие АБ. Эктопическая экспрессия MAdCAM-1 в печени вызывала локальное поддержание популяции энтеротропных клеток α4β7+ Treg17, что дополнительно уменьшало их накопление в опухолях и улучшало эффективность иммунотерапии у мышей. В когортах пациентов с раком легкого, почек и мочевого пузыря низкие уровни MAdCAM-1 в сыворотке имели отрицательное прогностическое значение. В заключение отметим, что ось MAdCAM-1 — α4β7 требует более пристального изучения в контексте противоопухолевого иммунологического надзора.

Дети и подростки с синдромом дефицита внимания и гиперактивностью, а также расстройствами аутистического спектра имеют разный состав микробиоты
КОММЕНТАРИИ К СТАТЬЕ - Раздел, посвященный детям
Проф. Эммануэль Мас (Emmanuel Mas)
Отделение гастроэнтерологии и нутрициологии, Детская больница, Тулуза, Франция

Отделение гастроэнтерологии и нутрициологии, Детская больница, Тулуза, Франция
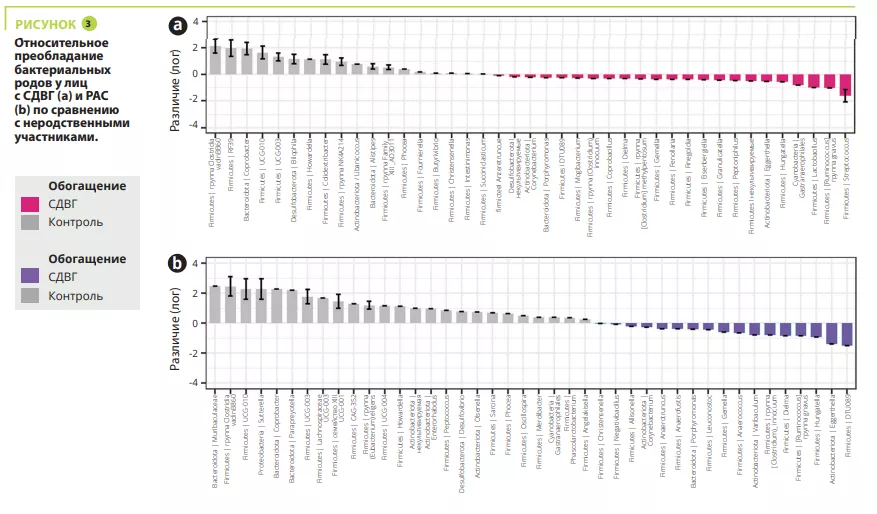
Была высказана гипотеза о связи между изменениями кишечной микробиоты и синдромом дефицита внимания и гиперактивности (СДВГ), а также расстройствами аутистического спектра (РАС). Авторы проанализировали состав кишечной микробиоты у детей и подростков с наличием или отсутствием этих расстройств с точки зрения системных эффектов бактерий. Исследуемая группа состояла из пациентов с диагнозами СДВГ, РАС и СДВГ/РАС, а контрольные — из их братьев/сестер и неродственных детей. Кишечную микробиоту анализировали путем секвенирования гена 16S рРНК в области V4, а также определяли концентрацию липополисахаридсвязывающего белка (ЛСБ), цитокинов и других сигнальных молекул в плазме. Важно отметить, что состав кишечной микробиоты у детей с СДВГ и РАС был очень схожим с точки зрения альфа- и бета-разнообразия, отличаясь от состава микробиоты у неродственных детей. В подгруппе участников с СДВГ и РАС отмечалась повышенная концентрация ЛСБ по сравнению со здоровыми детьми, что положительно коррелировало с уровнями интерлейкинов (ИЛ)-8, 12 и 13. Эти наблюдения указывают на нарушение кишечного барьера и иммунную дисрегуляцию у детей с СДВГ или РАС.
Что мы уже знаем?
Синдром дефицита внимания с гиперактивностью (СДВГ) и расстройство аутистического спектра (РАС) представляют собой нарушения развития нервной системы. У детей с СДВГ и РАС часто возникают желудочно-кишечные нарушения, такие как боль в животе и запор. Причина этих расстройств кроется в генетических нарушениях в сочетании с действием факторов риска внешней среды, особенно характера питания. По этой причине наряду с медикаментозной терапией можно предложить диетическое вмешательство, поскольку состав кишечного микробиома имеет важное значение для функционирования оси кишечник — головной мозг. Также мы знаем, что дети с РАС часто едят определенные виды пищи, что может объяснить изменение кишечной микробиоты. Кроме дисбиоза, при СДВГ и РАС описано увеличение кишечной проницаемости и системное воспаление низкой степени. Цель этого исследования состояла в том, чтобы проанализировать изменения кишечной микробиоты у пациентов с СДВГ, РАС и СДВГ/РАС по сравнению с их здоровыми братьями и сестрами и неродственными детьми. Вторичные цели заключались в оценке кишечной проницаемости и иммунной системы.
Что главное в этом исследовании?
В общей сложности 95 детей в возрасте 5-17 лет, включая 32 ребенка с СДВГ, 12 детей с РАС, 11 детей с СДВГ/РАС, 14, 5, 4 братьев и сестер пациентов и 17 неродственных детей. Желудочно-кишечные нарушения включали запор: СДВГ 15,6% (братья и сестры 7,1%), РАС 8,3% (братья и сестры 0%), СДВГ/РАС 18,2% (братья и сестры 0%), неродственные дети 5,9%; боль в животе: СДВГ 3,1% (братья и сестры 0%), РАС 16,7% (братья и сестры 0%), СДВГ/ РАС 18,2% (братья и сестры 0%), неродственные дети 0%; и реже — гастроэзофагеальный рефлюкс. Атипичная диета была наиболее распространена среди детей с РАС (50%), что было связано с однообразной пищей.
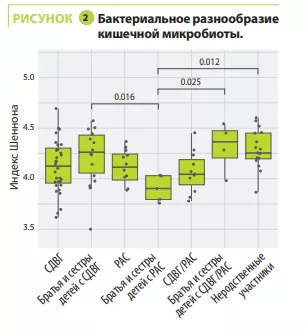
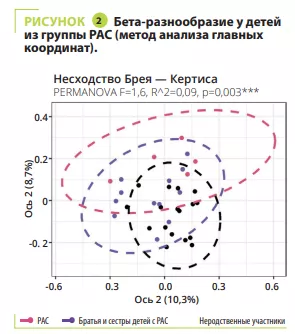
Анализ микробиоты кишечника не выявил каких-либо различий в альфа-разнообразии между участниками с СДВГ, РАС, СДВГ/РАС, их родственниками или неродственными детьми; напротив, оно было значимо ниже у братьев и сестер с РАС (рисунок 1). С точки зрения бета-разнообразия состав кишечной микробиоты был очень схожим у детей с СДВГ и РАС, значимо отличаясь между детьми с СДВГ, РАС и неродственными детьми (рисунок 2). В микробиоте некоторых детей с СДВГ, РАС или СДВГ/РАС содержалось меньше представителей типа Bacteroidetes и больше — Actinetobacteria. Во всех группах преобладали роды Bacteroides, Faecalibacterium, Blautia и Bifidobacterium; у некоторых детей наблюдалось высокое содержание Prevotella. Различия в численности родов бактерий были обнаружены между детьми с СДВГ, РАС и контрольной группой (рисунок 3), но не между детьми с СДВГ и РАС.
Между всеми исследуемыми и контрольными группами отсутствовали какие-либо различия по уровням фекального кальпротектина и ЛСБ. Однако корреляция между уровнями фекального кальпротектина и ЛСБ и бактериальным альфаи бета-разнообразием отсутствовала. Результаты измерения различных цитокинов и хемокинов не показали значимых различий между группами. Однако у нескольких детей с СДВГ и РАС уровни IL1-RA были выше по сравнению с неродственными детьми, а у 5 детей с СДВГ и одного ребенка с РАС концентрации IFN-g были выше, чем у неродственных детей. Наконец, были обнаружены слабо положительные корреляции между уровнями ЛСБ и ИЛ-8 (р=0,023), ИЛ-12 (р=0,018), ИЛ-13 (р=0,035) и PlGF (р=0,045), что позволяет предположить роль нарушений барьерной функции кишечника и иммунной регуляции.
- Подтверждено изменение кишечной микробиоты при нарушениях развития нервной системы, таких как СДВГ и РАС. Нарушения кишечной микробиоты и увеличение кишечной проницаемости, вероятно, связаны с системным воспалением низкой степени.
Каковы практические последствия?
Это исследование включало небольшое число участников, в первую очередь родственных контролей. Кишечная микробиота, а также кишечная проницаемость могут быть значимыми мишенями для терапевтического вмешательства у детей и подростков с СДВГ и РАС.
ЗАКЛЮЧЕНИЕ
Дети и подростки с СДВГ и РАС имели похожую кишечную микробиоту, отличную от таковой у неродственных участников контрольной группы. Различия в бета-разнообразии кишечной микробиоты и повышение уровня ЛСБ ассоциировались с различными концентрациями системных про- и противовоспалительных молекул.
Состав кишечного микробиома ассоциируется с будущим возникновением заболевания у ближайших родственников пациентов с болезнью Крона
КОММЕНТАРИИ К СТАТЬЕ - Раздел, посвященный взрослым
Проф. Гарри Сокол (Harry Sokol)
Отделение гастроэнтерологии и нутрициологии, больница Сен-Антуан, Париж, Франция

Комментарии к статье Raygoza Garay et al. в журнале Gastroenterology 2023 [1]
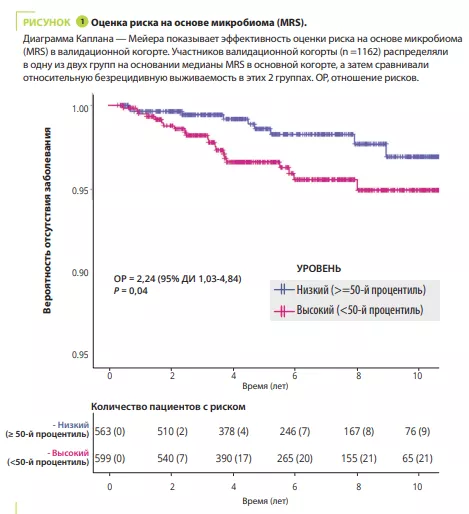
Основная информация и цели. Причины болезни Крона (БК) неизвестны. Согласно текущей гипотезе, микробные или экологические факторы вызывают воспаление кишечника у генетически восприимчивых людей, что приводит к развитию хронического воспалительного заболевания. В исследованиях методом случай-контроль с участием пациентов с БК удалось охарактеризовать изменения в составе кишечного микробиома, но не определить, являются ли они причиной БК или следствием воспаления или медикаментозного лечения. Методы: в проспективном когортном исследовании приняли участие 3483 здоровых ближайших (первая степень родства) родственника пациентов с БК, у которых определяли состав кишечного микробиома до начала заболевания, а также его предсказательную ценность в отношении риска возникновения БК. С помощью метода на основе машинного обучения авторы проанализировали состав кишечного микробиома (на основе секвенирования 16S рибосомной РНК) для определения микробных сигнатур, ассоциированных с будущим развитием БК. Эффективность модели оценивали в независимой валидационной когорте. Заключение: это первое исследование, результаты которого показали, что состав кишечного микробиома связан с последующим возникновением БК, из чего можно сделать вывод, что кишечный микробиом участвует в патогенезе болезни Крона.
Что мы уже знаем?
Болезнь Крона (БК) представляет собой воспалительное заболевание кишечника (ВЗК), характеризующееся рецидивирующим хроническим воспалением органов желудочно-кишечного тракта. Причины БК неизвестны. Согласно текущей гипотезе, микробные или экологические факторы вызывают воспаление кишечника у генетически восприимчивых людей, что приводит к развитию хронического воспалительного заболевания. В исследованиях методом случай-контроль с участием пациентов с БК удалось охарактеризовать изменения в составе кишечного микробиома [1]. Однако исследования не позволяют определить, являются ли изменения состава кишечного микробиома причиной БК или следствием воспаления или медикаментозного лечения. Чтобы ответить на эти вопросы, в рамках канадского проекта GEM (Genetic Environmental Microbial/ генетика микробного окружения) было проведено проспективное когортное исследование с участием здоровых ближайших родственников (первая степень родства) пациентов с болезнью Крона, предназначенное для определения характеристик, связанных с развитием болезни Крона. Авторы изучили профиль кишечного микробиома до развития БК и его прогностическую значимость в отношении риска возникновения БК. С помощью метода на основе машинного обучения был проанализирован состав кишечного микробиома в большой когорте здоровых ближайших родственников пациентов с болезнью Крона (N = 3483) с целью определения микробных сигнатур, ассоциированных с риском возникновения БК.
Что главное в этом исследовании?
На основе данных когорты GEM авторы разработали и валидировали оценку риска на основе микробиома (MRS), используя данные, полученные от лиц, у которых в будущем развилась БК. Таксонами, которые вносили наибольший вклад в MRS, были Ruminoccus torques и Blautia (увеличение преобладания), которые положительно коррелировали с MRS (предполагая вредное воздействие этих таксонов). В свою очередь, преобладание рода Roseburia отрицательно коррелировало с MRS (предполагая защитный эффект). Наконец, увеличение преобладания рода Faecalibacterium обратно коррелировало с увеличением MRS. Это первое исследование, показавшее, что уменьшение преобладания Faecalibacterium может быть доклинической сигнатурой БК, присутствующей за много лет до начала заболевания, предполагая причинно-следственную связь с уменьшением количества этих противовоспалительных бактерий [2]. Примечательно, что изменения в микробиоме, предшествующие возникновению БК, наблюдались незавиОР = 2,24 (95% ДИ 1,03-4,84) P = 0,04 Время (лет) Время (лет) Количество пациентов с риском Вероятность отсутствия заболевания - Низкий (≥ 50-й процентиль) - Высокий (=50-й процентиль) Высокий (<50-й процентиль) симо от наличия воспаления в кишечнике (определяемого по уровню фекального кальпротектина).
Авторы также провели метаболический анализ образцов кала в подгруппах когорты. Цитозин и его производное цитидин показали самую сильную отрицательную корреляцию с MRS.
Кроме того, сигнатура MRS, ассоциирующаяся с БК, была связана со снижением уровней метаболитов с противовоспалительной или антиоксидантной активностью, таких как гентизат и никотинат. Уровни этих защитных метаболитов также положительно коррелировали с преобладанием Faecalibacterium и Lachnospira, указывая на потенциальное биологическое взаимодействие между преобладанием этих метаболитов и составом микробиоты.
- The gut microbiota becomes altered several years before the diagnosis of Crohn’s disease, independently of the existence of intestinal inflammation, suggesting that the microbiome has a causal role in Crohn’s disease
- A Microbiome Risk Score may identify subjects at most risk of developing Crohn’s disease
- Early action targeting the microbiome may be proposed in patients identified as being at risk of developing Crohn’s disease
Каковы практические последствия?
Это исследование показывает, что анализ микробиома здоровых людей с риском развития болезни Крона может выявить лиц с наиболее высоким риском, обеспечить им тщательное наблюдение с возможностью проведения вмешательств, направленных на изменение микробного дисбаланса и, следовательно, снижение риска возникновения заболевания.
ЗАКЛЮЧЕНИЕ
В исследовании впервые показано, что изменения в составе кишечного микробиома происходят за много лет до постановки диагноза болезни Крона. Это значит, что кишечный микробиом участвует в патогенезе болезни Крона и может быть потенциальной мишенью для профилактических и/или терапевтических вмешательств.
1. Sartor RB, Wu GD. Roles for Intestinal Bacteria, Viruses, and Fungi in Pathogenesis of Inflammatory Bowel Diseases and Therapeutic. Approaches. Gastroenterology 2017; 152: 327-39.e4.
2. Sokol H, Pigneur B, Watterlot L, et al. Faecalibacterium prausnitzii is an anti-inflammatory commensal bacterium identified by gut microbiota analysis of Crohn disease patients. Proc Natl Acad Sci USA 2008; 105: 16731-6.
Основные новости конгресса UEGW 2023
Д-р Елена Полуэктова (Elena Poluektova)
Клиника пропедевтики внутренних болезней, гастроэнтерологии и гепатологии им. В. Х. Василенко Первого Московского государственного медицинского университета им. И. М. Сеченова, Москва, Россия

15-17 октября 2023 года в Копенгагене прошла 31-я Объединенная европейская гастроэнтерологическая неделя, на которой традиционно обсуждались важнейшие вопросы диагностики и лечения заболеваний желудочно-кишечного тракта.
Подавляющее большинство докладов содержали информацию о составе и функциях микробиоты и о микробиоте желудочно-кишечного тракта как терапевтической мишени при лечении различных заболеваний.
Специальный симпозиум («Грибы в нашем кишечнике: друзья или враги») был посвящен микобиому как одному из компонентов микробиома, формированию микобиома, факторам окружающей среды, влияющим на его состав, взаимодействию микобиома с бактериями (Selena Porcati, Италия); роли в патогенезе ВЗК (Dragos Ciocan, Франция) и потенциальному участию в канцерогенезе (Alexander Link, Германия).
Микробиом при СРК/ВЗК
Информация о роли микробиома в патогенезе синдрома раздраженного кишечника (СРК) и воспалительных заболеваний кишечника (ВЗК) продолжает расти и расширяться (симпозиум «Причины заболеваний: роль микроокружения кишечника при ВЗК и СРК»). Гарри Сокол (Франция) и Ринсе К. Веерсма (Нидерланды) сообщили, что изменения в составе микробиоты могут рассматриваться как биомаркер ВЗК и быть мишенью для терапевтических вмешательств с помощью пробиотиков, постбиотиков, бактериофагов и фекальной трансплантации. Изменения микробного состава желудочно-кишечного тракта у пациентов с СРК вносят неоспоримый вклад во все патогенетические механизмы заболевания (воспаление стенки кишечника, нарушение моторики, гиперчувствительность), поэтому назначение невсасывающихся антибиотиков и пробиотиков можно считать важной частью лечения СРК (Magnus Simren (Швеция) и Premysl Bercik (Канада).

Что такое здоровая микробиота?
Также были подняты некоторые вопросы, на которые пока нет однозначных ответов. Например, мы до сих пор не знаем, что на самом деле означает термин «здоровая микробиота». Предполагается, что более подходящим термином будет «нездоровая микробиота» (так называемый энтеротип B2), отражающий воспалительные изменения в кишечнике и ускоренный транзит (когда микробиота представлена в основном Bacteroides, содержит мало Firmicutes и имеет слабое микробное разнообразие). Воздействие на состав микробиоты с целью заставить ее отойти от энтеротипа B2, можно считать новой терапевтической стратегией (Jeroen Raes, Бельгия).
Кроме того, из-за неоспоримой важности состава кишечной микробиоты для поддержания здоровья человека и развития некоторых хронических неинфекционных заболеваний, в настоящее время клиницисты часто необоснованно рассчитывают использовать анализы микробного состава в качестве диагностического, прогностического или терапевтического инструмента. Все больше коммерческих организаций предлагают диагностические тесты на микробиоту, не имеющие четких показаний к применению или надежной схемы интерпретации результатов. Более 50 международных экспертов начали работу над согласительными рекомендациями, конечная цель которых — оптимизация диагностических тестов, подходов к лечению и продвижение знаний в области микробиома (Джанлука Яниро, Италия).
В дополнение к обсуждению микробиома как прямого патогенетического фактора и мишени для терапевтических вмешательств, были рассмотрены другие аспекты патогенеза и лечения заболеваний, связанных с дисбиозом кишечного микробиома. Среди них ВЗК и онкологические заболевания.
прогностического или терапевтического инструмента. Все больше коммерческих организаций предлагают диагностические тесты на микробиоту, не имеющие четких показаний к применению или надежной схемы интерпретации результатов. Более 50 международных экспертов начали работу над согласительными рекомендациями, конечная цель которых — оптимизация диагностических тестов, подходов к лечению и продвижение знаний в области микробиома (Джанлука Яниро, Италия). В дополнение к обсуждению микробиома как прямого патогенетического фактора и мишени для терапевтических вмешательств, были рассмотрены другие аспекты патогенеза и лечения заболеваний, связанных с дисбиозом кишечного микробиома. Среди них ВЗК и онкологические заболевания. Уже более 20 лет мы располагаем косвенными серологическими и генетическими доказательствами роли грибков в развитии воспалительных процессов в кишечнике пациентов с ВЗК. Из них можно упомянуть антитела к сахаромицетам у пациентов с болезнью Крона и генетический полиморфизм белка 9 (CARD9) и дектина-1, содержащего домен рекрутирования каспазы. Эти полиморфизмы обуславливают активацию провоспалительных цитокинов в ответ на сигналы от рецепторов распознавания паттернов. Многие исследования за последние 10 лет показывают, что у пациентов с ВЗК наблюдается снижение преобладания некоторых видов грибов по сравнению со здоровыми людьми. Изменения состава микобиоты связаны с плохим восстановлением слизистой оболочки (на животных моделях). Sacharomyces boulardii, применяемый в качестве пробиотика, может уменьшить воспаление в кишечнике посредством восстановления кишечного барьера (на животных моделях). Однако, подход в виде модификации грибкового сообщества для лечения ВЗК требует дальнейших исследований (Dragos Ciocan).
В последние годы растет интерес к потенциальной роли кишечных грибов и рецепторов их распознавания (например, рецепторов лектина С-типа) в развитии таких онкологических заболеваний у человека, как рак пищевода, желудка, поджелудочной железы, колоректальный рак, гепатоцеллюлярная карцинома, а также меланома и рак молочной железы. Некоторые исследования показывают, что грибковые патогены могут индуцировать воспалительные реакции, способствуя онкогенезу
LASPGHAN 2023 Обзор
Д-р Лигия де Соуза Лима Лауанд (Lygia de Souza Lima Lauand)
Отделение педиатрии, Сан-Паулу, Испания, Бразилия

В октябре в Рио-де-Жанейро, Бразилия, состоялись 24-й Латиноамериканский конгресс и 15-й Иберо-Американский конгресс по детской гастроэнтерологии, гепатологии и питанию, организованные LASPGHAN. Кроме того, 24 октября было проведено заседание по вопросам применения ПРОБИОТИКОВ, ПРЕБИОТИКОВ, ПОСТБИОТИКОВ В ПЕДИАТРИИ, включавшее практический клинический семинар.
Функциональные нарушения желудочно-кишечного тракта и микробиота
Кишечная микробиота двунаправленно влияет на моторику, висцеральную чувствительность, секреторную функцию, проницаемость ЖКТ и иммунную систему. Пробиотики — перспективное средство для лечения функциональных нарушений. При детских коликах ESPGHAN рекомендует некоторые штаммы Lactobacillus и Bifidobacterium детям, находящимся исключительно на грудном вскармливании. МР могут предлагать различные штаммы Lactobacillus при функциональных болях в животе или для уменьшения симптомов СРК [1].
Модулирование микробиоты влияет на жизнь младенцев
Такие факторы, как способ родоразрешения, грудное вскармливание [2], окружающая среда и отсутствие контакта с антибиотиками положительно влияют на колонизацию кишечника новорожденных, способствуя формированию здоровой кишечной среды, метаболическому балансу, гомеостазу и иммунной толерантности. И наоборот, преждевременные роды, кесарево сечение, отсутствие грудного вскармливания, нахождение в отделении интенсивной терапии и применение антибиотиков могут привести к дисбиозу, способствуя развитию иммуноопосредованных заболеваний. Стратегии модуляции и профилактики дисбиоза включают сбалансированное питание и использование пробиотиков, пребиотиков, синбиотиков и постбиотиков.

Микробиота грудного молока
Человеческое молоко содержит пробиотики, пребиотики, синбиотики и постбиотики, которые вносят вклад в баланс микробиоты у детей, находящихся на грудном вскармливании. Кожу матери и ротовую полость младенца считают основными факторами, которые влияют на молочную микробиоту. Факторы, модулирующие микробиоту грудного молока, включают гестационный возраст, пол младенца, способ родоразрешения, стадию лактации, режим кормления, географический регион, плотность социальной сети, состояние здоровья и рацион матери [3].

Инфекции верхних дыхательных путей (ИВДП) и микробиота
ИВДП приводят к неизбирательному назначению антибиотиков во всем мире, и, по оценкам ВОЗ, к 2050 году смертность, связанная с антибиотикорезистентностью, может достичь 10 миллионов человек. Согласно результатам систематического обзора, использование пробиотиков ассоциировалось со снижением заболеваемости ИВДП на 35%, уменьшением симптоматического периода на 2 дня и уменьшением использования антибиотиков на 45%. Некоторые пробиотические штаммы показали многообещающие результаты в плане уменьшения частоты вирусных ИВДП, тяжести инфекций и использования антибиотиков [4].

1. Szajewska H, Berni Canani R, Domellöf M, et al; ESPGHAN Special Interest Group on Gut Microbiota and Modifications. Probiotics for the Management of Pediatric Gastrointestinal Disorders: Position Paper of the ESPGHAN Special Interest Group on Gut Microbiota and Modifications. J Pediatr Gastroenterol Nutr 2023; 76: 232-47.
2. Levy M, Kolodziejczyk AA, Thaiss CA, et al. Dysbiosis and the immune system. Nat Rev Immunol 2017; 17: 219-32.
3. Boix-Amorós A, Collado MC, Van’t Land B, et al. Reviewing the evidence on breast milk composition and immunological outcomes. Nutr Rev 2019: nuz019.
4. Ozen M, Kocabas Sandal G, Dinleyici EC. Probiotics for the prevention of pediatric upper respiratory tract infections: a systematic review. Expert Opin Biol Ther 2015; 15: 9-20.
Может ли кишечная микробиота предсказать эффективность вакцины против Covid?
Новое исследование показало, что определенные характеристики кишечной микробиоты могут предсказать уровень антител к Covid через 6 месяцев после вакцинации. Впервые!

Покажите, как выглядит ваша микробиота, и я расскажу, как на вас подействует вакцина против Covid.
Так в двух словах можно описать результаты исследования1, опубликованные в сентябре прошлого года в академическом журнале «Signal Transduction and Targeted Therapy».
Ученые показали, что присутствие определенных бактерий и молекул в кишечнике на момент получения первой дозы вакцины может усилить эффекты и продолжительность защитного действия последней.
Перспективное направление для разработки новых адъювантов!
- 161 участник
- две вакцины против Covid-19
- шестимесячный период наблюдени
Такие результаты были получены у 161 добровольца, за которыми наблюдали в течение 6 месяцев.
121 участник получил две дозы вакцины Comirnaty (на основе мРНК) производства Pfizer-BioNTech, а остальные 40 — вакцину CoronaVac (на основе инактивированного вируса) производства китайской компании Sinovac Biotech. Во время исследования ни один из добровольцев не был инфицирован Covid. Непосредственно перед вакцинацией, а затем через месяц и полгода у участников брали следующие образцы:
- образцы крови для измерения концентрации (титра) антител;
- • образцы стула для выявления бактерий в кишечной микробиоте и измерения уровней метаболитов, вырабатываемых организмом и бактериями (витамин B3, ГАМК, фумаровая кислота и т. д. — т. н. «метаболом»).
Оказалось, что вакцина Comirnaty лучше формировала иммунитет, чем CoronaVac.
Как работают вакцины?
Чтобы эффективно защититься от болезни, нужно знать противника в лицо. Вот в чем заключается вакцинация против вирусов:
- Сначала в организм вводят антиген, т. е. инактивированный или ослабленный патоген или его фрагмент;
- Иммунные клетки продуцируют специфические антитела, нацеленные на этот антиген;
- Организм хранит сформированные клетки «памяти»;
- При заражении настоящим возбудителем происходит быстрая и эффективная активация клеток памяти иммунной системы (гораздо сильнее, чем при первом попадании возбудителя в организм);
- Происходит уничтожение патогена. Вакцина CoronaVac, получаемая из инактивированного вируса SARS-CoV-2, работает по этому принципу. Вакцина Comirnaty отличается тем, что содержит матричную РНК — «шаблон», по которому клетки производят белки, идентичные присутствующим на поверхности вируса Covid. Эти белки затем играют роль антигенов для производства антител.
Source: WHO 2
Состояние кишечной флоры модулирует иммунный ответ на вакцинацию
Через 6 месяцев в группе Comirnaty участники, в чьей микробиоте на момент первой инъекции преобладали Bacterium adolescentis,
(sidenote:
Бифидобактерии
Pод бактерий в форме буквы Y, большинство из которых полезны для человека. Они встречаются в кишечнике человека, а также в некоторых йогуртах.
Они:
- защищают кишечный барьер;
- участвуют в развитии иммунной системы и помогают бороться с воспалением;
- способствуют пищеварению и улучшению симптомов нарушений со стороны желудочно-кишечного тракта.
Sung V, D'Amico F, Cabana MD, et al. Lactobacillus reuteri to Treat Infant Colic: A Meta-analysis. Pediatrics. 2018 Jan;141(1):e20171811.
O'Callaghan A, van Sinderen D. Bifidobacteria and Their Role as Members of the Human Gut Microbiota. Front Microbiol. 2016 Jun 15;7:925.
Ruiz L, Delgado S, Ruas-Madiedo P, et al. Bifidobacteria and Their Molecular Communication with the Immune System. Front Microbiol. 2017 Dec 4;8:2345.
)
и Roseburia faecis, имели более высокие уровни антител к SARS-CoV-2 в крови. Такой же вариант более сильного и длительного иммунитета наблюдался у людей, чей метаболом был обогащен витамином B3 и ГАМК.
Кишечная микробиота
В группе CoronaVac низкое содержание Faecalibacterium prausnitzii и повышенное — Phocaeicola dorei (сигнатура, обнаруженная у пациентов, инфицированных Covid), а также более высокое содержание фумаровой кислоты (препятствует репликации вируса) в метаболоме ассоциировались с лучшим иммунитетом через 6 месяцев.
Кроме того, в группе Comirnaty большая доля бактериальных штаммов в микробиоте, измененных вакциной, не восстановила свое исходное состояние. Хотя последствия оценить довольно сложно, исследователи отмечают, что некоторые из затронутых штаммов были те же, что и у людей с длительным Covid.
На пути к разработке новых адъювантов
Известно, что микробиота, генетика и масса тела влияют на эффективность вакцин против Covid. Тем не менее, это первое исследование, показавшее, что структура микробиоты и метаболома накануне вакцинации может предсказать уровень иммунитета через 6 месяцев.
Хотя эти результаты должны быть подтверждены в более специфическом исследовании, они не исключают возможности использования бактерий или метаболитов в качестве адъювантов для повышения эффективности вакцин.







