Sinopse do curso:
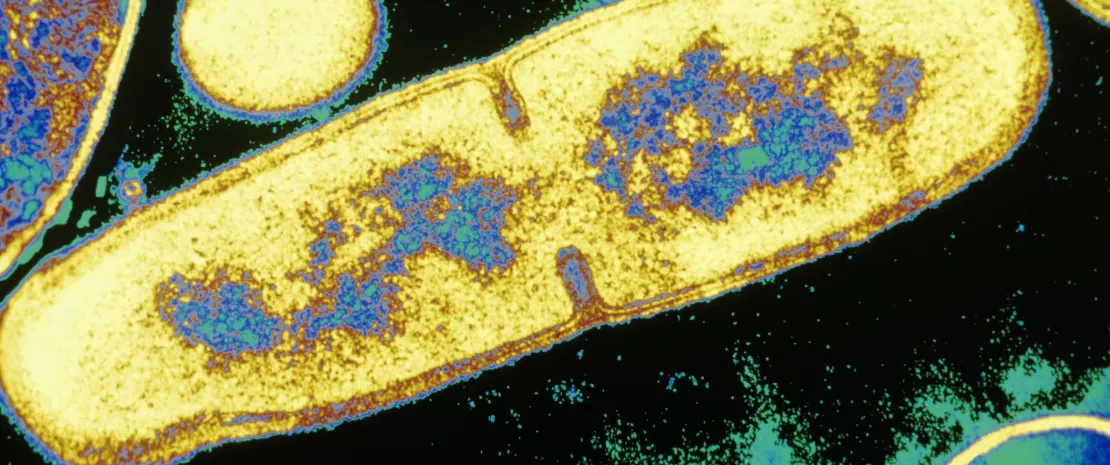
Esse curso credenciado tem como objetivo instruir ginecologistas, parteiras e farmacêuticos sobre a importância da microbiota, especialmente a microbiota vaginal, para a saúde íntima. Liderados por uma especialista renomada, a Dra. Graziottin, durante todo o curso os participantes obterão uma compreensão abrangente de como a microbiota afeta a saúde íntima ao longo da vida. Primeiro, abordaremos as percepções básicas sobre o microbioma intestinal antes de nos aprofundarmos na microbiota vaginal em diferentes estágios da vida, incluindo o potencial de uma placenta estéril, a microbiota neonatal e as mudanças durante a infância, a puberdade, os anos férteis e a menopausa. Não perca as recomendações práticas, os equívocos comuns e o resumo das principais conclusões que lhe proporcionarão o conhecimento e as habilidades necessárias em sua prática clínica.
Inscreva-se agora!
Esta atividade conta com o apoio financeiro irrestrito da Biocodex.
Quem é a Alessandra Graziottin?
Alessandra Graziottin, MD é uma ginecologista, oncologista, sexóloga e psicoterapeuta italiana. Ela é diretora do Centro de Ginecologia e Sexologia Médica do Hospital San Raffaele Resnati, em Milão.
- Em 2008, fundou a Fundação Alessandra Graziottin para o tratamento da dor em mulheres Onlus, da qual é presidente.
- Atualmente, é professora consultora do Mestrado Avançado em Andrologia e Medicina Sexual da Universidade de Firenze.
- Também foi professora consultora no Mestrado Avançado em Sexologia Clínica da Universidade de Pisa e professora no Curso de Mestrado em Medicina Sexual para Estudantes de Psicologia da Universidade de Veneza e da Universidade Salesiana (UPS) de Roma.
Ela é uma ginecologista renomada, tendo publicado 22 livros científicos e 7 livros populares (como autora, coautora ou editora), mais de 90 capítulos de livros científicos, 8 manuais educacionais para mulheres e mais de 400 artigos científicos sobre vários aspectos da ginecologia e sexologia médica.
Declaração de Conflitos de Interesse: A autora declara ter recebido honorários da Astellas, Fagron, Mammowave, Mylan, Named, Techdow, Uriach; ter participado como palestrante em eventos patrocinados pela Astellas, Biofemme, Bromatech, Lolipharma, Named, Techdow, Uriach; e fazer parte de conselhos consultivos da Astellas, Mylan, Techdow, Uriach.
A respeito da Xpeer
Xpeer Medical Education é a primeira aplicação de formação clínica acreditada do mercado, com cativantes vídeos de microaprendizagem de apenas 5 minutos.
Com um poderoso algoritmo para personalização da experiência do utilizador e dos conteúdos, inspirado no das mais populares plataformas de vídeo em streaming, oferece uma experiência totalmente renovada para a formação contínua e o desenvolvimento profissional dos profissionais de saúde.
Credenciada pela União Europeia de Médicos Especialistas, oferece componentes de formação clínica de elevada qualidade científica. Na Xpeer poderá encontrar este programa sobre a Microbiota e 500 horas de formação clínica de 2021 na sua especialidade, tecnologias, e competências profissionais e pessoais.
Mais informações sobre as acreditações:
A aplicação Xpeer é credenciada pelo European Accreditation Council for Continuing Medical Education (EACCME®) e atribui créditos ECMEC oficialmente reconhecidos em 26 países.
Os participantes do módulo obtêm 1 crédito FMF Europeu (ECMEC) por cada hora de formação (60 minutos úteis de e-learning, excluindo as introduções...). Este crédito é atribuído após a conclusão do módulo e a avaliação correspondente validada pelos participantes.

 Dermatite atópica: salvar a pele do fungo Malassezia
Dermatite atópica: salvar a pele do fungo Malassezia
 Gosta de se bronzear? Atenção à microbiota da sua pele!
Gosta de se bronzear? Atenção à microbiota da sua pele!