Diarreia bacteriana: microbiota intestinal, sua vítima potencial ou protetora contra ela?
Bactérias patogénicas como Shigella, Vibrio cholerae, Salmonella, E. coli, etc. provocam diarreia bacteriana, através de mecanismos que dependem da bactéria envolvida. As diarreias bacterianas são acompanhadas de disbiose intestinal. Analogamente, a microbiota intestinal exerce efeitos sobre a infeção bacteriana. Uma vez que uma microbiota intestinal "saudável" é mais resistente às infeções, os probióticos poderão reduzir a gravidade de muitas infeções bacterianas.
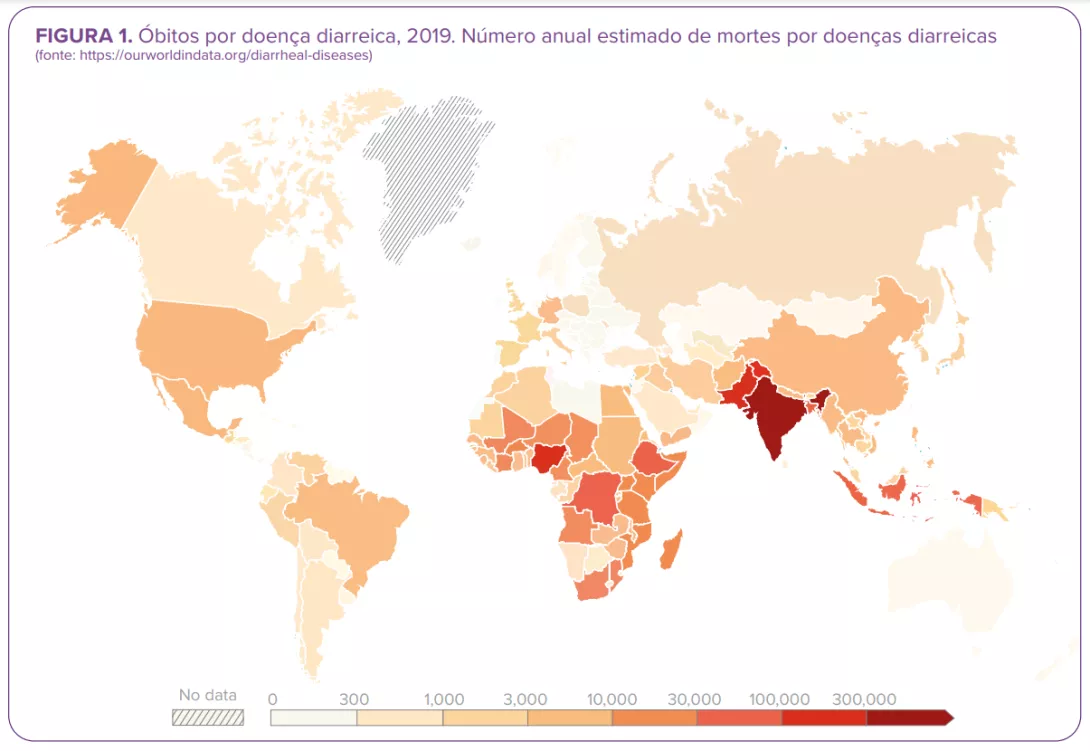
Sublinhando o quão letal uma diarreia bacteriana pode ser, estas 8 bactérias foram responsáveis por mais de um terço das mais de 1,65 milhões de mortes por diarreia infeciosa registadas em todo o mundo em 2016.2
Estas 8 bactérias
- Shigella: 212.438 mortes.
- Vibrio cholerae: 107,290 mortes
- Non-typhoidal Salmonella spp: 84,799 mortes.
- Campylobacter spp: 75,135 mortes.
- Enterotoxigenic E. coli: 51,186 mortes.
- Clostridioides difficile: 22,417 mortes.
- Aeromonas: 16,881 mortes.
- Enteropathogenic Escherichia coli: 12,337 mortes.
DA INFEÇÃO À DIARREIA
Os mecanismos que conduzem à diarreia bacteriana dependem das bactérias envolvidas. Transmitida através de àgua ou alimentos contaminados, ou por contacto entre pessoas, a Shigella infesta o trato gastrointestinal, produz uma enterotoxina e uma toxina do serotipo 1, destruindo o epitélio intestinal e provocando diarreia grave com sangue e muco3,5
As variantes patogénicas do Vibrio cholerae produzem uma toxina da cólera que ativa a secreção de aniões, inibe a absorção de NaCl eletroneutro e aniquila a função de barreira intestinal, induzindo assim a secreção maciça de fluidos no lúmen do intestino delgado e a perda de grandes quantidades de água, sódio, cloreto, bicarbonato e potássio3,5,13
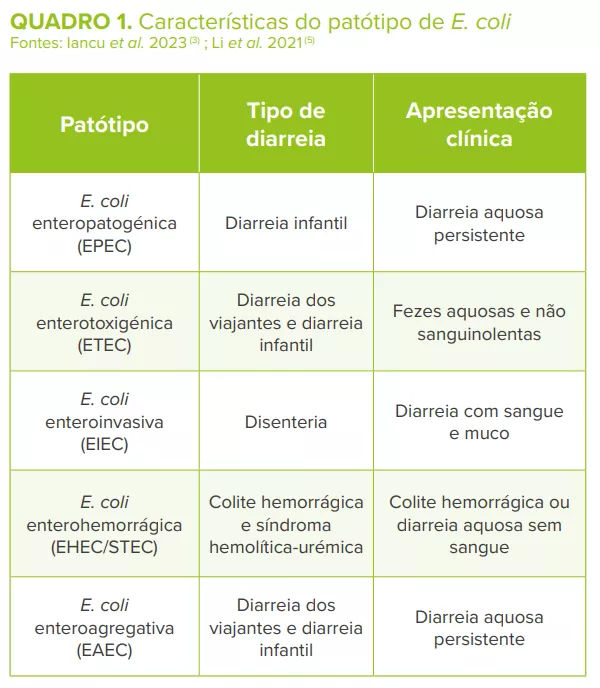
Diferentes estirpes patogénicas de E. coli, classificadas em diferentes patotipos (Quadro 1), causam diarreia ligeira a grave, normalmente acompanhada de febre. A E. coli adere às células epiteliais intestinais através das fímbrias de adesão, produz toxinas e exerce os seus efeitos patogénicos3,5
EFEITOS NA MICROBIOTA DOS AGENTES PATOGÉNICOS E DA DIARREIA
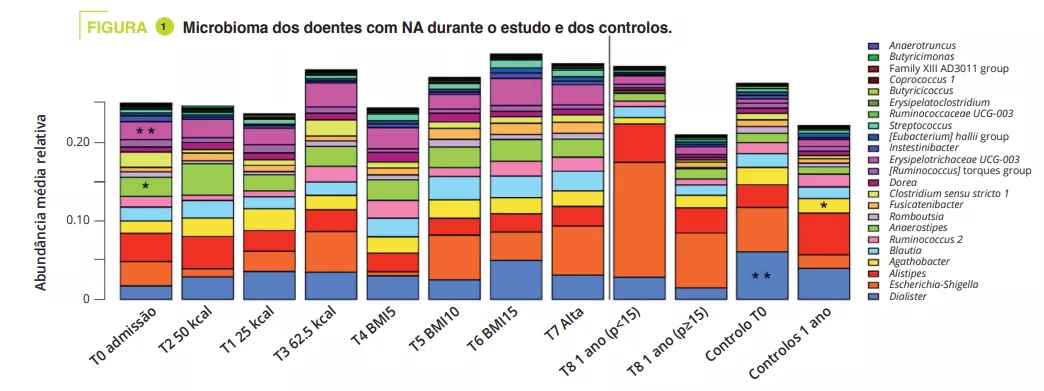
As diarreias bacterianas são acompanhadas de disbiose, geralmente com excessiva abundância de anaeróbios facultativos (Escherichia, Streptococcus, Enterococcus, etc.) na diarreia disentérica, e uma redução de bactérias com efeitos imunomoduladores conhecidos (Lactobacillus ruminis, Bifidobacterium pseudocatenulatum)7 (Figura 3).
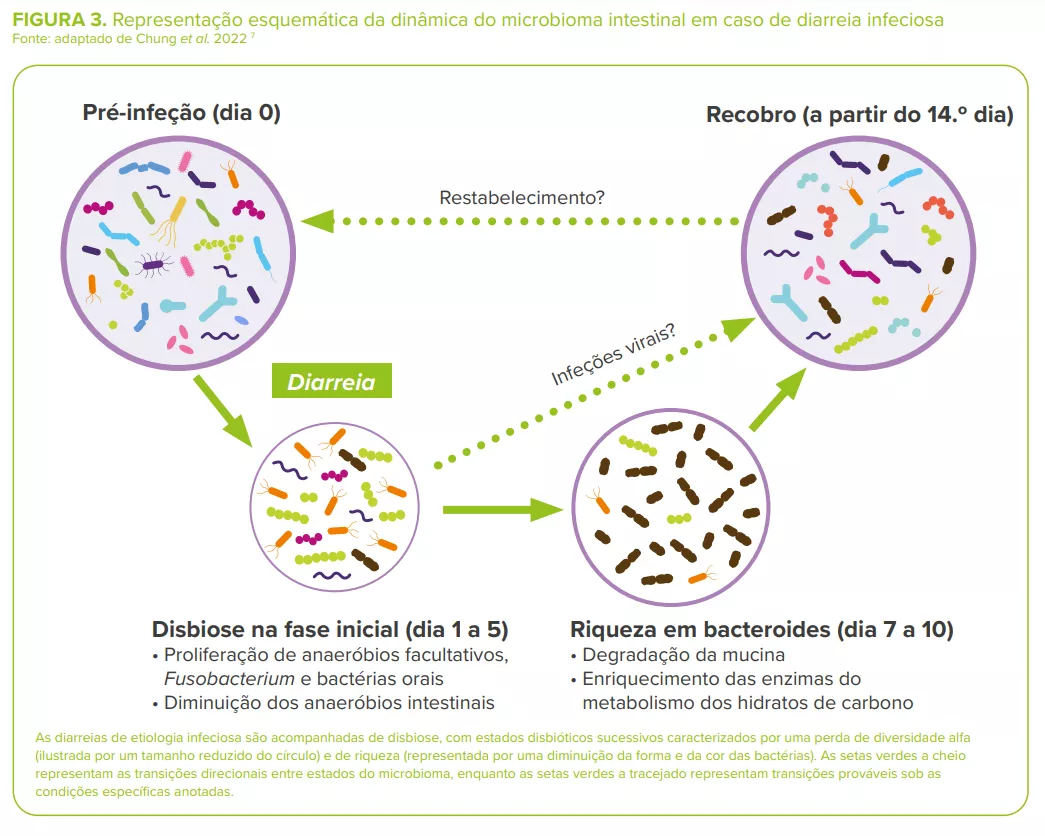
Por exemplo, na cólera, a microbiota intestinal é substancialmente modificada durante e após a infeção, em consequência da supressão da camada de muco juntamente com a comunidade microbiana intestinal residente e da produção da toxina pelo V. cholerae.13 Durante o recobro, a microbiota intestinal dos doentes com cólera repovoa-se lentamente através de um padrão de acumulação semelhante ao da maturação da microbiota intestinal observada nas crianças.3
Da mesma forma, as crianças infetadas com E. coli diarreica (DEC) apresentam uma composição microbiana intestinal distinta, com uma fração elevada de Bacteroidetes e Proteobactérias e uma abundância reduzida de Firmicutes. 13 O aumento das Proteobactérias pode ser parcialmente explicado por um aumento das espécies de Escherichia/Shigella (como causa de diarreia) e de outros membros das Enterobacteriaceae, como Citrobacter e Enterobacter (relacionados com a produção de histamina induzida por ambientes pró-inflamatórios e associados à aderência de E. coli).14 A utilização frequente de antimicrobianos pode também explicar parcialmente a disbiose observada7
A MICROBIOTA INTESTINAL OFERECE PROTEÇÃO CONTRA INFEÇÕES
Analogamente, a microbiota intestinal exerce efeitos sobre a infeção bacteriana. Em animais axénicos (germ-free), a falta de uma microbiota intestinal e a ausência de competição ecológica resulta num sistema imunitário imaturo que os torna altamente suscetíveis a agentes patogénicos diarreicos: 10 unidades formadoras de colónias (UFC) de Salmonella são suficientes para causar uma infeção letal, ao passo que para matar 50% dos ratos com uma microbiota intestinal intacta são necessárias 10³ a 10⁹ UFC.8
Nos seres humanos, foi demonstrado que Prevotella, Bifidobacterium e Blautia reduzem a colonização de V. cholerae. Inversamente, acredita-se que o Paracoccus promove o crescimento do agente patogénico.13 Esta é a razão pela qual a promoção de um microbioma intestinal "saudável" tem sido considerada uma abordagem útil na intervenção e prevenção da cólera.13
“O trato GI alberga ~1 a 10 vezes mais células bacterianas do que o número de células no corpo humano.” 16
BACTÉRIAS E LEVEDURAS PROBIÓTICAS, PREBIÓTICOS E TMF
A gravidade de várias infeções bacterianas pode ser reduzida pelos probióticos: por exemplo, a E. coli probiótica inibe a formação de biofilme de outras estirpes de E. coli e também das estirpes patogénicas Staphylococcus aureus e S. epidermidis.3 No que diz respeito à disenteria, uma combinação de estirpes de Lactobacillus e Bifidobacterium e de uma estirpe de Streptococcus reduz tanto a duração da diarreia sanguinolenta como o tempo de hospitalização.3
Inúmeros mecanismos poderão explicar por que razão os probióticos aliviam a diarreia:³ produção de substâncias antimicrobianas, exclusão competitiva, competição pelos locais de ligação celular, produção de ácidos e metabolitos que reduzem o pH circundante, reforço da barreira da mucosa intestinal, modulação da imunidade da mucosa intestinal e diversidade da microbiota intestinal. Por exemplo, a levedura probiótica Saccharomyces boulardii pode estimular o restabelecimento da microbiota intestinal em crianças com diarreia aguda.15
Os prebióticos também podem ter um impacto positivo na diarreia: ao aumentarem a produção bacteriana de ácidos gordos de cadeia curta (AGCC), como o butirato, que contribuem para a integridade da barreira intestinal; e ao antagonizarem a aderência dos agentes patogénicos às células epiteliais, inibindo assim a colonização e promovendo a eliminação dos agentes patogénicos do intestino.3
O transplante de microbiota fecal (TMF), que tem como objetivo restaurar uma microbiota intestinal saudável, provou ser eficaz e está apenas indicado no tratamento da infeção recorrente por C. difficile, tanto em adultos como em crianças.14
CASO CLÍNICO pelo Prof. Aldo Maruy
- Um menino de 2 anos de idade apresentou febre, dor abdominal e diarreia com muco e sangue. Tinha um historial de dois episódios semelhantes nos últimos seis meses, tratados apenas com antibióticos.
- Para evitar uma recaída, decidiu-se tratá-lo com antibióticos e probióticos. A diarreia cessou em 48 horas, o antibiótico foi suspenso ao 5.º dia, enquanto o probiótico foi mantido durante duas semanas; foi-lhe prescrita uma dieta rica em alimentos complementares e prebióticos.
- Para além de se tratar a infeção com antibióticos, recomenda-se, para prevenir um novo episódio diarreico, que a composição da microbiota intestinal seja restaurada através da dieta, juntamente com a administração de prebióticos e probióticos.

OPINIÃO DE ESPECIALISTA
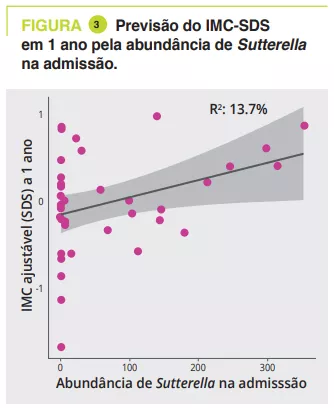
Ao longo da vida, uma microbiota saudável desempenha um papel importante na prevenção e tratamento da diarreia bacteriana. Há espécies específicas que demonstraram efeitos protetores contra a diarreia: Os taxa de Lactobacillus protegem contra a diarreia induzida por Shigella spp.; a presença de Sutterella spp., Prevotella copri e Bacteroides vulgatus prediz resistência à E. coli enterotoxigénica (ETEC). Por outro lado, a intervenção microbiana, através da modificação da dieta e da utilização de prebióticos, probióticos e TMF, pode regular a composição da microbiota intestinal para prevenir e tratar a diarreia. A investigação futura deverá expandir o nosso conhecimento do microbioma no que se refere à diarreia infeciosa, ajudando assim a conceber melhores intervenções preventivas e terapêuticas.
CONSEQUÊNCIAS DA DIARREIA DOS VIAJANTES
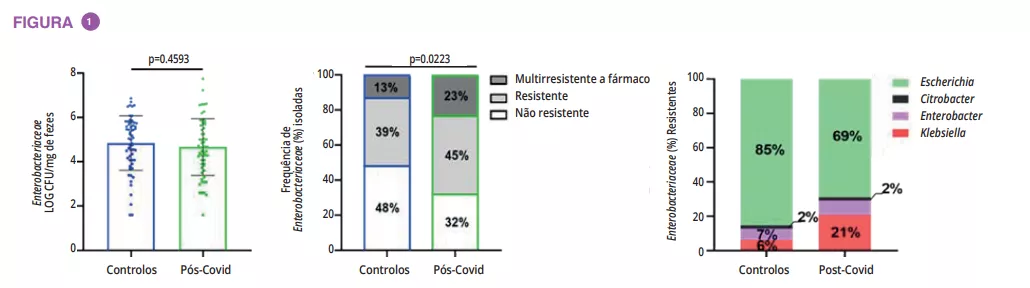
Quando visitam destinos de médio e alto risco, 10 a 70% dos viajantes de regiões com baixo risco de doenças infeciosas sofrem de diarreia. A diarreia do viajante é predominantemente causada por bactérias (≥80% a 90% dos casos), sendo os vírus intestinais responsáveis por um mínimo de 5% a 15% dos casos.52 As infeções por protozoários patogénicos poderão ser responsáveis por cerca de 10% dos diagnósticos, principalmente em pessoas que viajam por períodos prolongados. A microbiota dos viajantes que sofrem de diarreia apresenta uma muito maior variação ao longo da duração da sua estadia do que a dos viajantes saudáveis, associada a uma menor diversidade de base, que tem sido associada a uma maior suscetibilidade à infeção.51 Além disso, a diarreia reduz a capacidade de restabelecimento da microbiota (grande aumento da divergência em relação à linha de base) e leva à aquisição de organismos multirresistentes.51 Assim, de acordo com um estudo que incluiu 267 americanos que viajaram para fora dos Estados Unidos, um terço regressou com diarreia, 61% com disbiose intestinal e 38% com bactérias resistentes a antibióticos (a maioria E. coli), contribuindo para a disseminação global da resistência antimicrobiana.58
E. coli, Dorea fomigenerans, Bacteroïdes vulgarus, B. caocae, Odoribacter splanchnicus, etc.
Ruminococcus bromii, coprococcus, Clostridioides bartletti, etc.