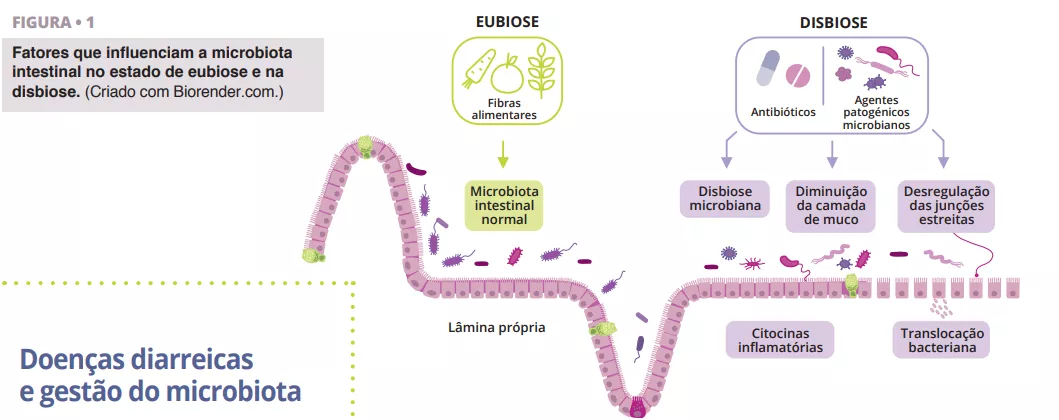
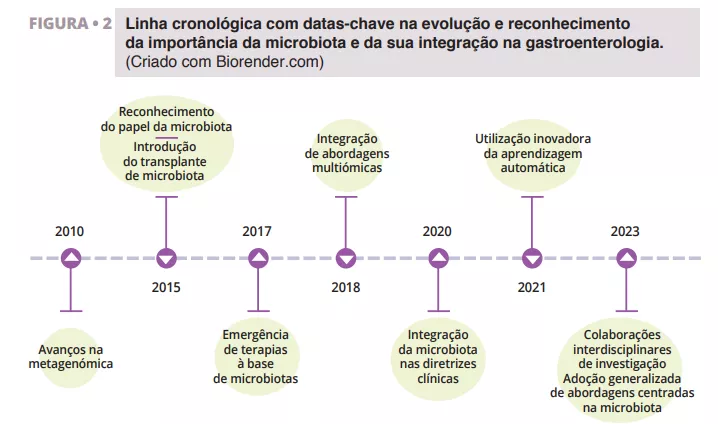
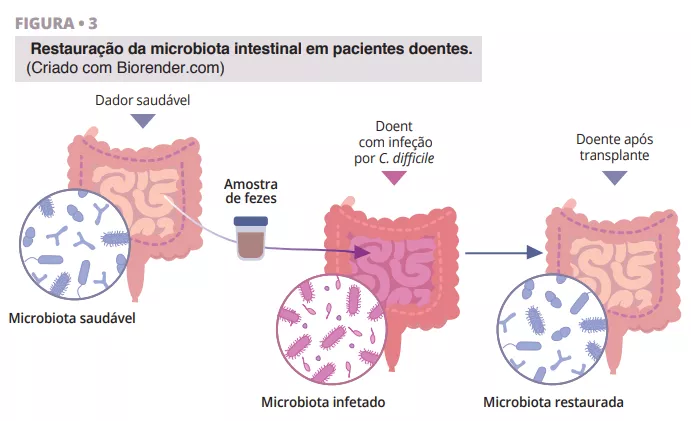
Transplante de microbiota fecal mais imunoterapia anti-PD-1 em melanoma avançado: um ensaio de fase I
ARTIGO COMENTADO - Fase adulta
Pelo Prof. Harry Sokol
Gastroenterologia e Nutrição, Hospital Saint-Antoine, Paris, França
Comentários sobre o artigo de Routy et al., Nature Medicine 2023 [1]
O transplante de microbiota fecal (FMT) representa uma estratégia potencial para ultrapassar a resistência aos inibidores do ponto de controlo imunitário em doentes com melanoma refratário; no entanto, o papel do FMT em contextos de tratamento de primeira linha não foi avaliado. Os autores realizaram um ensaio multicêntrico de Fase I que combinou FMT de dador saudável com os inibidores PD-1 nivolumab ou pembrolizumab em 20 doentes com melanoma avançado não tratados previamente. A segurança foi o objetivo primário. Não foram registados quaisquer eventos de grau 3 durante o FMT. Cinco pacientes (25%) apresentaram eventos adversos de grau 3 relacionados ao sistema imunológico devido à terapia combinada. Os principais endpoints secundários foram a taxa de resposta objetiva, alterações na composição do microbioma intestinal e análises imunológicas e metabolómicas sistémicas. A taxa de resposta objetiva foi de 65% (13 em 20), incluindo quatro (20%) respostas completas. A análise longitudinal do perfil do microbioma revelou que todos os doentes enxertaram estirpes dos seus respetivos dadores. No entanto, a semelhança adquirida entre os microbiomas do dador e do doente só aumentou ao longo do tempo nos doentes que responderam. Os respondedores registaram um enriquecimento de bactérias imunogénicas e uma perda de bactérias deletérias após a FMT. Os resultados mostraram que o FMT a partir de dadores saudáveis é seguro num contexto de primeira linha e justifica uma investigação mais aprofundada quando utilizado em combinação com inibidores do ponto de controlo imunitário.
O que é que já sabemos sobre isto?
Quase metade dos doentes com melanoma avançado que recebem monoterapia anti-PD-1 desenvolvem resistência primária, o que realça a necessidade de desenvolver novas estratégias terapêuticas para melhorar a resposta aos inibidores do ponto de controlo imunitário (ICI). Embora a combinação de anti-PD-1 e anti-CTLA4 (antigénio-4 associado aos linfócitos T citotóxicos) aumente a taxa de resposta, esta terapia é limitada pelo elevado número de eventos adversos relacionados com o sistema imunitário (EAI). O microbioma intestinal emergiu como um regulador essencial das respostas imunitárias locais e sistémicas. Vários estudos em doentes com cancro tratados com ICIs demonstraram que bactérias intestinais específicas estão associadas tanto à resposta do sistema imunitário como a eventos adversos [1]. Mais especificamente, a presença de certos géneros comensais, tais como Ruminococcus, Faecalibacterium e Eubacterium, foi associada a resultados positivos em doentes com melanoma [2]. O potencial terapêutico do microbioma intestinal foi demonstrado pela primeira vez em modelos de ratinhos combinando ICIs com FMT utilizando fezes de doentes não respondedores (NR) que estavam associados a resistência a ICIs [1]. Dois estudos mostraram que a FMT em doentes com uma resposta a longo prazo à terapêutica com ICI contornou a resistência aos anti-PD-1 em quase 30% dos doentes com melanoma refratário aos ICI [3, 4]. Nestes estudos, a microbiota dos doentes alterou-se após a FMT, tendo sido observado um aumento de Ruminococcaceae e Bifidobacteriaceae nos doentes que responderam (R), bem como uma reprogramação do microambiente tumoral com um aumento da infiltração de células T CD8+ e da sinalização de interferão-γ. Estes resultados clínicos confirmam o potencial das intervenções baseadas em microbiomas para ultrapassar a resistência aos ICI no melanoma.
Quais são as principais conclusões deste estudo?
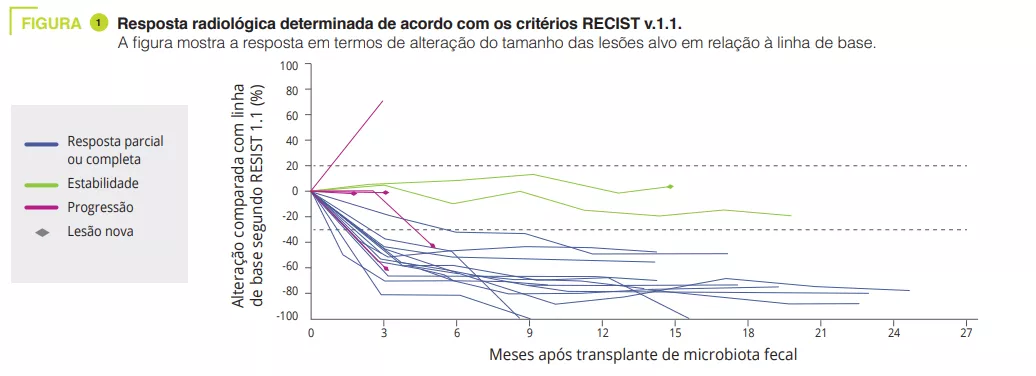
Neste artigo, os autores relataram os resultados clínicos e translacionais de um ensaio de Fase I (NCT03772899) que combinou FMT de dadores saudáveis com os inibidores PD-1 nivolumab ou pembrolizumab em doentes virgens de tratamento com melanoma avançado (figure 1). A toxicidade observada (85% de IR-AEs, dos quais 25% de toxicidade de grau 3 e zero de toxicidade de grau 4 ou 5) foi semelhante à relatada nos ensaios de Fase III para anti-PD-1. A eficácia clínica observada (resposta objetiva de 65%) foi superior à da monoterapia com nivolumab e pembrolizumab nos ensaios de Fase III (resposta objetiva de 42-45%) e nos dados do mundo real (resposta objetiva de 17,2-51,6%). No entanto, a ausência de um braço de controlo e a dimensão reduzida do estudo dificultaram a interpretação dos resultados.
Unlike the previous studies [3, 4], it included patients receiving first-line treatment, a single FMT was performed by oral capsule, donors were healthy subjects (and not ICI responders) and, finally, only PEG (without the use of antibiotics) was used for the preparation. By studying the Ao contrário dos estudos anteriores [3, 4], este incluiu doentes a receber tratamento de primeira linha, foi realizada uma única FMT por cápsula oral, os dadores eram indivíduos saudáveis (e não respondedores à ICI) e, finalmente, apenas foi utilizado PEG (sem o uso de antibióticos) para a preparação. Ao estudar a microbiota dos dadores e dos recetores, os autores observaram que a microbiota dos respondedores era enriquecida em Ruminococcus SGB15234 e SGB15229, Alistipes communis, Eubacterium ramuleus e Faecalibacterium SGB15346, enquanto a abundância de Enterocloster aldensis e Enterocloster clostridioformis diminuía. Em estudos anteriores, o aumento de Faecalibacterium foi também associado à resposta à ICI [3, 4].
Os autores experimentaram depois em ratinhos colonizados com microbiota humana e observaram uma eficácia semelhante do transplante fecal de indivíduos saudáveis neste contexto, com um efeito associado a um aumento da infiltração de linfócitos T de memória CD8+ no microambiente tumoral.
Quais são as consequências práticas?
Apesar das suas limitações, este estudo sugeriu que a modulação da microbiota através da FMT poderia aumentar a eficácia da ICI quando administrada num cenário de primeira linha para o melanoma metastático. Embora a utilização em larga escala da FMT pareça difícil na prática atual, a modulação da microbiota, em particular com probióticos de nova geração, em combinação com ICI poderia tornar-se um tratamento padrão.
- A microbiota intestinal desempenha um papel na resposta à ICI.
- O FMT de dadores saudáveis é viável e seguro em doentes tratados com ICI numa configuração de primeira linha para melanoma metastático.
- Apesar das limitações associadas à ausência de um braço de controlo e à pequena dimensão do estudo, a eficácia clínica observada nos doentes que receberam FMT em combinação com ICI foi superior à da monoterapia com ICI nos ensaios de Fase III e nos dados do mundo real.
CONCLUSÃO
Este estudo demonstrou que o FMT de dadores saudáveis é viável e seguro em doentes tratados com ICI numa situação de primeira linha para melanoma metastático. A modulação da microbiota através da FMT ou de outros métodos pode aumentar a eficácia da ICI, embora sejam necessários estudos controlados de maior dimensão para confirmar os dados.
1. Routy B, Lenehan JG, Miller WH Jr, et al. Fecal microbiota transplantation plus anti-PD-1 immunotherapy in advanced melanoma: a phase I trial. Nat Med 2023; 29: 2121-32.
2. Gopalakrishnan V, Spencer CN, Nezi L, et al. Gut microbiome modulates response to anti-PD-1 immunotherapy in melanoma patients. Science 2018 ; 359 : 97–103.
3. Baruch EN, Youngster I, Ben-Betzalel G, et al. Fecal microbiota transplant promotes response in immunotherapy-refractory melanoma patients. Science 2021 ; 371 : 602–9.
4. Davar D, Dzutsev AK, McCulloch JA, et al. Fecal microbiota transplant overcomes resistance to anti-PD-1 therapy in melanoma patients. Science 2021 ; 371 : 595–602.