МИКРОБИОМ ПИЩЕВОДА – ПРИЧИНА ИЛИ СЛЕДСТВИЕ НАРУШЕНИЙ ФУНКЦИЙ ПИЩЕВОДА?
ОБЗОР ЛИТЕРАТУРЫ
Автор: проф. Маркку Воутилайнен (Markku Voutilainen)
Медицинский факультет Университета Турку; больница Университета Турку, отделение гастроэнтерологии, Турку, Финляндия
Illustration showing gastroesophageal reflux.
В западном мире распространена гастроэзофагеальная рефлюксная болезнь. Синдром Баррета (СБ) является осложнением рефлюксной болезни и основным фактором риска развития аденокарциномы пищевода, при которой пятилетняя выживаемость составляет менее 20 %.
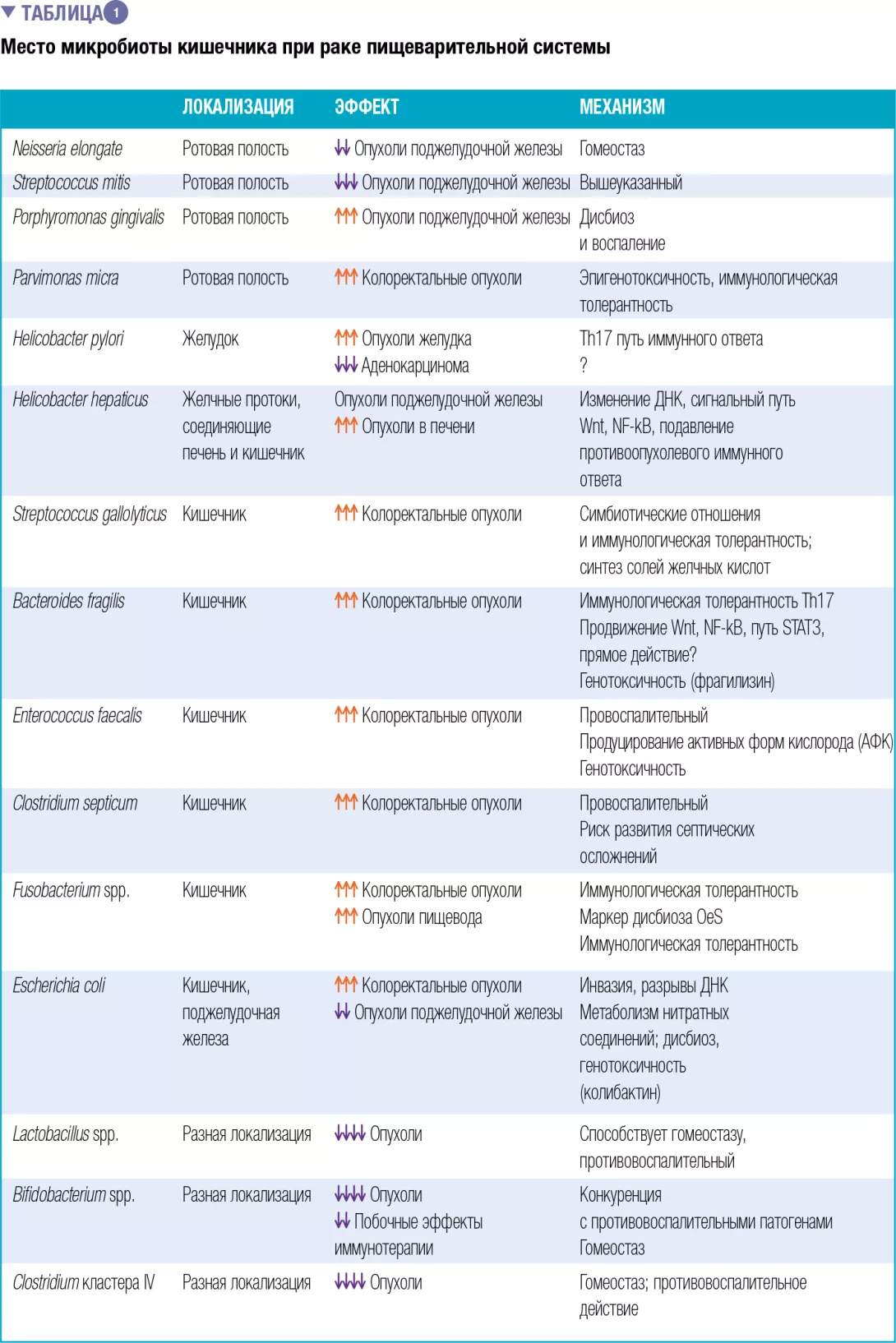
В недавнем обзоре изучалась роль микробиома пищевода при СБ и раке пищевода (3). Пищевод подвергается воздействию поступивших из полости рта микроорганизмов, а также микроорганизмов из содержимого желудка, поступившего в пищевод в результате рефлюкса. Микробиота пищевода не похожа ни на микробиоту полости рта, ни на микробиоту желудка. Первыми бактериями, обнаруженными в пищеводе, были Strectococcus viridans и Streptococcus группы D. Позднее были обнаружены шесть типов при секвенировании клона гена 16S рибосомальной ДНК широкого спектра, включая Firmicutes, Bacteroidetes, Actinobacteria, Proteobacteria, Fusobacteria и Streptococcus. СБ и дисплазия высокой степени были связаны с наибольшим количеством бактерий. У пациентов с эзофагитом и СБ количество Streptococcus уменьшилось, а количество грамотрицательных анаэробов и микроаэрофилов увеличилось.
СБ и аденокарцинома пищевода связаны с увеличением количества Escherichia coli. Другим грамотрицательным видом бактерий, обнаруженным у пациентов с раком пищевода, является Fusobacterium nucleatum. Кроме того, дисбиоз полости рта может быть связан с повышенным риском развития рака пищевода, в то время как желудочные бактерии Helicobacter pylori, по-видимому, защищают от развития рака пищевода. Дисбиоз желудка с увеличением численности бактерий Clostridiales и Erysipelotrichaceae связан с плоскоклеточной карциномой пищевода. Также грибы, например Candida albicans и C. glabrata, часто обнаруживаются во взятых из пищевода образцах у пациентов с аденокарциномой пищевода. Эпидемиологическое исследование показало дозозависимую связь между использованием пенициллина и повышенным риском развития рака пищевода. Также ингибиторы протонной помпы модифицируют микробиом желудка и пищевода.
Эти данные по микробиоте пищевода были получены у небольших, выбранных популяций пациентов с симптоматическим лечением в ходе кросс-секционных исследований. Таким образом, нельзя сделать никаких выводов о причинно-следственной связи между микробиотой пищевода и заболеваниями пищевода. Только у небольшой части пациентов с СБ развивается аденокарцинома, и необходимо проведение дальнейших исследований, чтобы определить роль дисбиоза пищевода в патогенезе рака. Одной из тем для дальнейших исследований является влияние ингибиторов протонной помпы на микробиоту пищевода и на риск возникновения заболеваний пищевода [3].
Эозинофильный эзофагит (ЭЭ) является аллергиче- ским хроническим воспалительным заболеванием, которое является наиболее распространенной причиной дисфагии у детей и молодых людей в развитых странах. ЭЭ имеет общие с другими аллергическими заболеваниями признаки воспаления, и воздействие аллергена, вероятно, играет центральную роль в патогенезе ЭЭ. Капуцилли (Capucilli) и Хилл (Hill) рассмотрели эпидемиологию, патогенез и лечение ЭЭ [4]. Микробиота пищевода может быть вовлечена в патогенез ЭЭ. Пищевод колонизируется сотнями видов бактерий, наиболее распространенными из которых являются представители типа бактерий Firmicutes и Bacteroidetes [4]. У пациентов с ЭЭ в активной стадии количество бактерий рода Streptococcus и Atopobium уменьшается, тогда как количество Neisseria и Corynebacterium увеличивается. Другое исследование показало, что общее количество бактерий пищевода и представителей рода Haemophilus особенно увеличилось при ЭЭ. Ингибиторы протонной помпы, которые используются при лечении ЭЭ, вызывают увеличение количества бактерий типа Proteobacteria. Бактериальная обсемененность пи- щевода увеличивается у пациентов с ЭЭ независимо от лечения или степени тяжести эозинофильной инфильтрации слизистой оболочки пищевода. Как и при других аллергических и аутоиммунных заболеваниях, повышенный риск развития ЭЭ связывают с лечением антибиотиками и родоразрешением путем кесарева сечения [4].
ЗАКЛЮЧЕНИЕ
Были проведены кросс-секционные исследования, и данные о стабильности микробиоты пищевода с течением времени отсутствуют. Необходимо проведение дополнительных исследований для определения роли микробиоты пищевода в патогенезе и активации ЭЭ.