МЕТАГЕНОМИКА ФЕКАЛЬНОГО ВИРОМА: КУМУЛЯТИВНОЕ ВЛИЯНИЕ КОЛИЧЕСТВА ПРИНИМАЕМОГО ГЛЮТЕНА И ЭНТЕРОВИРУСНОЙ НАГРУЗКИ НА РИСК РАЗВИТИЯ ЦЕЛИАКИИ У ПРЕДРАСПОЛОЖЕННЫХ ДЕТЕЙ. ДАННЫЕ ИССЛЕДОВАНИЯ TEDDY
РЕЦЕНЗИИ - РАЗДЕЛ ДЕТИ
Профессор Эммануэль Мас (Pr. Emmanuel Mas)
Отделение гастроэнтерологии и питания, Детская больница, Тулуза, Франция
Комментарий к оригинальной статье Линдфорс и соавт.( Lindfors et al. Gut 2019) [1]
Повышенное потребление глютена, частые желудочно-кишечные инфекции и аденовирус, энтеровирус, ротавирус и реовирус — все эти факторы были предложены в качестве средовых триггеров целиакии. Однако неизвестно, существует ли связь между количеством потребляемого глютена, действием вирусов и развитием целиакии. Авторы этого исследования поставили цель определить, являются ли вирусные инфекции сами по себе или в сочетании с потреблением глютена факторами риска целиакии у генетически предрасположенных детей. Был сделан вывод, что частые энтеровирусные инфекции в возрасте от 1 до 2 лет действительно связаны с повышенным риском развития целиакии, что указывает на кумулятивный эффект взаимодействия между энтеровирусами и повышенным потреблением глютена.
ЧТО НАМ УЖЕ ИЗВЕСТНО?
Целиакия — аутоиммунное заболевание, которое возникает у генетически предрасположенных людей с генотипом HLA DQ2 и/или DQ8 и характеризуется атрофией ворсинок и инфильтрацией эпителия тонкой кишки лимфоцитами. Глютен, присутствующий в рационе, вызывает аутоиммунный ответ, направленный против тканевой трансглутаминазы. Появление антител к трансглутаминазе указывает на наличие целиакии.
Рост числа аутоиммунных заболеваний вызывает подозрение, что факторы окружающей среды могут играть роль в их патогенезе. Данные наблюдательных исследований показывают, что вирусные инфекции могут вызывать потерю толерантности к глютену пищи и развитию целиакии.
ОСНОВНЫЕ РЕЗУЛЬТАТЫ
Это исследование случай-контроль внутри когортного исследования TEDDY (средовые детерминанты сахарного диабета у детей) включало 8676 детей в возрасте до 4,5 месяцев, которых наблюдали до возраста 15 лет. Основная цель исследования состояла в определении генетических и средовых факторов, связанных с развитием сахарного диабета 1 типа и целиакии. После формирования пар, подобранных по семейному анамнезу сахарного диабета 1 типа, полу и месту включения в исследование, в окончательный анализ вошли 83 пары (ребенок с предрасположенностью (случай) и контроль), для которых были доступны данные по составу фекального вирома после включения в рацион глютена. Из этих пар 16 имели семейный анамнез сахарного диабета 1 типа. В ходе последующего наблюдения у 28 детей с аутоиммунным статусом развилась целиакия.
У детей в возрасте от 3 месяцев до 2 лет каждый месяц собирали образцы стула и проводили тесты на наличие энтеровируса, аденовируса, астровируса, норовируса, реовируса и ротавируса. Каждые 3 месяца родители детей заполняли опросник по питанию, использовавшийся для сбора информации о грудном вскармливании и возрасте введения в рацион продуктов, содержащих глютен. Ведение дневника приема пищи позволило рассчитать количество глютена, потребленного за 6, 9, 12, 18 и 24 месяца.
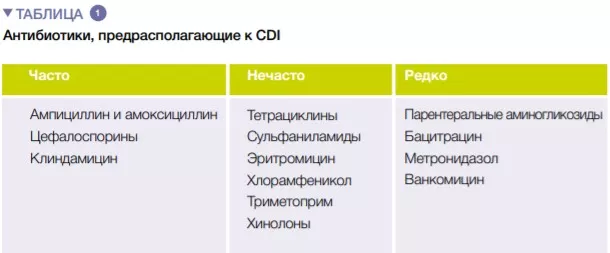
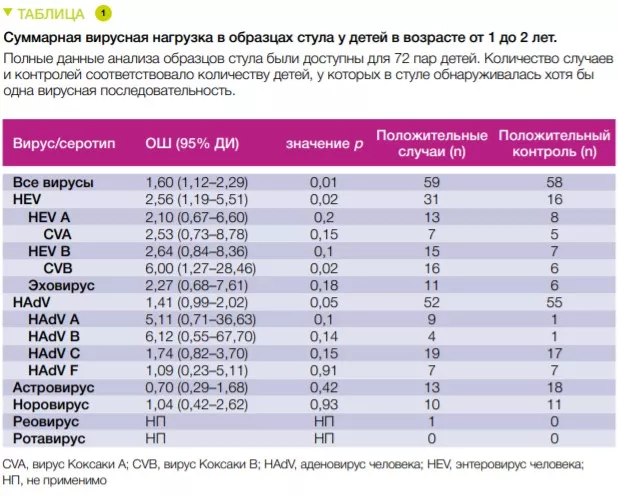
Доля образцов кала, содержащих любой из вирусов, колебалась от 22 до 50% без каких-либо возрастных пиков. Для энтеровирусов этот показатель составлял от 0 до 21% через 6 месяцев. В период от 1 до 2 лет энтеровирусы были обнаружены у 31 ребенка по сравнению с 16 в группе контроля (табл. 1). Суммарное количество образцов кала, содержащих какой-либо вирус, ассоциировалось с повышенным риском целиакии (ОШ 1,60; р = 0,01), причем для энтеровирусов эта ассоциация была наиболее сильной (ОШ 2,56; p = 0,02).
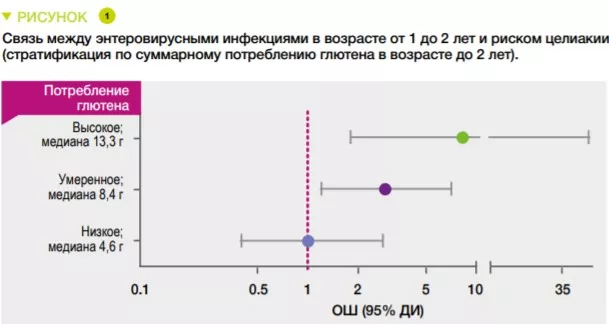
Риск целиакии не увеличивался при вирусных инфекциях, развившихся после возраста введения в рацион глютена, если грудное вскармливание все еще продолжалось. Напротив, после прекращения кормления грудью в образцах стула, собранных в возрасте от 1 до 2 лет после введения глютена, и суммарное число обнаруженных вирусов (ОШ 1,41; р = 0,05) и количество энтеровирусов (ОШ 2,47; р = 0,03) ассоциировались с риском целиакии. Между обнаружением энтеровируса в период между 1 и 2 годами и количеством глютена, потребленного до возраста 2 лет, существует значимая связь с риском развития целиакии (p = 0,03). Предполагается, что этот показатель растет по мере увеличения потребления глютена (Рисунок 1).
КЛЮЧЕВЫЕ ПОЛОЖЕНИЯ
-
Факторы окружающей среды играют определенную роль в развитии целиакии.
-
Контакт с энтеровирусом является фактором риска образования антител к трансглутаминазе у детей с наличием HLA DQ2 и/или DQ8.
-
Этот риск возрастает при потреблении большого количества глютена.
ЧТО ЭТО ЗНАЧИТ НА ПРАКТИКЕ?
Результаты этого исследования указывают на важность профилактики целиакии у детей из группы риска. Этого можно достичь путем тщательного контроля количества потребляемого глютена, в особенности, если ребенок перенес энтеровирусную инфекцию в период, когда он больше не находится на грудном вскармливании.
ВЫВОДЫ
Существует связь между энтеровирусными инфекциями желудочно-кишечного тракта и риском развития целиакии у детей из группы генетического риска. Этот риск увеличивается по мере поступления в организм большего количества глютена.