Дисбиоз
Знаете ли вы, что такое «дисбиоз»? Этим термином обозначают нарушение хрупкого баланса взаимоотношений миллиардов микроорганизмов, которые составляют нашу микробиоту, друг с другом и нашим организмом. Существует целый ряд факторов, которые приводят к дисбиозу. В частности, это генетические факторы, несбалансированная диета и антибиотики, причем в большинстве случаев дисбиоз вызывается сочетанием нескольких факторов. Научные исследования показали, что дисбиоз наиболее хорошо изученной микробиоты — микробиоты кишечника (а также других микробиот — влагалища, кожи и легких) — связан с различными заболеваниями, начиная от синдрома раздраженного кишечника и заканчивая ожирением, хроническим синуситом и экземой.
Но что именно приводит к дисбалансу микробиоты? Как дисбиоз влияет на наше здоровье? Как можно восстановить нарушенный баланс микробиоты? В данной статье мы ответим на эти вопросы.

Что такое дисбиоз?
Сначала рассмотрим само слово «дисбиоз». Этимология этого научного термина на самом деле очень простая.По-гречески слово bios означает «живой», а префикс dys - «плохой».
«Дисбиоз» можно определить как изменение состава и процессов функционирования микробиоты. Это изменение является результатом воздействия как факторов окружающей среды, так и факторов, связанных с конкретным человеком1
Природа дисбиоза: микробиота кишечника
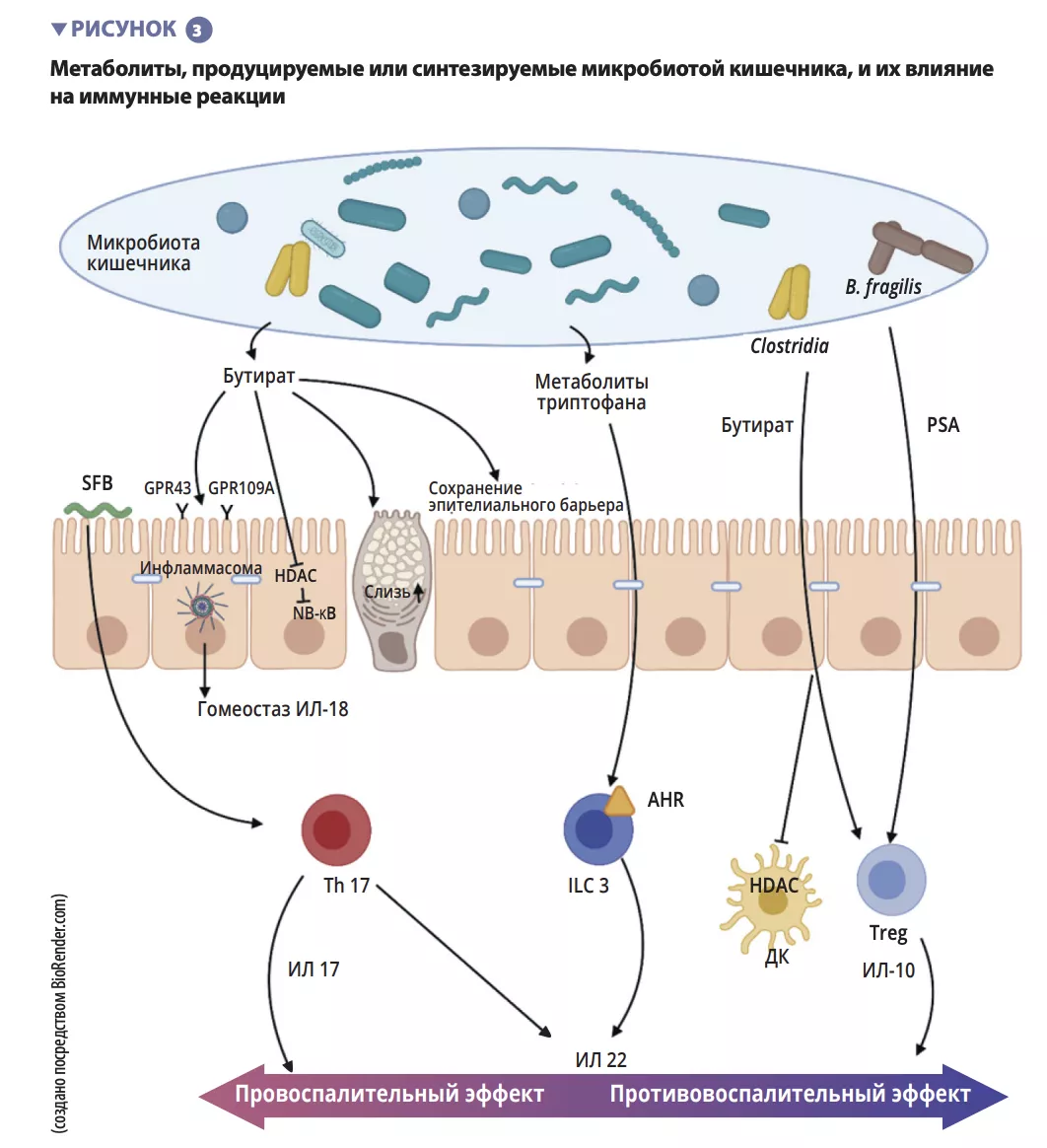
Наша кишечная микробиота — самая главная микробиота организма2. Она содержит не менее 1000 различных3 видов микроорганизмов — бактерий, грибов и вирусов. Группа бактерий Firmicutes (в которую входят хорошо изученные «благотворные» бактерии — лактобактерии) и группа бактерий Bacteroidetes вместе составляют 70–90% бактериального сообщества в нашей кишечной флоре2,4. Также наша микробиота содержит актинобактерии, к которым относятся бифидобактерии, известные своими полезными свойствами. Но в нашей микробиоте есть и бактерии, размножение которых может причинить ущерб нашему здоровью.Их называют « (sidenote: патоген это микроорганизм, который вызывает или может вызвать заболевание; см. Pirofski LA, Casadevall A. Q and A: What is a pathogen? A question that begs the point. BMC Biol. 2012 Jan 31;10:6. ) »,и обычно они находятся в меньшинстве 2. Термином «дисбиоз» описывают одно или несколько следующих состояний:
- значительное изменение относительного содержания основных семейств бактерий — в частности, снижение численности лактобактерий и бифидобактерий5;
- падение численности или полное исчезновение полезных микроорганизмов, обычно присутствующих в нашей микробиоте (так называемых «комменсальных» микроорганизмов)1;
- снижение разнообразия микроорганизмов микробиоты — уменьшение количества составляющих ее видов5;
- рост потенциально патогенных микроорганизмов в микробиоте1,5.
В результате наша микробиота ослабевает и «болезнетворные» бактерии берут верх над «благотворными»2. Микробиоте становится труднее защищать организм человека от заболеваний и выполнять свои основные функции, связанные с поддержанием нашего здоровья и благополучия1,6.
1000 Она содержит не менее 1000 различных видов микроорганизмов
Наш собственный уникальный дисбаланс микробиоты
Однако «дисбиоз» не является универсальным термином, который можно применить к любому человеку при любых обстоятельствах1. На самом деле состав микробиоты индивидуален, и на него влияют наши гены, а также микроорганизмы, которые колонизировали организм в первые годы нашей жизни («микроорганизмы» — это «очень мелкие живые организмы, которые нельзя увидеть невооруженным глазом», в их число входят бактерии, вирусы, грибы, археи, простейшие и т. д., в совокупности называемые « (sidenote: https://microbiologysociety.org/why-microbiology-matters/what-is-microbiology.html ) ». Микробиота настолько сильно варьируется от человека к человеку, что вполне может рассматриваться в качестве такой же уникальной характеристики, как и отпечатки пальцев7. Более того, она меняется в зависимости от нашего возраста, состояния здоровья, уровня стресса и рациона питания, а также от того, в каком месте мы живем и какие лекарства принимаем8. Это означает, что у каждого из нас может возникать свой специфический дисбиоз, при котором микробиота становится несбалансированной и перестает правильно функционировать в организме1.
Что такое сбалансированная микробиота?
Приставка dys- в слове «дисбиоз» противоположна по смыслу приставке eu- («благо-») или sym- («с»). Таким образом, можно говорить об «эубиозе» или «симбиозе», когда наша микробиота находится в здоровом состоянии, т. е. гармонично взаимодействует с нашим организмом, а ее микробное сообщество находится в равновесии1.
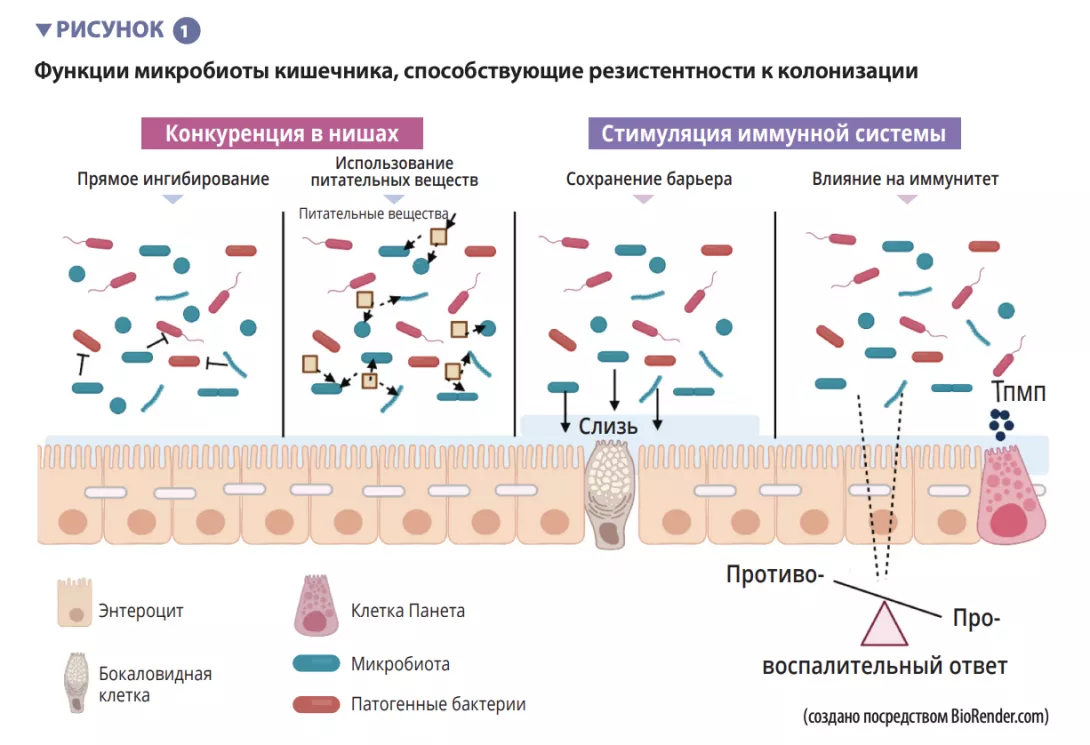
Отношения между нашим организмом и миллиардами микробов, которые составляют нашу микробиоту, — пример взаимовыгодного сотрудничества9. Каждый его участник играет отведенную ему роль: организм обеспечивает микробам «еду и кров», а микробы в свою очередь способствуют выполнению множества важных функций в организме, таких как пищеварение, усвоение питательных веществ, сохранение непроницаемости стенок кишечника и борьба с нежелательными микробами2,8,10. Это настоящая командная работа!
Различные микроорганизмы, составляющие микробиоту (в том числе потенциально патогенные), присутствуют в достаточном количестве и пропорциях, позволяющих мирно сосуществовать и выполнять свои полезные функции в организме. Тем не менее хрупкий баланс между микробными экосистемами в нашем организме может быть нарушен, и в этот момент эубиоз превращается в дисбиоз8.
Что вызывает дисбиоз?
Как следует из определения, дисбиоз возникает под влиянием целого ряда совершено различных и нередко взаимосвязанных факторов5. Перечислим наиболее распространенные из них.
Факторы, связанные с самим человеком:
- генетическая предрасположенность1;
- возраст11;
- некоторые заболевания и травмы1.
Факторы, связанные с окружающей средой:
- применение лекарственных препаратов — антибиотиков, противовоспалительных средств и т. д.2,5;
- инфекции12;
- образ жизни — несбалансированное питание или изменения в рационе питания, стресс, курение, плохая гигиена и т. д.1,5,8;
- загрязнение воздуха8.
Факторы, на которые следует обратить внимание
Открытие антибиотиков стало одним из важнейших открытий медицины XX века. С тех пор, как в 1928 году был открыт пенициллин, они спасли миллионы жизней . Однако, без разбора уничтожая благотворные и вредные бактерии, они нарушают баланс микробиоты. В краткосрочной перспективе дисбиоз, вызванный антибиотиками, может привести к развитию диареи или вагинальной молочницы . Также ученые предполагают, что дисбиоз кишечника, вызванный антибиотиками, оказывает долгосрочные эффекты, особенно при получении антибиотиков в детском возрасте, повышая риск возникновения различных хронических заболеваний, таких как ожирение и аллергия16.
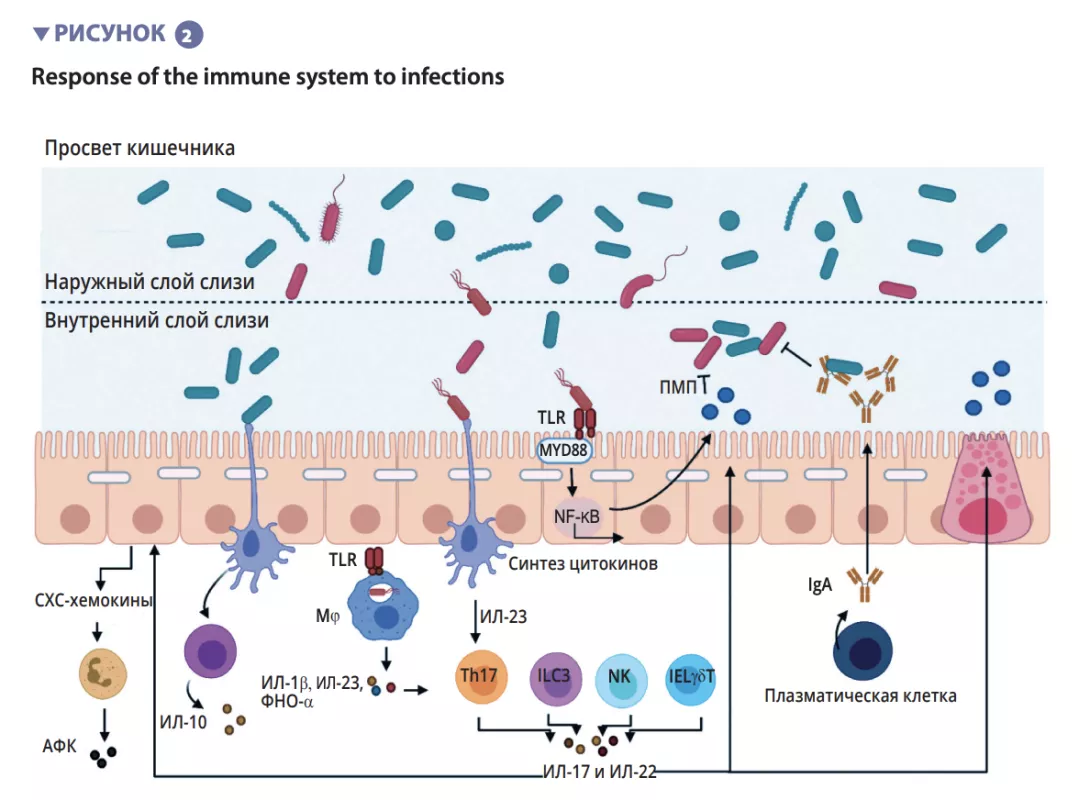
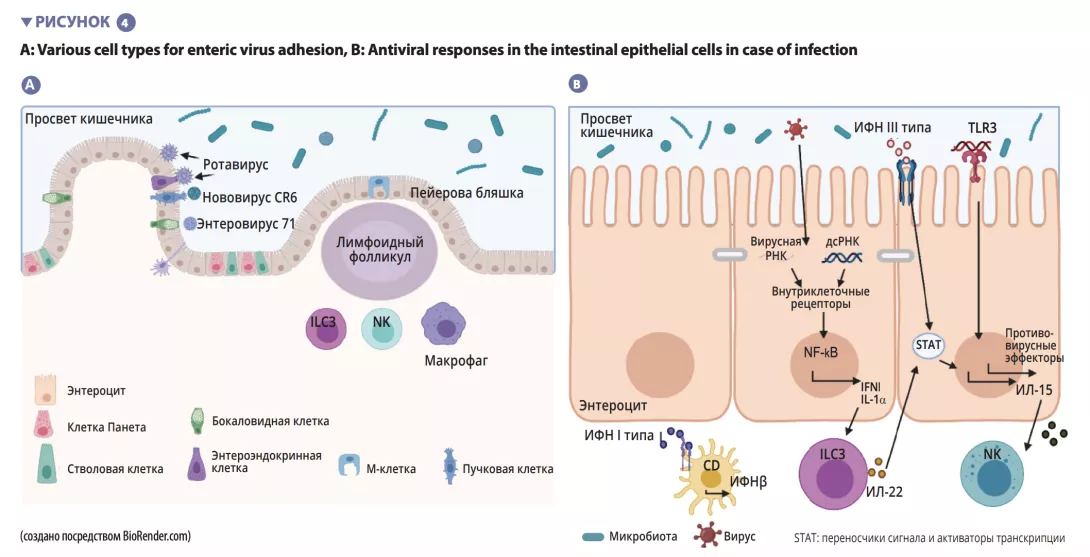
При таких инфекциях, как вирусный гастроэнтерит или пищевое отравление, вызванное сальмонеллой, в микробиоту проникают болезнетворные и агрессивные микробы. Они происходят не из самой микробиоты, а попадают в нее извне, передаваясь, например, через немытые руки или с загрязненной пищей. Эти инфекции вызывают сильную реакцию со стороны нашей иммунной системы, воспаление кишечника и диарею. Все это приводит к резкому нарушению равновесия нашей кишечной флоры. Более того, микробы, вызывающие эти инфекции, могут стимулировать рост других потенциально патогенных бактерий, уже присутствующих в микробиоте. Поэтому инфекции приводят к дисбиозу, которым пользуются любые болезнетворные бактерии1,12,17,18!
Состав еды влияет на нашу микробиоту на протяжении всей нашей жизни. Любые внезапные качественные и количественные изменения в рационе питания могут вызвать дисбиоз. Это не сиюминутный процесс: нормальные постепенные изменения в нашем рационе вызывают лишь временные изменения со стороны микробиоты, а тип пищи, которую мы едим, может вызвать длительные изменения в экосистеме желудочно-кишечного тракта5 и в конечном итоге стать фактором развития дисбиоза. Исследования показывают, что «западные» диеты, богатые жирами, сахарами и белками, повышают восприимчивость к нарушению баланса микробиоты кишечника, тогда как различные варианты диеты, богатой фруктами и овощами, могут защитить микробиоту от дисбиоза1,19.
Как можно восстановить нарушенный баланс микробиоты?
Как правило, после эпизода дисбиоза микробиота способна самостоятельно восстановить первоначальный баланс (хотя ее состав уже не будет в точности тем, какой был раньше): это своеобразный «эффект памяти»20. Но иногда этот «ре-биоз», или возврат к микробному равновесию, может занять длительное время: например, после приема антибиотиков даже у здорового взрослого человека на это может уйти 6 месяцев21. А иногда дисбиоз приводит к постоянному дисбалансу — ситуации, когда микробиота уже не способна возвратиться в нормальное состояние полностью, что может быть вредно для здоровья1.
Дисбиоз — причина или следствие болезни?
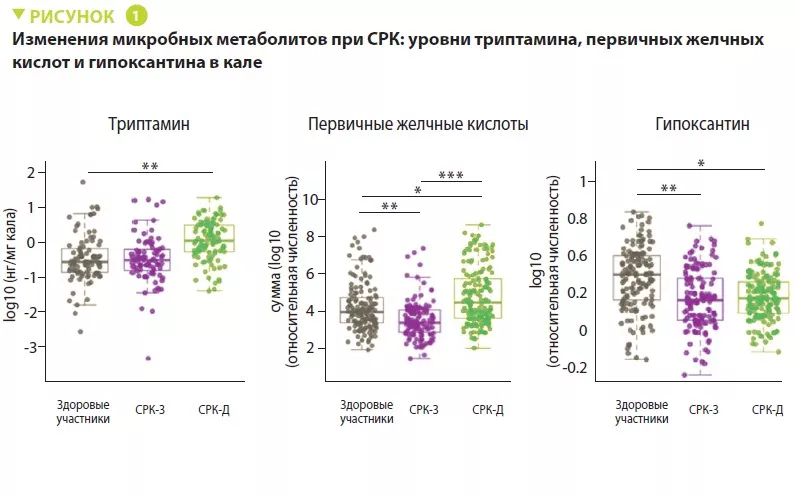
Многочисленные исследования по сравнению микробиоты больных и здоровых людей показали, что дисбиоз связан с целым рядом хронических заболеваний, таких как кишечные заболевания (синдром раздраженного кишечника и болезнь Крона), ожирение, аллергия, бронхиальная астма и некоторые виды злокачественных опухолей1. Но является ли дисбиоз причиной болезни или сама болезнь вызывает дисбиоз? Ученые не знают ответа на этот вопрос, и в настоящее время ведутся многочисленные исследования с целью это выяснить.
В 2019 году исследователи запустили Homo symbiosus — масштабный исследовательский проект, целью которого является поиск ответа на приведенный выше вопрос, а также сбор информации о связи различных хронических заболеваний с дисбиозом кишечника. Научная гипотеза заключается в том, что дисбиоз кишечника, рост микроорганизмов, воспаление и увеличение проницаемости стенки кишечника — взаимоподдерживающиеся процессы10.
Дисбиоз и заболевания, связанные с конкретной микробиотой
Дисбиоз кишечной микробиоты связан с различными заболеваниями органов желудочно-кишечного тракта, нарушениями метаболизма22, аллергиями23 и даже психическими24 расстройствами. Наряду с кишечной микробиотой в организме человека существуют уникальные микробные экосистемы, населяющие кожу25, мочевыводящие пути26, влагалище27, ротовую полость28 и легкие29. И в каждой из этих микробиот может возникнуть дисбаланс, создающий условия для развития определенных заболеваний.
Дополнительная информация о дисбиозе:
Восстановление баланса микробиоты = восстановление здоровья
Что делать, если у вас дисбиоз? Существует несколько потенциальных решений, которые помогут восстановить баланс микробиоты и укрепить здоровье.
Пробиотики — это «живые микроорганизмы, которые при употреблении в достаточном количестве приносят пользу здоровью человека»30,31. Здесь вы найдете информацию о пробиотиках: как они работают, как производятся и как выбрать для себя правильный пробиотик. Ознакомьтесь с нашей страницей о пробиотиках.
Пребиотики, получаемые в основном из пищевых волокон (фруктоолигосахариды, галактоолигосахариды, инулин и т. д.) — это неперевариваемые питательные вещества или субстраты, которые используются микроорганизмами микробиоты и положительно влияют на здоровье32,33. По этой ссылке можно узнать дополнительную информацию о том, как пребиотики влияют на микробиоту. Специальные продукты, содержащие пробиотики и пребиотики, называются симбиотиками34,35.
Особенности, а также качество и разнообразие пищи влияют на баланс кишечной микробиоты36,37, но также могут влиять на ее состав и, как следствие, вызывать определенные заболевания22. Проконсультируйтесь у своего врача и/или диетолога по поводу того, какие продукты полезны или вредны для вашего кишечника38.
Как и другие органы тела, микробиота может быть пересажена от одного человека к другому с целью восстановить баланс микробной экосистемы реципиента39,40. В настоящее время трансплантация микробиоты кишечника получает все более широкое признание. В этом контексте она известна как трансплантация фекальной микробиоты (ТФМ) и разрешена только для лечения рецидивирующих инфекций, вызванных Clostridioides difficile41. В настоящее время ведутся активные исследования ее применения при других заболеваниях кишечника41. Трансплантация влагалищной микробиоты (ТВМ) в настоящее время находится на этапе экспериментального применения и вполне может стать перспективным методом лечения рецидивирующего или рефрактерного бактериального вагиноза41. Исследования по трансплантации микробиоты кожи проводятся редко, однако полученные результаты достаточно многообещающие42,43.