МИКРОБИОТА КОЖИ #11
Профессор Маркку Вотилайнен
Медицинский факультет Университета Турку; Университетская клиника Турку, отделение гастроэнтерологии, Турку, Финляндия


Профессор Маркку Вотилайнен
Медицинский факультет Университета Турку; Университетская клиника Турку, отделение гастроэнтерологии, Турку, Финляндия

Kim HS, Yosipovitch G. The Skin Microbiota and Itch: Is There a Link? J Clin Med 2020 ; 9 : 1190.
Авторы обсуждают роль микробиоты кожи в патогенезе зуда. Ощущение зуда формируется в эпидермальных нервных волокнах под действием химических медиаторов, образующихся в результате сложного взаимодействия между кератиноцитами (KЦ), воспалительными клетками, нерв - ными окончаниями и микробиотой кожи. Дисбиоз кожи характеризуется выработкой протеаз, различных молекул, связанных с патогенами, и токсинов, что приводит к повреждению кожного барьера. Дегрануляция тучных клеток под действием дельта-токсина способствует развитию воспаления и зуда. Микробиота кожи и мозг взаимодействуют с помощью ней - рохимических медиаторов (ацетилхолин, гистамин, катехоламины, кортикотропин), которые синтезируются микробиотой кожи. Стресс усиливает зуд через ось «кожаголовной мозг». Считают, что в миндале - видном теле под действием микробных сигналов может изменяться ощущение зуда. При хроническом стрессе увеличива - ется выработка кортизола, который непо - средственно активирует кожные бактерии, что увеличивает вирулентность патогеных форм. Это приводит к ослаблению кожного барьера и усилению зуда. Авторы заклю - чают, что косметические/трансдермальные препараты, модулирующие микробиоту кожи, потенциально могут уменьшать ощу - щение зуда.
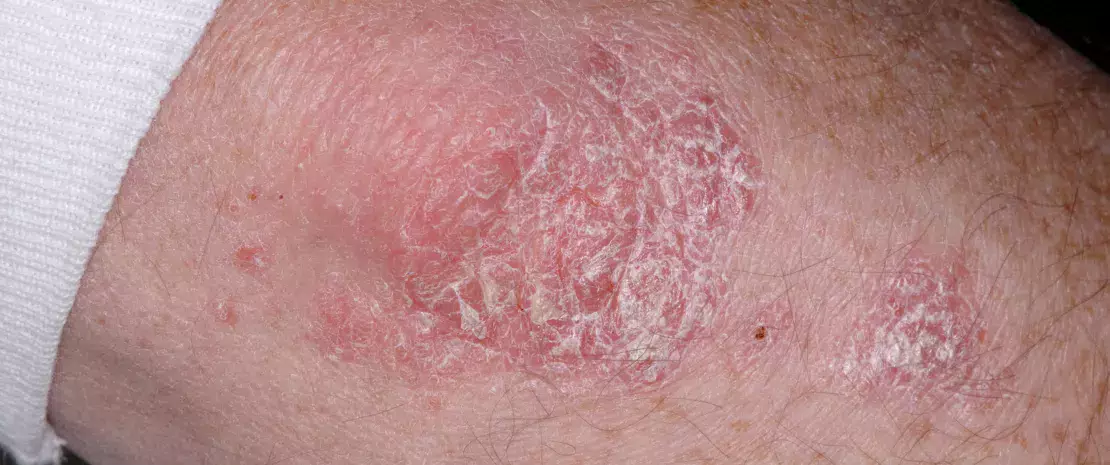
Авторы исследовали микробиоту псориатических бляшек и непораженной кожи у пациентов с обыкновенным псориазом (ОП) и здоровых добровольцев контрольной группы с помощью количественной ПЦР и секвенирования 16S рРНК. В отличие от непораженной и здоровой кожи, псориатические бляшки характеризовались более высокой бактериальной нагрузкой и меньшим микробным разнообразием. В бляшках было меньше Cutibacterium (Cu) и больше – Corynebacterium (Cr). В очагах поражения отношение Cr/Cu+Cr было выше, чем в непораженной коже. Эти результаты показывают, что ОП был основной причиной нарушения баланса между Cu и Cr в коже. Количество Cr коррелировало с тяжестью псориатических поражений, а Cu – с общим количеством бактерий в коже. Все это заставляет думать, что микробиота кожи может играть важную роль в патогенезе ОП.
Профессор Маркку Вотилайнен
Медицинский факультет Университета Турку; Университетская клиника Турку, отделение гастроэнтерологии, Турку, Финляндия
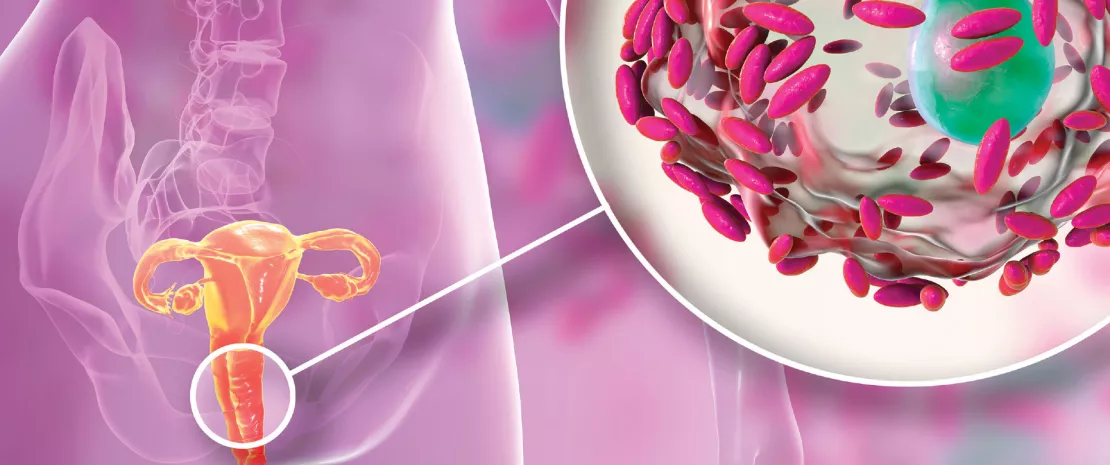
Неудачные повторные попытки проведения ЭКО (НППЭ) – это невозможность забеременеть после имплантации как минимум 4 жизнеспособных эмбрионов женщине в возрасте до 40 лет. НППЭ могут быть обусловлены различными факторами со стороны эмбриона, матки или системными заболеваниями матери, но в некоторых случаях причину неудачи определить не удается. Авторы изучали вагинальную микробиоту и метаболом женщин с НППЭ и обнаружили у них вагинальный дисбиоз, отличительными особенностями которого было более высокое разнообразие микроорганизмов с увеличением количества анаэробных и аэробных бактерий, которые могут быть связаны с бактериальным вагинозом и аэробным вагинитом или инфекцией мочевыводящих путей, соответственно. В то же время в их вагинальной микробиоте наблюдалось снижение числа представителей рода Lactobacillus (LB), при этом количество L. iners сократилась, а L. crispatus стал самым многочисленным видом. Увеличение бактериального разнообразия влагалища, уменьшение количества LB и связанные с этим метаболические изменения могут служить биомаркерами, позволяющими прогнозировать риск НППЭ.
В работе обсуждается роль вагинальной микробиоты в развитии инфекций мочевыводящих путей (ИМВП), поскольку появляется все больше данных, указывающих на то, что влагалище может служить резервуаром для уропатогенов, что повышает восприимчивость к ИМВП. Escherichia coli, самый частый возбудитель ИМВП, может колонизировать влагалище. Ее количество может возрасти при обеднении вагинальной микрофлоры представителями рода Lactobacillus. Некоторые вагинальные бактерии часто обнаруживаются в моче, но их обычно не считают уропатогенами, поскольку они труднообнаружимы в повседневной клинической практике. Например, при бактериальном вагинозе (БВ) наблюдается преобладание грамотрицательных анаэробов, Actinobacteria и Firmicutes, но в то же время недостаток LB, что делает таких женщин более восприимчивыми к ИМВП. Gardnerella vaginalis обнаруживается при БВ и может вызывать острые или рецидивирующие ИМВП. Streptococcus группы B может вызвать как аэробный вагинит, так и ИМВП. Наконец, некоторые вагинальные бактерии могут ненадолго попадать в мочевыводящие пути и влиять на работу местного иммунитета или вызывать повреждение, что нарушает сбалансированное взаимодействие между организмом и различными патогенами и иногда приводит к заболеваниям.
НОВОСТИ КОНГРЕССА
Доктор Драгош ЧоканОтделение гепатологии, гастроэнтерологии и нутрицевтики, Госпиталь Антуан-Беклер, Кламар, Франция

Несмотря на пандемию Covid-19, в этом году мы смогли воспользоваться онлайн-версией Journees francophones d'hépato-gastroenterologie (конгресс гепатологов и гастроэнтерологов из франкоговорящих стран) с возможностью доступа к презентациям за период с 3 по 20 июля 2020 г. Всего ресурс посетили 7924 пользователей, которые просмотрели 172 937 страниц. Как и раньше, на этом конгрессе были представлены результаты оригинальных исследований кишечной микробиоты (КМ).
Спорадический колоректальный рак (КРР) занимает третье место по частоте встречаемости у человека и развивается в результате взаимодействия между организмом и окружающей средой, в котором КМ играет не последнюю роль [1]. Профессор Собхани представил результаты исследования, в котором изучалась связь между эпигенетическими механизмами, реализуемыми бактериями КМ, и развитием КРР [2]. У мышей, которым трансплантировали образцы фекалий пациентов с КРР, развились предраковые поражения толстой кишки, связанные с увеличением гиперметилирования генов. У доноров с КРР наблюдались нарушения метилирования промоторов нескольких генов, связанных с дисбиозом кишечника. Используя идентифицированные микробные и эпигенетические сигнатуры, было проведено пилотное исследование (n = 266) на человеке с целью создания анализа крови для диагностики КРР. В качестве прогностического фактора был выбран кумулятивный индекс метилирования (КИМ, определяющий уровень гиперметилирования 3 генов) на момент установления диагноза КРР. Его ценность изучали в проспективной когорте из 1000 пациентов. Особенностью дисбиоза кишечника у пациентов с положительным КИМ являлось увеличение содержание прометилирующих видов бактерий. Полученные результаты указывают на то, что дисбиоз кишечника, ассоциированный с КРР, может способствовать канцерогенезу в толстой кишке за счет нарушения регуляции метилирования определенных генов. КИМ и/или наличие прометилирующих бактерий, таким образом, являются потенциальными биомаркерами для диагностики КРР или могут использоваться для оценки результатов лечения, направленного на изменение КМ у пациентов с КРР.
В исследовании, которым руководил профессор Сексик, авторы изучали роль МПМ (микробный противовоспалительный медиатор, производимый Faecalibacterium prausnitzii, уровень которого снижается у пациентов с болезнью Крона, БК [3]) как биомаркера дисбиоза кишечника и диагностического маркера при БК. Авторы показали, что утрата МПМ связана с диагнозом БК. Результаты, полученные в этом небольшом предварительном исследовании (24 пациента в стадии обострения, 24 в стадии ремиссии и 12 здоровых добровольцев в контрольной группе), открывают путь к диагностике БК на основе анализа КМ, однако требуют проверки в независимых когортах.
Известно, что бактерии воспринимают сигналы окружающей среды и реагируют на них (т.н. чувство кворума). У пациентов с хроническими воспалительными заболеваниями кишечника (ХВЗК) отмечается недостаток 3-оксо-C12:2 – молекулы, которая является частью этой системы. Его выраженность коррелирует со степенью дисбиоза кишечника [4]. Ученые изучили влияние этой молекулы на эпителиальные клетки кишечника и обнаружили, что она не влияет на параклеточную проницаемость, но частично восстанавливает функцию плотных контактов, нарушенную действием провоспалительных цитокинов. Другие показали, что 3-оксо-C12:2 подавляет провоспалительное действие иммунореактивных клеток, частично с участием t2R138 рецептора. Таким образом, 3-оксо-C12:2 может оказывать защитное действие на кишечный барьер, модулировать воспалительные реакции и, следовательно, может использоваться в лечении ВЗК.
НАУЧНЫЕ РЕЦЕНЗИИ - ДЕТИ
Профессор Эммануэль Мас
Отделение гастроэнтерологии и нутрициологии, Детская больница, Тулуза, Франция
В первые недели жизни микробиота играет решающую роль в поддержании здоровья, действуя как барьер против вторжения патогенов и поддерживая иммунный гомеостаз кишечника. У новорожденных с кишечной ишемией зарегистрированы случаи нарушения фекальной микробиоты. Целью исследования было изучение микробиоты кала и слизистой кишечника, а также иммунной системы слизистой у этих детей.
14 новорожденным была выполнена резекция кишечника по поводу кишечной ишемии. В зависимости от степени поражения были выделены две группы детей: с распространенной и очаговой ишемией кишечника. Выявлены различия между детьми обеих групп по характеристикам микробиоты кала и слизистой.
Микробиота кишечника новорожденных характеризуется более низким бактериальным разнообразием и более высокой долей патогенных бактерий. Более того, их кишечная иммунная система еще не сформировалась. Эти два фактора влияют на эпителиальный барьер кишечника и усиливают продукцию провоспалительных медиаторов.
Некротизирующий энтероколит (НЭК) представляет собой ишемическое и воспалительное заболевание желудочно-кишечного тракта, которое возникает у недоношенных новорожденных. Патофизиология НЭК изучена мало, но известно, что при этом имеет место дисбактериоз кишечника и воспалительный процесс в нем. Использование антибиотиков и антацидов способствует развитию дисбактериоза, а также увеличивает риск развития НЭК.
Новорожденные также могут страдать от других ишемических и воспалительных заболеваний, таких как заворот тонкой кишки и очаговая перфорация желудочно-кишечного тракта.
Авторы этого одноцентрового пилотного исследования определяли состав микробиоты кала (МК) и микробиоты слизистой (МС), а также профиль мононуклеарных клеток и провоспалительных цитокинов в собственной пластинке слизистой у доношенных и недоношенных новорожденных. У 7 младенцев имела место распространенная ишемия кишечника (РИК) (5 случаев НЭК, 1 случай заворота тонкой кишки и 1 – тотальной ишемии толстой кишки), у 7 – очаговая ишемия кишечника (ОИК) (4 изолированных перфорации и 3 случая атрезии кишечника). МК 9 доношенных новорожденных использовали в качестве контроля.
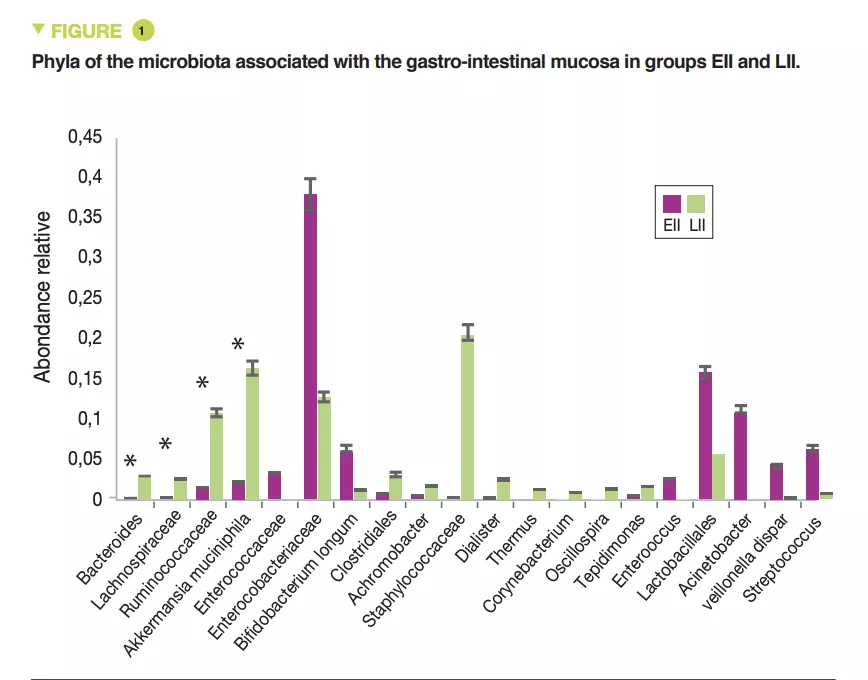
По сравнению с новорожденными с ОИК, МС детей с РИК содержала больше бактерий вида Proteobacteria (n = 0,049) и меньше Bacteroidetes (n = 0,007) и Verrucomicrobia (n = 0,01) (рис. 1), а также представителей Bacteroides, Lachnospiracee, Ruminococcaceae и Akkermansia muciniphila (n < 0,05).
МК была менее разнообразной (индекс Шеннона) у детей с РИК чем с ОИК (n = 0,01). Относительное количество Proteobacteria и Firmicutes в составе МС было одинаковым в обеих группах (n <0,05). У детей с ОИК было больше представителей Enterobacteriaceae, а у детей с РИК – Ruminococcaceae, Bacteroides, Lachnospiracee и Staphylococcaceae. У детей с ОИК отмечалось больше B-, T- и NK- (естественные киллеры) клеток, в частности CD3+ лимфоцитов и TH17 (рис. 2а), меньше регуляторов Т-лимфоцитов (Treg), и увеличение количества клеток, экспрессирующих TNFα (рис. 2b) и INFγ (рис. 2с).
Некротизирующий энтероколит – это тяжелая желудочно-кишечная патология, встречающаяся у недоношенных новорожденных
В развитии воспалительных и ишемических процессов при НЭК может быть задействована фекальная и желудочно-кишечная микробиота
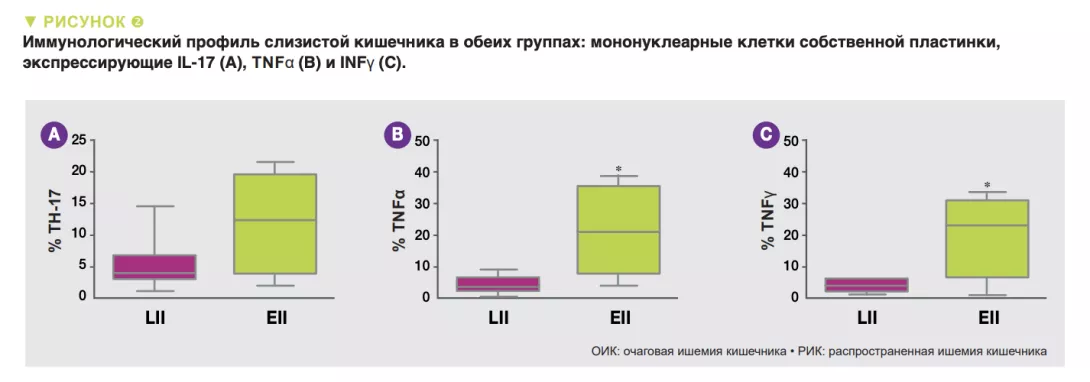
Результаты этого пилотного исследования подтверждают, что отсутствие бактериального разнообразия и преобладание Enterobacteriaceae являются факторами риска НЭК, так же как и уменьшение количества Akkermansia muciniphila.
Коррекция дисбиоза может устранить дисбаланс между TH17 и treg и уменьшить выработку медиаторов воспаления (TNFα и INFγ).
Микробиота кала и слизистой оболочки желудочно-кишечного тракта обладают специфическими характеристиками у недоношенных новорожденных с ишемическими поражениями кишечника. Необходимы дополнительные исследования, чтобы определить роль этих бактерий в развитии воспалительных и ишемических процессов при НЭК.
МИКРОБИОТА И COVID-19
Доктор Франсуа Троттен
Центр изучения инфекционных заболеваний и иммунитета в Лилле, Университет Лилля, Больница Лилля, Пастеровский институт в Лилле, Франция

Новая инфекция (COVID-19), вызываемая коронавирусом (SARS-CoV-2) 19, напоминает нам о том, что взаимодействия между кишечной микробиотой и иммунной системой имеют важное значение при респираторных вирусных инфекциях. Респираторные вирусы могут вызывать симптомы со стороны желудочно-кишечного тракта, что подчеркивает роль системы легкиекишечник в заболевании. Клинические исследования и экспериментальные модели показывают, что острые респираторные вирусные инфекции изменяют состав и функции кишечной микробиоты, которая вносит важный вклад в поддержание здоровья человека. Мы рассмотрим эти основные изменения и обсудим возможные причины развития дисбиоза кишечника. Мы также рассмотрим влияние дисбиоза кишечника, развивающегося во время инфекции, на исходы заболевания. В конце мы обсудим интервенционные стратегии, которые можно использовать для воздействия на микробиоту кишечника, чтобы уменьшить тяжесть респираторного вирусного заболевания.
Респираторные вирусные инфекции попрежнему вызывают серьезную озабоченность во всем мире, поскольку являются серьезной социально-экономической и медицинской проблемой. Несмотря на кампании по вакцинации и арсенал противовирусных препаратов, грипп продолжает оставаться наиболее опасным с точки зрения числа инфицирований (5- 10% мирового населения) и смертей (>600 000 в год). Наряду с ежегодными эпидемиями, каждые 10-20 лет грипп также вызывает пандемии, самой известной из которых является «испанка» 1918-1919 гг (50 миллионов смертей), а самой последней – пандемия гриппа H1N1 в 2009 г (400 000 дополнительных смертей) [1]. Как мы видим на примере COVID-19, пандемии не ограничиваются гриппом [2]. Что больше всего настораживает – это учащение пандемий за последние несколько десятилетий. Это частично можно объяснить изменениями климата и деятельностью человека в целом.
Микробиота кишечника играет важную роль в поддержании здоровья человека и имеет решающее значение в борьбе с (респираторными) инфекциями [3, 4]. Различные факторы могут изменить разнообразие и состав микробиоты кишечника, что ведет к дисбиозу. Среди них заболевания, такие как инфекции, хронические воспалительные процессы или нарушения обмена веществ могут вызвать глубокое изменение состава и функции кишечной микробиоты. Изменения кишечных бактериальных сообществ могут влиять на исход заболеваний даже в отдаленных органах (включая легкие) [3, 4], что подтверждено в экспериментах по переносу дисбиотической микробиоты. Ниже мы суммируем влияние острых респираторных вирусных инфекций на микробиоту кишечника
Данные клинических наблюдений указывают на развитие дисбиоза кишечной микробиоты при гриппе. При этом у больных гриппом H1N1 уменьшается содержание обычно многочисленных Actinobacteria, Erysipelotrichea, Clostridia и полезных продуцентов бутирата (Lachnospiraceae и Ruminococcaceae). С другой стороны, повышается содержание условно-патогенных микроорганизмов, таких как Escherichia-Shigella и Prevotella [5]. В экспериментальных (мышиных) моделях преходящий дисбиоз кишечника также обычно развивается через 5-7 дней после заражения [6-9]. Изменения происходят на таксономическом уровне без изменения альфа-разнообразия. Инфекция подавляет рост полезных бактерий, таких как Lactobacilli, Bifidobacteria и сегментированные нитчатые бактерии. Также поражаются многие виды, способные ферментировать пищевые волокна в короткоцепочечные жирные кислоты (КЦЖК). Соответственно, при гриппе резко снижается продукция КЦЖК [9]. Подавление роста полезных комменсалов сочетается с чрезмерным ростом вредных бактерий, включая Gammaproteobacteria (Escherichia coli) и бактерии, разрушающие слизь, такие как Verrucomicrobia (Akkermansia) и Ruminococcus. Инфекция SARS-CoV-2 также вызывает изменения микробиоты кишечника у пациентов, в том числе уменьшение количества продуцентов бутирата, таких как Ruminococcaceae и Lachnospiraceae (Roseburia) [5, 10]. С другой стороны, у них отмечается увеличение относительной численности условно-патогенных бактерий, включая Streptococcus (класс Bacilli), Rothia и Actinomyces, и грибков (Aspergillus и Candida) [11]. В совокупности респираторные вирусные инфекции приводят к обеднению микробиоты полезными комменсалами и обогащению условно-патогенными микробами. Предполагают, что изменения в структуре, составе и функциональной активности кишечной микробиоты могут служить биомаркерами тяжести заболевания.
Вероятно, существует несколько причин развития дисбиоза кишечника при респираторных вирусных инфекциях, которые могут включать высвобождение воспалительных цитокинов и снижение потребления пищи (рис. 1). Заболевание вызывает значительную потерю массы тела из-за утраты аппетита. Эксперименты с парным кормлением мышей показывают, что быстрое снижение потребления пищи вызывает изменения микробиоты кишечника, почти идентичные наблюдаемым при гриппе [8]. Недавно установлена роль, которую играет TNFа при дисбиозе, связанном с отсутствием аппетита при вирусной инфекции [12]. Интерфероны I и II, необходимые для противовирусного ответа организма, также играют роль в развитии дисбиоза кишечника [5,6].
Гипоксия (один из симптомов острой респираторной вирусной инфекции), нарушение работы нервной системы кишечника и местного иммунитета также могут участвовать в развитии дисбиоза кишечника [13] (рис. 1). В случае COVID-19, наряду с этими механизмами, местная репликация вируса также, вероятно, играет роль в дисбактериозе кишечника. Ангиотензинпревращающий фермент II (АПФ2), являющийся рецептором SARSCoV-2, играет важную роль в поддержании микробной экологии кишечника. Можно ожидать, что отсутствие доступного АПФ2 во время инфекции SARS-CoV-2 способно повлиять на состав и функции микробиоты кишечника [13].
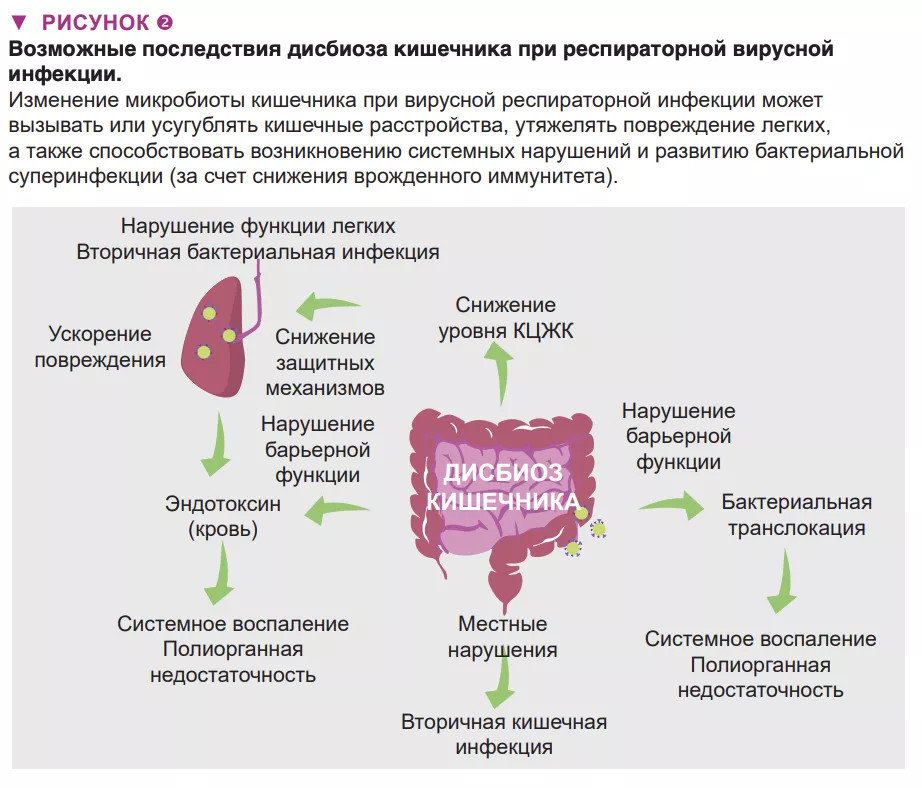
Дисбиоз кишечника при респираторной вирусной инфекции может иметь местные и отдаленные последствия, а также повлиять на тяжесть заболевания и способствовать летальному исходу (рис. 2). У пациентов с респираторной вирусной инфекцией могут развиться симптомы как при гастроэнтерите, такие как боль в животе, тошнота, рвота и диарея. Эти нарушения можно объяснить изменениями микробиоты кишечника. Также нельзя исключить, что эти изменения, включая появление патобионтов и бактерий, разрушающих слизь, играет роль в развитии воспаления в кишечнике и нарушении целостности кишечного барьера [6]. В свою очередь, последний фактор ведет к увеличению концентрации эндотоксинов в крови, что в конечном итоге вызывает воспаление, перепроизводство цитокинов и дисфункцию легких [14]. Острые вирусные респираторные инфекции могут привести к вторичным кишечным инфекциям и сепсису. Важную роль в этом играют дисбиоз кишечника (и снижение продукции КЦЖК). Действительно, КЦЖК играют ключевую роль в поддержании гомеостаза кишечника, целостности кишечной стенки и контроле кишечных патогенов [15]. Согласно последним данным, наряду с местными нарушениями дисбиоз кишечника может отдаленно влиять на защитные иммунные реакции в легких [9] (рис. 2). Микробиота кишечника здорового человека дистанционно защищает легкие от бактериальной инфекции, частично за счет усиления бактерицидной активности легочных макрофагов [16].
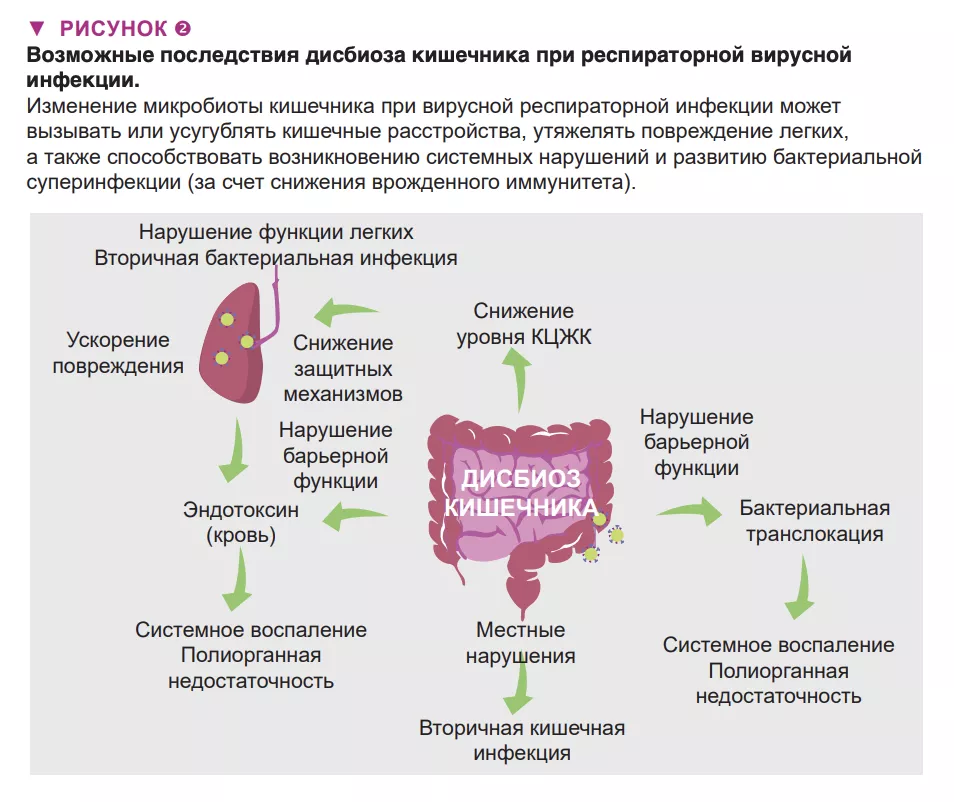
При гриппе функционирование этой оси нарушается и условно-патогенные бактерии проникают в легкие, вызывая бактериальную суперинфекцию, которая является основной причиной смерти во время эпидемий и пандемий гриппа [1]. Нам удалось показать, что снижение продукции ацетата (основы КЦЖК) кишечной микробиотой частично отвечает за этот эффект [9]. В целом дисбактериоз может влиять на желудочно-кишечные и легочные симптомы, а также общую смертность при вирусных респираторных инфекциях. Можем ли мы использовать ось «кишечник-легкие» в качестве основы для более эффективного контроля над тяжестью симптомов и смертностью от вирусных респираторных инфекций?
Микробиота кишечника жизненно важна для защиты легких от респираторных инфекций, поэтому разработка вмешательств, нацеленных на кишечных комменсалов, которые бы позволили заранее защитить легкие от вирусных патогенов, а микробиоту – от нарушений, связанных с вирусными инфекциями, представляет большой интерес (рис. 3). Это особенно важно для людей с общими нарушениями микробиоты кишечника, особенно пожилых и страдающих сопутствующей патологией, которые, как известно, более восприимчивы к инфекциям.
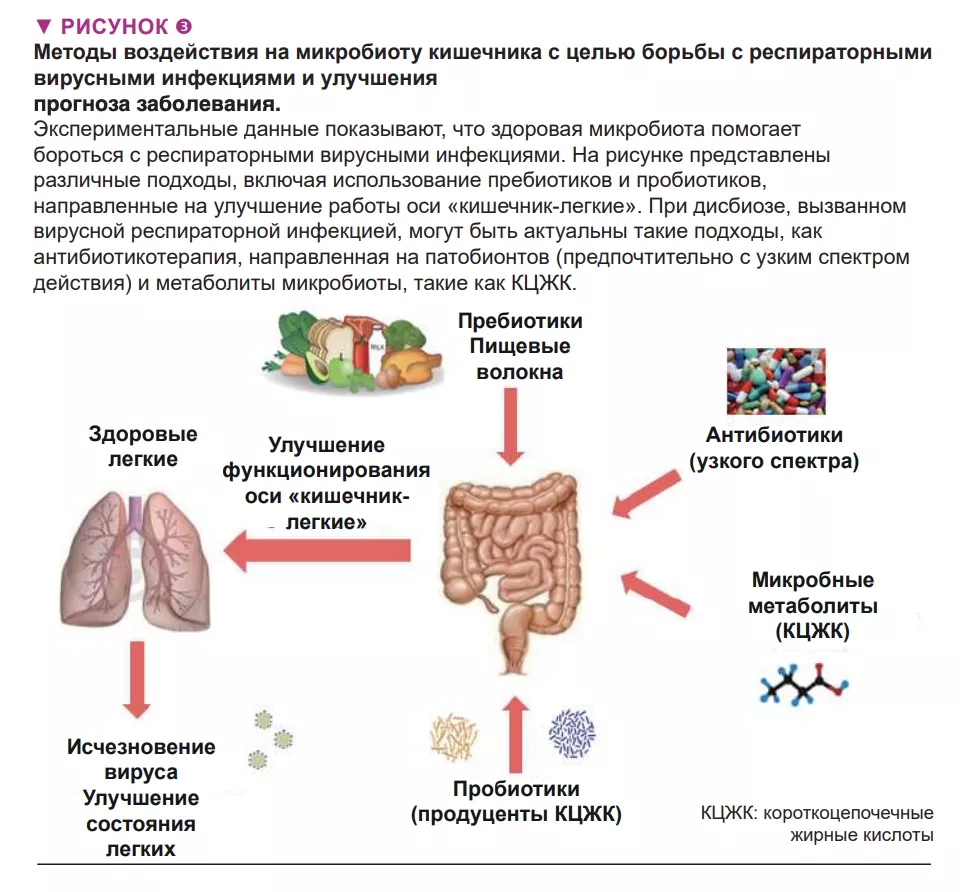
Представляют интерес такие подходы, как использование (i) компонентов диеты, предназначенных для питания наших полезных микроорганизмов (например, пребиотических волокон) и (ii) эндемичных бактерий (известных как пробиотики), восполняющих микрофлору нашего кишечника недостающими полезными представителями и, соответственно, их метаболическими функциями. Эти стратегии, особенно персонализированные (т.е. основанные на анализе микробиоты кишечника в группе риска), могут улучшить клинические исходы и ускорить выздоровление пациентов с острыми респираторными вирусными инфекциями. Пробиотики, в том числе Bifidobacteria и Lactobacillus spp, могут снизить степень тяжести гриппа с помощью еще не выясненных механизмов [17]. Согласно недавно полученным данным, пероральная бактериотерапия в дополнение к стандартной лекарственной терапии COVID-19 дала многообещающие результаты [18]
Функционирование оси «кишечник-легкие» имеет большое значение при респираторных вирусных инфекциях. Изменения кишечной микробиоты влияют на исходы заболевания. Воздействуя на кишечную микробиоту можно улучшить течение заболевания. Этого можно достичь с помощью компонентов диеты (например, пребиотических волокон) и пробиотиков.
ОБЗОР ЛИТЕРАТУРЫ
Проф. Маркку Вутилайнен (Markku Voutilainen)
Медицинский факультет Университета Турку; Университетская больница, отделение гастроэнтерологии, Турку, Финляндия
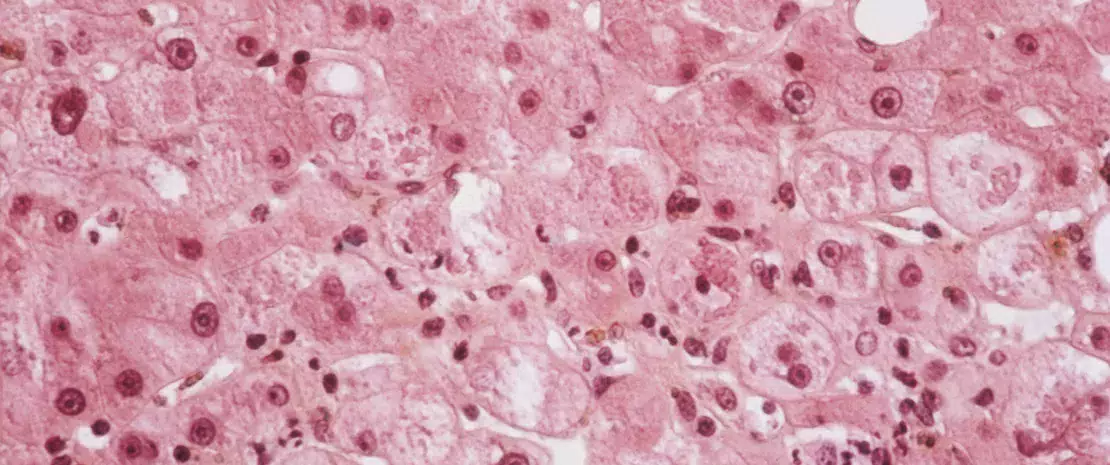
Alcoholic hepatitis. Light micrograph of a section through a liver affected by hepatitis (inflammation of the liver) caused by excessive alcohol intake.
[Способность кишечного микробиома к фермен- тации определяет эффективность физической активности как способа профилактики сахарного диабета]
Влияние физической нагрузки на кишечную микробиоту изучали у мужчин с предиабетом. Реакция на физическую нагрузку характеризовалась снижением уровня инсулина натощак и снижением инсулинорезистентности (HOMA-IR), тогда как в случае отсутствия такой реакции соответствующие показатели оставались неизменными или даже ухудшались. Физическая нагрузка приводила к преобладанию представителей родов Firmicutes, Bacteroides, Proteobacteria. Изменение состава микробиома кишечника коррелировало с уменьшением HOMA-IR. Синтез ДНК, метаболизм аминокислот (АК), синтез КЦЖК усиливались у тех, кто отвечал на действие физической нагрузки. В случае отсутствия такого ответа наблюдалось переключение с ферментации АК на продукцию кишечных газов и вредных соединений, что способствовало усилению инсулинорезистентности. Увеличение содержания КЦЖК в сыворотке крови, уменьшение содержания АК с разветвленной цепью и ароматических АК были обнаружены только при наличии ответа. КЦЖК играют благоприятную роль в обмене энергии и глюкозы, в то время как увеличение количества АК с разветвленной цепью коррелирует с поддержанием инсулинорезистентности. В заключение следует отметить, что при наличии ответа на физическую нагрузку микробиом кишечника начинал активно продуцировать КЦЖК при одновременном усилении расщепления АК с разветвленной цепью, в то время как в отсутствие подобной реакции отмечалось образование метаболически вредных соединений.
[Таргетное применение бактериофага уменьшает симптомы алкоголь- ной болезни печени]
У пациентов с алкогольным гепатитом отмечается повышенный уровень Enterococcus faecalis (EF) в кале, при этом EF выявляется у 80% пациентов с данной патологией. Безмикробным мышам, находящимся на этанольной диете, вводили цитолизин-положительную (CL+) фекальную микробиоту с EF, полученную от пациентов с алкогольным гепатитом. У этих мышей, развивалось более тя- желое этанол-ассоциированное поражение печени. Мышам, получавшим этанольную диету, и у которых отмечался повышенный рост кишечных энтерококков, давали бактериофаги, лизирующие CL + EF. У них поражение печени было выражено в меньшей степени. Таким образом, терапия бактериофагами может замедлить прогрессирование алкогольной болезни печени, вызванной CL + EF, а также улучшает прогноз при тяжелом алкогольном гепатите.
ОБЗОР ЛИТЕРАТУРЫ
Проф. Маркку Вутилайнен (Markku Voutilainen)
Медицинский факультет Университета Турку; Университетская больница, отделение гастроэнтерологии, Турку, Финляндия
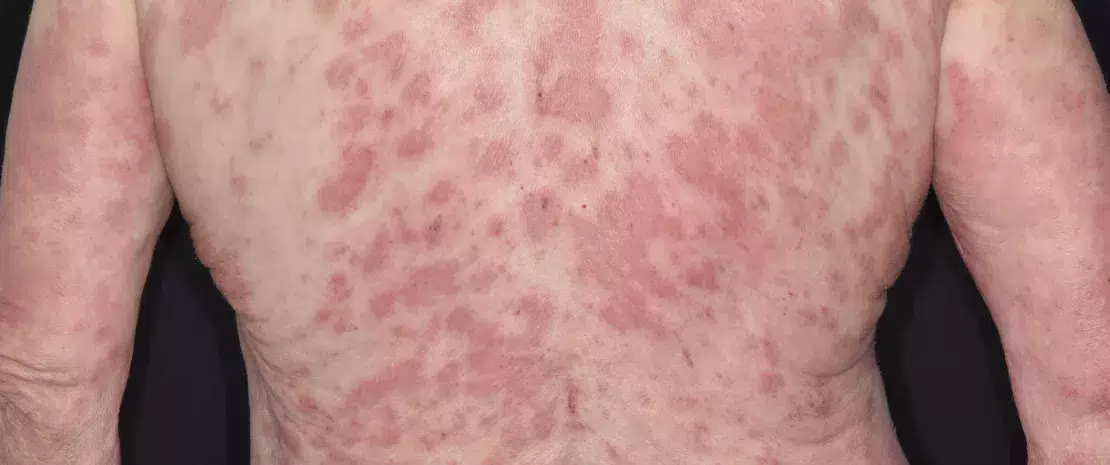
Atopic dermatitis on the upper body of an 83 year old male patient. Atopic dermatitis, also called atopic eczema, is an inflammatory skin reaction that occurs without any obvious external cause.
[Взаимодействие микроорганизма и организма-хозяина при атопическом дерматите и псориазе]
Авторы сравнили микробиоту при атопическом дерматите (АД) и псориазе (ПСО) с микробиотой здоровых добровольцев. Авторы выявили 26 и 24 микроорганизма, свойственных для АД и ПСО соответственно. Наиболее значимыми таксонами для АД были представители рода Staphylococcus, а для ПСО — Corynebacterium simulans, Neisseriaceae g. spp., C. kroppenstedtii, Lactobacillus spp. и L. iners. АД характеризуется преобладанием S. aureus. При ПСО может быть задействовано большое количес- тво различных бактерий, таких как Corynebacterium. Уменьшение количества Lactobacillus характерно для обоих заболеваний. При АД часто отмечается утрата облигатно анаэробных бактерий с уменьшением выработки молочной кислоты и КЦЖК, что приводит к повышению рН кожи. Взаимодействие между микроорганизмом и организмом хозяина играет важную роль как в поддержании гомеостаза кожи, так и в патогенезе заболеваний.
[Staphylococcus epidermidis: новый игрок в патогенезе акне?]
Чтобы различить комменсальные и оппортунистические бактерии, необходимо понимать связь между микробиотой кожи и самой кожей. В период полового созревания чрезмерная колонизация пилосебационных (фолликуло-сальных) единиц Cutibacterium acnes (CUA) может приводить к развитию акне. Некоторые штаммы S. epidermidis модулируют врожденные иммунные реакции хозяина, а некоторые изоляты обладают антимикробной активностью в отношении CUA. И наоборот, некоторые штаммы CUA обладают антимикробной активностью в отношении S. epidermidis, который также может контролировать CUA посредством образования янтарной кислоты. Применение местных антибиотиков может привести к развитию устойчивых к антибиотикам штаммов CUA и S. epidermidis. Устранение только CUA может привести к пролиферации S. aureus и S. epidermidis и увеличению риска инфекций. Лактобациллы (Lactobacillus) могут быть эффективны при акне и других воспалительных заболеваниях кожи. По мнению авторов, регулярное пероральное или местное поддержание микробиоты кожи может быть способом лечения акне.
ОБЗОР ЛИТЕРАТУРЫ
Проф. Маркку Вутилайнен (Markku Voutilainen)
Медицинский факультет Университета Турку; Университетская больница, отделение гастроэнтерологии, Турку, Финляндия
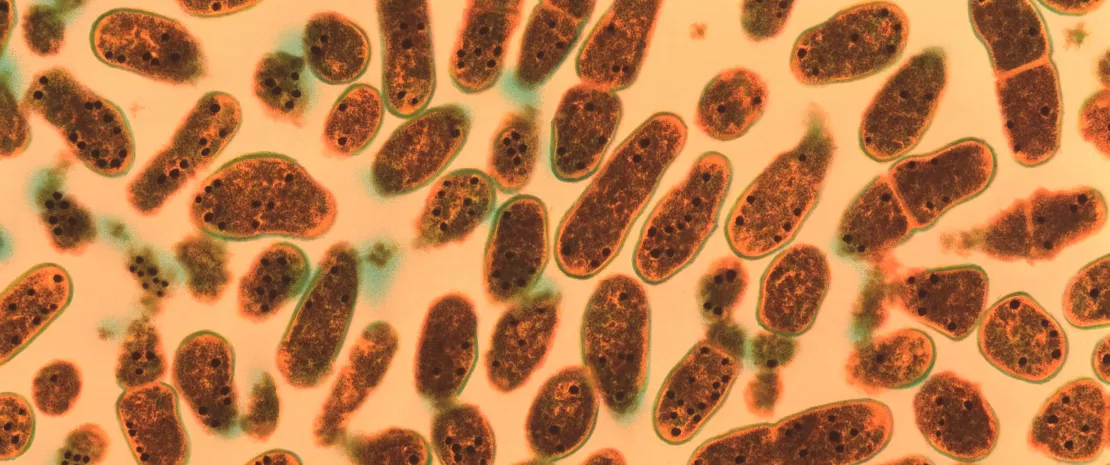
Gardnerella vaginalis bacteria. Coloured transmission electron micrograph (TEM) of Gardnerella vaginalis bacteria.
[Gardnerella и здоровье влагалища: истина где-то рядом]
Микробиота влагалища включает пять основных разновидностей микроорганизмов (микробных сообществ). Четыре из них представлены лактобактериями (Lactobacillus sp.). Врожденная вагинальная иммунная система, эпителиальные клетки, toll-подобные рецепторы и природные антимикробные пептиды являются компонентами защиты организма от различных возбудителей. Род Lactobacillus играет главную роль в реализации защитных механизмов влагалища, вырабатывая молочную кислоту и бактериоцины, а также предотвращая адгезию патогенных бактерий. Бактери- альный вагиноз (БВ) характеризуется избыточным ростом патогенных микроорганизмов и развитием полимикробной биопленки, которая плотно прилегает к эпителию влагалища. Gardnerella spp. — основной вид, представленный в данной биопленке, который отличается наибольшей вирулентностью. Для лечения БВ используют метронидазол, клиндамицин или тинидазол.
UМногие изоляты, содержащие Gardnerella spp., и другие возбудители устойчивы к действию метронидазола. Адъювантная терапия пробиотиками на основе лактобактерий (Lactobacillus) способствует улучшению эффективности метронидазола. Исследования, направленные на изучение полимикробных взаимодействий между вагинальными патогенами, могут привести к созданию экологически обоснованных методов лечения.
[Связь между вагинальным микробиомом и колонизацией грибами рода Candida у женщин репродуктивного возраста]
Candida albicans (CA) обнаруживается в составе вагинального микробиома у примерно 30% женщин. Колонизация грибами рода CA была выявлена у 42 (16%) из 255 небеременных женщин репродуктивного возраста. Были установлены самые распространенные вагинальные микробиомы: с преимущественным содержанием Lactobacillus crispatus (20%), с преимущественным содержанием L. iners (39%), а также смешанного характера (38%). CA чаще обнаруживается у женщин негроидной расы и с высоким уровнем L.iners по сравнению со здоровыми белыми женщинами и женщинами с преобладанием L. crispatus. В условиях in vitro, L. crispatus продуцирует больше лактата и ингибирует рН-зависимый рост СА. Основным результатом стало то, что виды Lactobacillus по-разному взаимодействуют с СА, а L. crispatus может предотвратить колонизацию бактерий более эффективно, чем L. iners, вследствие более высокого уровня продукции лактата..
ОБЗОР КОНГРЕССА
Проф. Гурдас Чоудхури (Gourdas Choudhuri)
Госпиталь Хортис, Хариана, Индия

Азиатско-Тихоокеанская конференция по заболеваниям пищеварительной системы, проходившая в Индии 12–15 декабря, была посвящена роли кишечной микробиоты в нормальной работе системы пищеварения. В конференции принимали участие более 5000 участников со всего мира, при этом залы на обоих крупных симпозиумах, посвященных этой теме, были переполнены.
Первый симпозиум начался с детального обзора, представленного доктором Хольтманом из Австралии. Он подчеркнул, что большое количество комменсальных бактерий, обычно обитающих в кишечнике человека, намного превышает количество клеток в человеческом организме, и обратил внимание на ключевую роль микроорганизмов в поддержании здоровья человека.
Кишечные микроорганизмы относятся к трем таксономическим классам: бактерии, археи и эукариоты. Хотя большинство из них трудно вырастить, они выполняют важнейшие функции переваривания пищи (особенно клетчатки), производства и поглощения витаминов, поглощения питательных веществ, защиты слизистой оболочки от колонизации патогенами, регуляции иммунной системы хозяина и перистальтики кишечника.
По мнению доктора Хольтмана, хотя микробиота, полученная из кала (люминальные микроорганизмы), является наиболее изученной, ученые теперь признают существование «микробиоты, ассоциированной со слизистыми оболочками», которую более сложно выделить, охарактеризовать и вырастить, но которая, по-видимому, играет гораздо более значимую роль в регуляции здоровья кишечника и иммунной системы человека.
Появляется все большее количество данных, свидетельствующих о роли SIBO (синдрома усиленного бактериального роста в тонком кишечнике) и дисбиоза в развитии ряда заболеваний. Например, было показано, что люминальная антибактериальная терапия улучшает работу печени у пациентов с хроническими заболеваниями печени и первич- ным склерозирующим холангитом, а клиническая эффективность часто отмечается у пациентов с синдромом/болезнью раздраженного кишечника (СРК/БРК).
Автор подчеркнул наличие значимых корреляций между кишечной микробиотой и различными заболеваниями ЖКТ и заболеваниями другой локализации и продемонстрировал увеличивающийся объем данных, свидетельствующих о возможности излечения или достижения контроля неизлечимых на данный момент заболеваний при применении способов терапии, направленных на кишечную микробиоту.
Чем больше мы понимаем работу кишечной микробиоты, тем больше методов мы можем использовать для ее изучения. Доктор Аиша Шах (Ayesha Shah) из Университета Квинсленда рассказала, как устаревают ранее применявшиеся методы (аспирация из тощей кишки, дыхательный тест) вследствие низкой специфичности, освобождая дорогу для новых, не связанных с выполнением посевов методов молекулярной диагностики, таких как определение плотности бактериальной культуры (qPCR) и определение профиля микробного сообщества с помощью секвенирования.
Профессор Питер Гибсон (Peter Gibson) из Мель- бурна, описывая роль модуляции микробиоты кишечника в процессе лечения, объяснил, что может стать идеальной тактикой. В самом начале необходимо определить наличие микробного или функционального дисбиоза у человека путем анализа микробиоты кала, биопсии слизистой оболочки или функционального анализа метаболитов. Это может помочь установить наличие желаемых изменений в микробиоте кишечника, таких как изменение конкретных сообществ или общего количества микробов. Впоследствии для достижения желаемых изменений можно использовать существующие методы лечения — например, использование антибиотиков, пробиотиков, диеты или трансплантацию фекальной микробиоты.
В качестве примера докладчик рассказал о методе, который позволяет увеличивать разнообразие кишечных бактерий при использовании различных подходов к питанию. Каждый продукт питания, особенно овощи и фрукты, по-видимому, способствует росту определенного вида бактерий из-за содержащихся в них пребиотиков; увеличение разнообразия овощей и фруктов в каждом приеме пищи может стать простым методом увеличения разнообразия микробиоты в кишечнике человека.
Пробиотики способствуют относительному преобладанию конкретных бактерий при определенных условиях. Среди изученных бактерий значимыми оказались такие виды, как Bifidobacteria, Faecalobacterium prausnitzii, а также некоторые представители рода Lactobacillus. С другой стороны, антибиотики, такие как рифаксимин, могут применяться для уменьшения количества ряда нежелательных бактерий, которые расщепляют сульфаты или белки и могут быть связаны с развитием заболевания.
СРК, наиболее частое заболевание ЖКТ, которое, как полагают, связано с пищей и, следовательно, может зависеть от состояния кишечной микробиоты, было предметом нескольких РКИ с использованием различных пробиотиков, таких как различные штаммы Lactobacillus, Bifidobacteria, Saccharomyces, и комбинированных препаратов. Несмотря на гете- рогенность СРК и невысокую вероятность достижения значимой эффективности, в РКИ было продемонстрировано улучшение состояния пациентов на фоне применения ряда пробиотиков. Наиболее значимые результаты были получены при использо- вании штамма Bifidobacterium infantis, который спсобствовал улучшению таких симптомов, как боль, вздутие живота и удовлетворенность степенью опорожнения кишечника более чем на 20% после 4–8 недель терапии. Положительное действие было также показано при применении отдельных штаммов B. animalis и L. plantarum.
Многие участники посетили интересный симпозиум «Антибиотики и изменение состава микробиоты», проходивший при поддержке компании Biocodex Pharma под председательством доктора Генри Коэ- на (Henry Cohen) (Уругвай) и доктора Кентаро Сугано (Kentaro Sugano) (Япония). Д-р К. Л. Гох (K. L. Goh) (Малайзия) описал количественные характеристики, разнообразие и роль кишечной микробиоты и отметил две сравнительные особенности: микробный геном имеет около 3 300 000 генов, а геном человека — 22 000, при этом межиндивидуальные различия составляют 80% у микроорганизмов и 0,01% у человеческих клеток!
Было показано, что нарушение состава этой чрезвычайно разнообразной кишечной микробиоты в результате приема антибиотиков ассоциировано с рядом патологических состояний. Помимо общеизвестной стимуляции инфекции, вызванной Clostridium difficile, часто развивается дисбиоз, который, в свою очередь, предрасполагает к развитию синдрома «дырявого кишечника» и активации иммунной системы.
Еще одной серьезной проблемой является развитие/передача устойчивости к антибиотикам путем горизонтального переноса генов. Нарушение состава врожденной микробиоты кишечника и появление в ней «патологических» микроорганизмов может предрасполагать к развитию различных нарушений, таких как ожирение и диабет.
Saccharomyces boulardii (Sb) продолжает играть ведущую роль в лечении антибиотик-ассоциированной диареи. Обнаруженный в 1920 году французским микробиологом Анри Буларом (Henri Boulard), этот вид продолжает доказывать свою эффективность в защите кишечника от нарушений, вызванных применением антибиотиков, и восстановлении его функций.
Участники встречи APDW рассказали о значитель- ных успехах в определении роли кишечной мик- робиоты в поддержании здоровья и развитии болез- ней у человека. В своих выступлениях международ- ные эксперты указали, что микробиота кишечника перешла из статуса недавно обнаруженного и ма- лозаметного явления в предмет самого тщательного изучения и терапевтического воздействия, откры- вающий новые возможности лечения заболеваний.
ОБЗОР КОНГРЕССА
Доктор Поль Карденас
Институт микробиологии, Universidad San Francisco de Quito, Эквадор

рамках недели UEG 2019 были рассмотрены интересные данные о влиянии кишечной микробиоты на профилактику, развитие и лечение общественно значимых заболеваний.
Микробиота представляет собой сложное мик- робное сообщество, созданное в индивидуально меняющихся экосистемах (например, в кишечнике человека). Поэтому ее формирование зависит от широкого спектра факторов и воздействий, о которых говорила Джорджина Холд (Georgina Hold) (Университет Южного Уэльса, Австралия). Триллионы микробов эволюционировали вместе с людьми и постоянно адаптируются к физиологии человека. Уже с момента рождения состав микробиоты варьирует в зависимости от таких факторов, как способ родоразрешения, особенности питания, географическая локализация, факторы, действующие на раннем этапе (загрязнение, ан- тибиотики), старение и генетические особенности организма-хозяина. Однако факторы окружающей среды, по-видимому, играют более важную роль в моделировании микробиоты, чем генетические особенности хозяина [1]. Ранняя микробиота является важным фактором, который определяет понимание механизма развития хронических за- болеваний, особенно у жителей городов, — бронхиальной астмы, аллергических заболеваний, экземы, воспалительных заболеваний кишечника (ВЗК), целиакии, ожирения.
Не существует одного определенного «нормального» паттерна микробиоты, поскольку ее метаболические и функциональные характеристики не зависят от вида микроорганизмов. Аналогичным образом в формировании микробиоты кишечника региональные факторы играют большую роль, чем межиндивидуальные особенности [2]. Результаты, опубликованные Cтю Мейникманом (Stijn Meijnikman) после исследования когорты HELIUS (Академический медицинский центр, Нидерланды), показали, что бактериальное разнообразие связано с этническим происхождением (вероятно, обусловливающим особенности питания и наследственные признаки). Считается, что на фоне западной диеты отмечается высокое соотношение бактероидов и превотелл, однако исследование функциональных возможностей микробиоты, как правило, приводит к противоречивым результатам. В результате термин «дисбиоз» является неточным, так как не определены понятия «здоровой», «нездоровой», «отличающейся» микробиоты.
Взаимодействие между микробиотой и организмом хозяина — двустороннее, при этом липополисахарид (ЛПС) является важным медиатором, секретируемым грамотрицательными микроорганизмами, запускающими процесс воспаления в стенке кишки, наряду с пролиферацией адипоцитов и инсулинорезистентностью, объяснил Реми Бурслен (Remy Burcelin) (Университет Поля Сабатье, Франция). Бактериальная транслокация в жировую ткань также играет важную роль в развитии метаболического синдрома. Кроме того, высокие концентрации бактериальной ДНК в адипоцитах можно рассматривать в качестве молекулярных биомаркеров сахарного диабета 2-го типа.
Синдром раздраженного кишечника (СРК) — это комплексное заболевание, при котором отмечается патофизиологическое взаимодействие микробиоты и организма хозяина, как рассказал Магнус Симрен (Magnus Simrén) (Университетская больница Сальгренска, Швеция). У некоторых пациентов с СРК отсутствует четкая картина микробиоты при сравнении со здоровыми лицами. В то же время была обнаружена связь тяжести симптомов с некоторыми специфическими паттернами [3]. У пациентов с СРК можно снизить симптоматику за счет изменения структуры микробиоты (при применении пробиотиков или невсасывающихся антибиотиков).
Применение лекарственных препаратов на- прямую связано с составом микробиоты кишечника, объясняет Ринз К. Веерсма (Rinse K. Weersma) (Университетский медицинский центр Гронинген, Нидерланды). Существуют три сценария: препарат воздействует на кишечную микробиоту, изменяя ее состав/функцию, микробиота метаболизирует препарат, активируя/инакти- вируя его; или микробиота оказывает косвен- ное влияние на эффективность препарата [4]. В первом случае применение ингибиторов протонной помпы приводило к увеличению количества потенциально вредоносных бактерий (Enterococcus, Streptococcus, Staphylococcus и Escherichia). На фоне применения других препаратов (метформин, слабительные, антидепрессанты и антибиотики) отмечалось значительное влияние на микробиоту кишечника. В рамках второго сценария наиболее часто изучают сульфасалазин (который активируется под действием микробиоты) и дигоксин (который инактивируется под действием определенных штаммов бактерий).
Косвенное влияние микробиоты кишечника на эффективность препаратов было продемонстрировано в отношении противоопухолевой иммунотерапии, о которой рассказал Гарри Сокол (Harry Sokol) (Больница Сент-Антуан, Франция). Эффек- тивность препаратов анти-PD-1 при иммунотерапии меланомы, немелкоклеточного рака легкого, рака почки и других опухолей напрямую меняется в результате применения антибиотиков. Кроме того, положительное действие ипилимумаба на течение меланомы непосредственно связано с наличием Faecalibacterium prausnitzii [5].
В других исследованиях были получены аналогичные результаты, но с другими бактериями, например Akkermansia muciniphila, однако похоже, что их противовоспалительный эффект реализуется посредством пути CTL4.
