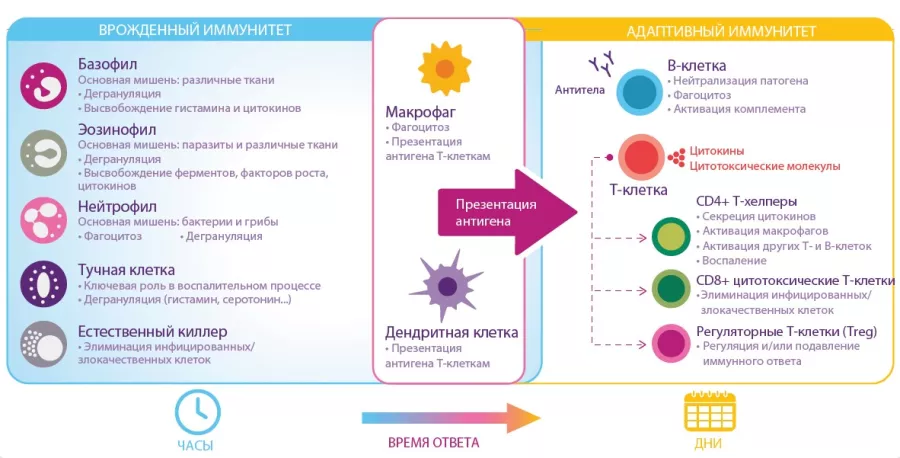
Воздействие на микробиоту кишечника для повышения эффективности вакцин
Доктор Джинелл Хили
С начала пандемии COVID-19 потребность в формировании надежного и стойкого иммунитета с помощью вакцин стала еще более очевидной20. Однако ответ на вакцинацию сильно варьируется от человека к человеку. Есть множество факторов, способных изменить иммуногенность и эффективность вакцины21 (рисунок 8). Therefore, gaining a better understanding of the factors driving variations in vaccine efficacy is critically important.
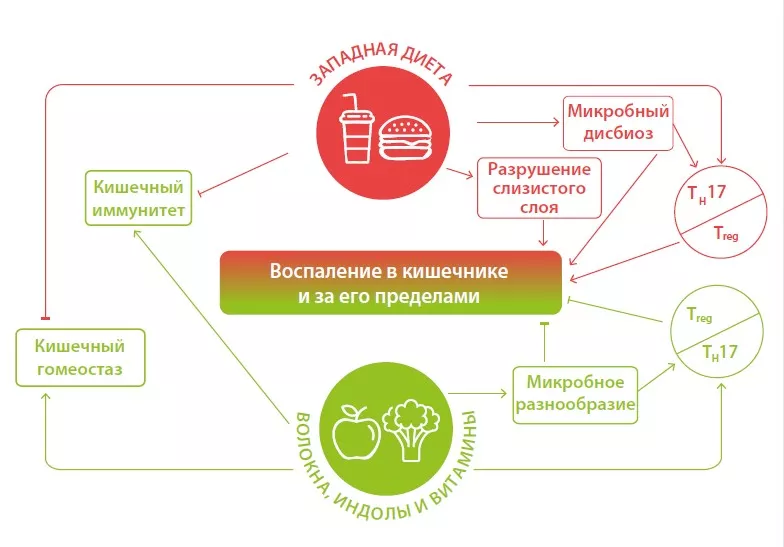
Ответ на вакцинацию сильно варьируется от человека к человеку. Есть множество факторов, способных изменить иммуногенность и эффективность вакцины. Одним из них может быть микробиота кишечника20
Одним из них может быть микробиота кишечника21. Интересно, что некоторые профили кишечной микробиоты (более высокое содержание Actinobacteria, Clostridium cluster XI и Proteobacteria) связаны с более сильным ответом на вакцинацию против таких патогенов, как ВИЧ и ротавирус22-26. Кроме того, недавно мы узнали, что вызываемый антибиотиками дисбиоз кишечной микробиоты приводит к снижению эффективности вакцинации против гриппа, что выражается снижением нейтрализации вируса с помощью антител и концентрации антител, вырабатываемых в ответ на вакцинацию.27 Эти и другие данные говорят о важном влиянии микробиоты кишечника на эффективность вакцин23,28.
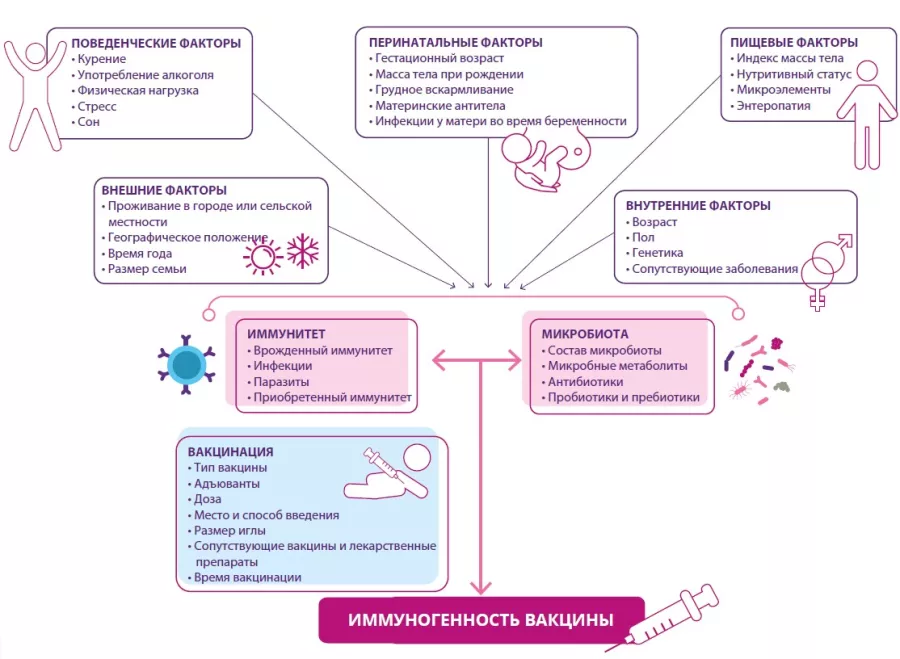
РИСУНОК 8. Возможные факторы, влияющие на иммуногенность и/или эффективность вакцин.
Большинство из них также влияют на иммунитет и состав микробиоты кишечника. Кроме того, иммуногенность вакцин зависит от их собственных характеристик.
По материалам Lynn DJ et al, 202120
До настоящего времени исследований влияния микробиоты кишечника на эффективность вакцин против SARS-CoV-2 не проводилось, но есть предположения, что у людей с дисбиозом кишечника эффективность вакцин может быть снижена. Поэтому очень важно провести исследования, которые прольют свет на влияние специфических характеристик микробиоты кишечника на эффективность вакцин против SARSCoV- 2.