ВВЕДЕНИЕ
Наиболее распространенное функциональное расстройство кишечника, синдром раздраженного кишечника (СРК), характеризуется болью или дискомфортом в животе в сочетании с изменениями частоты опорожнения кишечника и/или консистенции стула в отсутствие каких-либо определяемых структурных или биохимических аномалий, указывающих на органическое заболевание желудочно-кишечного тракта [1, 2]. Помимо боли в животе, пациенты отмечают такие симптомы, как вздутие живота и метеоризм. СРК можно разделить на подтипы в зависимости от консистенции стула: СРК-З (с преобладанием запора), СРК-Д (с преобладанием диареи) и СРК-С (смешанный вариант). С точки зрения патофизиологии СРК считается гетерогенным расстройством, в развитии которого задействовано множество механизмов, включая нарушение моторики желудочно-кишечного тракта, висцеральную гиперчувствительность, дисфункцию оси «головной мозг – кишечник». Также недавно было установлено, что к числу механизмов, участвующих в развитии СРК, относятся изменения состава и метаболизма солей желчных кислот, слабо выраженное воспаление, активация иммунной системы слизистых оболочек и изменения кишечной микробиоты [3].
В последнее десятилетие наблюдается значительный всплеск интереса к роли кишечной микробиоты в патогенезе СРК. Микробное сообщество кишечника выполняет ряд функций, включая метаболизм неперевариваемых полисахаридов, всасывание определенных питательных веществ и ионов, всасывание и запасание липидов, регуляцию метаболизма желчных кислот и выработку витаминов, таких как фолиевая кислота, биотин и витамин К [3, 4]. Конкурируя с микробными патогенами, микробное сообщество кишечника усиливает защитные характеристики желудочно-кишечного барьера. Интенсивно взаимодействуя со слизистой оболочкой, микробиота кишечника также влияет на иммунную систему и сигнальную ось «кишечник – головной мозг» [5]. Эти разнообразные свойства позволяют рассматривать микробиоту кишечника как один из ведущих потенциальных факторов развития СРК, а также как привлекательную мишень для терапии этого состояния.
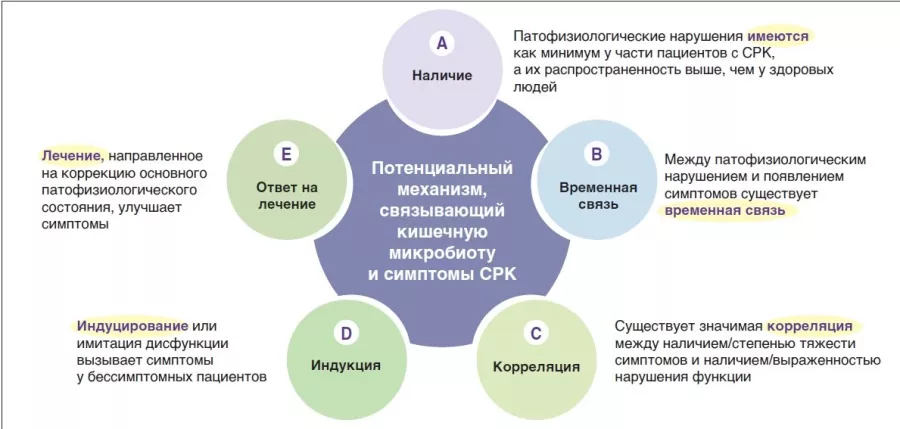
Действительно, в исследованиях патофизиологии СРК было выявлено множество механизмов, связанных с микробной экосистемой кишечника. Для многих из них получены доказательства связи с развитием СРК. Чтобы лучше разобраться в вопросе, нужно определить уровень значимости каждого предполагаемого патофизиологического процесса — это позволит расширить наши знания и начать поиск возможных терапевтических мишеней. Несколько лет назад группа международных экспертов разработала пять критериев оценки важности механизмов, лежащих в основе функциональных нарушений со стороны желудочно-кишечного тракта, таких как СРК [6]. Они основаны на таких аспектах, как наличие, временная связь, корреляция между уровнем нарушения и тяжестью симптомов, индукция у здоровых лиц и ответ на лечение (или соответствующее естественное течение, если лечение невозможно) (рисунок 1). В следующих разделах рассматривается предполагаемая гипотеза, которая учитывает факторы изменения микробиоты кишечника в качестве механизма формирования и проявления симптомов СРК. С учетом текущих знаний о кишечной микробиоте в контексте СРК это позволяет определить направления дальнейших исследований.
РИСУНОК 1
Возможные патофизиологические механизмы, связывающие СРК и микробиоту кишечника [6].
ВОЗМОЖНАЯ ПАТОФИЗИОЛОГИЧЕСКАЯ РОЛЬ МИКРОБИОТЫ КИШЕЧНИКА ПРИ СРК
НАЛИЧИЕ ИЗМЕНЕННОЙ КИШЕЧНОЙ МИКРОБИОТЫ ПРИ СРК (A)
Первый критерий заключается в том, что изменения микробиоты кишечника обнаруживаются как минимум у части пациентов с СРК [6]. В нескольких исследованиях изучали наличие и типы изменений кишечной микробиоты при СРК по сравнению со здоровыми людьми. Pittayanon и соавт. опубликовали в 2019 году систематический обзор 24 исследований из 22 публикаций, в которых кишечную микробиоту пациентов с СРК (в основном взрослых) сравнивали с микробиотой здоровых людей [7]. Они пришли к выводу, что у пациентов с СРК представители семейства Enterobacteriaceae, семейства Lactobacillaceae и рода Bacteroides были представлены сильнее, а представители Clostridiales I, рода Faecalibacterium и рода Bifidobacterium — слабее по сравнению с контрольной группой [7]. Хотя эти наблюдения указывают на возможную связь между изменениями микробиоты и СРК, между результатами разных исследований наблюдалась значительная неоднородность, объемы выборок в основном были невелики, а большинство исследований проводилось в специализированных медицинских учреждениях. Кроме того, во многих исследованиях статистические данные не были скорректированы с учетом множественных анализов, не учитывались диетические факторы и предшествующее использование пробиотиков или антибиотиков. Также авторы не выявили различий между пациентами с разными подтипами стула [7]. Точно установить долю пациентов с СРК, у которых выявляются изменения состава микробиоты кишечника, оказалось невозможно.
ВРЕМЕННАЯ СВЯЗЬ МЕЖДУ ИЗМЕНЕНИЯМИ МИКРОБИОТЫ КИШЕЧНИКА И СИМПТОМАМИ СРК (B)
Наилучшие доказательства временной связи между изменениями микробиоты кишечника и возникновением симптомов СРК можно получить из клинических наблюдений, когда СРК развивается после перенесенной инфекции (ПИ-СРК) [8]. Приблизительно у 10% пациентов, перенесших инфекционный энтерит, развивается ПИ-СРК, при этом факторами риска являются женский пол, более молодой возраст, психологический дистресс во время гастроэнтерита и степень тяжести острой инфекции. Развитие ПИ-СРК связано с изменениями микробиома кишечника и нарушениями со стороны слизистой оболочки (слабая степень выраженности воспаления, гиперплазия энтероэндокринных клеток) [8]. В то же время изменения микробиоты при ПИ-СРК, по-видимому, отличаются от тех, которые описаны у пациентов с СРК в целом.
КОРРЕЛЯЦИЯ МЕЖДУ ВЫРАЖЕННОСТЬЮ ИЗМЕНЕНИЙ МИКРОБИОТЫ КИШЕЧНИКА И ТЯЖЕСТЬЮ СИМПТОМОВ СРК (C)
Очень немногие исследователи пытались соотнести тяжесть симптомов СРК со степенью изменения состава микробиоты кишечника, также известного как «дисбиоз». Большинство из них не выявили значимых корреляций между различиями в численности или составе фекальной микробиоты и тяжестью симптомов СРК [7, 9]. Гётеборгская группа ученых использовала метод машинного обучения на большом наборе данных пациентов с СРК, что дало возможность выявить микробные сигнатуры кишечника, позволяющие прогнозировать тяжесть симптомов СРК [9], т. е. была установлена количественная связь между изменениями микробиоты кишечника и тяжестью СРК. Однако полученные результаты требуют подтверждения в других исследованиях, в том числе на материале образцов пациентов, не получающих лечения, вариации тяжести симптомов которых могут быть еще более выраженными.
ИНДУКЦИЯ СИМПТОМОВ СРК У ЗДОРОВЫХ ДОБРОВОЛЬЦЕВ ЧЕРЕЗ ИЗМЕНЕНИЯ КИШЕЧНОЙ МИКРОБИОТЫ (D)
Четвертый критерий, описанный в оригинальной статье [6], является одним из наиболее сложных для проверки. У нас есть совсем немного данных для проверки возможных патофизиологических механизмов, лежащих в основе СРК, в том числе изменений микробиоты кишечника. Наибольшую доказательную ценность имеет наблюдение, когда СРК развивается после системной антибиотикотерапии инфекций, не затрагивающих желудочно-кишечный тракт [10]. Характер нарушений кишечной микробиоты после применения антибиотиков и их сходство с нарушениями при СРК до сих пор не изучены.
ОТВЕТ НА ЛЕЧЕНИЕ, НАПРАВЛЕННОЕ НА МОДУЛЯЦИЮ СОСТАВА КИШЕЧНОЙ МИКРОБИОТЫ (E)
У нас есть достаточный объем данных, чтобы предположить, что изменения состава микробиоты кишечника могут выступать в роли патофизиологического механизма возникновения СРК.
Об этом говорит хороший терапевтический эффект плохо всасывающихся антибиотиков, которые главным образом воздействуют на микробиоту кишечника [11, 12]. Результаты двух исследований с применением неомицина и пяти исследований с применением рифаксимина показали хорошую эффективность этих местных препаратов широкого спектра у пациентов с СРК без запора [11-14]. Кроме того, в исследовании по оценке безопасности и эффективности повторного лечения рифаксимином была показана эффективность такой терапии при рецидиве симптомов СРК [15].
Пробиотики определяются как препараты, содержащие живые микроорганизмы, которые приносят пользу человеку при приеме в достаточных количествах. Несколько метаанализов подтвердили эффективность различных пробиотиков в отношении улучшения симптомов СРК [11, 16]. Однако, неоднородность дизайнов и конечных точек, а также малое число исследований, посвященных конкретным типам пробиотиков, не позволяют сделать достоверные выводы об эффективности отдельных препаратов. Напротив, по данным недавних метаанализов пребиотики, т. е. субстраты, которые избирательно используются микроорганизмами, приносящими пользу для здоровья, не показали эффективности в улучшении симптомов СРК [11, 17].
Трансплантация фекальной микробиоты (ТФМ) — вероятно, самый прямой способ воздействия на микробиоту кишечника для контроля симптомов СРК [18]. Проведенные исследования показали крайне разнообразные результаты, от отсутствия эффекта и облегчения симптомов до их ухудшения, что привело к противоречивым выводам авторов метаанализов [19, 20]. Тем не менее, недавние исследования показали, что ТФМ-индуцированные изменения в составе микробиоты кишечника приносят как минимум временное облегчение симптомов, выраженность которого зависит от характеристик доноров [21, 22].
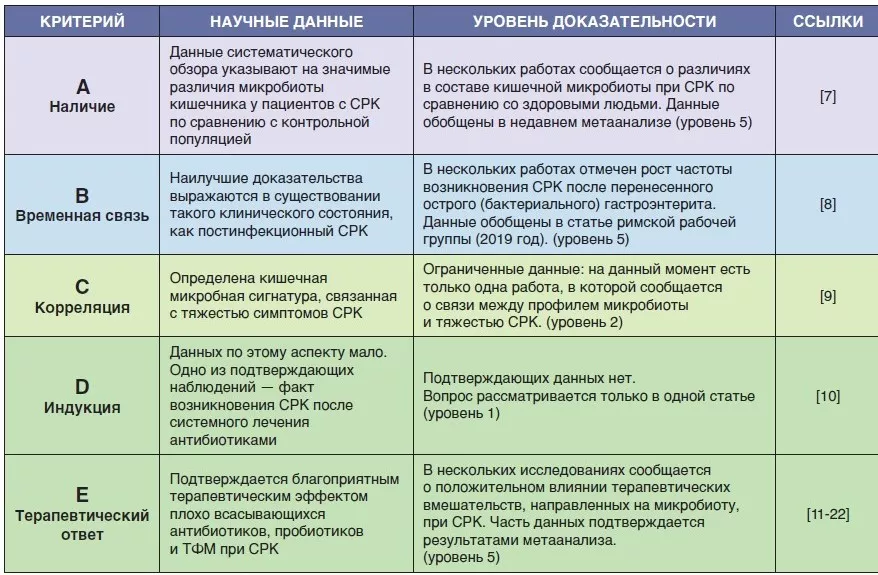
ТАБЛИЦА 1
Доказательства связи между измененной кишечной микробиотой и СРК.
НЕРЕШЕННЫЕ ВОПРОСЫ И БУДУЩИЕ ИССЛЕДОВАНИЯ
В целом изменения состава микробиоты кишечника соответствуют критериям того, чтобы их можно было рассматривать в качестве одного из патофизиологических механизмов, лежащих в основе СРК [6]. Эти данные обобщены на рисунке 2. Однако, налицо явная потребность в дополнительной информации и научных исследованиях. Необходимо проведение большего числа количественных и хорошо контролируемых исследований по изучению микробиоты кишечника при СРК у здоровых людей (контроль), с большим количеством участников, включая пациентов из неспециализированных лечебно-профилактических учреждений широкого профиля. Это позволит лучше понять изменения микробиоты кишечника при СРК на всех уровнях лечения, а также установить более точные связи между степенью изменений в составе микробиоты кишечника и тяжестью симптомов СРК. Кроме того, нужны продольные исследования для установления временной связи между изменениями микробиоты кишечника, характером и степенью тяжести симптомов во время и после рассматриваемого медицинского вмешательства.
Необходимы более качественные исследования пробиотиков при СРК с использованием стандартизированных протоколов лечения и валидированных конечных точек, аналогичных тем, которые используются в классической фармакологии. Наконец, ожидается, что будет получено много новых данных о ТФМ при СРК, что позволит определить наилучшие методики и эффективность процедуры.
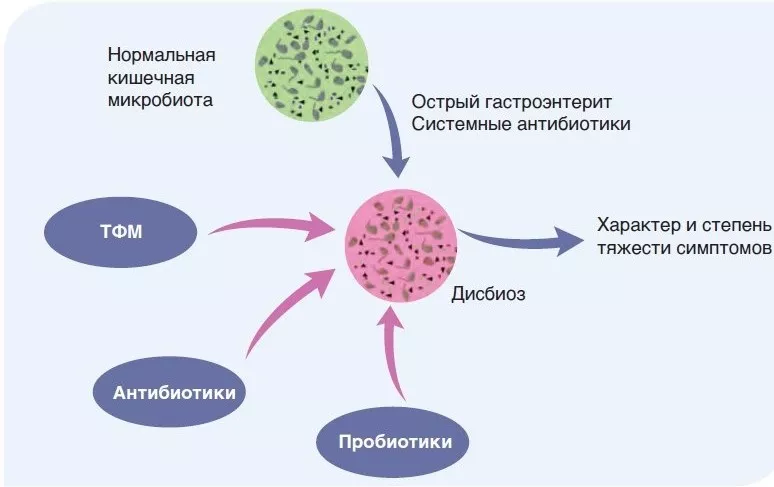
РИСУНОК 2
Патофизиологическая значимость изменений микробиоты кишечника при СРК.
Нормальный состав микробиоты кишечника отражает состояние здоровья и не связан с симптомами СРК. Острые состояния, такие как гастроэнтерит или системное применение антибиотиков, могут изменить состав микробиоты кишечника, что приводит к возникновению симптомов СРК. Состояние поддается лечению с помощью невсасывающихся антибиотиков, пробиотиков или трансплантации фекальной микробиоты.



 Микробиота ротовой полости и кишечника: к вопросу о различной тактике при менопаузе
Микробиота ротовой полости и кишечника: к вопросу о различной тактике при менопаузе
 Натуральные средства против остеопороза?
Натуральные средства против остеопороза?


 ВЗК: роль вирусов в составе кишечной микробиоты
ВЗК: роль вирусов в составе кишечной микробиоты