МИКРОБИОТА В КОНТЕКСТЕ ПАНДЕМИИ COVID-19
ОБЗОРНАЯ СТАТЬЯ
Проф. Консейсао Кальяу (Conceição Calhau)
Медицинская школа NOVA, Новый университет Лиссабона, Португалия
Проф. Педро Повоа (Pedro Povoa)
Медицинская школа NOVA, Новый университет Лиссабона, Португалия; Отделение интенсивной терапии, Больница Сан-Франциско Ксавье, Лиссабон, Португалия; Центр клинической эпидемиологии Оденсе, Университетская больница, Дания

Разнообразие микробиоты кишечника было впервые упомянуто в качестве прогностического биомаркера тяжести Covid-19. Изменения микробиоты — надежный биомаркер в контексте Covid-19, который открывает новые грани патогенеза этого заболевания, подчеркивает важность его профилактики и предлагает новые возможности лечения. В 2020 году новый коронавирус серьезно затронул жизнь пожилых людей и пациентов с ожирением, артериальной гипертензией и сахарным диабетом [1]. Важно отметить, что у всех этих пациентов был выявлен дисбиоз [2, 3].
МИКРОБИОТА КИШЕЧНИКА У ПАЦИЕНТОВ С COVID-19
Поскольку кишечная микробиота играет ключевую роль в формировании иммунитета и развитии воспаления, авторы попытались оценить связь между изменениями в составе микробиоты и особенностями клинического течения Covid-19 [4]. Было проведено национальное многоцентровое перекрестное исследование с участием 115 пациентов с Covid-19, которых разделили на группы с учетом 1) места выздоровления от Covid-19 (на дому, в обычном стационаре или отделении интенсивной терапии) и 2) особенностей течения Covid-19 (бессимптомное, легкое/умеренное или тяжелое). У тяжелых пациентов отмечались глубокие изменения в составе микробиоты кишечника по сравнению с теми, чье заболевание протекало легко или умеренно в условиях домашней изоляции или обычного стационара (рисунок 1). Эти изменения включали: 1) более низкое общее микробное разнообразие кишечника; 2) более низкое содержание полезных бутират-продуцирующих бактерий, таких как Roseburia и Lachnospira; 3) более низкое соотношение Firmicutes/Bacteroidetes; 4) более высокое содержание Proteobacteria. Также в образцах кала пациентов были обнаружены вирусные частицы, что следует учесть в противоэпидемических рекомендациях [5, 6]. В других публикациях отмечается, что низкое разнообразие микробиоты может быть прогностическим биомаркером более тяжелого течения заболевания [7-9].
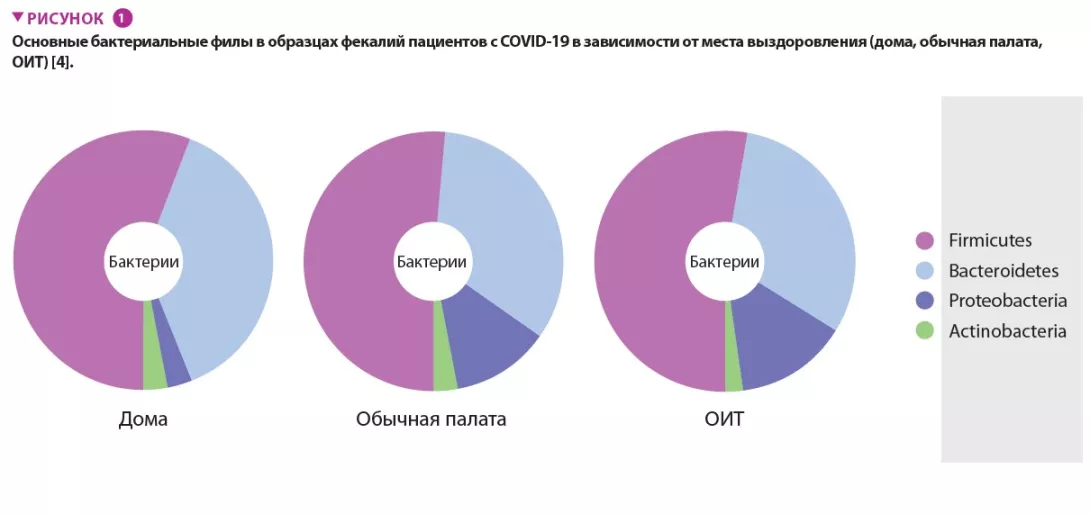
МИКРОБИОТА ОРГАНОВ ДЫХАНИЯ У ПАЦИЕНТОВ С COVID-19, НАХОДЯЩИХСЯ В КРИТИЧЕСКОМ СОСТОЯНИИ
Не так давно считалось, что здоровые легкие стерильны. Однако результаты изучения микробиоты показали, что это не так. Легкие также колонизированы бактериями, но в очень малой степени по сравнению с кишечником [10]. Разные отделы дыхательных путей (ротоглотка, трахея и бронхи, легкие) отличаются составом микробиоты, что связано с источниками колонизации, скоростью заселения и элиминации микроорганизмов. Считается, что основным источником колонизации является полость рта [11]. Недавние исследования у тяжелых пациентов с Covid-19 показали, что дисбиоз микробиоты дыхательных путей (по данным анализа жидкости, полученной п р и б р о н х о а л ь в е о л я р н о м л а в а ж е ) а н а л о г и ч е н д и с б и о з у , н а б л ю д а е м о м у п р и и н ф е к ц и я х н и ж н и х д ы х а т е л ь н ы х путей, например, пневмонии [12, 13]. Кроме того, в легких умерших пациентов чаще всего обнаруживали Acinetobacter, распространенный грамотрицательный неферментирующий патоген, вызывающий тяжелую пневмонию у пациентов ОИТ, находящихся на искусственной вентиляции легких (ИВЛ) [14]. У части умерших пациентов в ротовой полости выявляли тех же самых патогенов, что и в легких [15]. Авторы показали, что в результате иммунной дисрегуляции при Covid-19 повышается риск внутрибольничных инфекций, особенно ИВЛ-ассоциированной пневмонии, что также подтверждается результатами нескольких э п и д е м и о л о г и ч е с к и х и с с л е д о в а н и й . У п а ц и е н т о в с C o v i d - 1 9 р и с к И В Л - ассоциированной пневмонии был в два раза выше, чем у пациентов без Covid-19 [16].
ЗАКЛЮЧЕНИЕ
Исследования микробиоты при Covid-19 открывают перспективы для разработки терапевтических вмешательств (пробиотики, пребиотики и пр.), направленных на коррекцию дисбиоза, наблюдаемого у тяжелых пациентов с Covid-19. Ожидается, что эти вмешательства увеличат общее бактериальное разнообразие и преобладание комменсальных бактерий, способствуя подавлению чрезмерного роста условно- патогенных микроорганизмов. Эти исследования также могут открыть путь к разработке эффективных вакцин для профилактики Covid-19, поскольку одним из известных факторов, влияющих на эффективность вакцин, является микробиота кишечника.