ОСНОВНЫЕ НОВОСТИ КОНГРЕССА UEG WEEK 2021
ОБЗОР КОНГРЕССА
Проф. Эрик Мануэль Торо Монхараз (Erick Manuel Toro Monjaraz)
Национальный институт педиатрии, Отделение гастроэнтерологии, Мехико, Мексика

Европейская Гастро Неделя (UEG) — это Европейский конгресс по проблемам диагностики и лечения заболеваний желудочно-кишечного тракта, на котором обсуждаются последние достижения и открытия, в том числе вопросы, связанные с микробиотой. Конгресс отличает высокое качество представляемых работ, самые интересные из которых будут рассмотрены в этой статье.
НАПРАВЛЕННОЕ ВОЗДЕЙСТВИЕ НА МИКРОБИОТУ КИШЕЧНИКА ПРИ СРК
Д-р Джерард Кларк (Gerard Clark), изучающий взаимодействия и роль микробиоты при СРК, показал способность микробиоты регулировать висцеральную боль у мышей. Стерильные животные демонстрируют повышенную реакцию на стресс, а введение им пробиотиков снижало уровень кортизона, вызванный стрессом. Это взаимодействие объясняется рядом механизмов, одним из которых является серотонин. Д-р Кларк отметил статью Марко Константе, который показал, что микробиота пациентов с СРК и сопутствующей тревожностью вызывает дисфункцию ЖКТ и тревожно-подобное поведение у реципиентных животных. Это позволяет использовать пребиотики, пробиотики и ферментированные продукты в качестве психобиотиков (пробиотики, вызывающие эффекты со стороны центральной нервной системы), помогая при симптомах СРК и психических состояниях, связанных с СРК [1].
РЕЗИСТОМ В КОНТЕКСТЕ ЭРАДИКАЦИИ HELICOBACTER PYLORI
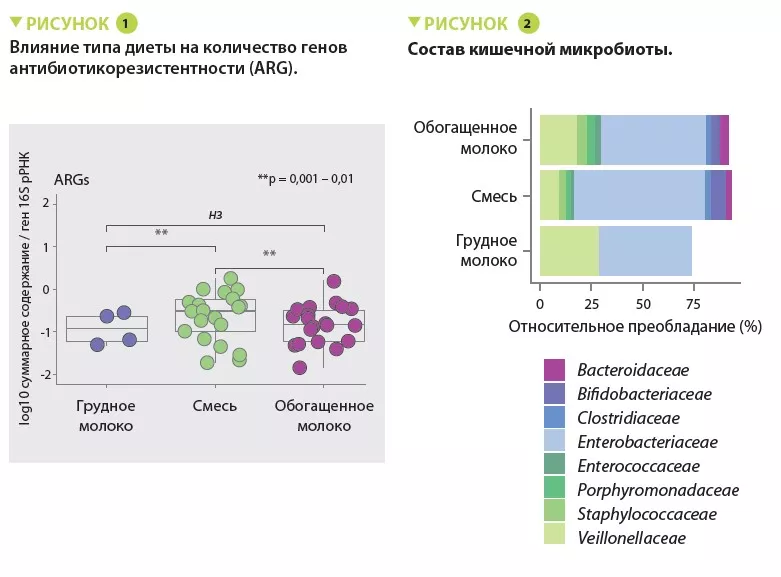
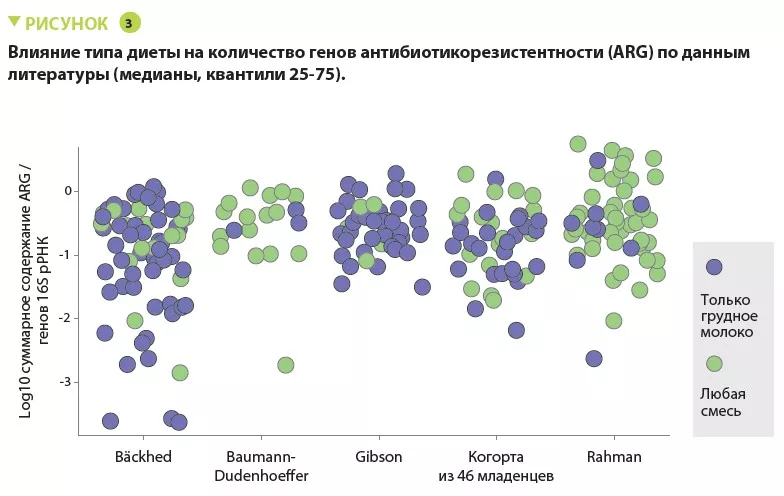
Мы знаем, что в мире растет устойчивость к противомикробным препаратам, а кишечная микробиота является резервуаром генов резистентности. Как показали предыдущие исследования, некоторые полезные для здоровья диеты и продукты, помимо своей питательной ценности, способны модифицировать резистом кишечника, что открывает многообещающие возможности. Доказано, что некоторые пробиотические штаммы уменьшают содержание мультирезистентных бактерий в кишечнике. В Кито, Эквадор, д-р Сифуэнтес (Cifuentes) и ее коллеги сравнили резистом кала пациентов, получавших лечение для эрадикации H. pylori (трехкомпонентная терапия) с добавлением определенных штаммов пробиотиков и без пробиотиков. Потребление некоторых штаммов пробиотиков уменьшало содержание генов устойчивости к противомикробным препаратам. Предлагаемый механизм — модуляция микробиоты кишечника и иммунной системы и выработка жирных кислот с антимикробными и ингибирующими свойствами в сочетании [2].
МОЖНО ЛИ ПРЕДОТВРАТИТЬ ВОСПАЛИТЕЛЬНОЕ ЗАБОЛЕВАНИЕ КИШЕЧНИКА, ВОЗДЕЙСТВУЯ НА МИКРОБИОТУ КИШЕЧНИКА?
Проф. Марла Дубински (Marla Dubinsky) постаралась ответить на этот вопрос в своем докладе. В мире отмечается рост количества пациентов с воспалительными заболеваниями кишечника (ВЗК) среди малолетних детей, а также иммигрантов второго поколения, чьи родители прибыли из регионов с низкой заболеваемостью. Это может быть связано с изменениями микробиоты кишечника. Полученные данные о роли микробиоты в развитии ВЗК, например, в исследовании MECONIUM, проведенном Torres J et al., показали, что микробиота детей, родившихся от матерей с ВЗК, отличается от микробиоты здоровых детей. Кроме того, особую роль при ВЗК играет диета. В частности, она влияет на микробиоту. Западная диета известна своими провоспалительными свойствами, в первую очередь за счет уменьшения содержания Prevotella spp в кишечнике, что приводит к повышению содержания в нем эндотоксинов. Благодаря технологическому прогрессу, в будущем мы сможем выявить конкретные популяции микроорганизмов и предотвращать ВЗК без побочных эффектов [3].
1 O’Mahony SM, Clarke G, Borre YE, et al. Serotonin, tryptophan metabolism and the brain-gut-microbiome axis. Behav Brain Res 2015; 277: 32-48.
2 Galipeau HJ, Caminero A, Turpin W, et al. Novel Fecal Biomarkers That Precede Clinical Diagnosis of Ulcerative Colitis. Gastroenterology 2021; 160: 1532-45.
3 Newman AM, Arshad M. The Role of Probiotics, Prebiotics and Synbiotics in Combating Multidrug-Resistant Organisms. Clin Ther 2020; 42: 1637-48.