A resistência aos antibióticos é uma teia de diferentes problemas
Como monitorizar os genes resistentes aos antibióticos? Como preveni-lo? Qual a relação entre a resistência aos antibióticos e a microbiota? Todas as suas perguntas respondidas aqui.

Para assinalar a Semana Mundial da Consciencialização Antimicrobiana (18-24 de novembro), o Instituto Microbiota está a divulgar a palavra a dois peritos em resistência aos antibióticos: (sidenote: A Dra. Windi Muziasari ganhou anos de experiência e conhecimentos para monitorizar a resistência aos antibióticos no ambiente utilizando um perfil genético de alto rendimento durante o seu doutoramento e pós-doutoramento na Universidade de Helsínquia, Finlândia. Queria que outros investigadores tivessem acesso fácil a esta tecnologia e foi por isso que passou da academia para o empreendedorismo, fundando a Resistomap em 2018. Sediada em Helsínquia, a missão da Resistomap é mitigar a propagação da resistência aos antibióticos, disponibilizando ferramentas robustas para a monitorização. A Resistomap combina métodos de genética molecular e ciência de dados para fornecer um serviço de deteção e quantificação de genes de resistência aos antibióticos a partir de amostras ambientais, como águas residuais e solos. Desde que entrou em pleno funcionamento em janeiro de 2019, a Resistomap já serviu mais de 250 projetos e analisou mais de 7.000 amostras ambientais em 40 países. ) , PhD, CEO da Resistomap, e Pr. (sidenote: O Christian G. Giske o médico chefe de bacteriologia, micobacteriologia e micologia no Hospital Universitário de Karolinska, em Solna, na Suécia. É também chefe das Divisões de Microbiologia Clínica e de Imunologia Clínica do Departamento de Medicina Laboratorial do Instituto Karolinska, onde também lidera um grupo de investigação. As atividades de investigação mais importantes no grupo de investigação de Giske dizem respeito à caracterização profunda dos mecanismos moleculares de resistência, virulência e epidemiologia molecular de bacilos entéricos extensivamente resistentes a medicamentos. A investigação de Giske é fortemente translacional, envolvendo uma extensa colaboração com as doenças infeciosas (incluindo a micobacteriologia), a hematologia e os cuidados intensivos. Giske tem também uma ampla colaboração internacional, servindo no conselho consultivo da vigilância europeia da resistência do CEPCD, e como presidente do Comité Europeu de Testes de Suscetibilidade Antimicrobiana. ) do Instituto Karolinska na Suécia.
O que é a Semana Mundial de Sensibilização para os Antimicrobianos?
Todos os anos, desde 2015, a OMS organiza a Semana Mundial de Sensibilização para os Antimicrobianos (WAAW), que tem como objetivo aumentar a sensibilização para a resistência aos antimicrobianos a nível global. Realizada entre 18 e 24 de novembro, esta campanha incentiva o público em geral, os profissionais de saúde e os decisores a utilizarem cuidadosamente os antimicrobianos, a fim de evitar o surgimento de uma maior resistência aos antimicrobianos.
Porque a resistência aos antibióticos é um grande problema de saúde pública?

Dr. Windi Muziasari
A resistência aos antibióticos é de facto uma ameaça global à saúde que causa anualmente mais de 1,2 milhões de mortes1. A resistência aos antibióticos é o que acontece quando os antibióticos já não são eficazes para tratar infeções bacterianas. Isto pode levar-nos de volta à era anterior à descoberta dos antibióticos por Alexander Fleming em 1928. Doenças de infeção bacteriana, como tuberculose, pneumonia, e simplesmente a infeção do trato urinário poderiam matar-nos novamente e, na pior das hipóteses, a realização de qualquer cirurgia e o parto de um bebé poderia ter elevadas taxas de mortalidade. Os antibióticos são fortemente utilizados tanto em medicamentos para uso humano como animal, o que acelera o aumento dos níveis de resistência aos antibióticos nas bactérias.

Pr. Christian G. Giske
A resistência aos antibióticos é, de facto, uma teia de vários problemas. Varia muito entre cenários geográficos, quer o problema se limite a infeções adquiridas em hospitais ou também generalizadas na comunidade. Os resultados da resistência aos antibióticos estão bem documentados: leva ao aumento da mortalidade, ao prolongamento da hospitalização, ao aumento dos custos de cuidados de saúde, e a mais efeitos secundários relacionados com o tratamento. Em muitos casos, algumas infeções adquiridas em hospitais podem ser extremamente difíceis de tratar. A resistência aos antibióticos levará também ao receio de complicações em cirurgias complicadas e/ou tratamentos imunossupressores - infeções com estirpes altamente resistentes aos medicamentos que comprometerão gravemente os resultados de outros tratamentos. Normalmente, as infeções adquiridas nos hospitais não afetarão tantos indivíduos, mas ainda assim representam um problema de saúde pública devido ao receio de que as infeções resistentes não possam ser geridas. Ao nível individual do paciente, as consequências podem ser terríveis, mas também para os pacientes da mesma unidade no hospital, aos quais podem ser transmitidas estirpes resistentes. As infeções adquiridas na comunidade afetarão mais indivíduos e também levarão a um aumento da hospitalização e, por conseguinte, afetarão a capacidade de cuidados de saúde. Não existe uma única solução para o problema da resistência aos antibióticos. É antes necessária uma combinação complexa de várias abordagens de mitigação.
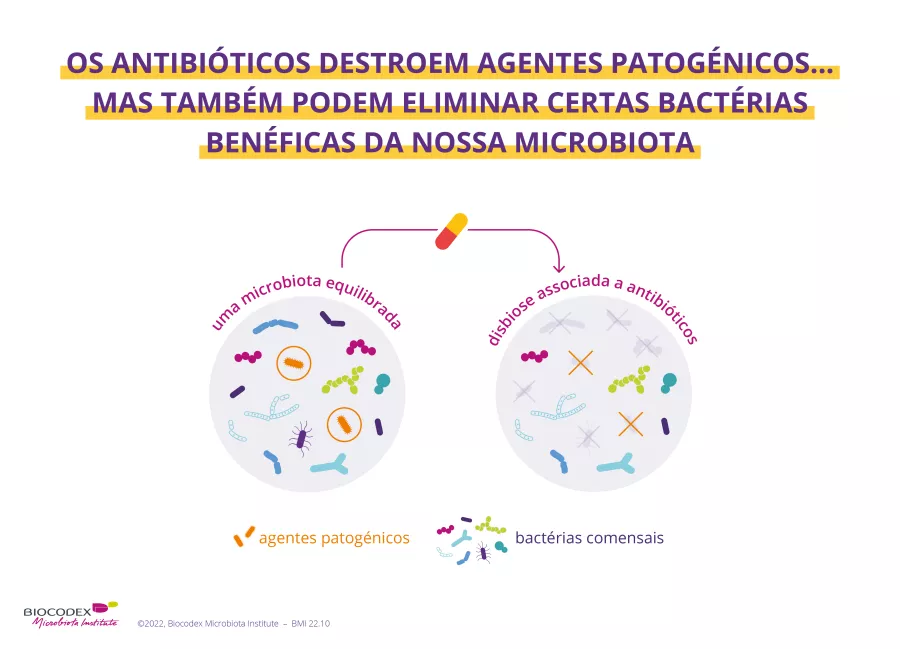
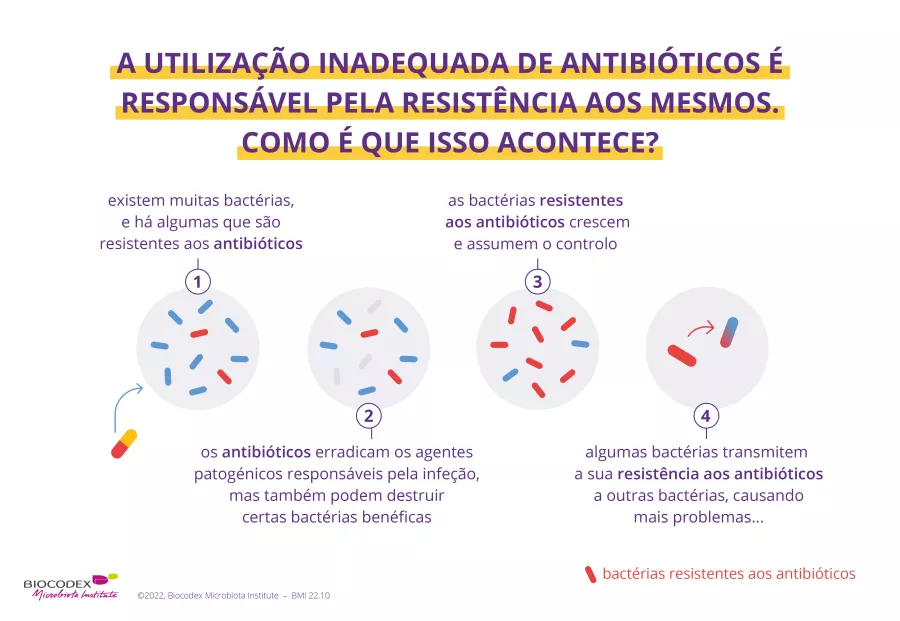
Pedra angular do moderno arsenal terapêutico, os antibióticos salvaram milhões de vidas. Por outro lado, a sua utilização excessiva e por vezes inadequada pode levar ao aparecimento de múltiplas formas de resistência dos microrganismos. Todos os anos, a Organização Mundial de Saúde (OMS) organiza a Semana Mundial de Sensibilização para os Antimicrobianos (WAAW) para aumentar a sensibilização para este problema de saúde pública. Leia a página dedicada:
Resistência aos antibióticos: a microbiota em primeiro plano
Está a monitorizar os genes resistentes aos antibióticos nos hospitais através da recolha de amostras de águas residuais. Pode explicar porque não está a recolher amostras diretamente dos pacientes para quantificar estes genes?
W. Muziasari: Existem duas importantes limitações à forma como a resistência aos antibióticos é atualmente monitorizada nos hospitais. Em primeiro lugar, a monitorização atual centra-se principalmente num número limitado de bactérias patogénicas. Em segundo lugar, baseia-se frequentemente na vigilância passiva de bactérias isoladas dos pacientes. Isto leva à deteção tardia de surtos, dados não comparáveis, e à incapacidade de capturar outras bactérias patogénicas e perfis de resistência a antibióticos que são frequentemente transportados por bactérias comensais.
A monitorização com base em águas residuais será um acréscimo potencialmente valioso às opções atuais de monitorização da resistência aos antibióticos nos hospitais. Embora não substitua os métodos de monitorização existentes, a monitorização das águas residuais pode fornecer dados que de outra forma seriam difíceis de obter e tornar-se o meio mais fácil de obter informações completas sobre a prevalência da resistência nos hospitais. Uma vez que os resíduos de todos os doentes são libertados nas águas residuais, a monitorização das águas residuais pode cobrir uma variedade mais ampla de perfis de resistência aos antibióticos em comparação com os dados parciais de algumas bactérias patogénicas selecionadas. Além disso, a análise das amostras de águas residuais não requer o consentimento informado, limitando assim as preocupações éticas. As barreiras práticas e logísticas para as amostras das águas residuais também são limitadas. Desta forma, a monitorização baseada nas águas residuais pode ser utilizada para compreender melhor o desenvolvimento e propagação de bactérias resistentes aos antibióticos nos hospitais e servir como um sistema de alerta precoce para futuros surtos.
Como é que a sua investigação e tecnologia ajuda os médicos a prevenir a resistência aos antibióticos?
W. Muziasari: Através da monitorização baseada nas águas residuais, os médicos terão informação aprofundada sobre os níveis de resistência aos antibióticos dos seus hospitais ao longo do tempo.
Resultado 1. Os hospitais ganham consciência das tendências para possíveis surtos.
Os hospitais terão uma visão mais completa sobre a presença dos genes de resistência aos antibióticos e bactérias patogénicas, o que lhes permitirá identificar possíveis surtos numa fase mais precoce. Assim, os hospitais estarão melhor preparados para tomar medidas de mitigação que levarão à diminuição de surtos de bactérias resistentes aos antibióticos nos hospitais.
Resultado 2. Os hospitais ganham consciência das implicações das atuais práticas de prescrição relativamente ao surgimento de resistência aos antibióticos.
Os hospitais poderão comparar os níveis de resistência aos antibióticos com a utilização de antibióticos dentro de um período específico. Desta forma, os hospitais tomarão consciência das implicações das atuais práticas de prescrição sobre o surgimento de resistência aos antibióticos. Portanto, os hospitais serão encorajados a melhorar a regulamentação sobre a prescrição de antibióticos, o que levará a uma utilização otimizada dos antibióticos nos hospitais.
Resultado 3. Os hospitais ganham consciência da qualidade dos fluxos das águas residuais libertados no ambiente.
Geralmente, as águas residuais hospitalares são tratadas numa instalação municipal ou própria de tratamento de águas residuais antes de serem libertadas em ambientes aquáticos. Os hospitais terão informações adicionais sobre a qualidade do fluxo de saída libertado na comunidade. Espera-se que esta informação encoraje os hospitais a melhorar a sua gestão das águas residuais, o que garantirá que as comunidades locais tenham acesso a água que é protegida da resistência aos antibióticos.
Qual a relação entre a resistência aos antibióticos e a microbiota?
C. G.Giske: Muitas estirpes resistentes são primeiro adquiridas como colonizadores no microbioma humano, quer seja intestinal ou respiratório. Assim que as estirpes sejam adquiridas no microbioma, podem estabelecer-se aí como transporte a longo prazo e, por vezes, causarão infeções no hospedeiro, ou podem propagar-se a outros indivíduos que possam ser mais suscetíveis a infeções bacterianas. Assim, o transporte de estirpes resistentes é um risco significativo de infeções resistentes, quer no hospedeiro, quer noutras pessoas próximas do hospedeiro original. No microbioma, as estirpes também podem facilmente trocar material genético e assim transmitir resistência a outras estirpes bacterianas. Por vezes, as estirpes que estão mais adaptadas ao intestino desse indivíduo e podem, portanto, permanecer no microbioma por muito tempo. A monitorização do transporte das estirpes resistentes no microbioma continua a ser uma parte importante do controlo de infeções, pois pode informar as decisões sobre os pacientes que precisam de ser hospitalizados em quartos individuais por pessoal dedicado, por exemplo, para evitar transmissões.
Apresentamos-lhe o Professor Sørensen, galardoado com a Bolsa Internacional 2022 da Biocodex Microbiota Foundation.
Su equipo fue el primero en lanzar un estudio de gran evergadura sobre el resistoma de 700 niños, que permitirá dar un paso agigantado en la comprensión de la evolución y diseminación de la resistencia a los antimicrobianos en el intestino humano al principio de la vida.
Poderá a microbiota ajudar os investigadores a combater a resistência aos antibióticos?
C. G.Giske: O microbioma é complexo e contém uma variedade de microrganismos, entre os quais também vírus. Alguns dos vírus, os chamados bacteriófagos, podem infetar seletivamente as estirpes bacterianas e matá-las. Esses bacteriófagos podem ser isolados do microbioma e podem ser utilizados terapeuticamente para tratar infeções em doentes. Numerosos estudos destacam o potencial in vitro e in vivo das suas utilizações terapêuticas e, embora tenham sido realizados vários ensaios clínicos ao longo da última década, o maior desafio continua a ser o de produzir dados adicionais que apresentem um sólido argumento regulamentar para a sua utilização clínica2. Além disso, a monitorização da resistência no microbioma pode ser altamente informativa para compreender o conjunto de genes de resistência disponíveis numa população e pode ser muito útil para conceber estratégias para combater a resistência aos antibióticos.