A Microbiota Vaginal #15
Pelo Pr. Markku Voutilainen
Faculdade de Medicina da Universidade de Turku, Gastroenterologia, Hospital Universitário de Turku, Finlândia



Pelo Pr. Markku Voutilainen
Faculdade de Medicina da Universidade de Turku, Gastroenterologia, Hospital Universitário de Turku, Finlândia

Prever o risco de nascimento prematuro utilizando um método simples, rápido e barato é um desafio para os obstetras, que ainda carecem de um método de previsão fiável para esta complicação clínica, a principal causa de morte em crianças com menos de cinco anos de idade. Os fatores de risco são bem conhecidos: disbiose vaginal associada a inflamação local. Uma equipa de investigadores teve a ideia de utilizar o seu método de análise DESI-MS (Desorption Electrospray Ionization Mass Spectrometry) recentemente descrito para identificar – em menos de 3 minutos e sem necessidade de preparação de amostras – os metabolitos presentes na mucosa cervicovaginal. As suas hipóteses? O metaboloma assim caracterizado pode tornar possível prever a composição da microbiota vaginal e as respostas imunitárias e inflamatórias locais, e monitorizar o seu desenvolvimento para estados associados ao risco de nascimento prematuro. O DESI-MS foi utilizado para analisar mais de 1.000 amostras cervicovaginais de 365 mulheres grávidas em duas coortes.
Entre os metabolitos detetados, 113 permitiram distinguir eficazmente dois tipos de microbiota: uma esgotada e a outra dominada por lactobacilos, um marcador de boa saúde vaginal. O perfil metabólico obtido utilizando o DESI- MS também previu os níveis de vários marcadores imunitários (IL-1β, IL-8, C3b/ iC3b, IgG3, IgG2, MBL – Manose-Binding Lectine) medidos num subgrupo de 391 mulheres. Alguns destes (C3b, IL-1β, IgG2, IgG3) foram encontradas a níveis elevados em microbiomas vaginais sem Lactobacillus, o que indica a ativação da resposta imunitária inata e adaptativa local. Numa série final de testes, o perfil metabólico vaginal obtido utilizando o DESI- MS não podia prever com fiabilidade o risco direto de nascimento prematuro. No entanto, os investigadores preveem potenciais aplicações clínicas. A monitorização dos metabolitos vaginais utilizando o DESI-MS poderia ajudar a detetar alterações na microbiota vaginal e nos marcadores imunitários locais associados ao parto prematuro.
Pelo Pr. Markku Voutilainen
Faculdade de Medicina da Universidade de Turku, Gastroenterologia, Hospital Universitário de Turku, Finlândia
O cancro da próstata (PC) é um dos cancros mais comuns nos homens. Como o crescimento e progressão dos tumores dependem dos níveis de androgénio, a terapia de privação de androgénio (ADT), a castração cirúrgica ou química é utilizada para tratar doentes com PC. No entanto, alguns deles desenvolvem um cancro da próstata resistente à castração (CRPC) que resulta na progressão do tumor e estão a ser investigadas novas estratégias de tratamento. Desde que estudos recentes destacaram o papel da microbiota tanto no desenvolvimento do cancro como no sucesso da terapia, os autores utilizaram modelos de ratinhos de PC e dados de doentes para examinar o papel da microbiota intestinal na carcinogénese de PC. O enriquecimento de Ruminococcus spp e Bacteroides acidifaciens foi detetado após o desenvolvimento de CRPC mas a ablação da microbiota intestinal abrandou o crescimento tumoral em ratinhos com CRPC. O transplante de microbiota fecal resistente à castração (FMT) de ratinhos resistentes à castração (CR) e a administração de R. gnavus levaram ao aumento dos níveis de androgénio circulante e ao aumento do crescimento de PC e do desenvolvimento de CRPC. O crescimento do PC foi controlado por FMT a partir de indivíduos com PC sensíveis às hormonas e à administração de Prevotella stercorea. Os doentes com CRPC tiveram enriquecimento dos géneros Ruminococcus e Bacteroides, associando se a resultados fracos, enquanto os doentes com PC sensíveis às hormonas tiveram uma maior abundância do género Prevotella associada a resultados mais favoráveis.
A microbiota intestinal comensal em doentes e ratinhos com privação de androgénios produz androgénios que, através da circulação sistémica, promovem o crescimento de PC e o desenvolvimento de CRPC. A modulação da microbiota intestinal poderia, teoricamente, ser utilizada como terapia adicional para o PC.
Doença pulmonar obstrutiva crónica (DPOC) refere-se a doenças pulmonares (enfisema, bronquite e asma) caracterizadas por progressiva dificuldade respiratória. Estudos recentes revelaram que as mudanças na microbiota intestinal são semelhantes ao desenvolvimento da doença nos pulmões. Embora considerada principalmente uma doença respiratória, normalmente, a DPOC ocorre de forma concomitante com doenças crónicas do trato gastrointestinal. No presente estudo, os autores interessaram-se pelo eixo intestino-pulmão ligado à DPOC. As análises das fezes revelaram que os doentes com DPOC grave tinham uma menor abundância de Bacteroidetes, mas uma maior abundância de Firmicutes. Das famílias bacterianas, a abundância de Prevotellaceae foi maior na DPOC ligeira, enquanto que as abundâncias de Bacteroidaceae e Fusobacteriaceae foram menores na DPOC grave em comparação com os controlos saudáveis. Os níveis de ácido gordo de cadeia curta (SCFA) foram significativamente mais baixos na DPOC grave. A transferência de microbiota fecal (FMT) para ratinhos de doentes com DPOC causou uma redução significativa do peso e hipersecreção do muco das vias respiratórias em ratinhos. A aceleração do declínio da função pulmonar foi detetada em ratinhos FMT durante a exposição ao fumo de biomassa. Este estudo revelou que os doentes com DPOC têm disbiose da microbiota intestinal com níveis reduzidos de SCFA. Estas alterações estão possivelmente ligadas à inflamação das vias respiratórias e à progressão da DPOC.
Os inibidores de pontos de controlo imunitários (ICI) melhoraram drasticamente o prognóstico de vários cancros avançados. As provas demonstraram que a microbiota intestinal pode modular a resposta ao tratamento para ICI, e pode também estar envolvida na patogénese de eventos adversos relacionados com a imunidade (IRAE). Embora se saiba que os antibióticos deterioram o prognóstico dos doentes com cancro tratados com ICI, pouco se sabe sobre o efeito na microbiota de várias co-medicações quando administradas no início de ICI. No presente estudo, os autores analisaram o efeito das co-medicações dadas 1 mês antes ou depois da administração da terapia ICI nos resultados do tratamento e a ocorrência de IRAE.
O uso de antibióticos, glicocorticoides (dose diária > 10 mg), inibidores da bomba de protões, fármacos psicotrópicos, morfina e insulina foi associado a uma sobrevida significativamente encurtada e a uma resposta tumoral reduzida. A terapia de combinação com estes medicamentos diminuiu a sobrevida mais do que a monoterapia. Estes medicamentos foram também associados a uma diminuição da incidência de IRAE. A co-administração de estatinas, inibidores de enzimas conversoras de angiotensina e/ou bloqueadores de recetores de angiotensina II, anti-inflamatórios não esteroides, aspirina e medicamentos antidiabéticos orais não teve impacto na sobrevida dos doentes. O presente estudo mostrou que a co-medicação influencia tanto a resposta como os IRAE do tratamento ICI. O impacto da co-medicação pode ser mediado através de microbiota ou outros mecanismos imunomoduladores. Na prática clínica, as co-medicações de base devem ser cuidadosamente avaliadas quando a terapia ICI é planeada. Os medicamentos com impacto negativo na terapia ICI devem ser evitados sempre que possível.
FEEDBACK DE CONGRESSOS
Pelo Pr. Eamonn M M Quigley
Lynda K and David M Underwood Center for Digestive Disorders, Division of Gastroenterology and Hepatology, Houston Methodist Hospital and Weill Cornell Medical College, Houston, Texas, USA

A WCOG 2020 estava programada para se realizar em Praga, a capital da República Checa, no final de 2020, mas foi adiada devido à pandemia da Covid e decorreu como uma reunião híbrida de 9 a 11 de dezembro de 2021. Graças à diligência e capacidade de organização de todos os envolvidos, foi desenvolvida uma excelente plataforma de reuniões virtuais que permitiu a transmissão de simpósios que abrangeram todo o espectro da especialidade, palestras especiais, comunicações livres originais e cartazes para o mundo inteiro. Nestas sessões, especialistas de todo o mundo juntaram- se aos professores da República Checa para abordar temas «quentes» e controversos. Aqui está um enfoque no microbioma intestinal.
Em 2020, o tema do Dia Mundial da Saúde Digestiva, patrocinado pela WGO, foi «Questões Globais do Microbioma». Eamonn MM Quigley, em nome dos muitos colegas que contribuíram para este programa, apresentou os seus trabalhos que encapsularam uma visão geral do microbioma intestinal. Os fatores que influenciam o microbioma e moldam o seu desenvolvimento através desse período crítico e vulnerável desde o nascimento até à primeira infância foram delineados e o papel da dieta, ao longo da vida do indivíduo, sublinhado. Embora tenha sido proposto um papel para o microbioma em muitos estados patológicos, muitos estudos descrevem a associação, não a causa.
Uma doença em que um papel para o microbioma tem gerado muito entusiasmo é a síndrome do intestino irritável (SII). Mirjana Rajilic-Stojanovic explorou isto em pormenor e delineou os fatores que compõem a interpretação dos estudos microbiológicos na SII (por exemplo, pequeno tamanho da população estudada, heterogeneidade do fenótipo, conceção variável do estudo) que, sem dúvida, contribuem para a ausência de uma assinatura microbiana consistente na SII. Ela alertou-nos para dois organismos que podem ser de particular interesse: Methanobrevibacter smithii e Faecalibacterium prausnitzii; o primeiro através da sua produção de metano e o segundo através do seu papel na sinalização de células enterocromafínicas levando ao aumento da biossíntese da serotonina – um neurotransmissor fundamental do sistema nervoso entérico e alvo de muita farmacologia da SII.
O microbioma oferece um enorme potencial terapêutico. Francisco Guarner atualizou a orientação probiótica da WGO e o fascinante tema do Transplante de Microbiota Fecal (FMT) foi abordado por Pavel Drastich. Ele contrastou a eficácia do FMT em doenças relacionadas com Clostridioides difficile com os dados muito mais mistos de outros estados patológicos. Entre estes últimos, a colite ulcerosa fornece os melhores dados (embora ainda classificados como de qualidade apenas moderada). Aqui, a interpretação dos resultados é obstaculizada pelos mesmos fatores que confundem tantos estudos de FMT: variabilidade na seleção da população, pontos finais de estudo e protocolo de estudo. Este último inclui variáveis tão incómodas como a utilização de fezes frescas vs. congeladas, via de administração (naso-jejunal, vs. enema, vs. colonoscopia vs. cápsula engolida), número de tratamentos (único vs. múltiplo) e fonte de material (único doador vs. material agrupado de múltiplos doadores). O mais fascinante foi o vislumbre que ele deu sobre o futuro do FMT, prevendo uma evolução do FMT tal como o conhecemos atualmente (isto é, amostras de fezes inteiras) através do desenvolvimento de combinações específicas ou consórcios de micróbios (uma área de atividade científica e comercial frenética) para a elaboração de compostos biológica e terapeuticamente ativos a partir de micróbios. Tanto a promessa como as limitações do FMT na SII foram desenvolvidas por Mirjana Rajilic-Stojanovic. Aqui os confundidores são vividamente expostos: um fenótipo altamente heterogéneo com uma gama variável e gravidade de sintomas que flutuam ao longo do tempo, uma compreensão incompleta do papel do microbioma e um conceito, na melhor das hipóteses, especulativo de como o FMT poderia funcionar. Não é de admirar que os resultados, até à data, sejam tão variáveis.
Francisco Guarner liderou uma das sessões de abertura de todo o programa sobre um tema que retive até ao fim desta peça – a situação atual da investigação da microbiota. Esta foi uma palestra tipicamente atenciosa e perspicaz e muito oportuna, dado o impacto da epidemia da COVID-19 e da crise global de resistência aos antibióticos; será que precisamos de mais lembranças da importância dos micróbios que coabitam este planeta connosco? Voltou ao tema global ilustrando a primazia da dieta pobre na mortalidade global de risco, mas salientou habilmente que estas mesmas dietas empobrecem não só os humanos, mas também os seus micróbios e produtores de butirato em particular. Baixos níveis de diversidade microbiana intestinal foram ligados a vários estados patológicos, sendo um dos exemplos mais convincentes a asma infantil. Olhando para o futuro, salientou as inadequações de uma abordagem taxonómica ao estudo do microbioma em estados patológicos e ilustrou este ponto mostrando que em indivíduos normais a composição do microbioma intestinal é altamente dinâmica; até 90% das estirpes aparecem e desaparecem com o tempo! Assim, apelou a uma nova abordagem à definição de microbiomas normais vs. anormais (ou eubiose vs. disbiose, como alguns preferem) que enfatizava a competência funcional e a estabilidade ecológica (incorporando conceitos como a resistência à mudança estrutural da comunidade ao longo do tempo e a resiliência, a capacidade de regressar rapidamente à linha de base quando perturbada, como por exemplo por um antibiótico). Estes são conceitos-chave e refletem o atual afastamento da simples enumeração de números, espécies e estirpes microbianas para a descrição do potencial funcional utilizando a metagenómica e os ensaios de produtos metabólicos através da metabolómica e da metatranscriptómica.
ARTIGO COMENTADO - RUBRICA PEDIÁTRICA
Pelo Pr. Emmanuel Mas
Gastroenterologia e Nutrição, Hospital Saint-Antoine, Paris, França

Os lactantes correm um risco elevado de contrair infeções fatais cujo tratamento depende do funcionamento dos antibióticos. Os genes de resistência aos antibióticos (ARGs) estão presentes em grande número nos microbiomas intestinais dos lactantes nunca tratados com antibióticos, e a mortalidade infantil causada por infeções resistentes é elevada.
Neste artigo os autores pretendem determinar o impacto da exposição precoce à fórmula na carga de ARG em recém-nascidos e lactantes nascidos antes do termo ou de termo. Uma suposição foi que a dieta exerce uma pressão seletiva que influencia a comunidade microbiana no intestino dos lactantes e a exposição a fórmulas aumenta a abundância de ARG que transportam taxa.
O estudo mostrou que os lactantes alimentados com fórmulas tinham uma maior abundância relativa de agentes patogénicos oportunistas como Staphylococcus aureus, S. epidermidis, Klebsiella pneumoniae, K. oxytoca e Clostridioides difficile. Os lactantes alimentados com fórmulas também tinham significativamente menos bactérias infantis típicas, como as bifidobactérias, que têm potenciais benefícios para a saúde.
A nova conclusão de uma correlação entre a exposição a fórmulas e uma maior carga de ARG neonatal mostra que os clínicos devem considerar o modo de alimentação, além do uso de antibióticos nos primeiros meses de vida, para minimizar a proliferação de bactérias intestinais resistentes a antibióticos em lactantes.
As bactérias resistentes aos antibióticos são a causa de muitas mortes neonatais. O aparecimento de bactérias resistentes é favorecido pelo uso de antibióticos, que está associado a um maior número de genes de resistência aos antibióticos (ARGs) transportados por estas estirpes bacterianas resistentes ou multirresistentes. Os elementos genéticos móveis (MGEs) transmitem os ARGs entre bactérias. Sabe-se também que o tipo de dieta modifica a microbiota intestinal, assim como a quantidade de ARGs. A magnitude do impacto da dieta infantil na resistência não tem sido adequadamente descrita na literatura.
Os autores incluíram 46 lactantes nascidos prematuros entre as 26 e as 37 semanas de gestação dos quais 21 foram alimentados com fórmula, 20 com leite materno fortificado e 5 com leite materno. Foram recolhidas fezes no prazo de 36 dias para analisar a composição da microbiota intestinal e a presença de ARGs. Trinta lactantes receberam um tratamento antibiótico: as fezes foram recolhidas cerca de duas semanas após o final do tratamento para limitar os efeitos de confusão.
Para comparar os resultados com os dados da literatura, foi analisada em paralelo uma meta-análise de cinco estudos, incluindo 696 recém-nascidos com dados semelhantes.
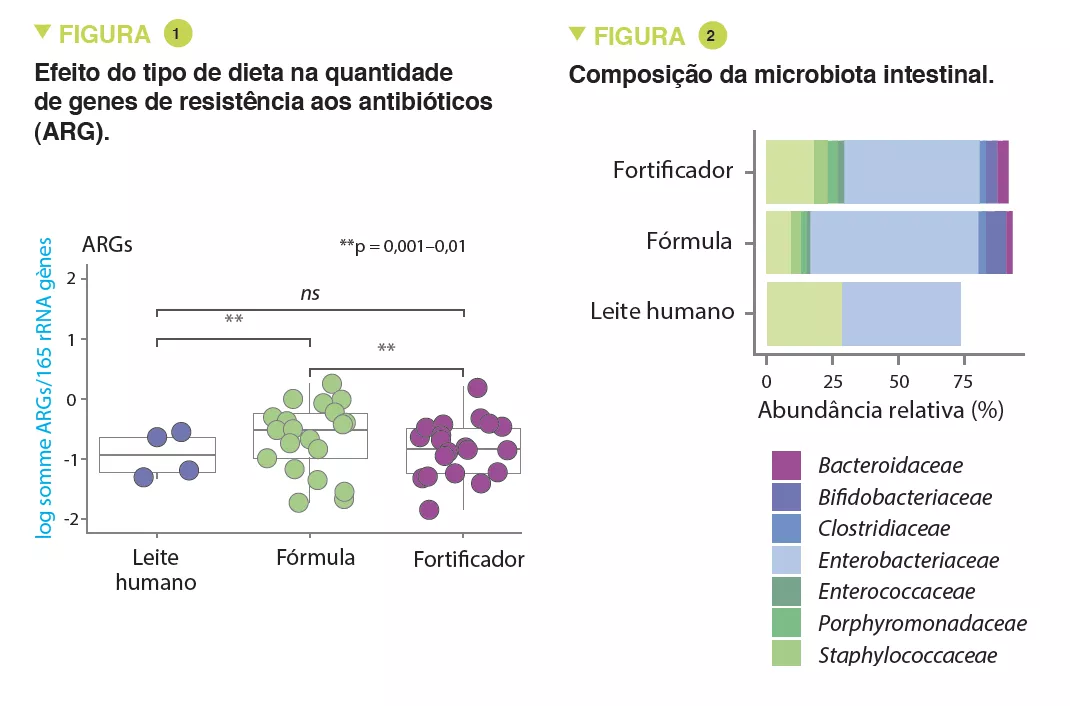
Os resultados mostraram que os lactantes alimentados com fórmula tinham quantidades significativamente mais elevadas de ARGs do que os lactantes alimentados com leite materno fortificado (x 3,6; 95% CI, 1,61-8,9) ou leite materno (x 4,3; 95% CI, 1,61-11,56) (p<0,01) (Figura 1).
A abundância de MGEs aumentou de forma semelhante (p<0,05). A abundância de Enterobacteriaceae, cujo genoma é conhecido por conter mais ARGs móveis, foi maior em lactantes alimentados com fórmulas (p<0,05) (Figura 2) e tendeu a estar inversamente correlacionada com a idade gestacional (p<0,1). Observou- se que quanto mais longa a gestação, menor a abundância destes ARGs (x 0,72; 95% CI, 0,57-0,89) (p<0,001). Vários ARGs eram significativamente mais abundantes em lactantes alimentados com fórmulas, incluindo genes que codificam a beta-lactamase de espectro alargado presente em Klebsiella (p<0,05).
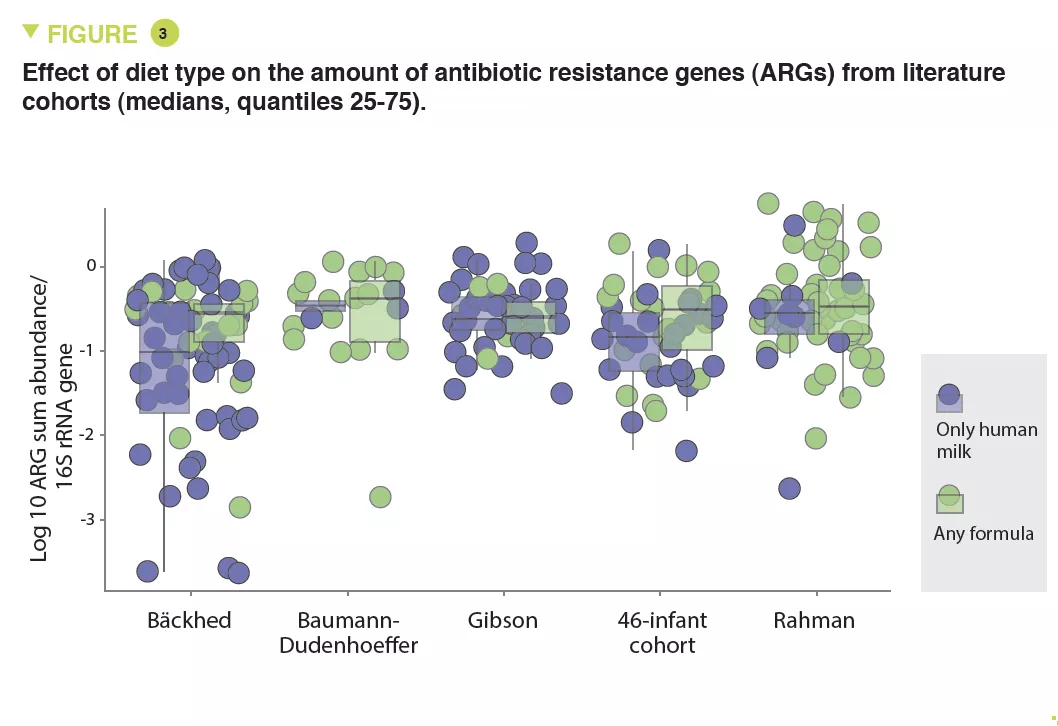
Resultados semelhantes foram observados na meta-análise com um aumento relativo de 70% de ARGs em recém-nascidos alimentados com fórmulas (p=0,013). A carga mediana de ARG foi mais elevada nos lactantes alimentados com fórmulas em todas as coortes (Figura 3). Por último, uma análise da microbiota intestinal revelou que as bactérias pertencentes às famílias Bifidobacteriaceae, Veillonellaceae, Clostridiaceae, Lachnospiraceae e Porphyromonadaceae (incluindo as bactérias anaeróbias estritas) eram escassas em recém-nascidos alimentados com fórmula infantil; pelo contrário, as bactérias anaeróbias facultativas pertencentes às famílias Enterobacteriaceae, Staphyloccoccaceae e Enterococcaceae estavam aumentadas (p<0,05). Do mesmo modo, várias espécies potencialmente patogénicas incluindo espécies anaeróbias facultativas, como S. aureus, S. epidermidis, K. pneumoniae, K. oxytoca, e uma espécie anaeróbia rigorosa Clostridioides difficile, foram enriquecidas em recém-nascidos alimentados com fórmulas (p<0,001). Assim, a utilização de fórmulas infantis aumenta a proliferação de bactérias patogénicas com ARGs.
Estes resultados apoiam o benefício do aleitamento materno. A alimentação de recém nascidos prematuros com leite materno está associada a um aumento de 70% dos ARGs em comparação com os alimentados exclusivamente com leite materno. O leite materno enriquecido resulta num menor aumento destes ARGs.
Além do uso adequado de antibióticos, é importante considerar o tipo de dieta para recém-nascidos prematuros, com preferência pelo leite materno para evitar a proliferação de bactérias resistentes.
ARTIGO COMENTADO - FASE ADULTA
Pelo Pr. Harry Sokol
Gastroenterologia e Nutrição, Hospital Saint-Antoine, Paris, França
Apesar do sucesso geral, os inibidores de pontos de controlo das células T para o tratamento do cancro (imunoterapia anticancerígena) continuam a ser eficazes apenas numa minoria de doentes. Verificou-se recentemente que a microbiota intestinal modula criticamente a imunidade anticancerígena e a resposta terapêutica. Neste artigo os autores identificaram os membros Clostridiales da microbiota intestinal associados a uma menor carga tumoral em modelos de ratinho com cancro colorretal (CCR). Curiosamente, estas espécies comensal estão também significativamente reduzidas em doentes com CCR, em comparação com controlos saudáveis. A administração por sonda gástrica de uma combinação de quatro estirpes de Clostridiales (CC4) em ratinhos preveniu e até tratou com sucesso o CCR como terapia autónoma. Este efeito esteve dependente da infiltração intratumoral e ativação das células T CD8+. A administração de uma única estirpe de Roseburia intestinalis ou Anaerostipes caccae foi ainda mais eficaz do que CC4. Numa comparação direta, a suplementação da combinação CC4 superou a terapia anti-PD-1 nos modelos CCR e melanoma de ratinho. Estas conclusões fornecem uma forte base pré-clínica para explorar as bactérias intestinais como nova terapia autónoma contra tumores sólidos.
A microbiota intestinal desempenha um papel importante no desenvolvimento do sistema imunitário e na manutenção da homeostase imunitária. A microbiota intestinal influencia o sistema imunitário tanto a nível local como sistémico, mantendo uma resposta imunitária equilibrada. Em comum com uma vasta gama de doenças como a obesidade, doença inflamatória crónica do intestino, doenças neuropsiquiátricas e cancro colorretal (CCR), está implicada uma perturbação do equilíbrio microbiano (disbiose).
O CCR, enquanto uma das doenças malignas mais frequentemente diagnosticadas, continua a ser a principal causa de mortes por cancro a nível mundial relacionadas com o estilo de vida (dieta, tabaco, álcool) ou fatores de risco de obesidade, todos intimamente relacionados com alterações na composição da microbiota intestinal saudável.
A microbiota intestinal é alterada em doentes com CCR, com um aumento dos taxa como Bacteroides ou Fusobacterium [2] e uma diminuição dos taxa bacterianos Clostridiales em comparação com indivíduos saudáveis [3]. A maioria dos tumores colorretais têm baixa imunogenicidade e, por conseguinte, não respondem às imunoterapias atuais de ativação de células T. Os anticorpos monoclonais anti-PD-1, anti- PD-L1 e/ou anti-CTLA4 só são eficazes em 4-5% dos tumores do CCR com um defeito de reparação sem correspondência ou instabilidade elevada dos microssatélites [4]. Estudos recentes mostraram como alguns membros da microbiota intestinal são capazes de modular a eficácia dos tratamentos anticancerígenos [5, 6]. Neste estudo, os autores avaliaram se um cocktail de quatro estirpes bacterianas, especificamente associado a uma baixa carga tumoral num modelo experimental de CCR, poderia desencadear uma resposta imunitária antitumoral eficaz.
Com base em modelos animais, os autores observaram que os ratinhos com uma microbiota baixa em bactérias Clostridiales (famílias Ruminococcaceae e Lachnospiraceae) tinham uma maior suscetibilidade ao CCR. Com base nestas análises, os autores selecionaram uma combinação de quatro espécies de Clostridiales (CC4), ou seja, Roseburia intestinalis, Eubacterium hallii (Anaerobutyricum hallii), Faecalibacterium prausnitzii e Anaerostipes caccae, cuja abundância diminui em doentes com CCR, para realizar estudos adicionais em modelos de ratinhos. A administração de CC4 teve um efeito na microbiota dos ratinhos, com um aumento das espécies pertencentes às famílias Ruminococcaceae e Lachnospiraceae.
Em vários modelos de cancro sólido, incluindo CCR, cancro do pulmão e da mama, a administração de CC4 retardou o crescimento do tumor. Este benefício foi principalmente mediado por linfócitos, uma vez que desapareceu em ratinhos sem linfócitos maduros (ratinhos Rag2 KO). Os principais candidatos são células T CD8+ citotóxicas produtoras de interferão-gama, que se infiltram de forma massiva no tumor em animais que recebem o CC4. O efeito protetor foi também observado individualmente com cada uma das estirpes bacterianas testadas num modelo CCR, mas com diferentes graus de eficácia (Figura 1). O efeito terapêutico não esteve relacionado com as bactérias produtoras de butirato.
Por último, no modelo CCR (MC-38), o cocktail CC4 teve um efeito superior à imunoterapia anti-PD-1. Além disso, não foi observado qualquer efeito aditivo entre os ratinhos que receberam imunoterapia e as quatro bactérias.
Este estudo demonstrou que, além de terem um papel adjuvante no tratamento imunoterapêutico do cancro, algumas bactérias da microbiota exercem o seu próprio efeito anticancerígeno em modelos de ratinhos com tumores sólidos. Estes resultados abrem o caminho para o desenvolvimento de tratamentos do cancro no homem com base na microbiota intestinal. Estas terapias poderiam ser utilizadas isoladamente ou em combinação com outros tratamentos “convencionais” anticancerígenos. Contudo, os grupos de doentes que mais beneficiariam com este tipo de abordagem terapêutica ainda estão por determinar.
Este estudo em ratinhos mostrou que as estirpes bacterianas Clostridiales, que são significativamente mais baixas em doentes com cancro colorretal, são eficazes para estimular uma resposta anticancerígena a tumores sólidos. Os mecanismos envolvem a ativação de células T CD8+ e são independentes da imunoterapia anti-PD-1.
Síntese
Pelo Pr. Conceição Calhau
NOVA Medical School, Universidade Nova de Lisboa, Portugal
Pelo Pr. Pedro Povoa
NOVA Medical School, Universidade Nova de Lisboa, Portugal; Unidade de Cuidados Intensivos Polivalente, Hospital de São Francisco Xavier, CHLO, Lisboa, Portugal; Centro de Epidemiologia Clínica, OUH Odense, Hospital Universitário, Dinamarca

Pela primeira vez, a diversidade da microbiota intestinal é apontada como um biomarcador prognóstico da gravidade da Covid-19. Assim, as alterações da microbiota como biomarcadores fiáveis no contexto da Covid-19 representa uma peça chave do puzzle da doença, destacando assim a prioridade clínica para a prevenção e possivelmente novas estratégias terapêuticas. Em 2020, o novo coronavírus afetou gravemente determinados grupos da população, mais especificamente, os idosos e as pessoas com obesidade, hipertensão, diabetes [1]. Curiosamente, as publicações mostraram que a disbiose é um fator comum em todos estes doentes [2, 3].
Como a microbiota intestinal tem sido considerada um tema quente na comunidade científica com um papel central nas funções imunitárias e inflamatórias do hospedeiro, investigámos se alterações na composição da microbiota intestinal estão associadas a uma maior gravidade clínica da Covid-19 [4]. Foi realizado um estudo multicêntrico nacional transversal em 115 doentes com Covid-19 categorizados por: 1) local de recuperação da Covid-19: ambulatório (isolamento doméstico), enfermaria ou unidade de cuidados intensivos; e 2) escala de gravidade da Covid-19: assintomática/moderada ou grave. Os doentes gravemente doentes apresentaram alterações profundas na composição da microbiota intestinal, em comparação com os doentes ligeiros a moderados em ambulatório ou internados na enfermaria do hospital (Figura 1). Estas alterações incluíram: 1) menor diversidade microbiana intestinal global; 2) menor abundância de bactérias produtoras de butirato benéficas, como Roseburia e Lachnospira; 3) menor relação Firmicutes/Bacteroidetes; 4) maior abundância de Proteobactérias. Além disso, detetámos o vírus em amostras fecais, o que deve ser considerado nas recomendações de saúde pública [5, 6] Publicações de outros colegas mostraram que a baixa diversidade pode ser um biomarcador clínico que prevê um maior risco de gravidade [7-9].
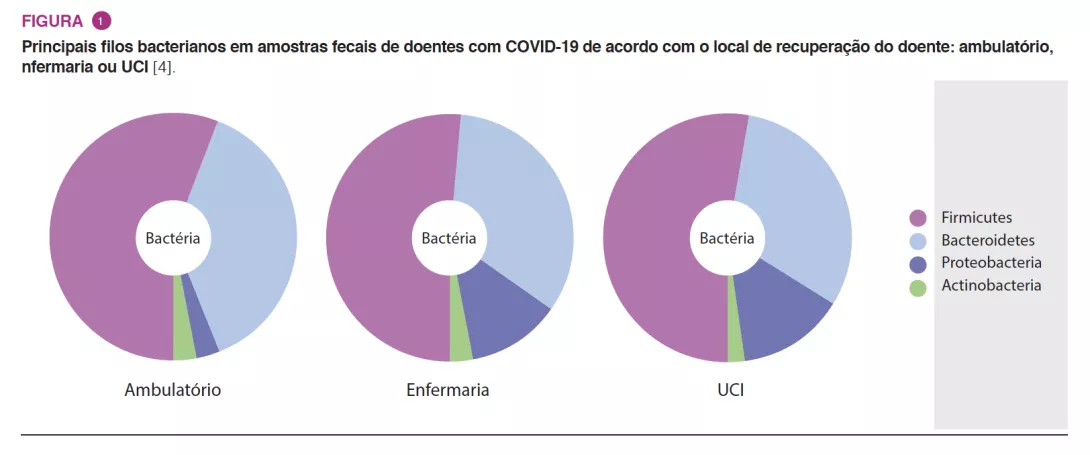
A sabedoria convencional era que os pulmões saudáveis eram estéreis. Na última década, a aplicação de técnicas de investigação de microbiota mostrou claramente que não era esse o caso. Os pulmões são colonizados por uma carga bacteriana muito baixa em comparação com o intestino [10]. As diferentes partes do trato respiratório (orofaringe, vias respiratórias, pulmões) apresentam diferentes diversidades e composições relacionadas com as fontes de colonização, taxas de colonização, taxas de extinção e distâncias entre si, de acordo com o modelo adaptado da ilha, sendo o «continente» a cavidade oral [11]. Estudos recentes em doentes com Covid-19 grave mostraram disbiose da microbiota das vias aéreas (analisada em amostras de BALF) semelhante à disbiose observada durante infeções do trato respiratório inferior, pneumonia, por exemplo [12, 13]. Além disso, Acinetobacter – um agente patogénico gram-negativo comum de bacilos não fermentadores da pneumonia associada à ventilação mecânica, que é a infeção mais grave adquirida na UCI em doentes submetidos a ventilação mecânica invasiva – foi um género bacteriano comum encontrado nos tecidos pulmonares em doentes falecidos [14]. A presença de alguns agentes patogénicos no pulmão de doentes falecidos e na cavidade oral está relacionada com a migração do modelo de ilha adaptada. [15] Em resultado da desregulação imunitária associada à Covid- 19, vários estudos epidemiológicos mostraram um risco acrescido de infeções hospitalares adquiridas, nomeadamente pneumonia associada à ventilação mecânica, como o nosso grupo demonstrou. No nosso estudo descobrimos que os doentes com Covid-19 apresentaram o dobro do risco de pneumonia associada à ventilação mecânica em comparação com os doentes não Covid 19 [16].
Os estudos de microbiota e Covid-19 podem abrir perspetivas para o desenvolvimento de intervenções terapêuticas (probióticos, prebióticos...) que visam corrigir a disbiose observada em doentes graves com Covid-19. Espera-se que estas intervenções aumentem a diversidade bacteriana global e a abundância de bactérias comensais, contribuindo assim para inibir o crescimento excessivo de agentes patogénicos oportunistas. Estes estudos poderão também ter implicações na conceção de vacinas eficazes contra a Covid 19, pois um fator conhecido para controlar a eficácia da vacina poderá ser a microbiota intestinal.
Síntese
Pelo Dr. Vincent Trebossen
Departamento de Psiquiatria da Criança e do Adolescente, Hospital Robert-Debré, APHP, Paris, França
Pelo Dr. Pierre Ellul
Departamento de Psiquiatria da Criança e do Adolescente, Hospital Robert-Debré, APHP, Imunologia - Imunopatologia - Imunoterapia, Hospital Pitié Salpêtrière, U959 Inserm, Paris, França
Pelo Dr. Alexis Mosca
Serviço de Gastroenterologia Pediátrica, Hospital Robert-Debré, APHP, Paris, França
Pelo Pr. Richard Delorme
Departamento de Psiquiatria da Criança e do Adolescente, Hospital Robert-Debré, APHP, Genética Humana e Funções Cognitivas, Institut Pasteur, UMR3571 CNRS, Universidade Paris-Cidade, Paris, França

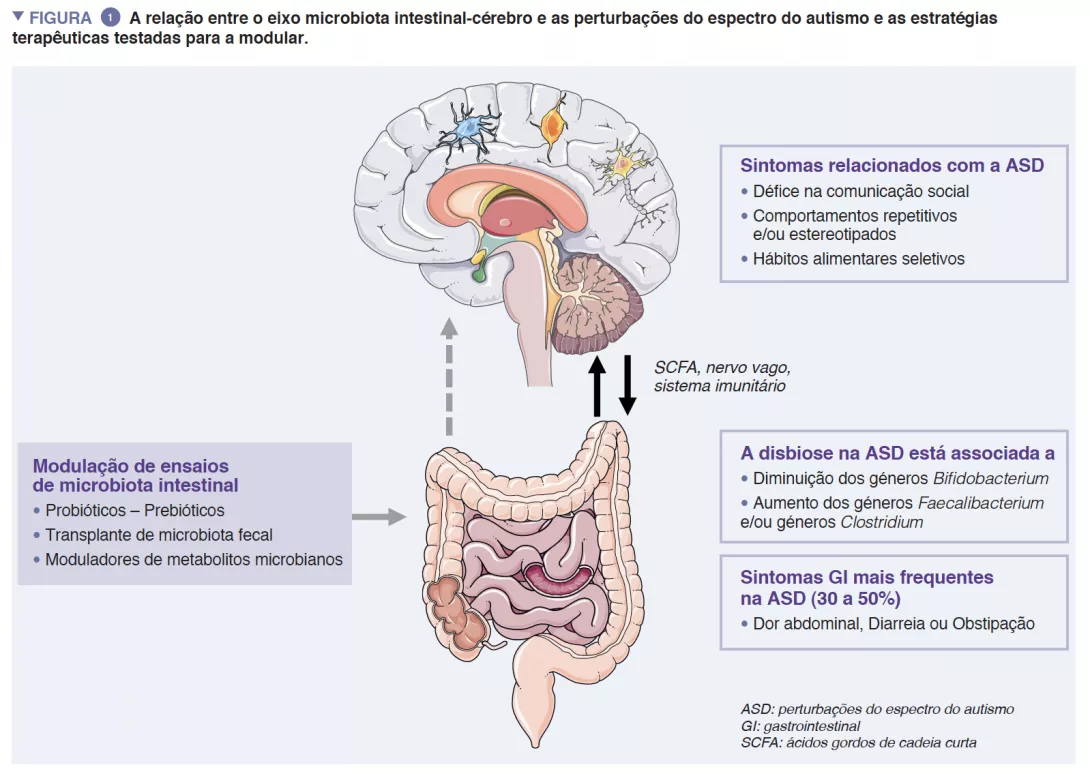
As Perturbações do Espectro do Autismo (ASD) são perturbações complexas do neurodesenvolvimento que afetam 1% da população em geral e que se caracterizam por um défice na comunicação social e comportamentos repetitivos/ estereotipados. Os mecanismos fisiopatológicos por detrás das ASD são ainda mal compreendidos [1]. Trinta a 50% dos indivíduos com ASD apresentam sintomas gastrointestinais (GI), como dor abdominal, diarreia, obstipação, que afetam a sua qualidade de vida e o seu funcionamento global. Curiosamente, a ocorrência e a gravidade dos sintomas GI estão fortemente correlacionados com sintomas de autismo [2]. Enquanto que a etiologia dos sintomas GI é ainda desconhecida, vários estudos sugeriram que as ASD poderão resultar de um desequilíbrio na composição da microbiota intestinal (GM) [3]. Achados consistentes sugerem interações robustas entre a GM e o sistema nervoso central (SNC). A GM afeta diretamente o neurodesenvolvimento através do impacto da neurogénese, sobrevivência dos neurónios, crescimento do cérebro e mielinização. A modulação da GM utilizando pro- ou prebióticos ou transplante de microbiota fecal (FMT) em indivíduos com ASD mostra efeitos benéficos e a longo prazo nos sintomas GI e n os sintomas centrais do autismo. No entanto, são necessários ensaios aleatorizados maiores em dupla ocultação para confirmar a eficácia das terapias de base microbiana nas ASD, especificamente numa fase precoce e crítica do neurodesenvolvimento.
A microbiota intestinal (GM) humana é constituída por aproximadamente 1013 microrganismos, principalmente bactérias, fungos e vírus. A GM desempenha um papel central na saúde humana, assegurando a função de barreira intestinal, modulação da resposta imunitária e síntese metabólica, mas também uma proteção direta contra infeções. A disbiose caracterizada por uma GM desequilibrada tem sido associada a várias doenças, como doenças inflamatórias intestinais, cancros, diabetes ou obesidade [4]. Achados consistentes também sugerem interações robustas entre a GM e o sistema nervoso central (SNC) [5] (Figura 1).
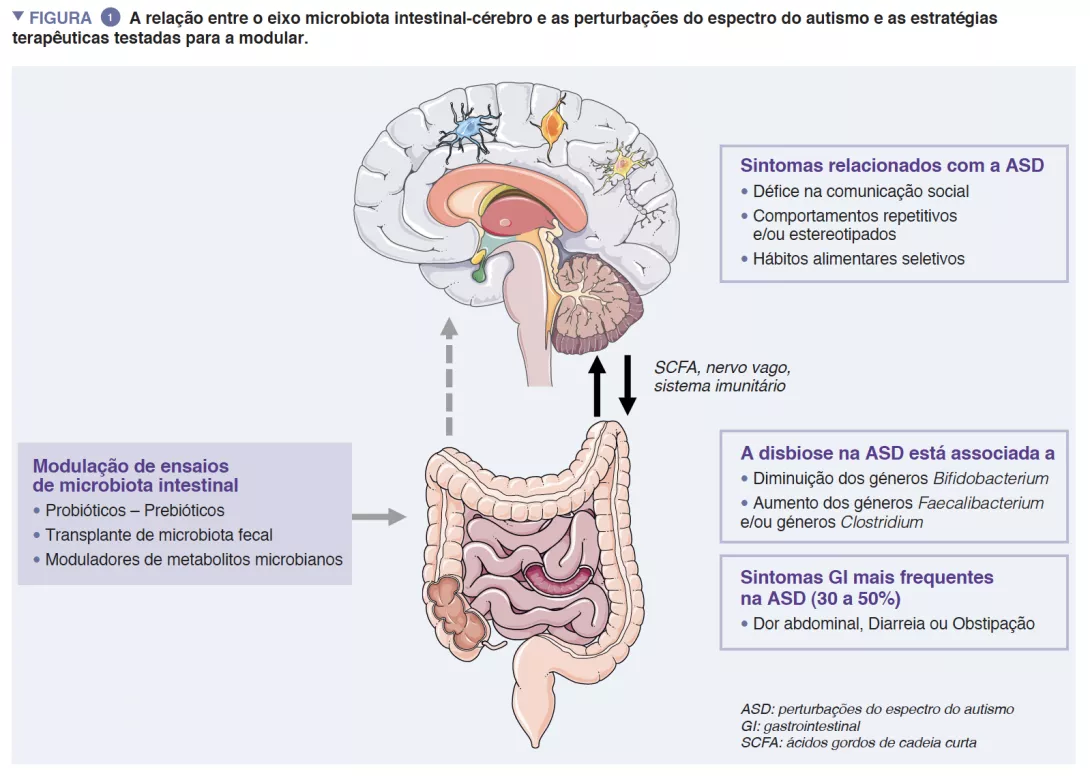
Um cruzamento recíproco entre o cérebro e a GM é mediado por metabolitos microbianos (principalmente ácidos gordos de cadeia curta) e moduladores imunitários diretamente, atravessando tanto as barreiras intestinal e cerebral como indiretamente através da estimulação do nervo vago [6]. As provas apoiam o envolvimento da GM na regulação tanto dos comportamentos humanos como dos cognitivos - especificamente das competências de comunicação social – mesmo que os seus mecanismos exatos sejam ainda desconhecidos [5].
As ASD são perturbações do neurodesenvolvimento caracterizadas por deficiências na comunicação social, interações sociais e comportamentos repetitivos/estereotipados, de início na infância que afetam cerca de 1% da população em geral. O determinismo das ASD é principalmente impulsionado por fatores genéticos, com uma heritabilidade estimada em 0,8 0,9, mas os eventos ambientais pré e pós-natais podem funcionar como fatores precipitantes ou moduladores da gravidade dos sintomas. A trajetória do desenvolvimento do cérebro numa fase precoce da vida sobrepõe-se às da GM. Esta última começa a desenvolver-se cedo após o nascimento e a sua composição estabiliza-se num perfil semelhante ao de um adulto por volta dos 3 anos de idade. A composição precoce da GM é profundamente influenciada por fatores ambientais, como o local de nascimento, modo de parto, amamentação e xenobióticos (por exemplo, utilização de antibióticos).
Os ratinhos sem germes são um modelo sem todos os microrganismos, por exemplo, são microbiologicamente axénicos (nenhum organismo vivo pode ser cultivado a partir de espécimes de ratinhos sem germes). Os modelos de ratinhos sem germes são valiosos para decifrar os mecanismos subjacentes aos papéis da GM no neurodesenvolvimento, mas também a relação entre o microbioma e a doença. Estudos demonstraram que os ratinhos sem germes apresentam i) defeito na permeabilidade da barreira cérebro-sangue; ii) maior volume cerebral; iii) expressão mais imatura do gene da microglia e menor resposta imunitária microglial; iv) aumento da mielinização; e v) diminuição da expressão do fator neurotrófico derivado do cérebro e numa subunidade de recetores de N-Metil-D-Aspartato [5, 7]. Todos estes dados salientam o papel da GM na formação e integridade da barreira hemato- encefálica, neurogénese, homeostase da microglia, mielinização e crescimento/ função cerebral.
Os ratinhos sem germes apresentaram comportamentos do tipo autista, como evasão social, comportamentos repetitivos/ estereotipados, falta de interesse pela novidade social. Alguns destes comportamentos desapareceram após a colonização por uma GM a partir de ratinhos do tipo selvagem, enquanto que a colonização pela GM a partir de modelos de ratinhos ASD aumentou estes comportamentos. A GM parece, de facto, crucial para a programação e apresentação de competências sociais e comportamentos adaptativos [8]. Um número crescente de provas mostra que os sintomas GI estão sobre-representados nas crianças com ASD. Sintomas GI, como dor abdominal, obstipação, diarreia, são reportados em quase 30-50% dos doentes com ASD e têm um impacto profundo na qualidade de vida das crianças [1]. A gravidade dos sintomas GI foi correlacionada com a gravidade dos sintomas autísticos e a disbiose intestinal está bem documentada, mesmo que ainda não exista uma assinatura específica relacionada com sintomas autísticos. Estudos que exploram a GM reportaram diferenças na diversidade da microbiota e padrões anormais de metabolitos, quando comparados com controlos saudáveis. Duas meta-análises recentes que exploram a composição da GM em doentes com ASD reportaram uma diminuição em Bifidobacterium e um aumento dos géneros Faecalibacterium e Clostridium em doentes com ASD [9, 10] em comparação com os controlos. A exploração do metaboloma fecal também mostrou um aumento do p-cresol, um metabolito bacteriano derivado da tirosina, em indivíduos com ASD. Todos juntos, estes dados podem indicar a potencial associação entre anomalias da GM e sintomas GI em doentes com ASD.
No entanto, a maioria dos estudos tem resultados heterogéneos e limitações metodológicas. Fatores meramente confundidores, como diferentes países com diferentes estilos de vida e hábitos alimentares, são os principais inconvenientes destes estudos. De facto, um estudo recente numa grande coorte de 247 indivíduos com ASD não reportou ligações diretas entre o diagnóstico de ASD ou sintomas de autismo e a disbiose da GM. A disbiose foi associada a uma dieta menos diversificada que é comum em doentes com ASD [8].
Praticamente 30 a 50% dos doentes com ASD reportaram sintomas GI, como dor abdominal, diarreia, obstipação. A disbiose da GM em doentes com ASD foi bem explorada e confirmada através de metaanálise, mesmo que não haja uma assinatura específica do microbioma [9, 10]. A ligação entre a disbiose da GM e as ASD ainda é mal compreendida. Alguns estudos sugerem ligações diretas através do eixo GM-cérebro que influenciam sintomas autísticos e sintomas gastrointestinais. Mais recentemente, um estudo sugere que a disbiose da GM em doentes com ASD está principalmente ligada à dieta restritiva que é frequente em doentes com ASD [8].
Um número crescente de estudos explorou o impacto potencial das estratégias terapêuticas baseadas na microbiota para melhorar os sintomas GI e os principais sintomas em indivíduos com ASD.
Os probióticos, microrganismos vivos, têm sido utilizados nas ASD e podem ter um efeito benéfico nos doentes com ASD. Alguns estudos pré-clínicos mostraram um aumento das interações sociais com a suplementação de probióticos (Bacteroides fragilis NCTC9343, Lactobacillus reuteri MM4-1A) em modelos de ratinhos com ASD. A melhoria da comunicação social foi ligada a uma expressão aumentada de oxitocina no SNC. Nos humanos, vários estudos reportaram efeitos positivos dos tratamentos probióticos na composição de GM e sintomas GI nas ASD [11]. No entanto, poucos deles reportaram uma melhoria dos sintomas principais de autismo. A maioria dos ensaios clínicos que forneceram probióticos em indivíduos autistas mostrou inconsistência em termos de probióticos, administração de dosagem por dia ou no total e duração de todo o tratamento. Mesmo que alguns estudos sugiram que os probióticos poderão ser interessantes para prevenir sintomas GI em doentes com ASD, os resultados exigem a replicação para garantir o efeito positivo de tal estratégia.
Do mesmo modo, a eficácia dos prebióticos, como o galacto-oligossacarídeo (GOS) ou o fructo oligossacarídeo, foi explorada nas ASD [12]. Ratinhos com stress crónico mostraram alterações na GM e uma diminuição do interesse social. Utilizando este modelo de ratinho, a administração de prebióticos foi associada a um aumento das interações sociais nestes ratinhos. Nos humanos, a utilização de GOS associados a uma dieta sem caseína e sem glúten mostrou uma melhoria nos sintomas GI e nas interações sociais, juntamente com um aumento da abundância de Bifidobacterium da GM. São necessários estudos clínicos aleatorizados em dupla ocultação adequados para confirmar as provas preliminares.
O transplante de microbiota fecal (FMT) também tem sido estudado nas ASD. O FMT envolve o transplante de GM de um doador para modificar a GM do recetor. A sua eficácia na infeção por Clostridioides difficile está agora bem demonstrada, mesmo em crianças. Um recente ensaio clínico exploratório sem ocultação e não aleatorizado que envolveu 18 crianças diagnosticadas com ASD e GI avaliou o efeito da terapia de transferência de microbiota (MTT) - um protocolo modificado do FMT [13]. A MTT consistiu num tratamento antibiótico de duas semanas, uma limpeza intestinal, antes de receber o tratamento MTT que consistiu numa dose elevada através de administração oral ou retal seguida de uma dose de manutenção oral durante 7 a 8 semanas. Foram observados eventos adversos no início do tratamento com vancomicina (comportamentos perturbadores, hipercinesia) mas desapareceram espontaneamente após 3 dias de tratamento. O protocolo MTT levou a uma melhoria significativa dos sintomas GI após o seguinte inquérito às 8 semanas. Mais surpreendentemente, também tinha sido observada uma melhoria dos sintomas principais do autismo (comportamentos estereotipados e repetitivos, competências de comunicação social) 8 semanas após a MTT. Curiosamente, a melhoria dos sintomas GI e sintomas de autismo persistiu 2 anos após o tratamento e foi correlacionada com o aumento da diversidade da GM [14]. Dois anos após a MTT, a redução média da Escala de Classificação dos Sintomas Gastrointestinais (GSRS) era ainda superior a 50%. As alterações nos sintomas autísticos medidas com a Escala de Avaliação do Autismo Infantil - CARS, a Escala de Responsabilidade Social - SRS, ou a Lista de Verificação do Comportamento Autista - ABC foram todas positivamente correlacionadas com as alterações percentuais na pontuação GSRS. Estes resultados ainda não são confirmados por estudos aleatorizados em dupla ocultação controlados por placebo.
Recentemente, um ensaio clínico piloto sem ocultação em ASD explorou o efeito de um adsorvente oral restrito a GI (AB- 2004) modulando vários metabolitos GM. Os autores reportaram uma diminuição dos comportamentos de ansiedade em ratinhos, impulsionada por uma diminuição do metabolito microbiano intestinal [15]. O estudo também apresentou resultados preliminares de um ensaio clínico em que uma dose do AB-2004 ajustada ao peso foi administrada, durante 8 semanas, a 30 adolescentes com ASD. Na semana 8, foram observados níveis reduzidos de metabolitos GM no plasma e na urina. Mais interessante, após o tratamento, menos sujeitos apresentaram sintomas GI mas também comportamentos associados às ASD, ansiedade, e irritabilidade. Houve também um efeito remanescente com uma persistência da eficácia às 4 semanas após a interrupção do tratamento [15]. Os fatores que ligam as melhorias clínicas e a administração do AB-2004 continuam por determinar, alguns fatores indiretos não foram estudados, como o efeito do AB-2004 nas mudanças nutricionais, no estado imunitário ou na função gastrointestinal. Estudos maiores e em dupla ocultação controlados por placebo são justificados para dissecar ainda mais o papel do AB-2004 na comunicação social no ser humano.
No contexto da falta de tratamento específico para os sintomas GI e sintomas autísticos em doentes com ASD, novas estratégias terapêuticas bem toleradas que visem metabolitos GM ou microbianos, como FMT/MTT, precisam de ser mais especificamente realizadas nas fases iniciais e críticas do desenvolvimento cerebral durante a infância.
O FMT é uma nova forma eficiente de modular a GM utilizada em doenças gastrointestinais e endócrinas. O transplante de microbiota fecal (FMT) poderá representar uma nova e eficiente oportunidade de modular/reinicializar a GM nas ASD. Utilizando modelos de ratinho de ASD, o FMT melhorou eficazmente os sintomas centrais do autismo, como défices de comunicação social e comportamentos estereotipados. Nos humanos, um ensaio piloto sem ocultação em adultos com ASD sugeriu que o FMT poderá melhorar não só os sintomas GI mas também a reciprocidade social e os comportamentos estereotipados. Ocorreu um efeito remanescente com uma eficácia persistente 2 anos após a interrupção do tratamento. Curiosamente, a eficácia foi associada a uma maior diversidade da GM. O FMT poderá ser uma nova estratégia terapêutica de vanguarda para tratar os sintomas gastrointestinais e comportamentais em crianças com ASD, e apenas abrir novos caminhos para a fisiologia da comunicação social no ser humano.

O impacto da microbiota intestinal na trajetória de neurodesenvolvimento das crianças permanece em grande parte inexplorado. Neste momento, não existem estudos que explorem o impacto da modulação da microbiota intestinal na fase inicial do desenvolvimento infantil, particularmente nas competências de comunicação social. Estudos preliminares em adultos e crianças demonstraram que a modulação da GM leva a uma melhoria dos sintomas GI e dos comportamentos autísticos. Com base nestes dados, iremos realizar um ensaio clínico em dupla ocultação em crianças mais novas com ASD numa fase muito precoce do seu desenvolvimento cognitivo (antes dos 6 anos de idade). O nosso objetivo é compreender se o FMT realizada num período crítico de desenvolvimento resultará numa melhoria significativa a longo prazo da trajetória de desenvolvimento infantil.
Existirá um eixo intestino-bexiga que contribuirá para a recorrência das infeções do trato urinário? Como? Através da disbiose intestinal e de uma resposta imunitária ineficaz durante a colonização bacteriana da bexiga. Explicações.
Habituais e recorrentes. Este é o retrato-robô das infeções urinárias que tendem a afligir sempre as mesmas mulheres: 20 a 30% delas sentem a infeção regressar, com até 6 episódios por ano ou mesmo mais. Como o intestino serve de reservatório a bactérias patogénicas que ascendem pela vulva, os investigadores têm se interessado sobre a existência potencial de um eixo "intestino-bexiga":
Para responder a estas questões, foi realizado um estudo clínico longitudinal de um ano englobando 15 mulheres com histórico de infeções urinárias recorrentes face a 16 mulheres saudáveis.
Os resultados demonstram que as mulheres com histórico de IUr apresentavam uma microbiota intestinal menos diversificada, com mais Bacteroidetes e menos Firmicutes e bactérias produtoras de butirato como Blautia. Contudo, sabe-se que estas últimas regulam a inflamação. De facto, as análises ao sangue comprovam que as mulheres sensíveis às infeções possuíam caraterísticas indicativas de inflamação de baixo grau. Tudo isto sugere que a suscetibilidade a IUr é parcialmente mediada por um eixo intestino-bexiga, através da disbiose intestinal e de uma alteração da imunidade sistémica.
20 a 30% das mulheres com diagnóstico de infeção urinária apresentarão infeções recorrentes do trato urinário (IUr).
Foram relatadas 24 infeções do trato urinário durante o estudo, todas no grupo das mulheres IUr, e causadas por E. coli em 82% dos casos. No entanto, a disbiose observada nas mulheres IUr não pareceu ter impacto na dinâmica dessa bactéria: as populações de E. coli no intestino e bexiga mantiveram-se comparáveis entre os 2 grupos, tanto em termos de abundância relativa como de filogrupos. Simultaneamente, nenhum sintoma de infeção do trato urinário se manifestou nos controlos saudáveis, o que indica que conseguiram por si mesmos eliminar a E. coli das respetivas bexigas. Outra conclusão: as cepas de E. coli responsáveis pela infeção do trato urinário colonizam frequentemente o intestino de forma persistente, sem serem definitivamente eliminadas pela exposição repetida a antibióticos. Em outras palavras: os antibióticos poderão curar a curto prazo ao eliminarem a E. coli da bexiga, mas não protegerão contra as recorrências a longo prazo causadas por E. coli intestinal residual.
O que leva a questionar o interesse da prescrição de antibióticos que, aliás, podem exacerbar a disbiose intestinal e a inflamação dela resultante... E a mudar o foco para as potenciais alternativas da microbiota no sentido de restabelecer uma comunidade bacteriana saudável no intestino.

"Achei interessante!!" -@BevisHTR25 (Da Biocodex Microbiota Institute em X)
Já se sabia que o consumo de pimentão ajudava a combater a inflamação e a prevenir a obesidade, mas até agora não se sabia como.
O mistério parece ter sido resolvido graças aos resultados de um estudo in vitro sobre a flora intestinal, realizado a partir de amostras de fezes... Um estudo a que não falta tempero picante!

Pica, queima, aquece as bochechas, faz palpitar as papilas gustativas e até o estômago, mas faz bem à saúde! Anti-inflamatória, anticolesterol, anti-hipertensiva, antiobesidade, etc. As virtudes da comida picante parecem ser infinitas!
Essas propriedades saudáveis são atribuídas à capsaícina, o composto presente no pimentão que queima na boca. Embora seja difícil, de um ponto de vista gustativo, passar ao lado do efeito picante, os mecanismos envolvidos ainda suscitam dúvidas. De acordo com uma das hipóteses avançadas, o consumo de capsaícina causará um enriquecimento da microbiota intestinal em bactérias produtoras de
(sidenote:
Ácidos Gordos de Cadeia Curta (AGCC)
Os Ácidos Gordos de Cadeia Curta são uma fonte de energia (carburante) das células do indivíduo, interagem com o sistema imunitário e estão envolvidos na comunicação entre o intestino e o cérebro.
Silva YP, Bernardi A, Frozza RL. The Role of Short-Chain Fatty Acids From Gut Microbiota in Gut-Brain Communication. Front Endocrinol (Lausanne). 2020;11:25.
)
, aos quais serão atribuíveis esses múltiplos benefícios.
Para verificar esta hipótese e evitar as possíveis interações da capsaícina com outros elementos do organismo humano, uma equipe sino-americana optou por realizar um estudo in vitro. Os investigadores recolheram fezes de dois indivíduos saudáveis, introduziram-nas num biorreator a reproduzir as condições do cólon e, em seguida, adicionaram capsaícina ou uma solução de controlo. Passadas duas semanas, analisaram a composição das duas amostras e compararam os resultados com os que tinham obtido no início do estudo, antes da adição da solução – com ou sem capsaícina.
Garante de boa saúde, a diversidade das bactérias que integravam a composição das duas amostras de microbiota intestinal tratadas com capsaícina aumentou acentuadamente durante o estudo, confirmando os dados observados in vivo em vários estudos realizados em humanos e em ratos. A produção de alguns ácidos gordos de cadeia curta também variou, mas de forma diferente de amostra para amostra: ambas produziram mais ácido propenoico (conhecido pelo seu papel na regulação do apetite), mas apenas a primeira produziu mais ácido butanoico (ou ácido butírico, dotado de reconhecidas propriedades inflamatórias).
Embora estes resultados validem a hipótese de que as virtudes do pimentão estão ligadas à interação do seu principal composto (capsaícina), também confirmam que os efeitos benéficos variam de acordo com a composição inicial da microbiota. São virtudes "explosivas", mas não são para todos...
 Uma dieta mediterrânica boa para o corpo e boa para o coração
Uma dieta mediterrânica boa para o corpo e boa para o coração
Um estudo no European Urology Oncology1 revela que as bactérias da microbiota prostata-urinária, das quais algumas são desconhecidas até agora, estão associadas a um risco mais elevado de cancro agressivo da próstata. Se a sua função enquanto marcador de agressividade tumoral for confirmada, elas poderia revolucionar o tratamento da doença.

Sendo o segundo cancro mais frequente no homem em todo o mundo, o cancro da próstata também é o quinto mais mortífero, com mais de 375.000 óbitos em 20202. Apesar destes números, o cancro de próstata caracteriza-se por uma evolução muito heterogénea (nos Estados Unidos, uma sobrevivência estimada de 90% aos 5 anos1).
Hoje, é a agressividade do tumor que indica a direção das decisões de tratamento. Ela é avaliada, entre outras, pela pontuação histopatológica de Gleason após uma biópsia, um procedimento invasivo. A identificação de marcadores urinários permitem, em combinação com outros dados clínicos, detetar as formas agressivas da doença, facto que provoca um grande interesse por parte dos clínicos.
2º cancro mais frequente no homem
5º cancro mais mortífero em todo o mundo
Estudos já haviam revelado a relação entre o cancro do próstata e um perfil microbiano particular, como também diferenças entre as comunidades de bactérias prostáticas segundo a pontuação de Gleason. Foi, então, para o microbioma prostatourinário, o qual ainda não está completamente caracterizado, que os investigadores britânicos se viraram para explorar o seu potencial prognóstico1. Graças a ferramentas como a microscopia de fluorescência, a cultura bacteriana anaeróbica e a sequenciação genómica, eles analisaram amostras de urina e de secreção de tecido prostático colhidas de mais de 600 indivíduos examinados no hospital por suspeita de cancro da próstata ou hematúria. Os indivíduos foram divididos em grupos clínicos e os doentes diagnosticados com cancro da próstata classificados de acordo com a pontuação de d'Amico.
Os investigadores encontraram uma associação significativa entre a presença de bactérias na urina e um risco aumentado de cancro da próstata. Eles também descobriram quatro novas espécies de bactérias nas amostras urinárias, secreções prostáticas e nos tecidos. Elas pertenciam ao filo dos Firmicutes (Fenollariasp. nov. e Peptoniphilus sp. nov), das Actinobacterias (Varibaculum sp. nov) e das Bacteroidetes (Porphyromonas sp. nov). Cinco espécies anaeróbicas, incluindo três entre estas novas bactérias, estavam associadas a um risco multiplicado por 2,6 de evolução desfavorável da doença e poderiam servir de potenciais biomarcadores de prognóstico
Os investigadores chegaram a uma hipótese: estas bactérias anaeróbias atuariam em certos processos metabólicos.
Por exemplo, a conversão do colesterol em androstenediona, um precursor da testosterona que estimula o crescimento de tumores, ou a degradação do citrato, um conhecido marcador da agressividade do cancro da próstata. Mas uma relação causal entre a sobrerepresentação destas bactérias nos doentes e a progressão da doença não pode ser estabelecida nesta fase.
Portanto, devem ser empreendidas novas investigações neste sentido: se esta ligação for confirmada, poderá ser desenvolvido um teste de prognóstico de urina muito prático para a clínica. Melhor ainda, tratamentos antibióticos específicos poderiam controlar ou mesmo impedir a progressão da doença.
1. Hurst R, Meader E, Gihawi A, et al. Microbiomes of Urine and the Prostate Are Linked to Human Prostate Cancer Risk Groups. Eur Urol Oncol. 2022 Apr 18:S2588-9311(22)00056-6.
3. Survival Rates for Prostate Cancer_American Cancer Society
 Um novo marcador inesperado para prever a evolução do cancro da próstata: a microbiota intestinal
Um novo marcador inesperado para prever a evolução do cancro da próstata: a microbiota intestinal