Les infections urinaires (UI) sont parmi les infections bactériennes les plus courantes dans le monde, elles surviennent lorsque des bactéries, provenant de la peau ou du rectum, pénètrent dans l'urètre et infectent les voies urinaires.1,2 Une récente étude américaine a permis de suivre durant un an une trentaine de femmes souffrant d’infections urinaires et sous traitements antibiotiques. Le constat est sans appel : c’est un véritable cercle vicieux pour les femmes sujettes aux infections urinaires. Les antibiotiques prescrits pour soulager la crise du moment pourraient faire le lit de la suivante.
Au commencement, le microbiote intestinal
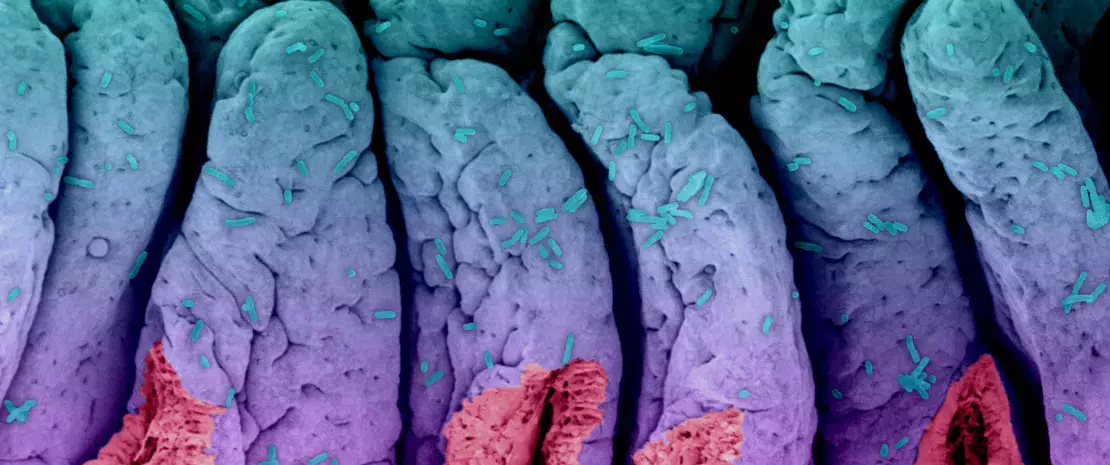
Tout commencerait dans l’intestin. Quelques bactéries appelées Escherichia coli remonteraient via la vulve, située à proximité de l’anus, dans les voies urinaires. Jusque-là, rien d’anormal puisque l’on observe le même phénomène chez les femmes non sujettes à de telles infections. Habituellement, le système immunitaire se charge d’éliminer les indésirables. Sauf que chez les femmes sujettes aux infections urinaires chroniques, le système immunitaire ne serait pas au top de sa forme. La faute, sans doute, aux traitements antibiotiques répétés qui ont en partie éliminé les bactéries en charge de réguler notre immunité via de petites molécules fabriquées dans nos intestins et qui passent ensuite dans notre sang.
Conséquence directe : E. coli déclenche une nouvelle infection urinaire… et le médecin, démuni, prescrit un nouveau traitement antibiotique. Et c’est reparti pour un tour puisque ce nouveau traitement va certes éliminer les bactéries de la vessie, mais pas le réservoir de ses sœurs dorlotées dans notre tube digestif.
Pire : le traitement risque de perturber davantage les gentilles bactéries de notre microbiote intestinal qui tentaient, tant bien que mal, de réguler notre système immunitaire pour qu’il puisse lutter contre les E. coli remontant dans la vessie.
Changer de stratégie
Bilan des courses : 20 à 30 % des femmes verront rapidement revenir leur infection urinaire.
Sans parler du développement de résistances aux antibiotiques qui compliquent le traitement de la nouvelle crise. Comment sortir de ce cercle vicieux ? Peut-être en changeant de stratégie. Au lieu de tenter d’éliminer les indésirables, quitte à faire des victimes collatérales (les gentilles bactéries qui régulent notre immunité) et donc des dommages à long terme, quid de bichonner les bactéries qui assurent l’équilibre de notre microbiote intestinal ? Car les femmes sujettes aux infections urinaires ont un microbiote intestinal en berne, moins diversifié et moins riche en gentilles bactéries.
D’où la suggestion des auteurs de se concentrer sur les thérapies du microbiote pour restaurer la communauté bactérienne des femmes sujettes aux infections.

 Les deux visages des Antibiotiques : Sauveurs de Vie et Perturbateurs de Microbiote
Les deux visages des Antibiotiques : Sauveurs de Vie et Perturbateurs de Microbiote
 Impact des antibiotiques sur le microbiote intestinal : quelle importance ?
Impact des antibiotiques sur le microbiote intestinal : quelle importance ?