Antibiotiques : quels impacts sur le microbiote et notre santé ?
Malgré leur incontestable utilité dans la lutte contre les infections, les antibiotiques posent aujourd'hui de sérieux enjeux de santé publique: leur usage excessif et inapropprié fait émerger de nombreuses résistances, ce qui, à terme risque de les rendre inefficaces. D'autre part, les antibiotiques peuvent également détruire certaines bactéries bénéfiques au sein de nos microbiotes.


À l'occasion de la Semaine mondiale de sensibilisation à la résistance aux antimicrobiens organisée chaque année par l’OMS, le Biocodex Microbiota Institute fait le point.
70 % des personnes affirment savoir que les antibiotiques ont un impact sur le microbiote
Depuis 2015, l’OMS organise chaque année la Semaine mondiale de sensibilisation à la résistance aux antimicrobiens (WAAW), qui a pour but de mieux faire connaître le phénomène mondial de résistance aux antimicrobiens.
La résistance aux antimicrobiens survient lorsque les bactéries, les virus, les parasites et les champignons évoluent et résistent aux effets des médicaments. En raison de cette pharmacorésistance, les antibiotiques et autres médicaments antimicrobiens perdent leur efficacité et les infections deviennent plus difficiles, voire impossibles à traiter, ce qui augmente le risque de propagation des maladies, de pathologie grave et de décès.
Organisée du 18 au 24 novembre, cette campagne invite le grand public, les professionnels de santé et les décideurs politiques à faire un usage raisonné des antibiotiques, des antiviraux, des antifongiques et des antiparasitaires afin de prévenir le développement accru de la résistance aux antimicrobiens.
Antibiotiques : quels sont les impacts sur notre microbiote ?
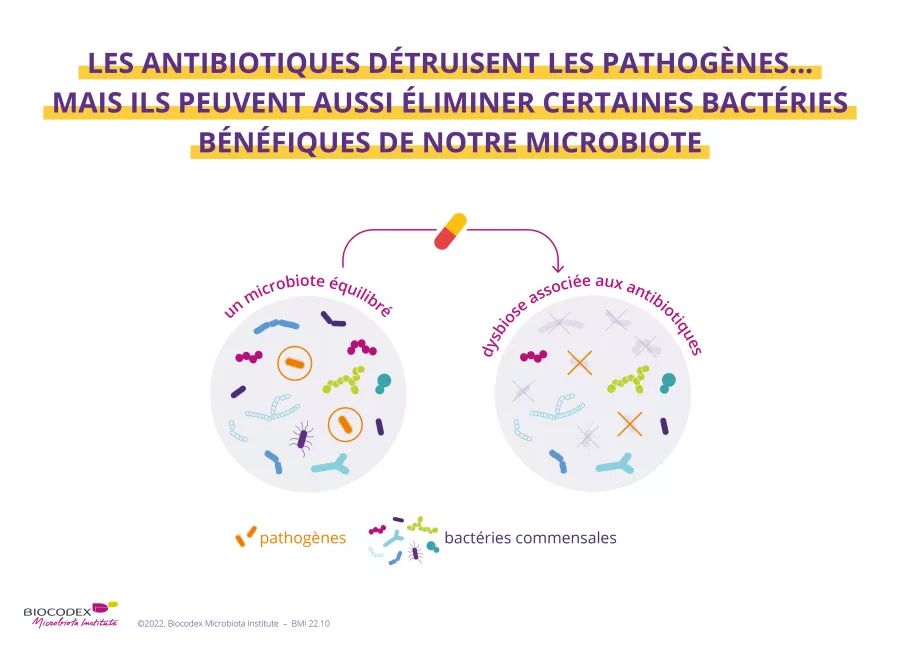
Les antibiotiques ne font pas toujours la différence entre bonnes et mauvaises bactéries. Ils détruisent non seulement les bactéries pathogènes, mais aussi celles bénéfiques du microbiote intestinal. Ces perturbations réduisent la diversité bactérienne, ce qui amène une fragilité dans nos défenses naturelles, favorisant certains déséquilibres.
Découvrez nos articles pour mieux comprendre comment les antibiotiques influencent notre microbiote :
Antibiotiques : quels sont les effets à long terme sur notre santé ?
L’exposition répétée aux antibiotiques peut influencer la composition du microbiote et accroître le risque de troubles immunitaires, digestifs ou allergiques. Les effets ne s’arrêtent pas toujours à la fin d’un traitement. Leur influence sur le microbiote peut laisser des traces importantes pour notre santé. Ces perturbations rappellent l’importance d’un usage raisonné pour protéger notre santé sur le long terme et limiter les déséquilibres du microbiote.
Découvrez comment les antibiotiques peuvent influencer notre santé dès le bas-âge :
Antibiotiques : pourquoi parle-t-on de diarrhée associée aux antibiotiques ?
La diarrhée post-antibiotique est une conséquence fréquente d’un microbiote intestinal perturbé par un traitement médicamenteux. En altérant la flore protectrice, certains antibiotiques ouvrent la voie à des déséquilibres ou à la prolifération de bactéries opportunistes. Restaurer cet équilibre est essentiel pour préserver la santé digestive.
Explorez nos articles pour comprendre le lien entre antibiotiques, microbiote et diarrhée :
Antibiotiques : c'est quoi la "résistance aux antibiotiques" ?
La résistance aux antibiotiques apparaît quand certaines bactéries ne sont plus tuées par les médicaments. Les antibiotiques détruisent les microbes responsables des infections, mais aussi d’autres bactéries utiles. Celles qui résistent peuvent ensuite se multiplier et transmettre leur résistance à d’autres, ce qui rend les infections plus difficiles à soigner.
Découvrez nos articles pour mieux comprendre la résistance aux antibiotiques:
Antibiotiques : peut-on protéger son microbiote ?
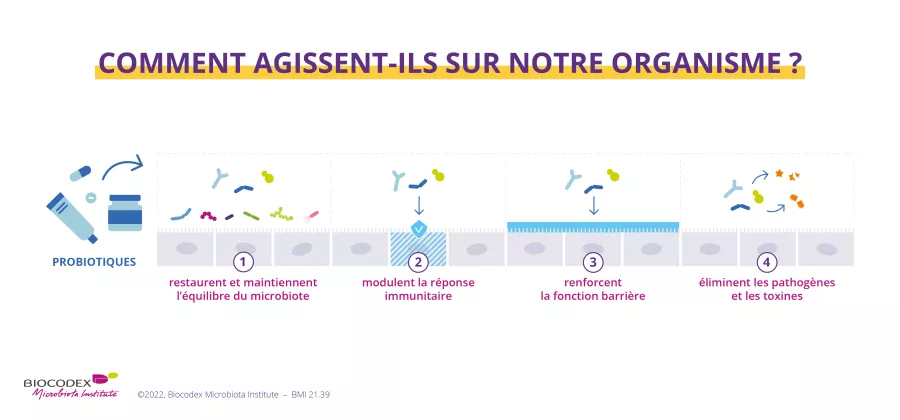
Face aux perturbations provoquées par les antibiotiques, des solutions existent pour soutenir le microbiote : une exposition réduite aux traitements avec les antibiotiques, une alimentation variée et l’utilisation de prébiotiques, probiotiques. Ces alliés aident à restaurer l’équilibre bactérien et à réduire les effets de la perturbation induite par les traitements, pour une meilleure santé globale.
Découvrez comment préserver l’équilibre du microbiote face aux antibiotiques:
L'Observatoire International des Microbiotes
Recommandé par notre communauté

"Oui, à manier avec précaution. Sinon ils n'auront plus aucun effet car tous les germes et les microbes" - Commentaire traduit de Kathy Perratore
"Quelqu'un aurait dû dire cela depuis longtemps." - Commentaire traduit de Daniel Matthew Covey
"C'est vrai." - Commentaire traduit de Connie Booth
"C'est vrai" - Commentaire traduit de Linda LeBlanc