Já se sabia que as bactérias intestinais pagavam o preço dos tratamentos com antibióticos. Mas parece que não são as únicas. Embora a maioria dos estudos se concentre no impacto dos antibióticos sobre as bactérias, são raros os que avaliam esse efeito sobre os outros microrganismos, fungos por exemplo, cujo papel não deve ser subestimado. A existência de uma disbiose da microbiota fúngica (ou micobiota) tem sido associada a várias patologias (doenças inflamatórias crónicas do intestino ou DICI, doença celíaca ou cancro colorretal). Ora, essa micobiota desenvolve-se gradualmente durante os primeiros anos de vida, da mesma forma que a colonização bacteriana, dependendo do tipo de parto, da alimentação ou mesmo dos eventuais tratamentos com antibióticos.
Um estudo com 37 lactentes sem tratamentos prévios por antibióticos
Para saber mais, os investigadores acompanharam durante 9,5 meses 37 bebés com a idade média de 2 meses, os quais nunca tinham recebido antibióticos. Os lactentes em causa estavam hospitalizados devido a infeção por vírus sincicial respiratório (VSR). Foram colhidas amostras de fezes antes, durante e após os 1 a 4 tratamentos com por antibióticos (amoxicilina, macrólidos) que foram prescritos a 21 dessas crianças devido a complicações (otite, etc.). Os outros 16 bebés, não tratados, serviram como controlos.
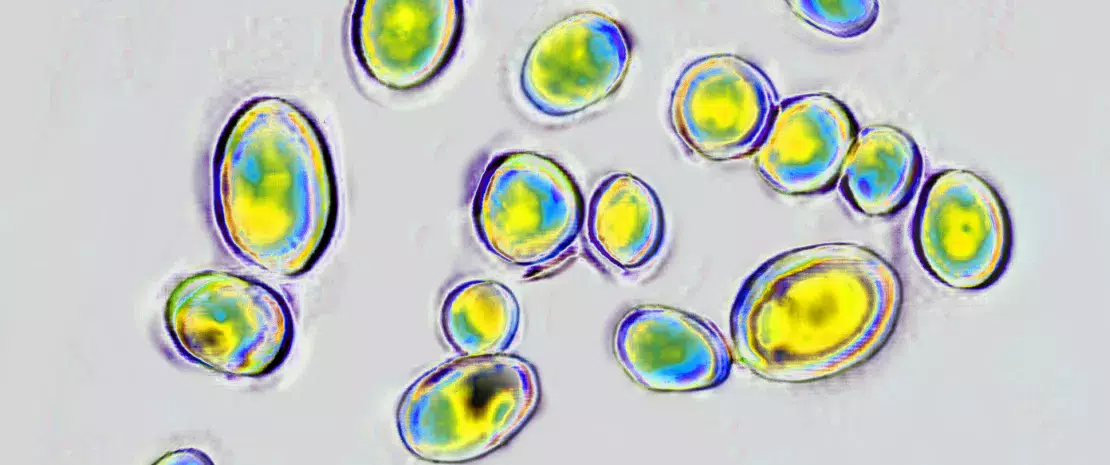
No momento de sua hospitalização (portanto, antes do tratamento), a micobiota dos 37 lactentes encontrava-se amplamente dominada por Saccharomyces e, em menor grau, por Malassezia, Candida e Cladosporium
Quanto mais Candida, maior diversidade e riqueza
Um a 2 dias após o início do tratamento com antibióticos, a abundância de Candida aumentou muito nos lactentes que receberam amoxicilina, em detrimento das Saccharomyces. Continuou a observar-se sobreabundância de Candida 6 semanas após o início do tratamento.
Além disso, os antibióticos, que se sabe induzirem um colapso na diversidade e na riqueza da microbiota bacteriana, surgiram associados a um aumento da riqueza e da diversidade da micobiota, que surgiu nos 3 a 5 dias após o início do tratamento e persistiu até muito depois (> 6 semanas); a diferença manifestou-se mais acentuada no grupo tratado com macrólidos.
Bactérias reguladoras?
Esses resultados sugerem fortemente a existência de uma regulação permanente da micobiota pelas bactérias intestinais. Essa regulação assume a forma de competição por fontes de nutrientes, através da produção de compostos antifúngicos pelas bactérias e, inversamente, de compostos antibacterianos pelos fungos. Quando as bactérias sofrem os efeitos de um antibiótico, o seu papel regulador poderá será alterado e certos fungos, em particular Candida, poderão ter rédea solta para se desenvolverem. Assim, uma disbiose da micobiota intestinal após apenas um único tratamento antibiótico poderá, juntamente com uma alteração das bactérias intestinais, estar na origem dos efeitos a longo prazo dos antibióticos sobre a saúde humana.

 Síndrome Coronária aguda (SCA): a microbiota intestinal no coração do risco?
Síndrome Coronária aguda (SCA): a microbiota intestinal no coração do risco?
 Dieta mediterrânica verde: que ligações entre a saúde cardiometabólica e a microbiota intestinal?
Dieta mediterrânica verde: que ligações entre a saúde cardiometabólica e a microbiota intestinal?